Dorota Roguś-Skorupska
Bliznowce – epidemiologia, etiopatogeneza i leczenie
Keloids – epidemiology, etiopathogenesis and treatment
z Wojewódzkiej Przychodni Skórno-Wenerologicznej w Lublinie
Kierownik Przychodni: dr n. med. Bogusław Wach
Streszczenie
Summary
The current data regarding epidemiology, etiopathogenesis and treatment of keloids was reviewed. While there is a substantial progress in the field of basic sciences still the results of treatment of this disfiguring disease are far from our expectations. The introduction of new treatment methods like lasers, cytokines (interferon-g) and cytostatic agents (bleomycin) is very promising step toward complete solution of this serious therapeutic problem.

WSTĘP
Zmiana skórna określana jako bliznowiec (keloid) została po raz pierwszy opisana blisko 200 lat temu przez Aliberta (1). Obecnie wiadomo, że bliznowiec to nieswoisty, łagodny rozrost włóknisty skóry występujący najczęściej w następstwie jej uszkodzenia. Klinicznie jest to guzowaty twór o wzmożonej spoistości, gładkiej i lśniącej powierzchni, często z obecnością wypustek przechodzących poza pierwotny obszar uszkodzenia.
EPIDEMIOLOGIA
Częstość występowania bliznowców pozytywnie koreluje z zawartością pigmentu w skórze i u rasy czarnej może sięgać aż 16% (2, 3). Badania nad populacją zamieszkującą Wyspy Hawajskie wykazały, że u osób pochodzenia japońskiego bliznowce były pięciokrotnie częstsze, a u osób wywodzących się z Japonii, trzykrotnie częstsze niż u przedstawicieli rasy białej (4). Co ciekawe, nigdy nie opisano przypadku wystąpienia bliznowca u albinosa.
Bliznowce mogą pojawić się w każdym wieku, ale najczęściej choroba zaczyna się między 10 a 30 rokiem życia (5, 6). Wydaje się, że zmiany występują częściej u kobiet niż u mężczyzn. Być może różnica w zachorowalności między płciami wynika z większej dbałości kobiet o wygląd, a zatem częstszego zgłaszania się ich do lekarza w celu uzyskania porady.
Etiologia choroby nie została dokładnie poznana. Mimo istnienia szeregu czynników predysponujących i prowokujących nie ma jednoznacznej odpowiedzi na pytanie dlaczego tego typu zmiany powstają tylko u niektórych osób.
Bliznowce, podobnie jak i przerosłe blizny, są odbiciem zaburzeń procesu gojenia się ran. Różnicowanie tych dwóch zmian jest ważne, bowiem decyduje o prawidłowym postępowaniu. W przypadku bliznowców proces włóknienia szerzy się poza miejsce pierwotnego uszkodzenia skóry, włókna kolagenu są grube, szkliste, występuje duża ilość mukoidowej substancji międzykomórkowej. Zmiany nie wykazują skłonności do ustępowania. W przerosłych bliznach proces włóknienia ogranicza się tylko do obszaru pierwotnego urazu, występują nieliczne grube włókna kolagenu, jak również niewielka ilość mukoidowej substancji międzykomórkowej. W przeciwieństwie do bliznowców choroba wykazuje tendencję do samoistnej regresji (7).
Ważnym czynnikiem predysponującym do wystąpienia bliznowców jest ciemna karnacja skóry. Prawdopodobnie wiąże się to z wpływem hormonu stymulującego melanocyty (MSH) na metabolizm tkanki łącznej.
Ponad 90% bliznowców pojawia się w pierwszych trzech dekadach życia, co prawdopodobnie wiąże się z faktem, że w tym okresie biosynteza kolagenu jest największa. Ponadto, pojawianiu się zmian sprzyja występujące u młodych ludzi wzmożone napięcie skóry (ryc. 1). Wiadomo bowiem, że bliznowce występują częściej w miejscach cechujących się fizjologicznie wzmożonym napięciem takich jak: okolica pępka, ramiona, mostek, płatki uszne. Często obserwujemy bliznowce indukowane cięciem chirurgicznym poprowadzonym poprzecznie do linii działania sił rozciągających skórę. Najlepszym przykładem działania tego mechanizmu są przypadki choroby występujące po operacjach gruczołu tarczowego.
U osób z wieloogniskowymi zmianami pewną rolę mogą odrywać predyspozycje wrodzone. Wcześniejsze badania wskazywały zarówno na autosomalny dominujący, jak i autosomalny recesywny sposób dziedziczenia choroby (8, 9). Najnowsze opracowanie przyniosło jednak dowody pozwalające stwierdzić, że jakkolwiek większość przypadków choroby nie ma tła genetycznego, to pozostałe dziedziczą się autosomalnie dominująco z niepełną penetracją i ekspresją cech klinicznych (10). Do niedawna nie udało się wykazać związku między wzrostem ryzyka zachorowania a typem antygenów zgodności tkankowej z grup HLA-A i HLA-B. Jednak ostatnie prace wskazują na częstsze występowanie bliznowców u osób z HLA typu B 21, B 16, B 114, BW 35 oraz HLA DR 5 i DQW3.

Ryc. 1. Typowa lokalizacja bliznowca w miejscu wzmożonego napięcia skóry (mężczyzna w wieku 22 lat).
Znaczenie hormonów w etiopatogenezie choroby jest nadal dyskutowane. Niewątpliwie ciąża usposabia zarówno do wystąpienia jak i progresji uprzednio istniejących zmian. Zjawisko to wskazuje na wpływ wysokich stężeń estrogenów we krwi kobiet ciężarnych na rozwój choroby. Za związkiem z układem endokrynnym może również przemawiać zwiększona skłonność do powstawania bliznowców w okresie pokwitania oraz u osób chorych na akromegalię (11, 12).
Czynnikami prowokującymi powstawanie bliznowców są oczywiście urazy skóry. Największe zagrożenie niesie ze sobą oparzenie, uszkodzenie skóry podczas zabiegów chirurgicznych (ryc. 2) oraz zabiegów dermabrazji i szczepień (zwłaszcza BCG) (ryc. 3). Istotną przyczyną powstania zmian są ukąszenia owadów oraz wykonywanie tatuaży. Bliznowce mogą być stanem zejściowym trądziku bliznowaciejącego (ryc. 4, 5, 6), półpaśća, ospy wietrznej, zapalenia mieszków włosowych. W tych ostatnich wymienionych przypadkach mechanizm infekcji odgrywa główną rolę w powstawaniu zmian. Bliznowce mogą także towarzyszyć takim chorobom jak progeria, sklerodermia, osteogenesis imperfecta, zespół Ehlersa-Danlosa, osteopoikilosis i zespół Rubinsteina-Teabi.
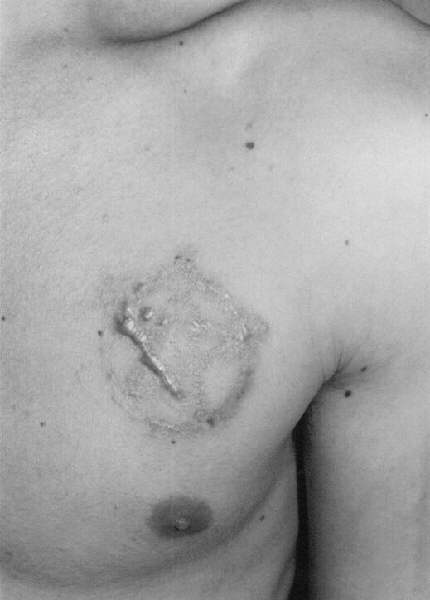
Ryc. 2. Bliznowiec po zabiegu laseroterapii wykonanym w celu usunięcia tatuażu.
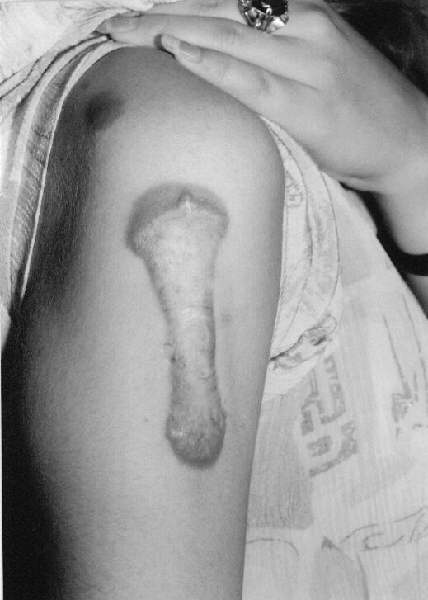
Ryc. 3. Bliznowiec na skórze ramienia powstały po szczepieniu BCG.


Ryc. 4, 5. Bliznowiec jako powikłanie trądzika bliznowaciejącego (mężczyzna w wieku 26 lat).
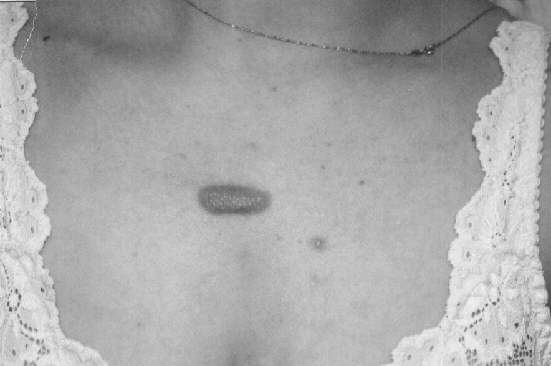
Ryc. 6. Bliznowiec na skórze klatki piersiowej powstały po usunięciu krosty trądzikowej.
Obecnie kwestionuje się występowanie tzw. samoistnych bliznowców, bowiem wiadomo, że zmiany mogą pojawić się nawet po długim czasie od zadziałania czynnika inicjującego proces chorobowy.
W przypadku prawidłowo przebiegającego procesu naprawy uszkodzeń skóry dochodzi do napływu do miejsca urazu makrofagów i granulocytów, a następnie do proliferacji fibroblastów. Fibroblasty są najliczniejszymi komórkami tkanki łącznej. Przypisuje się im podstawową rolę w odnowie innych rodzajów komórek tej tkanki. Komórki te są także odpowiedzialne za produkcję włókien oraz proteoglikanów istoty międzykomórkowej. Fibroblasty zachowują zdolność do podziałów mitotycznych. Podczas gojenia tkanki łącznej zdecydowanie zwiększa się częstość podziałów mitotycznych, wzrasta także synteza kolagenu i neoangiogeneza. Odkładające się włókna kolagenowe tworzą zbitą, ubogokomórkową strukturę zwaną blizną.
Proces ten w bliznowcach jest nieprawidłowy i cechuje się nadmiernym zwiększeniem aktywności fibroblastów oraz zachwianiem równowagi między syntezą a degradacją kolagenu spowodowanym podwyższoną ekspresją genów dla kolagenu typu I i III (13).
Na powstanie bliznowców może mieć wpływ wzrost poziomu siarczanu chondroityny w tkance łącznej. Jest to jeden z siedmiu rodzajów glikozaminoglikanów wchodzących w skład istoty podstawowej. Glikozaminoglikany łączą się z białkami tworząc makrocząsteczki, nazywane proteoglikanami, które wypełniają przestrzenie istoty podstawowej. W bliznowcach siarczan chondroityny jest prawdopodobnie czynnikiem hamującym degradację kolagenu. Dzieje się to poprzez wiązanie proteoglikanu z nowo zsyntetyzowanym kolagenem. Proces ten nie tylko zapoczątkowuje usieciowanie tkanki łącznej w ranie, ale też zabezpiecza białka przed degradacją przez enzymy kolagenolityczne.
a-2 makroglobulina i fibronektyna mogą również odgrywać rolę w etiopatogenezie choroby. Pierwsza z wymienionych substancji inaktywuje enzymy kolagenolityczne, czego skutkiem jest zwiększenie tkankowej zawartości kolagenu. Fibronektyna zaś, może w sposób ciągły pobudzać fibroblasty i w ten sposób przedłużać proces gojenia się rany oraz być przyczyną wzmożonej syntezy włókien kolagenowych. Stężenie fibronektyny w ranie najwyższe wartości osiąga między pierwszą a drugą dobą po urazie (14). W zdrowej skórze stężenie fibronektyny ulega szybkiej normalizacji, zaś w bliznowcu utrzymuje się na podwyższonym poziomie.
W poszukiwaniu mechanizmów patogenetycznych coraz częściej wskazuje się na znaczenie apoptozy, która w prawidłowej skórze ogranicza się do warstwy podstawnej naskórka, zaś w bliznowcach występuje w naskórku i skórze właściwej (15).
Wyniki badań nad zawartością cytokin w tkance bliz-nowca wykazują wzrost stężenia interleukiny-6 (IL-6), czynnika martwicy nowotworów-a (TNF-a), interferonu-b (IFN-b) oraz obniżenie poziomu interferonu-a (IFN-a), interferonu-g (IFN-g) i czynnika martwicy nowotworów-b (TNF-b) (16).
Na podkreślenie zasługują wyniki badań Cobbolda (17), który wykazał zwiększone stężenie tlenku azotu (NO) w wycinkach pobranych z bliznowca. Badacz ten sugeruje również, że źródłem NO będącego aktywnym czynnikiem stymulującym syntezę kolagenu jest warstwa podstawna naskórka.
OBRAZ KLINICZNY CHOROBY
Bliznowiec występuje pod postacią zgrubienia skóry o różnym kształcie i wielkości, często ze smugowatymi wypustkami, które bez wyraźnej granicy przechodzą na otaczającą skórę. Zmiany mają gładką, lśniącą powierzchnię i znacznie wzmożoną spoistość. W początkowej fazie rozwoju zmiana ma zabarwienie czerwone i towarzyszy jej świąd oraz ból. Z upływem czasu, gdy proces aktywnego wzrostu ustaje, bliznowiec staje się twardy, blednie, a objawy podmiotowe choroby zanikają. Bliz-nowiec może pojawić się wszędzie, ale charakterystyczna jest predylekcja zmian do określonych okolic ciała.
OBRAZ HISTOPATOLOGICZNY
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
24 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
59 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
119 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 28 zł
Piśmiennictwo
1. Datubo-Brown D.D: Keloids: a review of the literature. Br. J. of Plast. Surg. 1990, 43:70-77. 2. Kamin A.J.: The etiology of keloids: a review of the literature and a new hypothesis. S. Afr. Med. J. 1964, 38:913-916. 3. Oluwasanmi J.O.: Keloids in the African. Clin. Plast. Surg. 1974, 1:179-195. 4. Alhady S.M., Sivanan Tharajah K.: Keloids in various races: a review of 175 cases. Plast. Reconstr. Surg. 1969; 44:564-566. 5. Cosman B. et al.: The surgical treatment of keloids. Plast. Reconstr. Surg. 1961, 27:335-358. 6. Ketchum L.D. et al.: Hypertrophic scars and keloids: a collective review. Plast. Reconstr. Surg. 1974, 53:140-154. 7. Peacock E.E. Jr et al.: Biologic basis of treatment of keloid and hypertrophic scars. South Med. J. 1970, 63:755-760. 8. Bloom D.: Heredity of keloids: review of the literature and report of a family with multiple keloids for five generations. New York State J. Med. 1956, 56:511-519. 9. Omo-Dare P.: Genetic studies on keloids. J. Natl. Med. Assoc. 1975, 67:428-432. 10. Marneros A.G. et al.: Arch. Dermatol. 2001, 137:1429-1434. 11. Asboe-Hansen G.: Hormonal effects on connective tissue. Am. J. Med. 1959, 26:470. 12. Asboe-Hansen G.: Hypertrophic scars and keloids: etiology pathogenesis, and dermatologic therapy. Dermatologica 1960, 120:178. 13. Zhang L.-Q et al.: Normal and hyperthrophic scars: quantification and localization of messenger RNAs for type I, III and VI collagenes. British J. of Dermatology 1994, 130:453-459. 14. Peacock E.E. Jr.: Inflammation and celluar response to injury. In Wound Healing. 1984. Third edition. Philadelphia: W.B. Saunders. 15. Desmouliere A. et al.: Apoptosis mediates the decrease in cellularity during the transition between granulation tissue and scar. Am. J. Pathol. 1995, 146:56-66. 16. Murray J.C., Pinnel S.R.: Keloids and excessive dermal scarring. W: Kelman Cohen I., Diegelmann R.F., Lindblad W.J., red. Wound Healing-Biochemical and Clinical Aspects. Philadelphia: W.B. Saunders 1992, 500-509. 17. Cobbold C.A.: The role of nitric oxide in the formation of keloid and hypertrophic lesions. Med. Hypotheses 2001, 57:497-502. 18. Maguire H.C.: Treatment of keloids with triamcinolone acetonide injected intralesionally. JAMA 1965, 192:325-327. 19. Shons A.R., Press B.H.J.: The treatment of earlobe keloids by surgical excision and postoperative triamcinolone injection. Ann. Plast. Surg. 1983, 10:480-482. 20. Lawrence W.T.: In search of the optimal treatment of keloids: report of a series and a review of the literature. Ann. Plast. Surg. 1991, 27:164-178. 21. Mayou B.J.: D-Penicillamine in the treatment of keloids. Br. J. of Dermatol. 1981, 105:87-89. 22. Janssen de Limpens A.M.: The local treatment of hypertrophic scars and keloids with topical retinioc acid. Br. J. of Dermatol. 1980, 103:319. 23. Chiu H.C. et al.: Effects of dextran sulphate on the growth of cultured fibroblasts derived from normal human skin and keloid lesions. J. of the Formosan Med. Assoc. 1987, 86:264. 24. Bosse J.P. et al.: Clinical study of a new antikeloid agent. Ann. of Plastic Surg. 1979, 3:13. 25. Granstein R.D. et al.: A controlled trial of intralesional recombinant interferon-gamma in the treatment of keloidal scaring. Arch. Dermatol. 1990, 116:1159-62. 26. Mercer N.S.G.: Silicone gel in the treatment of keloid scars. Br. J. Plast. Surg. 1989, 42:83-87. 27. Ahn S.T. et al.: Topical silicone gel for prevention and treatment of hypertrophic scar. Arch. Surg. 1991, 126:499-504. 28. Berman B., Flores F.: The treatment of hypertrophic scars and keloids. Eur. J. Dermatol. 1998, 8:591-595. 29. Cosman B., Wolff M.: Correlation of keloid recurrence with completeness of local excision. Plast. Reconstr. Surg. 1972, 50:163-165. 30. DaCosta J.C.: Modern Surgery. Philadelphia: W.B. Saunders, 1903. 31. Berman B., Flores F.: The treatment of hypertrophic scars and keloids. Eur. J. Dermatol. 1998, 8:591-595. 32. Espana A. et al.: Bleomycin in the treatment of keloids and hypertrophic scars by multiple needle punctures. Dermatol. Surg. 2001, 27:23-27.






