Stanisław Zabielski1, Marek Antiszko1, Alicja Rączka2, Jan Lach3
Zastosowanie testu HYBRID CAPTURE SYSTEM II w diagnostyce skąpo- i bezobjawowych zapaleń cewki moczowej (NGU) o etiologii Chlamydialnej
The use of the HYBRID CAPTURE SYSTEM II test in the diagnosis of mildly manifested and asymptomatic urethritis (NGU) caused by Chlamydia
1 z Kliniki Dermatologicznej Centralnego Szpitala Klinicznego Wojskowej Akademii Medycznej
im. gen. dyw. B. Szareckiego w Warszawie
Kierownik Kliniki: płk prof. dr hab. med. Stanisław Zabielski
2 z Zakładu Diagnostyki Laboratoryjnej Centralnego Szpitala Klinicznego Wojskowej
Akademii Medycznej im. gen. dyw. B. Szareckiego w Warszawie
Kierownik Zakładu: płk dr hab. med. Wiesław Piechota
3 z Zakładu Higieny i Ekologii Wojskowego Instytutu Higieny i Epidemiologii
im. gen. K. Kaczkowskiego w Warszawie
Kierownik Zakładu: płk prof. dr hab. Jerzy Bzdęga
Streszczenie
Summary
Screening tests have been carried out in a group of young men using the Hybrid Capture System II method.The usefulness of this method was demonstrated in diagnosing infections caused by Chlamydia trachomatis, especially while the disease is mildly manifested or asymptomatic.

Nierzeżączkowym zapaleniem cewki moczowej (NGU) określamy zapalenie cewki moczowej bez mikroskopowych cech zapalenia rzeżączkowego. Schorzenie ma charakter polietiologiczny i może być wywoływane przez bakterie, wirusy, pierwotniaki i grzyby (5, 7).
W wielu przypadkach nie udaje się ustalić czynnika przyczynowego zakażenia. Trudności diagnostyczne spowodowane są niejednokrotnie brakiem odpowiedniego sprzętu i zaplecza diagnostycznego. Często pomijane są pierwsze symptomy choroby i rozpoczęcie diagnostyki następuje w okresie poważnych powikłań, które są następstwem pierwotnego, bezobjawowego lub skąpoobjawowego zakażenia (4, 6, 14, 20, 21).
Głównym czynnikiem patogennym tej choroby jest bakteria Chlamydia trachomatis, która jest odpowiedzialna za 23-55% ogółu zakażeń. Odsetek zakażeń obniża się do 19-31% przy wykorzystaniu w diagnostyce testów o większej czułości wykrywających materiał genetyczny drobnoustrojów w badanej próbce (4, 6, 7).
Odsetek bezobjawowych infekcji układu moczowego wywoływanych przez chlamydie może przekraczać 25% u mężczyzn, a u kobiet z zakażeniem w obrębie szyjki macicy nawet do 76% (24, 25).
Jest to ważne z epidemiologicznego punktu widzenia, ponieważ chorzy ci nie odczuwając objawów chorobowych są źródłem zakażenia swoich partnerów z najbliższego otoczenia (3).
Wpływ na stopień rozprzestrzeniania się choroby, zwłaszcza wśród ludzi młodych o największej aktywności seksualnej, ma również kilkakrotnie dłuższy okres inkubacji niż w rzeżączce, który wynosi od 3 do 7 tygodni (25).
W fazie przewlekłego zakażenia może dochodzić do poważnych powikłań ze strony układów: moczowo-płciowego, krążenia, oddechowego, narządu wzroku oraz zaburzeń ogólnoustrojowych (17).
Najczęstszymi powikłaniami NGU u mężczyzn są: zapalenie jąder i najądrzy, zapalenie gruczołu krokowego, leukocytospermia, niepłodność, zapalenie spojówek, zespół Behceta, Reitera – z zapaleniem dużych stawów kończyn oraz kręgosłupa, ostrym zapaleniem stawu krzyżowo-biodrowego, zapaleniem błony naczyniowej oczu oraz przyczepów ścięgien (5, 25).
U kobiet obserwuje się najczęściej wstępujące zakażenie dróg moczowo-płciowych z zapaleniem kanału szyjki macicy, ciąże pozamaciczne, niepłodność, poronienia i trudności z donoszeniem ciąży (5, 8, 13, 25).
Dyskutowana jest rola chlamydii jako kofaktora w rozwoju raka szyjki macicy wspólnie z zakażeniem onkogennymi wirusami HPV oraz w rozwoju raka jajnika (23).
Ze strony układu krążenia może wystąpić zapalenie aorty, niedomykalność zastawki aorty, zapalenie osierdzia, zaburzenia przewodnictwa i nasilenie zmian miażdżycowych. W przypadku powikłań dotyczących układu pokarmowego obserwowano: zapalenie błony śluzowej odbytu, zespół Fitz Huga Curtisa z zajęciem tkanki okołowątrobowej z możliwością wytworzenia ropni, a także zajęcie innych narządów miąższowych np. śledziony oraz nerek (25).
Do zakażenia noworodków szczepami okulogenitalnymi dochodzi w czasie akcji porodowej od chorych matek, które mogą spowodować zapalenie spojówek, płuc, a nawet choroby przewodu pokarmowego. Zakażenie okołoporodowe przyczynia się również do wzrostu śmiertelności noworodków na co zwracają uwagę liczni autorzy (12, 16, 25).
W odpowiedzi na antygeny Chlamydia trachomatis może dojść do produkcji cytokin i aktywacji systemu immunologicznego oraz wystąpienia zmian skórnych o charakterze naczyniowym (leukoklastyczne zapalenie naczyń) (1, 18).
Biorąc pod uwagę liczbę oraz różnorodność możliwych, poważnych powikłań wynikających ze skąpoobjawowego przebiegu zakażenia, przeprowadzono badania przesiewowe w wybranym środowisku podwyższonego ryzyka jakim są młodzi mężczyźni odbywający służbę wojskową.
Za cele badań przyjęto:
– Ocenę częstości występowania zakażeń cewki moczowej Chlamydia trachomatis oraz współistnienia zakażenia dwoinką rzeżączki u młodych mężczyzn.
– Przypadkowość wykrycia i skuteczność wybranej metody w skąpoobjawowym okresie schorzenia.
MATERIAŁ I METODY
Badania przeprowadzone zostały na jednorodnym pod względem wieku, płci i warunków bytowych materiale klinicznym, co stworzyło porównywalną grupę badanych. Grupę badaną stanowiło 500 żołnierzy zasadniczej służby wojskowej w wieku 19-25 lat (przedział wiekowy badanych związany jest ze szczytem zachorowań na NGU) z klinicznymi objawami zakażenia układu moczowego: (objawy dysuryczne, ból i dyskomfort w obrębie miednicy, zespół cewkowy, częstomocz) oraz bez uchwytnych objawów klinicznych zakażenia układu moczowego. Średnia wieku badanych wynosiła 21 lat. Byli to w większości młodzi mężczyźni prowadzący aktywne, często nieustabilizowane życie płciowe.
U wszystkich badanych przeprowadzono badanie podmiotowe i przedmiotowe, ponadto pobrano próbki moczu oraz wymazy z cewki moczowej do badań laboratoryjnych.
Wywiad obejmował:
1. Dane ogólne (dane personalne, stan cywilny, wykształcenie, zawód oraz dane środowiskowe).
2. Wywiad chorobowy uwzględniający inne choroby układu moczowo-płciowego, dotychczasowe leczenie farmakologiczne i operacyjne.
3. Główne dolegliwości ze strony układu moczowo-płciowego oraz objawy towarzyszące ze strony innych narządów i układów.
4. Wywiad seksuologiczny w celu wykrycia ewentualnych źródeł zakażenia, dotychczasowych kontaktów, orientacji seksualnej i stosowanych metod antykoncepcji.
Badanie fizykalne obejmowało ocenę zewnętrznych narządów płciowych i charakter wydzieliny z cewki moczowej.
Wymaz z cewki moczowej pobierano przy pomocy zestawu Digene Sampler i umieszczano w podłożu transportowym (Specimen Transport Medium). Próbki umiesz-czano w lodówce w temperaturze 4°C.
Próbki moczu o objętości 20-30 ml pobierano do jałowych pojemników z hermetycznym zamknięciem. Próbkę stanowiła pierwsza porcja moczu po nocnej przerwie. Każdy badany był poinformowany o konieczności nie oddawania moczu przynajmniej godzinę przed badaniem. Próbki moczu i wymazy transportowano w warunkach chłodniczych w temperaturze 2-8°C do laboratorium. Materiał opracowywany był w ciągu 4 dni (mocz) i 7 dni (wymazy). Pozostałe próbki zamrażano do czasu wykonania badań w temp. -20°C.
Test hybrid capture system II wykonywano w pracowni specjalistycznej z zachowaniem reżimu dekontaminacyjnego, przy użyciu rękawiczek bezpudrowych w celu uniknięcia zanieczyszczeń pyłem i kurzem. Test wykonywano w temperaturze otoczenia 20-25°C. Przed wykonaniem testu wszystkie próbki i odczynniki pozostawiano do ogrzania w temperaturze pokojowej 20-25°C i mieszano. Pierwszym etapem testu była denaturacja próbek. (Denaturacja DNA w badanych próbkach przy użyciu odczynnika denaturującego – Denaturation Reagent, którym był roztwór zasady sodowej).
Przygotowywano odczynnik denaturujący, a kalibratory i próbki umieszczano w statywach do prób. Kolejno dodawano odczynnik denaturujący do każdej próbki badanej oraz do kalibratorów pozytywnych i negatywnych. Kontrolę ujemną (Negative Calibrator) stanowił nośnik DNA w płynnym podłożu transportowym z azydkiem sodu. Kontrolę dodatnią CT/GC (CT/GC Positive Calibrator) stanowiło sklonowane CT/GC DNA (1,0 pg/ml) na nośniku DNA w płynnym podłożu transportowym. Następnie wszystkie próbki i kalibratory mieszano na worteksie minimum 5 sekund na najwyższej prędkości (kolor kalibratorów i prób powinien zmienić się na ciemnopurpurowy) i inkubowano w łaźni wodnej w temp. 65 ± 2°C przez 45 ± 5 min. W czasie inkubacji i denaturacji próbek przygotowywano sondę Probe Mix (CT/GC Probe) – jest to zbuforowany roztwór zawierający komplementarne RNA CT/GC.
Drugim etapem testu była hybrydyzacja. Do każdej probówki hybrydyzacyjnej dodawano po 25 ml Probe Mix. Po wymieszaniu próbek i kalibratorów na worteksie przenoszono po 75 ml ich zawartości do odpowiednio oznaczonych probówek hybrydyzacyjnych używając 4-kanałowej pipety EXPAND-4. Próbki zakrywano naklejką i mieszano na wytrząsarce w 1100 ± 100 rpm przez 2-3 min. (kolor wszystkich prób powinien zmienić się na żółty). Następnie próbki poddawano inkubacji w łaźni wodnej przez 60 ± 5 min. w temperaturze 65 ± 2°C.
Po przygotowaniu mikropłytek (Capture Mikroplate – 96-dołkowa mikropłytka opłaszczona przeciwciałami dla hybryd RNA:DNA) i luminometru rozpoczęto etap opłaszczania. Opłaszczanie – (powstałe hybrydy RNA:DNA wychwytywane są przez specyficzne dla hybryd RNA:DNA przeciwciała opłaszczone na ściankach mikrodołków). W tym celu przenoszono dokładnie całą zawartość każdej probówki hybrydyzacyjnej do odpowiedniego dołka mikropłytki, używając do tego celu pipety 8- kanałowej Titerman. Zakrywano płytkę naklejką, a następnie mieszano na wytrząsarce w 1100 ± 100 rpm w temp. 20-25°C przez 60 ± 5 min. W tym czasie przygotowywano bufor płuczący – Wash Buffer. Po zakończeniu mieszania wylewano zawartość mikropłytki i osuszano ją na bibule absorpcyjnej.
Kolejnym etapem testu było wykrywanie (reakcja immobilizowanych hybryd na ściankach dołków z alkaliczną fosfatazą skoniugowaną ze specyficznymi dla hybryd RNA:DNA przeciwciałami i wykrywanie chemiluminescencyjnym substratem). W tym celu do każdego dołka mikropłytki dodawano po 75 m odczynnika detekcyjnego 1 (Detection Reagent 1). Następnie zakrywano mikropłytkę parafilmem i inkubowano w 20-25°C przez 30 ± 3 min.
Następnie wylewano zawartość mikropłytki, osuszano na bibule i przechodzono do kolejnego etapu – płukania. Po osuszeniu mikropłytki płukano każdy dołek sześciokrotnie i osuszano ją na papierze absorpcyjnym przez 5 minut.
Kolejnym etapem testu było generowanie sygnału. W tym celu dodawano po 75 ml odczynnika detekcyjnego 2 (Detection Reagent 2) do każdego dołka mikropłytki a następnie poddawano ją inkubacji w temperaturze 20-25°C przez 15 minut.
Ostatnim etapem testu był odczyt mikropłytki w luminometrze oraz walidacja testu i interpretacja wyników badania. W przypadku potwierdzenia zakażenia testem Digene CT/GC Test (test hybrydyzacji Ch. trachomatis/ /N. gonorrhoeae) wykonywany był test hybrydyzacji DNA w kierunku Ch. trachomatis (Digene CT – ID Test) – potwierdzający wynik dodatni lub test hybrydyzacji N. gonorrhoeae (Digene GC – ID Test) – potwierdzający obecność DNA Neiseria gonorrhoeae.
WYNIKI
Przeprowadzone badania wykazały obecność Chlamydia trachomatis u 24/500 (4,8%) badanych (ryc. 1). W badanej grupie nie stwierdzono zakażeń Neisseria gonorrhoeae.
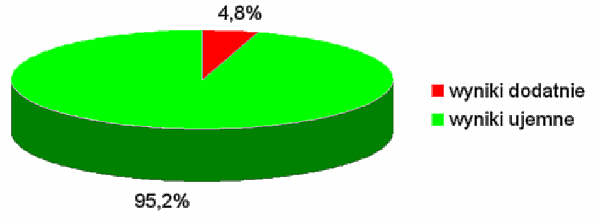
Ryc. 1. Badania laboratoryjne: liczba zakażonych Chlamydia trachomatis ogółem, N= 500.
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
24 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
59 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
119 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 28 zł
Piśmiennictwo
1. Betsou F. et al.: Serological investigation of Chlamydia trachomatis heat shock protein 10. Infect. Immun. 1999, 67:10:5243-5246. 2. Brodine S.K. et al.: Asymptomatic sexually transmitted disease prevalence in four military populations: application of DNA amplification assays for Chlamydia and gonorrhea screening. J. Infect. Dis. 1998, 178, 4:1202-1204. 3. Catry M.A. et al.: Comparison of the Amplicor Chlamydia trachomatis test and cell culture for the detection of urogenital Chlamydial infections. Genitourin. Med. 1995, 71:247-250. 4. Cohen D.A. et al.: A school-based Chlamydia control program using DNA amplification technology. Pediatrics. 1998, 101:1. 5. Dajek Z.: Przenoszone drogą płciową zakażenia cewki moczowej i narządu rodnego. Dermatologia – Nowości. 2000, 18:7-10. 6. Deguchi T. et al.: Comparison among performances of a ligase chain reaction-based assay and two enzyme immunoassays in detecting Chlamydia trachomatis in urine specimens from men with nongonococcal urethritis. J. Clin. Microbiol. 1996, 34, 7:1708-1710. 7. Erbelding E.J., Quinn T.C.: Urethritis treatment. Dermatol. Clin. 1998 Oct. 16, 4:735-738. 8. Gaydos C.A. et al.: Chlamydia trachomatis infections in female military recruits. N. Engl. J. Med. 1998, 10, 339(11):739-744. 9. Gaydos C.A. et al.: Use of ligase chain reaction with urine versus cervical culture for detection of Chlamydia trachomatis in an asymptomatic military population of pregnant and nonpregnant females attending Papanicolaou smear clinics. J. Clin. Microbiol. 1998, 36, 5:1300-1304. 10. Girdner J.L. et al.: Evaluation of the digene hybrid capture II CT-ID test for detection of Chlamydia trachomatis in endocervical specimens. J. Clin. Microbiol. 1999, 37, 5:1579-1581. 11. Howell M.R. et al.: Control of Chlamydia trachomatis infections in female army recruits: cost-effective screening and treatment in training cohorts to prevent pelvic inflammatory disease. Sex. Transm. Dis. 1999, 26, 9:519-526. 12. Iskandar N.M., Naquib M.B.: Chlamydia trachomatis: an underestimated cause for rhinitis in neonates. Int. J. Pediatr. Otorhinolaryngol. 1998, 42:233-237. 13. Leng Z. et al.: Characterization of ciliary activity in distal Fallopian tube biopsies of women with obstructive tubal infertility. Hum. Reprod. 1998, 13, 11:3121-3127. 14. Mardh P.A. et al.: Symptoms and signs in single and mixed genital infections. Int. J. Gynaecol. Obstet. 1998, 63, 2:145-152. 15. Modarress K.J. et al.: Detection of Chlamydia trachomatis and Neisseria gonorrhoeae in swab specimens by the Hybrid Capture II and PACE 2 nucleic acid probe tests. Sex. Transm. Dis. 1999, 26, 5:303-308. 16. Mouton J. et al.: Detection of Chlamydia trachomatis in male and female urine specimens by using the Amolified Chlamydia trachomatis Test. J. Clin. Microbiol.1997, 35, 6:1369-1372. 17. Quinn T.C. et al.: Epidemiologic and microbiologic correlates of Chlamydia trachomatis infection in sexual partnerships. JAMA. 1996, 276, 21:1737-1742. 18. Rasmussen S. et al.: Secretion of proinflammatory cytokines by epithelial cells in response to Chlamydia infection suggests a central role for epithelial cells in Chlamydial pathogenesis. J. Clin. Invest. 1997, 99:77-87. 19. Schachter J. et al.: Ability of the digene hybrid capture II test to identify Chlamydia trachomatis and Neisseria gonorrhoeae in cervical specimens. J. Clin. Microbiol. 1999, 37, 11:3668-3671. 20. Schepetiuk S. et al.: Detection of Chlamydia trachomatis in urine samples by nucleic acid tests: comparison with culture and enzyme immunoassay of genital swab specimens. J. Clin. Microbiol.1997, 35, 12:3355-3357. 21. Stary A.: Urethritis. Diagnosis of nongonococcal urethritis. Dermatol. Clin. 1998, 16, 4:723-726. 22. Stephenson J.M.: Screening for genital Chlamydial infection. Br. Med. Bull. 1998, 54, 4:891-902. 23. Takac I., Gorisek B.: Chlamydia trachomatis infection in women with and without cervical intraepithelial neoplasia. Int. J. STD. AIDS. 1999, 10, 5:331-333. 24. Vuylsteke B. et al.: Chlamydia trachomatis prevalence and sexual behaviour among female adolescents in Belgium. Sex. Transm. Infect. 1999, 75, 3:152-155. 25. Żak-Prelich M. et al.: Kliniczny obraz zakażeń układu moczowo-płciowego wywołanych przez Chlamydia trachomatis. Nowa Medycyna 1997, 6-11.

