Katarzyna Zbarańska1, Małgorzata Tomczyk2, Grażyna Chodorowska3
Rogowiak kolczystokomórkowy
Kerathoacanthoma
1z Wojewódzkiej Poradni Skórno-Wenerologicznej Samodzielnego Publicznego Zakładu Opieki Zdrowotnej w Lublinie
2 z Oddziału Dermatologii Samodzielnego Publicznego Zakładu Opieki Zdrowotnej w Puławach
3 z Katedry i Kliniki Dermatologii, Wenerologii i Dermatologii Dziecięcej Akademii Medycznej w Lublinie
prof. nadzwyczajny, dr hab. n. med. Grażyna Chodorowska
Streszczenie
Summary
Kerathoacanthoma is a common benign squamosus neoplasm that is characterised by rapid growth and spontaneus involution. These lesions usually present as solitary, dome-shaped, skin-coloured papules with a central keratinous core descriptively referred to as a „volcano”. The cause of keratoacanthoma is unclear; however, suspected causes include ultraviolet light, genetic factors, immunosupresion, chemical carcinogens, viruses and trauma.

WSTĘP
Rogowiak kolczystokomórkowy (keratoacanthoma, K.A.) został opisany w 1889 roku przez Jonathana Hutchinsona jako „crateiform ulcer of face”, natomiast samego terminu „keratoacanthoma” użył po raz pierwszy Frendenthal (14, 24) w 1936 roku. W piśmiennictwie światowym stosowano wiele synonimów określających tą zmianę chorobową, takich jak np.: acanthokeratoma, molluscum sebaceum, molluscum pseudocarcinomatosum, verrucoma, „self-healing carcinoma of squamosus cells” (14, 15).
DEFINICJA
K.A. jest przykładem rozrostu rzekomonowotworowego, histologicznie i klinicznie podobnego do raka kolczystokomórkowego. Jest stanem łagodnym, samoograniczającym się, cechującym się szybkim wzrostem i tendencją do samoistnego ustępowania. Jego etiologia nie jest do końca poznana.
EPIDEMIOLOGIA
W USA badania dotyczące białej populacji Hawajów podawały występowanie średnio 104 przypadków K.A. na 100 tys. osób (2). Szacowały one także stosunek ilościowy K.A. do raka kolczystokomórkowego (SCC) jak 1:1, w przeciwieństwie do innych źródeł, gdzie wynosił on 1:3 (14). Wśród chorych przeważają mężczyźni.
Występuje w każdym wieku, a szczyt zachorowań przypada na 50-69 rok życia (6).
ETIOLOGIA
Etiologia K.A. nie jest do końca poznana. Wymienianych jest kilka czynników ryzyka (14):
- przewlekła ekspozycja na promieniowanie UV, czego dowodem jest częstsze występowanie w obrębie odkrytych części ciała,
- PUVA – terapia (18),
- zawodowe narażenie na kontakt z dziegciami i produktami smołowcowymi, w szczególności z sumującym się wpływem nasłonecznienia (13, 21),
- przypadkowe i zawodowe urazy (18), oparzenia oraz pobieranie przeszczepów skóry (22),
- wirusy brodawczaka ludzkiego (7,16), zwłaszcza podtyp HPV-26, HPV-37,
- czynniki genetyczne (18),
- wiek,
- zaburzenia immunologiczne (23), immunosupresja pozakaźna i polekowa (5).
Jednak przypadki rozwoju K.A. w obrębie zakrytych obszarów skóry oraz błon śluzowych, a także występowanie tej choroby w młodym wieku zdają się dowodzić, że żaden z tych czynników nie ma roli decydującej.
Dyskutowany jest związek K.A. z SCC. Jako ogniwo łączące podawany jest tzw. samogojący się mnogi rak skóry (multiple self- healing primary scc). Za powiązaniem etiopatogenetycznym tych chorób przemawia również podobna grupa czynników ryzyka oraz możliwe przekształcanie się K.A. w SCC, zwłaszcza w przypadku przedłużającego się narażenia na te czynniki (14).
OBRAZ KLINICZNY
K.A. występuje najczęściej w postaci pojedynczego, kopulastego guzka o wzmożonej spoistości osiągającego średnicę do około 1-2 cm. Ma on zazwyczaj barwę skóry prawidłowej lub perłową, przeświecającą. W części środkowej znajduje się kraterowate zagłębienie wypełnione masami rogowymi, które czasem zostają wydalone, co powoduje wytworzenie krwistego strupa. Skóra otaczająca wykwit jest niezmieniona. Subiektywnie może być odczuwany lekki świąd (9).
Przebieg można podzielić na trzy fazy (1,14)
- faza wzrostu – 2-12 tygodni,
- faza stacjonarna – 2-8 tygodni,
- faza regresji – 4-8 miesięcy.
Guzki K.A. ustępują najczęściej z pozostawieniem powierzchownej blizny. Opisano również przypadki, kiedy zmiany szerzyły się w ciągu wielu lat cofając się z następowym rozległym bliznowaceniem.
Wykwity umiejscowione są najczęściej na głowie (52%), głównie na nosie, wargach, małżowinach usznych, na kończynach górnych (36%), głównie na grzbietach rąk, rzadziej w innych okolicach ciała, np.: na kończynach dolnych (6,5%), tułowiu (5,5%), a także na błonach śluzowych jamy ustnej, w okolicach narządów płciowych, na spojówkach oka. Cechą charakterystyczną jest powstawanie wykwitów na skórze niezmienionej, a nie w obrębie stanów przedrakowych (ryc. 1).
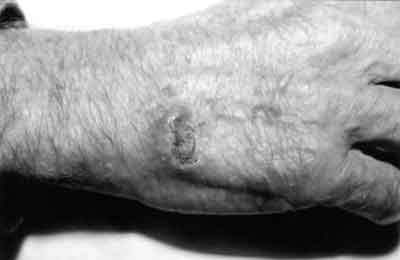
Ryc. 1.
ODMIANY
Obecnie wyróżnia się tzw. pojedynczy K.A. (solitary K.A.) oraz postać mnogą, wysiewną (generalised K.A.) (14).
Kliniczne warianty pojedynczego K.A.(14):
- keratoacanthoma crateriforme (K.A. crater-like) – najczęstsza, typowa postać z widocznym zwykle czopem rogowym w centrum ogniska,
- keratoacanthoma, postać tarczkowata – postać płaska ze słabo zaznaczonym rogowaceniem,
- keratoacanthoma giganteum, (giant form K.A.) – cechuje się dużymi rozmiarami powyżej 3 cm, ciągłym wzrostem i brakiem tendencji do regresji. Występuje najczęściej na twarzy, a zwłaszcza na nosie oraz na grzbietach rąk,
- keratoacanthoma centrifugum marginatum (centrifugal marginal K.A., multinodular K.A.) – rzadka odmiana charakteryzująca się martwicą a następnie zanikiem w części środkowej, występowaniem guzków na obwodzie oraz szybkim początkiem i powolnym szerzeniem się . Może osiągać średnicę do 20 cm (17, 23),
- keratoacanthoma aggregatum – w sąsiedztwie ogniska obserwuje się rozwój nowych wykwitów,
- -keratoacanthoma subunguale – rzadka, zazwyczaj bolesna i powodująca dużą destrukcję postać. Zajmuje tkanki pod dystalną częścią płytki paznokciowej lub proksymalny wał paznokciowy. W odróżnieniu od typowego K.A. rozwija się w skórze pozbawionej mieszków włosowych. Naciekanie kości i perforacja tkanek jest dość częsta. Spontaniczna regresja jest rzadko spotykana,
- keratoacanthoma mucosae (K.A. mucosal) – rzadka odmiana spotykana na błonach śluzowych jamy ustnej i spojówkach oka. Tak jak poprzednia nie ma związku z mieszkami włosowymi oraz tendencji do samoistnego ustępowania,
- keratoacanthoma perianale et genitale – rzadko opisywana postać występująca na błonach śluzowych narządów płciowych i w okolicy odbytu.
Kliniczne warianty mnogich K.A. (12,14):
- Typ Ferguson-Smith (10) – opisany w 1934 roku jako tzw. samoistnie gojące się raki kolczystokomórkowe. Wykwity podobne są do typowych dla odmiany pojedynczej. Powstają w dzieciństwie, okresie dojrzewania lub wczesnej młodości, następnie tworzą się kolejne po jednym lub kilka w danym okresie czasu przez wiele lat. Średni wiek pojawiania się zmian to 25-27 lat. Zajmują głównie miejsca eksponowane na promieniowanie UV, ale mogą także występować na skórze osłoniętej, błonach śluzowych i w miejscach urazów. Goją się samoistnie z pozostawieniem zanikowej blizny. Jest to prawdopodobnie odmiana o dziedziczeniu autosomalnym dominującym.
- Typ Grzybowskiego – są to uogólnione, wysiewne, występujące w liczbie setek a nawet tysięcy (16), drobne wykwity o średnicy 2-3 mm. Mogą występować na dłoniach, podeszwach, błonach śluzowych i innych obszarach skóry (1). Pojawiają się w wieku dojrzałym, mają tendencję do zlewania się i koebneryzacji. Wysiewom często towarzyszy świąd. Odmiana ta nie ma podłoża genetycznego. Może być związana z zawodowym narażeniem na chemiczne czynniki karcynogenne (oleje, smary, dziegcie) i zakażeniem wirusem HPV.
- Typ Witten-Zak – to rzadki rodzinny zespół, który łączy cechy obu powyższych wariantów tzn. jednocześnie występują drobne wysiewne zmiany i duże wykwity guzkowe.
- Typ multiplex persistans – rzadko opisywana odmiana występująca u osób dorosłych na dłoniach, spojówkach oka i prąciu. Wykwity są nieliczne, rozwijają się i ustępują powoli.
- Typ wtórny – powstaje w miejscach urazów, czasem w bliznach po uprzednio wyciętych K.A. Włącza się do tej odmiany także zmiany powstające w miejscach po wygojonym półpaścu, w wykwitach lichen planus hypertrophicus, DLE, łuszczycy, epidermolysis bullosa dystrophica i innych stanów zapalnych.
- Typ związany z zespołami chorobowymi (syndroma related) – spotykany jest w zespole Muir-Torre, gdzie typowym wykwitom K.A. towarzyszą mnogie guzy gruczołów łojowych i nowotwory przewodu pokarmowego lub moczopłciowego. Występuje rodzinnie i jest dziedziczony w sposób autosomalny dominujący (17). Poza tym wariant ten może towarzyszyć xeroderma pigmentosum i znamionom łojowym Jadachssona.
HISTOGENEZA
K.A. wywodzi się z mieszków włosowych, a bujanie sopli naskórkowych zaczyna się w zewnętrznej pochewce włosa nad ujściem gruczołu łojowego lub w obrębie samego gruczołu. Samoistne ustępowanie może mieć związek z cyklem rozwojowym włosa lub dojrzewaniem komórek w obrębie czopa rogowego (9). Zmiany rozwijają się w obrębie skóry niezmienionej a nie na bazie stanu przedrakowego (9, 14).
OBRAZ HISTOPATOLOGICZNY
W obrazie histopatologicznym zaznaczona jest akantoza z hyperkeratozą i niewielką parakeratozą. We wczesnych zmianach widoczna jest atypia i figury mitotyczne u podstawy wykwitu. Komórki w centrum guza mają szklisty wygląd (24). Stwierdza się obecność centralnie położonego czopa rogowego wklinowanego w podścielisko łącznotkankowe i otoczonego żywym naskórkiem. Charakterystyczna jest obecność w partiach brzeżnych tzw. daszka (wargi) z uciskanego od wewnątrz prawidłowego naskórka. Nacieki zapalne wokół wykwitu są niewielkie, w fazie wzrostu zdominowane przez histiocyty, w fazie dojrzałości neutrofile, limfocyty i plazmocyty a w fazie regresji przez przez napływające do podścieliska monocyty. W obrazie histologicznym obserwuje się również mikroropnie, gniazdka dyskeratotyczne i kwasochłonne wybarwianie się keratyny. Dla fazy regresji charakterystyczny jest odczyn ziarninowy z następowym włóknieniem (14). Typowe jest zachowanie integralności błony podstawnej naskórka i nie przekraczanie granicy przydatków skóry oraz brak naciekania naczyń i nerwów (24).
DIAGNOSTYKA RóŻNICOWA
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
24 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
59 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
119 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 28 zł
Piśmiennictwo
1. Chorzelski T.P. i wsp.: Keratoacanthoma Multiplex - Varietas Grzybowski. Dalsza siedmioletnia obserwacja chorego w pełni potwierdza koncepcję autora. Przegląd Dermatologiczny. 1995, 5:405-411. 2.Chuang T. Y.: Keratoacanthoma in Kauai, Hawaii. The first documented incidence in a defined population. Arch. Dermatol. 1993, 129(3):317-319. 3.Dendorfer M. et al.: Topical treatment with imiquimod may induce regression of facial keratoacanthoma. Eur. J. Dermatol. 2003, 13:80-82. 4.Donaldson M. J.: Periocular keratoacanthoma. Ophtalmology. 2003, Vol. 110, nr 7:1403-1407. 5.Esser A.C. et. al.: Acute development of multiple keratoacanthomas and squamosus cell carcinomas after treatment with infliximab. J. Am. Acad. Dermatol. 2004, Vol. 50, nr 5:75-77. 6.Gilbey S. et. al.: Vulvar keratoacanthoma. Obstetrics&Gynecology. 1997,Vol.89, nr 5, Part 2:848-850. 7.Grob J.J. et. al.: Large keratoacanthomas treated with intralesional interferon alfa -2a. J. Acad. Dermatol. 1993, 29:237-241. 8.Hurst L. N.: Intralesional methotrexate in keratoacanthoma of the nose. British Journal of plastic surgery. 1995, 48:243-246. 9.Jabłońska S.: Choroby skóry. 1980, t.II:830-833. 10.Kato N. et al.: Ferguson Smith type multiple keratoacanthomas and a keratoacanthoma centrifugum marginatum in a woman from Japan. J. Am. Acad. Dermatol. 2003, Vol. 49, nr 4:741-746. 11.Kawczyk-Krupka A. i wsp.: Rola diagnostyki i terapii fotodynamicznej w stanach przednowotworowych i nowotworowych jamy ustnej. Magazyn Stomatologiczny. 2000, 10:27-29. 12.Kaźmierowski M., Bowszyc-Dmochowska M.: Skojarzone leczenie kriochirurgiczne i retinoidami chorego z licznymi keratoacanthoma. Postępy Dermatologii. 1997, 14:397-402. 13.Letzel S., Drexler H.: Occupationally related tumors in tar refiner workers. J. Am. Acad. Dermatol. 1998, 39:712-720. 14.Miedziński F.: Rogowiak kolczystokomórkowy w ujęciu patogenetycznym i kliniczno-histologicznym, jego 40-letnia rocznica. Postępy dermatologii 1990, 7:61-70. 15.Miedziński F.: Dermatologia. 1982, t.II:690-693. 16.Norgauer J. et. al.: Human papillomavirus and Grzybowski"s generalized eruptive keratoacanthoma. J. Am. Acad. Dermatol. Vol. 49, nr 4:771-772. 17.Ogasawara Y. et. al.: A case of multiple keratoacanthoma centrifugum marginatum:Response to oral etretinate. J. Am. Acad. Dermatol. 2003, Vol. 48, nr 2:282-285. 18.Patttee S.F., Silvis N.G.: Keratoacanthoma developing in sities of previous trauma: A report of two cases and review of the literature. J. Am. Acad. Dermatol. 2003, Vol. 48, nr 2:35-38. 19.Sanders S. et. al.: Intralesional corticosteroid treatment of multiple eruptive keratoacanthomas: case report and review of a controversial therapy. Dermat. Surg. 2002, 28:954-958. 20.Sayama S., Tagami H.: Treatment of keratoacanthoma with intralesional bleomycin. Br. J. Dermatol. 1983, 109(4):449-452. 21.Schwartz R.A.: Keratoacanthoma. J. Am. Acad. Dermatol. 1994, 30(1):1-19. 22.Tamir G. et. al.: Synchronous appearance of keratoacanthomas in burn scar and skin graft donor site shortly after injury. J. Am. Acad. Dermatol. Vol. 40, nr 2, Part 2:870-871. 23.Vanhooteghem O. et. al.: Multinodular keratoacanthoma and T cell lymphoma. J. Eur. Acad. Dermatolog. Venerolog. 1996, 6:50-56. 24.Weedon D.: Keratoacanthoma: a personal perspective. Current Diagnostic Pathology. 2003, 9:260-265.

