© Borgis - Nowa Stomatologia 3/2001, s. 41-46
Małgorzata Nędzi-Góra, Renata Górska, Marcin Kacprzak
Obserwacje dotyczące stosowania preparatu Skinsept® oral we wspomagającym leczeniu zapalenia przyzębia – w fazie przyczynowej oraz po zabiegach chirurgicznych na przyzębiu
Observations about the Skinsept® oral application in the treatment of periodontitis – during initial phase of treatment and after periodontal surgical procedures
z Zakładu Chorób Błony Śluzowej i Przyzębia Akademii Medycznej w Warszawie
Kierownik Zakładu: prof. AM dr hab. med. Renata Górska

WSTĘP
Podstawowym postępowaniem w leczeniu zapalenia dziąseł oraz zapalenia przyzębia związanego z płytką jest usunięcie złogów płytki i kamienia nazębnego, a także instruktaż higieny jamy ustnej i motywacja pacjenta. Zabiegi higieniczne wykonywane przez pacjentów w warunkach domowych, szczególnie we wstępnej fazie leczenia przyczynowego, nie zawsze są wystarczające. Wielu pacjentów przy użyciu szczotki, pasty, nici stomatologicznej nie jest w stanie utrzymać należytego stanu higieny jamy ustnej, na takim poziomie, który zabezpieczy przed ponownym odłożeniem płytki i rozwojem zapalenia dziąseł. Mechaniczna kontrola płytki jest więc niewystarczająca. W takich sytuacjach dodatkowo stosuje się środki chemiczne pozwalające na kontrolę płytki. Najbardziej rozpowszechnioną ich formę stanowią płukanki o działaniu przeciwzapalnym i przeciwbakteryjnym. Mogą być one stosowane przez pacjentów w warunkach domowych. Zalecane są m.in. jako preparaty wspomagające w leczeniu zapalenia dziąseł i w fazie przyczynowej leczenia zapalenia przyzębia oraz po zabiegach chirurgicznych na przyzębiu. Zadaniem płukanek jest ograniczenie odkładania się płytki nazębnej, zmniejszenie ilości bakterii, ograniczenie krwawienia, zapobieganie nawrotom zapalenia oraz przeciwdziałanie powikłaniom zapalnym po zabiegach chirurgicznych na przyzębiu. W skład płukanek o działaniu przeciwzapalnym i przeciwbakteryjnym mogą wchodzić: związki antyseptyczne (bisbiguanidy np. chlorheksydyna; związki fenolowe np. Listeryna, Triclosan; czwartorzędowe związki amoniowe np. chlorek cetylopirydyny, antyseptyki roślinne np. Sanguinaryna, jony metali np. cyny i cynku), czynniki utleniające (nadtlenek wodoru, boran sodu), enzymy, czynniki aktywne powierzchniowo (1). Związki te mogą wchodzić w skład jednego preparatu pod warunkiem, że nie wykazują wzajemnych interakcji.
Najbardziej rozpowszechnionym i najgruntowniej przebadanym antyseptykiem jest chlorheksydyna. Najczęściej występuje jako 0,2 % roztwór diglukonianu chlorheksydyny. Badania Ernsta i wsp. (1998) (2) wykazały, że zmniejszenie stężenia chlorheksydyny w płukance do 0,12 % nie powoduje zmniejszenia skuteczności preparatu w działaniu przeciwpłytkowym i przeciwzapalnym. Wydaje się więc, że stężenie 0,12 % jest wystarczające. Chlorheksydyna działa na bakterie G+, G-, drożdże i grzyby. Od wielu lat zastanawiano się z czego wynika większa skuteczność przeciwpłytkowa chlorheksydyny w porównaniu z innymi stosowanymi klinicznie antyseptykami. Nowa koncepcja mówi o budowie cząsteczki i o jej zachowaniu się w roztworze wodnym. Cząsteczki chlorheksydyny posiadają na dwóch końcach fragment hydrofobowy, co powoduje, że w przeciwieństwie do cząsteczek innych antyseptyków nie tworzą w roztworze micelli. Podczas płukania chlorheksydyną błona śluzowa jamy ustnej i zęby są poddane działaniu dużego stężenia aktywnych monomerów nie połączonych w micelle (3). Chlorheksydyna należy do tzw. antyseptyków drugiej generacji (4). W przeciwieństwie do środków pierwszej generacji działa przeciwbakteryjnie nie tylko w czasie kontaktu, a więc w czasie płukania jamy ustnej. Dodatnio naładowane cząsteczki chlorheksydyny adsorbują się do ujemnie naładowanych glikoprotein śliny oraz błonki nabytej, pokrywających błonę śluzową jamy ustnej oraz powierzchnie zębów. Uwalniają się powoli, utrzymując przez 7-8 godzin po płukaniu jamy ustnej swoją aktywność antyseptyczną. Niestety, adsorpcja chlorheksydyny do powierzchni struktur jamy ustnej decyduje również o jej najpoważniejszym i kłopotliwym działaniu ubocznym. Już po kilkakrotnym płukaniu występują przebarwienia zębów, wypełnień, uzupełnień protetycznych oraz błony śluzowej (głównie języka). Chlorheksydyna może również powodować zaburzenia smaku, złuszczanie nabłonka i w nielicznych przypadkach nadwrażliwości na ten związek chemiczny, powstawanie nadżerek na błonie śluzowej. Wszystkie te objawy ustępują po odstawieniu preparatu, decydują jednak o przeciwwskazaniach do długotrwałego stosowania chlorheksydyny. Zalecane dawkowanie, to płukanie dwa razy dziennie przez minutę 10 ml roztworu przez okres maksymalnie miesiąca (2-3 tygodnie) (5). Przeciwbakteryjne działanie chlorheksydyny także wynika z jej zdolności adsorpcyjnych. Cząsteczki tego związku wy-kazują duże powinowactwo do ujemnie naładowanych błon komórkowych drobnoustrojów, wiążą się z nimi, zaburzają równowagę osmotyczną, zwiększają przepuszczalność błony i prowadzą do zahamowania wzrostu lub śmierci komórki. Stosowanie płukanek z chlorheksydyną powoduje znaczną redukcję (80-90%) liczby mikroorganizmów w jamie ustnej oraz hamuje namnażanie płytki naddziąsłowej (5). Nie działa jednak wystarczająco mocno, żeby móc w pełni zastąpić mechaniczne oczyszczanie zębów szczoteczką. Dlatego terapia chlorheksydyną jest jedynie postępowaniem pomocniczym przy skalingu i wszystkich zabiegach mających na celu mechaniczne usunięcie płytki. Stosowanie płukanek z chlorheksydyną jest również wskazane po zabiegach chirurgicznych (również na przyzębiu) (6), przy leczeniu szynami chirurgicznymi i wyciągami międzyszczękowymi oraz aparatami ortodontycznymi, a także u osób niepełnosprawnych, mających kłopoty z oczyszczaniem zębów.
Drugim ważnym związkiem, który często wchodzi w skład płukanek o działaniu przeciwzapalnym i przeciwbakteryjnym jest nadtlenek wodoru (Hydrogenium peroxydatum). Woda utleniona (3% wodny roztwór nadtlenku wodoru) jest używana w stomatologii od ponad 70 lat. Skuteczność jej działania wykazano głównie w leczeniu wrzodziejąco-nekrotyzującego zapalenia dziąseł (ANUG), do płukania i przepłukiwania kieszonek dziąsłowych (5). W warunkach domowych najczęściej zaleca się stosowanie 0,2 % roztworu – 1 łyżka na szklankę wody. Po miejscowym zastosowaniu na zapalnie zmienione tkanki, nadtlenek wodoru jest rozkładany przez enzym katalazę (obecny we krwi, ropie, tkankach martwiczych), na tlen atomowy i wodę. Uwolniony tlen atomowy denaturuje białko drobnoustrojów. Poza tym uwalniający się tlen tworzy pianę, która mechanicznie oczyszcza zainfekowane miejsca. Egzogenny nadtlenek wodoru dostarczony do śliny zwiększa również skuteczność układu peroksydazy ślinowej. W skład tego układu wchodzą rodanki produkowane przez komórki przewodów wyprowadzających gruczołów ślinowych oraz peroksydaza syntetyzowana przez komórki gronek gruczołów ślinowych. Peroksydaza zużywa nadtlenek wodoru wytwarzany w ślinie przez bakterie i neutrofile do utleniania rodanków do bakteriobójczego kwasu hypotiocyjanowego (1). Lake i wsp. (7) wykazali, że środki utleniające (w tym woda utleniona) powodują zmniejszenie wzrostu szczepów bakterii beztlenowych np. Porphyromonas gingivalis. Marshall i wsp. (1995) (8) wykazali, że przedłużone stosowanie H2O2 w stężeniu 1-3% zmniejsza wskaźnik płytki i krwawienia oraz przyspiesza gojenie tkanek po zabiegach chirurgicznych. Woda utleniona jest również skutecznym środkiem w zwalczaniu fetor ex ore (9). Znane są także wybielające właściwości nadtlenku wodoru. Stosowany jest do wybielania zębów metodą wewnętrzną (dokomorową) i zewnętrzną. Powszechnie znany Endoperox, to 10-15% nadtlenek mocznika, który w stężeniu 10% rozkłada się na 3% nadtlenek wodoru i 7% mocznik (10). Grundemann i wsp. (2000) (11) wykazali, że użycie środków utleniających redukuje powstawanie osadu nazębnego związanego ze stosowaniem chlorheksydyny. Skłania to do rozważenia połączenia chlorheksydyny i wody utlenionej w jednym preparacie.
Do leków stosowanych miejscowo w chorobach przyzębia, niektórzy autorzy zaliczają również alkohole – 70% etanol oraz 25% glicerol (5). Niszczą one wegetatywne formy drobnoustrojów i część wirusów, ale nie działają na formy przetrwalnikowe. Mechanizm ich działania polega na denaturacji białka mikroorganizmów.
Znanym faktem jest, że poszczególne substancje czynne preparatów odkażających posiadają tzw. luki w spektrum działania w stosunku do mikroorganizmów. Poprzez odpowiednie połączenie substancji czynnych można osiągnąć szersze spektrum działania w stosunku do mikroorganizmów. Steinberg i wsp. (12) wykazali, że chlorheksydyna i woda utleniona wykazują synergistyczne działanie w stosunku do niektórych szczepów bakteryjnych (Streptococcus i Staphylococcus). Mechanizm synergistycznego działania tych związków może polegać na tym, że chlorheksydyna wpływa na ścianę komórek bakteryjnych i zwiększa zdolność wody utlenionej do penetrowania i reagowania z organellami wewnątrzkomórkowymi bakterii. Dona i wsp. (13) również stwierdzili pozytywną interakcję pomiędzy chlorheksydyną i wodą utlenioną. Z badań ich wynika, że jednoczesne płukanie oboma związkami chemicznymi bardziej redukuje wskaźnik płytki niż płukanie samą chlorheksydyną.
Preparat Skinsept® oral zawiera jako aktywne i uzupełniające się składniki diglukonian chlorheksydyny oraz nadtlenek wodoru. Poprzez kombinację z roztworem podstawowym, zawierającym etanol, uzyskano spektrum działania, które wykracza poza spektra działania poszczególnych składników.
CEL PRACY
Celem pracy była ocena skuteczności preparatu Skinsept® oral we wspomagającym leczeniu zapalenia przyzębia w fazie przyczynowej oraz po zabiegach chirurgicznych na przyzębiu.
GRUPA BADANA
Badaniem objęto 30 osób leczonych w Zakładzie Chorób Błony Śluzowej i Przyzębia IS AM w Warszawie (13 kobiet i 17 mężczyzn, średnia wieku 39, 45 lat) z rozpoznaniem zapalenie przyzębia związane z płytką nazębną (dorosłych – AP) lub gwałtownie postępujące zapalenie przyzębia (RPP). Rozpoznanie postawiono na podstawie badania podmiotowego i klinicznego oraz analizy zdjęć rtg. Żaden z pacjentów nie zgłaszał współistniejących chorób ogólnych i nie przyjmował żadnych leków. 10 pacjentów zakwalifikowano do leczenia chirurgicznego. Pozostałe 20 osób zakwalifikowano do leczenia zachowawczego (w grupie tej 10 osób stosowało preparat Skinsept® oral, a pozostałe 10 osób stanowiło grupę kontrolną).
METODY
Badanie podmiotowe przeprowadzone wstępnie u wszystkich pacjentów obejmowało szczegółowy wywiad ogólnomedyczny i stomatologiczny. Badanie przedmiotowe uw-zględniało pomiar uproszczonych wskaźników płytki (PI) i krwawienia (BI), wyrażające stosunek powierzchni krwawiących/z płytką do wszystkich powierzchni zębowych oraz określenie średniej głębokości kieszonek (PD). U wszystkich pacjentów wykonano wstępnie skaling nad- i poddziąsłowy oraz udzielono instruktażu higieny jamy ustnej. Następnie, dziesięciu losowo wybranym osobom wydano 300 ml preparatu Skinsept® oral do płukania jamy ustnej w domu, w dawce 10 ml dwa razy dziennie przez okres dwóch tygodni. Kolejnym dziesięciu osobom zlecono jedynie domowe zabiegi higieniczne i stanowili oni grupę kontrolną. Po uzyskaniu znaczącej redukcji wskaźników płytki i krwawienia (PI <15%, BI <10%) u pacjentów u których stwierdzono głębokie kieszonki przyzębne (> 6 mm) oraz pionowe ubytki kostne wykonano zabiegi chirurgiczne. U 4 pacjentów wykonano zabieg zmodyfikowanej operacji płatowej z zastosowaniem preparatu Bio-Oss + Bio-Gide, u 4 zabieg kiretażu otwartego, a u 2 zabieg zmodyfikowanej operacji płatowej z zastosowaniem preparatu Biogran. Pacjentom wydano 300 ml preparatu Skinsept® oral do płukania jamy ustnej w domu w dawce 10 ml dwa razy dziennie przez okres dwóch tygodni w celu utrzymania osiągniętych w fazie wstępnej wskaźników płytki i krwawienia, oraz zapobieżenia powikłaniom zapalnym. Wizyty kontrolne wyznaczono na 7 i 14 dni po przeprowadzonych zabiegach.
Po upływie dwóch tygodni u wszystkich pacjentów ponownie oznaczono PI, BI oraz PD. Dodatkowo u pacjentów stosujących Skinsept® oral przeprowadzono szczegółowe badanie jamy ustnej, oceniając ewentualne przebarwienia błony śluzowej policzków i języka oraz występowanie przebarwienia zębów. Przeprowadzono również szczegółowy wywiad dotyczący subiektywnych odczuć związanych ze stosowaniem preparatu.
WYNIKI
Wyniki przedstawiono w tabelach oraz zobrazowano na rycinach 1-3).
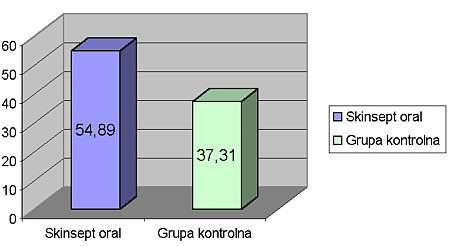
Ryc. 1. Obniżenie wskaźnika płytki w dwóch grupach badanych.
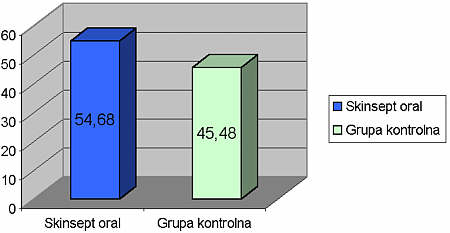
Ryc. 2. Obniżenie wskaźnika krwawienia w dwóch grupach badanych.

Ryc. 3. Obniżenie głębokości kieszonek w dwóch grupach badanych.
OMÓWIENIE WYNIKÓW I DYSKUSJA
U pacjentów z grupy kontrolnej po leczeniu przyczynowym, stwierdziliśmy obniżenie wskaźnika płytki o 37,31%, wskaźnika krwawienia o 45,48% i średniej głębokości kieszonek o 20,8%. Dla wszystkich badanych parametrów różnica pomiędzy wynikiem wstępnym, a wynikiem po 2 tygodniach była znamienna statystycznie (tab. 1).
Tabela 1. Średnie wartości wskaźnika płytki (PI), wskaźnika krwawienia (BI) oraz średniej głębokości kieszonek (PD) u pacjentów z grupy kontrolnej.
| | Pomiary wstępne | Pomiary po 2 tygodniach | Różnica | % | Istotność statystyczna |
| PI | 54,03 | 33,87 | 20,16 | 37,31 | p <0,05 |
| BI | 41,77 | 22,77 | 19 | 45,48 | p <0,05 |
| PD | 1,49 | 1,18 | 0,31 | 20,8 | p <0,5 |
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
24 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
59 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
119 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 28 zł
Piśmiennictwo
1. David M. Williams: Patologia przyzębia. Sanmedica 1995. 2. Ernst C.P. et al.: The effectiveness and side effects of 0.1% and 0.2% chlorhexidine mouthrinses; a clinical study. Quintessence Int, 1998 Jul, 29:7, 443-8. 3. Proceedings of the 2nd European Workshop on Periodontology. Chemicals in Periodontics. Quintessence, 1996. 4. Periodontologia kliniczna cz. 1 pod red. Marii Wierzbickiej. Sanmedica 1992. 5. „Kompendium farmakoterapii dla stomatologów” pod red. Zbigniewa Jańczuka Volumed s.c. Wrocław 1998 r. 6. Zucchelli G. et al.: The effect of chlorhexidine mouthrinses on early bacterial colonization of guided tissue regeneration mwmbranes. An in vivo study. J periodontal, 2000 Feb, 71:2, 263-71. 7. Leke N. et al.: Effects of hydrogen peroxide on growth and selected properties of Porphyromonas gingivalis; FEMS Microbiol Lett, 1999 May 15, 174(2), 347-53. 8. Marshall M.V. et al.: „Hydrogen peroxide: a review of its use in dentistry”. J. Periodontol, 1995 Sep, 66:9, 786-96. 9. Grigor J. et al.: Reduction in the levels of oral malodor precursors by hydrogen peroxide: in vitro and in vivo assessments. J Clin Dent, 1992, 3(4): 111-5. 10. Endodoncja pod red. B. Arabskiej-Przedpełskiej. Med. Tour Press Int. 1996. 11. Grindemann L.J. et al.: Stain, plaque and gingivitis reduction by combining chlorhexidine and peroxyborate. I Clin Periodontol, 2000 Jan, 27:1, 9-15. 12. Steinberg D. et al.: Antibacterial synergistic effect of chlorhexidine and hydrogen peroxide against Streptococcus sorbinus, Streptococcus faecalis and Staphylococcus aureus. J Oral Rehabil, 1999 Feb, 26(2): 151-6. 13. Dona B.L. et al.: The inhibitory effects of combining chlorhexidine and hydrogen peroxide on 3-day plaque accumulation. J Clin Periodontol, 1998 Nov, 25(11 Pt 1), 879-83. 14. Iwanicka-Frankowska Ewa i wsp.: Zastosowanie 0,3% roztworu chlorheksydyny w leczeniu zapalenia dziąseł. Czasopismo Stomatologiczne, 1996 tom LII. 15. Balbuena L. et al.: Effects of topical oral antiseptic rinses on bacterial counts of saliva in healthy human subjects. Otolaryngol Head Neck Surg, 1998 May, 118:5, 625-9. 16. Christie P. et al.: The use of 0.2 % chlorhexidine in the absence of a structured mechanical regimen of oral hygiene following the non-surgical treatment of periodontitis. J Clin Periodontol, 1998 Jan, 25:1, 15-23. 17. Shibly O. et al.: Clinical evaluation of the effect of hydrogen peroxide mouth rinse, sodium bicarbonate dentifrice, and mouth moisturizer on oral health. J Clin Dent, 1997, 8:5, 145-9. 18. Dorefr Ch.E. et al.: Regenerative periodontal surgery in interproximal intrabony defects with biodegradable barriers. J. Clin Periodontol, 2000, 27, 162-168. 19. Levkovic V. et al.: A comparison between enamel matrix proteins used alone or in combination with bovine porous bone mineral in the treatment of intrabony periodontal defects in humans. J Periodontol, 2000, VOI 7, No 7, 1110-1116. 20. Ratka-Kruger P. et al.: Guided tissue regeneration with bioresorbable membranes versus conventional surgery in the treatment of infrabony periodontal defects. J Clin Periodontol, 2000, 27, 120-127. 21. Zybutz M.D. et al.: Treatment of infrabony defects with resorbable materials, non-resorbable materials and flap debridement. J Clin Periodontol, 2000, 27, 169-178.




