© Borgis - Nowa Pediatria 3/2006, s. 70-72
Kinga Rejner2, Karolina Nędzi2, *Teresa Jackowska1
Skuteczność szczepienia przeciwko wirusowemu zapaleniu wątroby typu B w pierwszym roku życia u dzieci z rozpoznaną ostrą białaczką
Efficacy of immunization to hepatitis B during the first year of life in children with diagnosed acute leukemia
1Katedra i Klinika Pediatrii, Hematologii i Onkologii AM w Warszawie
Kierownik Kliniki: prof. dr hab. med. Michał Matysiak
2Studenckie Koło Naukowe przy Klinice Pediatrii Hematologii i Onkologii AM w Warszawie
Kierownik Kliniki: prof. dr hab. med. Michał Matysiak
Streszczenie
Background. Effective vaccines against hepatitis B in Poland have been available since 1994-1996. Common vaccination to hepatitis B virus decreased the frequency of hepatitis B in Poland. However children with leukemia´s are still at higher risk of this infection. The aim of the study was to asses the efficacy of prophylaxis of hepatitis B in children with leukemia.
Materials and methods. Vaccination was performed in 99 children during first year of live (91- acute lymphoblastic leukemia; 8-acute myeloblastic leukemia; 48 boys and 51 girls; ages 1-9 year). We assessed the level of anti-HBs antibodies.
Results. Serological conversation was observed in 84% children. 14% of children have not achieved the protective levels of antibodies in spite of active prophylaxis during the first years of live (0-1-6 months or 0-1-2-12 months). No statistically significant difference according to sex, time after vaccination. The lowest levels of anti-HBs antibodies we observed after 6 years, the highest after 5 years of vaccinations.
Conclusions. In children with leukemia, in spite of vaccinations, the level of anti-HBs antibodies should be controlled before treatment.

Wstęp
Obowiązkowe szczepienia noworodków przeciwko WZW typu B zostały wprowadzone w Polsce w 1994 roku i stopniowo do 1996 roku objęły swym zasięgiem cały kraj. Od tego czasu zapadalność na hepatitis B obniżyła się ponad 7-krotnie (z 28,3/100000 w 1994 do 3,86/100000 w 2004), co niewątpliwie jest ogromnym sukcesem wprowadzonych szczepień (1). Uważa się, że skuteczną ochronę przed zakażeniem można uzyskać poprzez pełny cykl szczepień i wytworzenie przeciwciał anty-HBs w surowicy krwi w mianie powyżej 10 IU/l. Skuteczność takiego postępowania wynosi ponad 96% w zdrowej populacji (2, 3).
U dzieci chorych na ostre białaczki istnieje wyższe niż w populacji zdrowej ryzyko zakażenia wirusem hepatitis B (4). W roku 1988 u 20% dzieci, u których rozpoznano ostrą białaczkę, występowały markery zakażenia HBV, a w czasie zakończenia leczenia odsetek ten wzrastał do ponad 90% (5). Przyczyn tak wysokiego ryzyka zakażeń WZW B upatrywano w dużej liczbie zabiegów diagnostyczno-terapeutycznych, jakim poddawani są pacjenci, stosowaniu preparatów krwi, leczeniu immunosupresyjnym, a także dużym zagęszczeniu na oddziałach hematologiczno-onkologicznych oraz złych warunkach sanitarnych.
Materiał i Metody
Celem pracy była ocena skuteczności przeprowadzonego w okresie niemowlęcym szczepienia przeciwko wirusowemu zapaleniu wątroby typu B u dzieci z rozpoznaną ostrą białaczką.
Przeanalizowano miana przeciwciał anty-HBs u 99 pacjentów (51 dziewczynek i 48 chłopców) w wieku 1-9 lat (średnia wieku wynosiła 5 lat), przyjętych do Kliniki Pediatrii, Hematologii i Onkologii Akademii Medycznej w Warszawie w latach 1994-2004. U 91 pacjentów rozpoznano ostrą białaczkę limfoblastyczną, u 8 ostrą białaczkę mieloblastyczną. Dzieci były szczepione szczepionką Engerix B lub Euvax w pierwszym roku życia w schemacie 0/1/2/12 (4 dawki) lub 0/1/6 (3 dawki), w dawce 10 mg, zgodnie z obowiązującym wówczas kalendarzem szczepień.
Poziom przeciwciał mierzono przy przyjęciu do Kliniki metodą immunoenzymatyczną. Wyniki były oceniane według następujących kryteriów: brak odpowiedzi immunologicznej dla miana anty-HBs poniżej 10 IU/l, niska odpowiedź – 10-100 IU/l, średnia odpowiedź – 100-1000 IU/l, odpowiedź wysoka – powyżej 1000 IU/l. Za brak ochronnego poziomu przeciwciał uznawano miana poniżej 10 IU/l.
Wyniki
U badanych dzieci średni poziom przeciwciał anty-HBs wynosił 398,8 (0,0-1000,0) (IU/l).
14% dzieci (n=14) nie odpowiedziało na szczepienie (miano przeciwciał poniżej 10 IU/l). U 19% badanych (n=19) stwierdzono odpowiedź niską (miano przeciwciał 10-100 IU/l), u 39% (n=39) odpowiedź średnią (miano 100-1000 IU/l), a odpowiedź wysoką (miano powyżej 1000IU/l) stwierdzono u 27% badanych (n=27) (ryc. 1).
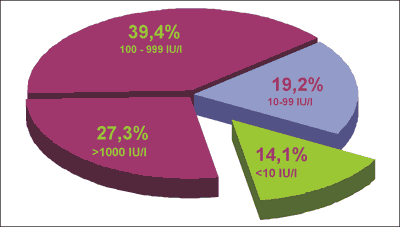
Ryc. 1. Poziomy przeciwciał anty-HBs u dzieci z ostrą białaczką.
Przeanalizowano również różnice miana przeciwciał anty-HBs w zależności od czasu, jaki upłynął od zakończenia szczepienia. Nie stwierdzono znamiennej statystycznie różnicy w poziomach przeciwciał anty-HBs między grupą, w której czas od zakończenia szczepienia był krótszy niż 5 lat (431,3 IU/l), a grupą, w której czas ten był dłuższy (383,2 IU/l). Średnie poziomy przeciwciał anty-HBs w kolejnych latach od zakończenia szczepienia wynosiły 139-446 IU/l, ich średnie wartości były więc ochronne w każdej z grup wiekowych (ryc. 2). W poszczególnych grupach wiekowych od 0-4 dzieci nie stwierdzano seroprotekcji (ryc. 3).
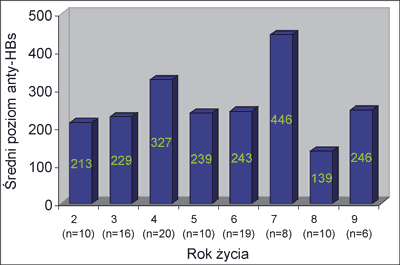
Ryc. 2. Średnie poziomy przeciwciał anty-HBs w zależności od wieku pacjentów przy rozpoznaniu białaczki.
Analizowano także średnie miana anty-HBs w zależności od płci. Były one wyższe u dziewcząt (średnia geometryczna 458 IU/l) niż u chłopców (średnia geometryczna 391 IU/l), nie była to jednak różnica znamienna statystycznie (p=0,43).
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
24 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
59 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
119 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 28 zł
Piśmiennictwo
1. www.pzh.gov.pl/biblioteka, Meldunki o zachorowaniach na choroby zakaźne 1979-2004.2. Madaliński K., i wsp.: Immunogenicity of Engerix B vaccine in 786 children with risk of hepatitis B infection. Hep. Pol., 1998, 5 (supl. 1): 93-98.3. Rokicka-Milewska R., i wsp.: Zapobieganie zakażeniu wirusem zapalenia wątroby typu B szczepionką Engerix B u dzieci chorych na hemofilię i choroby rozrostowe układu krwiotwórczego. Pediat. Pol.,1992, 67, 3-4, 131-137.4. Zalewska-Szewczyk B., i wsp.: Ocena skuteczności czynno-biernej profilaktyki wirusowego zapalenia wątroby typu B u dzieci poddanych chemioterapii. Prz. Pediat., 2004, Vol 34, nr 3/4, 228-231.5. Jackowska T., i wsp.: Zakażenie wirusem zapalenia wątroby typu B u dzieci chorych na białaczki i chłoniaki. Wiad. Lek., 1990, 43, 13.6. Petersen K.M., et al.: Duration of hepatitis B immunity in low risk children receiving hepatitis B vaccinations from birth. Pediatr. Infect. Dis. J., 2004, 23(7): 650-655.7. Van Damme P., Vorsters A.: Hepatitis B control In Europe by universal vaccination programmes: The situation in 2001. J. Med. Virol., 2002 67: 433-439.8. Lin H.H., et al.: Decline of hepatitis B carrier rate in vaccinated and unvaccinated subjects: Sixteen years after newborn vaccination program In Taiwan. J. Med. Virol., 2003, 69: 471-474.9. Petersen K.M., et al.: Duration of hepatitis B immunity in low risk children receiving hepatitis B vaccinations from birth. Pediatr. Infect. Dis. J., 2004, 23(7): 650-655.


