© Borgis - Nowa Pediatria 3/2002, s. 137-141
Barbara Iwańczak, Franciszek Iwańczak
Zakażenie Helicobacter pylori u dzieci
Helicobacter pylori infection in children
z II Katedry i Kliniki Pediatrii, Gastroenterologii i Żywienia Akademii Medycznej we Wrocławiu
Kierownik Kliniki: prof. dr hab. n. med. Franciszek Iwańczak
Streszczenie
Epidemiology, clinical course, diagnostic methods and treatment of Helicobacter pylori in children are presented in the work.

Helicobacter pylori (H. pylori) jest bakterią najbardziej rozpowszechnioną w świecie, która została uznana za najczęstszy patogen człowieka. W 1896 r. Walery Jaworski (1) w Krakowie stwierdził obecność spiralnych bakterii w osadzie z treści żołądka, jednak wykrycie tej bakterii zawdzięczamy Warrenowi i Marshallowi (2) z Australii, którzy w 1983 r. opublikowali pracę o obecności spiralnych bakterii w bioptatach błony śluzowej żołądka, w aktywnym przewlekłym zapaleniu żołądka. W następnych latach okazało się, że zakażenie H. pylori odgrywa istotną rolę w etiopatogenezie chorób przewodu pokarmowego (3).
CZYNNIKI CHOROBOTWÓRCZE H. PYLORI
Patogenne działanie tej bakterii zależy od:
1. zdolności do kolonizacji błony śluzowej żołądka, którą zapewnia poruszanie się w gęstym śluzie żołądka;
2. przylegania do komórek nabłonka;
3. wytwarzania ureazy i czynników modyfikujących wydzielanie żołądka;
4. zdolności do przetrwania w kwaśnym środowisku treści żołądka;
5. zdolności do powodowania zmian zapalnych błony śluzowej.
KLINIKA ZAKAŻENIA H. PYLORI
Zakażenie H. pylori wywołuje zmiany zapalne błony śluzowej żołądka oraz odpowiedź immunologiczną makroorganizmu. Proces zapalny błony śluzowej żołądka ma charakter postępujący i po wielu latach prowadzi do rozwoju zmian zanikowych błony śluzowej, choroby wrzodowej, chłoniaka żołądka typu MALT (mucosal associated limphoid tissue), metaplazji, dysplazji, a następnie adenocarcinoma (4, 5). Hipotetyczne następstwa zakażenia H. pylori wg Tytgata przedstawiono na rycinie 1 (str. 138). U dzieci zakażenie H. pylori jest główną przyczyną choroby wrzodowej dwunastnicy i żołądka oraz przewlekłego zapalenia błony śluzowej żołądka (6-8). U większości osób zakażonych H. pylori przez okres całego życia mogą nie występować żadne objawy. Natomiast u 15% zakażonych istnieje ryzyko wystąpienia choroby wrzodowej, u 0,1% ryzyko wystąpienia nowotworu żołądka w postaci lymphoma lub adenocarcinoma (9). Rozwój raka żołądka jest zależny od genotypu H. pylori (9). Wg niektórych autorów również od genetycznego zróżnicowania drobnoustroju zależy możliwość rozwoju wymienionych chorób oraz skuteczność eradykacji, która jest niższa u pacjentów z zakażeniem H. pylori cag A.
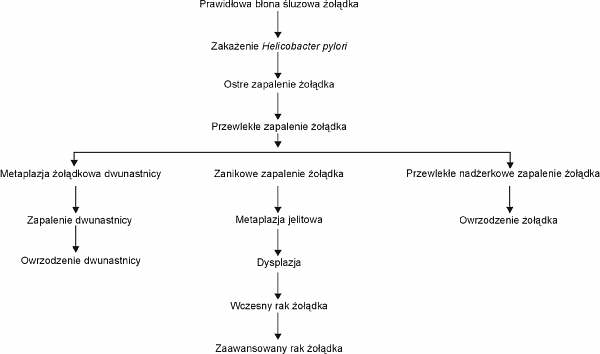
Ryc.1. Hipoteza możliwych konsekwencji zakażenia H. pylori wg Tytgata.
W ostatnich latach wykazano, że zakażenie H. pylori zmniejsza integralność bariery nabłonkowej żołądka, zwiększa przepuszczalność nabłonka dla makromolekuł i zwiększa transport białek w postaci niezmienionej przez nabłonek żołądka (5, 10, 11).
Jest to przyczyną zwiększonego wchłaniania antygenów, stymulacji układu immunologicznego, stanu zapalnego błony śluzowej żołądka, który może utrzymywać się nawet po eradykacji bakterii. Wzrost przepuszczalności białek przez błonę śluzową żołądka może ponadto powodować u dzieci i dorosłych z predyspozycją genetyczną nasilenie reakcji alergicznych (12-14). Może to mieć związek z działaniem cytotoksyny wakualizującej vacA H. pylori, która może powodować degradację lizosomalną makromolekuł komórki nabłonka błony śluzowej żołądka (10, 15). W badaniach doświadczalnych na myszach zakażonych H. felis. żywionych białkiem mleka krowiego, wykazano wzrost miana przeciwciał przeciw kazeinie w klasie IgG i wzrost miana przeciwciał w klasie IgE (16). U chorych z cukrzycą stwierdzano korelację między mianem przeciwciał przeciw białku mleka krowiego i przeciwciał przeciw H. pylori (17). Murakami i wsp. (18) opisali korzystny wpływ eradykacji H. pylori na przebieg atopowego zapalenia skóry. U pacjentów z przewlekłym zapaleniem błony śluzowej żołądka w przebiegu zakażenia H. pylori stwierdzano w surowicy obecność przeciwciał klasy IgE specyficznych dla antygenu H. pylori (19).
Zwiększona przepuszczalność błony śluzowej żołądka w przebiegu zakażenia H. pylori może odgrywać ważną rolę w karcynogenezie i innych objawach narządowych tego zakażenia. Ocenia się, że ryzyko wystąpienia ciężkiej choroby organicznej, spowodowanej zakażeniem H. pylori, wynosi w ciągu życia 10-15% i wzrasta z czasem utrzymywania się zakażenia. Wykazano także związek pomiędzy zakażeniem H. pylori a niskorosłością oraz niedokrwistością z niedoboru żelaza. Związek pomiędzy zakażeniem H. pylori a chorobą refluksową przełyku jest złożony. Niektórzy autorzy wykazali nasilenie refluksu po eradykacji (9).
EPIDEMIOLOGIA H. PYLORI
Do zakażenia H. pylori dochodzi głównie w dzieciństwie. W pierwszych 6 miesiącach życia dziecka przeciwciała przekazane przez matkę, jak również znajdujące się w pokarmie kobiecym, chronią większość niemowląt przed zakażeniem H. pylori. Głównym źródłem zakażenia jest człowiek. Zakażenie przenosi się drogą kałowo-pokarmową lub ustno-ustną (20, 21). Znane są duże różnice w częstości występowania zakażenia H. pylori u dzieci mieszkających w krajach rozwijających się i w krajach rozwiniętych. Na podstawie danych epidemiologicznych można przypuszczać, że w krajach wysoko rozwiniętych podstawową drogą przenoszenia jest droga ustno-pokarmowa, a w krajach rozwijających się droga kałowo-pokarmowa. Możliwa jest również droga ustno-ustna. H. pylori może przez pewien okres przeżyć w soku żołądkowym. W czasie zwracania treści żołądkowej kolonizacji może ulegać jama ustna i płytka nazębna. W tej sytuacji transmisja bakterii jest możliwa za pośrednictwem śliny lub przedmiotów zanieczyszczonych śliną i przenoszenie H. pylori odbywa się głównie w rodzinie między małżonkami, matką i dzieckiem, a także pomiędzy rodzeństwem (22, 23). Stopień rozprzestrzeniania zakażenia H. pylori na świecie jest bardzo różny, zależny od regionu geograficznego. Dzieci żyjące w złych warunkach socjalnych i materialnych znacznie częściej ulegają zakażeniu. W pierwszych 5 latach życia odsetek dzieci zakażonych może wynosić nawet 50-60% w takich krajach jak Peru, Etiopia czy RPA (24-26). W krajach uprzemysłowionych, np. w Belgii, tylko 1% lub mniej niemowląt jest serododatnich.
DIAGNOSTYKA ZAKAŻENIA H. PYLORI
Zakażenia H. pylori należy poszukiwać wyłącznie u dzieci, u których objawy kliniczne sugerują chorobę organiczną górnego odcinka przewodu pokarmowego i są wskazaniem do wykonania badania endoskopowego (27). Wykrycie zmian patologicznych w trakcie badania endoskopowego, zwłaszcza wrzodu trawiennego lub zmian zapalnych błony śluzowej żołądka, jest wskazaniem do pobrania wycinków błony śluzowej żołądka w celu wykrycia zakażenia H. pylori. Nie należy poszukiwać zakażenia H. pylori u dzieci bez objawów chorobowych. Eradykacja H. pylori wskazana jest u dzieci z potwierdzonym czynnym zakażeniem H. pylori i obecnością objawów choroby przewodu pokarmowego. Potwierdzeniem czynnego zakażenia jest wykazanie H. pylori w badaniu histologicznym wycinka błony śluzowej lub wyizolowanie w hodowli wycinków tkankowych inkubowanych w specjalnych podłożach. Metody mające na celu wykrycie zakażenia H. pylori dzielimy na inwazyjne i nieinwazyjne (tab. 1).
Tabela 1. Testy diagnostyczne stosowane do wykrywania zakażenia H. pylori.
1. Badania inwazyjne wymagające wykonania endoskopii górnego odcinka przewodu pokarmowego:
a. testy oceniające aktywność ureazy w wycinkach błony śluzowej
(CLO-test),
b. badanie histologiczne wycinków błony śluzowej,
c. posiew,
d. polimerazowa reakcja łańcuchowa (PCR).
2. Badania nieinwazyjne:
a. oznaczanie swoistych przeciwciał w surowicy, pełnej krwi, w ślinie i
moczu,
b. oznaczanie antygenu H. pylori w kale,
c. test oddechowy z mocznikiem znakowanym izotopem 13C. |
Badania inwazyjne wymagają wykonania endoskopii górnego odcinka przewodu pokarmowego i pobrania wycinków błony śluzowej z jednego lub kilku miejsc. Pobrane wycinki służą do rozpoznawania zakażenia szybkim testem ureazowym (CLO-test), badania histologicznego lub posiewu. W badaniu histologicznym wycinków możemy wykazać obecność H. pylori oraz ocenić nasilenie zakażenia i zmian zapalnych błony śluzowej, rodzaj zmian zapalnych, występowanie metaplazji jelitowej oraz chłoniaka (MALT-lymphoma).
Posiew bakteriologiczny posiada bardzo ważne znaczenie kliniczne. Pozwala ocenić wrażliwość H. pylori na antybiotyki, określić zjadliwość bakterii, cag A, vac A i inne cechy, mogące mieć związek z przebiegiem choroby i rokowaniem.
Polimerazowa reakcja łańcuchowa pozwala na wykrycie DNA bakteryjnego w tkankach, płynach ustrojowych, kale, wodzie pitnej. Dostarcza informacji na poziomie molekularnym, ważnych w badaniach epidemiologicznych i klinicznych.
Badania nieinwazyjne polegają na wykorzystaniu testów serologicznych do wykrywania swoistych przeciwciał, badaniu obecności antygenu H. pylori w kale oraz na teście oddechowym z mocznikiem znakowanym izotopem 13C.
Do oceny odpowiedzi humoralnej ustroju na zakażenie H. pylori stosuje się różne testy serologiczne służące do wykrywania przeciwciał przeciwko H. pylori. Najczęściej stosowanymi są testy immunoenzymatyczne oparte na technice ELISA oraz western-blot. Najczęściej jest oznaczane stężenie przeciwciał klasy IgG, które są wykrywane w surowicy oraz w krwi pełnej. Czułość wymienionych testów u dzieci wynosi około 70%, a dodatni wynik nie jest przekonywującym dowodem czynnego zakażenia, gdyż może świadczyć również o przebytym zakażeniu H. pylori. Badania serologiczne nie są też wiarygodnym sposobem oceny skuteczności eradykacji H. pylori, gdyż dodatnie miano przeciwciał we krwi może się utrzymywać przez kilka miesięcy po wyeliminowaniu drobnoustroju.
TESTY SEROLOGICZNE DO WYKRYWANIA SWOISTYCH PRZECIWCIAŁ PRZECIWKO H. PYLORI
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
24 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
59 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
119 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 28 zł
Piśmiennictwo
1. Jaworski W.: Podręcznik chorób żołądka. Wydawca Dzieł Lekarskich 1899: 32; cyt. za Konturek J. W., Konturek S.J.: Gastric secretion and the pathogenesis of peptic ulcer in the Helicobacter pylori infection. J. Physiol. Pharmacol. 1996. 47:5-19. 2. Warren J.R., Marshall B.J.: Unidentified curved bacilli on the gastric epithelium in active chronic gastritis. Lancet 1983, 1:1273-1275. 3. Lee A., Mégraud F.: Helicobacter pylori: techniques for clinical diagnosis and basic research. W.B. Saunders Company Ltd., London 1996. 4. Blaser M.: Hypothesis on the pathogenesis and natural history of Helicobacter pylori – induced inflammation. Gastroenterology 1992, 102:720-727. 5. Matysiak-Budnik T.: Helicobacter pylori et modifications de la perméabilité épithéliale gastrique. Thése No 767 pour le doctorat de l´Université Bordeaux 2, 2000. 6. Iwańczak F. i wsp.: Częstość występowania zakażenia Campylobacter pylori w chorobach żołądka i dwunastnicy u dzieci. Ped.Pol.1990.supl., 1:149-154. 7. Celińska-Cedro D. i wsp.: Zakażenie Helicobacter pylori u dzieci z przewlekłymi bólami brzucha. Przegl. Ped. 1993, 23, supl:3:207-212. 8. Iwańczak B. i wsp.: Częstość występowania zakażenia Helicobacter pylori w przewlekłym zapaleniu błony śluzowej żołądka u dzieci. Gastroenterol. Pol. 1997, 4:607-610. 9. Vandenplas Y.: The role of Helicobacter pylori in paediatrics. Curr. Opin. Infect. Dis. 2001, 14:315:321. 10. Pelicic V. et al.: Helicobacter pylori VacA cytotoxin associated with the bacteria increases epithelial permeability independently of its vacuolating activity. Microbiology 1999, 145:2043-2050. 11. Sutherland L.R. et al.: A simple noninvasive marker of gastric damage: sucrose permeability. Lancet 1994, 343:998-1000. 12. Bartuzi Z. et al.: Correlation between Helicobacter pylori infection and food allergy in chronic gastritis. Med. Sci. Monit. 2000, 6:530-538. 13. Corrado G. et al.: Positive association between Helicobacter pylori infection and food allergy in children. Scand. J. Gastroenterol. 1998, 33:1135-1139. 14. Figura N. et al.: Food allergy and Helicobacter pylori infection. Ital. J. Gastroenterol. Hepatol. 1999, 31:186-191. 15. Cover T.L., Blaser M.J.: Purification and characterization of the vacuolating toxin from Helicobacter pylori. J. Biol. Chem. 1992, 267:10570-10575. 16. Li X.M. et al.: A murine model of IgE-mediated cow milk hypersensitivity. J. Allergy Clin. Immunol. 1999, 103:206-214. 17. Pocecoo M. et al.: High risk of Helicobacter pylori infection associated with cow´s milk antibodies in young diabetics. Acta Pediatr. 1997, 86:700-703. 18. Murakami K. et al.: Atopic dermatitis successfully treated by eradication of Helicobacter pylori. J. Gastroenterol. 1996, 31:77-82. 19. Aceti A. et al.: Basophil-bound and serum immunoglobulin E directed against chronic gastritis. Gastroenterology 1991, 101:131-137. 20. Axon A.T.R.: Review article: is Helicobacter pylori transmitted by the gastrooral route?. Aliment. Pharmacol. Ther. 1995, 9:585-588. 21. Mégraud F.: Transmission of Helicobacter pylori: faecal-oral versus oral-oral route. Aliment. Pharmacol. Ther. 1995, 9, suppl. 2:85-91. 22. Singh V. et al.: Helicobacter pylori: evidence for spouse-tospouse transmission. J. Gastroenterol. Hepatol. 1999, 14:519-522. 23. Potyrała M. i wsp.: Rodzinne występowanie zakażenia Helicobacter pylori. Gastroenterol. Pol. 1999, 6:437-442. 24. Bardhan K.P.: Epidemiological features of Helicobacter pylori infection in developing countries. Clin infect. Dis. 1997, 25973-978. 25. Lindkvist P. et al.: Age of acquisition of Helicobacter pylori infection: comparison of a high and a low prevalence country. Dcand. J. Infect. Dis. 2996, 28:181-184. 26. Pelser H.H. et al.: Prevalence of Helicobacter pylori antibodies in children in Bloemfontein. South Africa. J. Pediatr. Gastroenterol. Nutr. 1997, 24:135-139. 27. Postępowanie w zakżeniu Helicobacter pylori (rok 2000). Wytyczne opracowane przez Grupę Roboczą Polskiego Towarzystwa Gastroenterologii. Gastronterol. Pol. 2001, 8:11-18. 28. Blecker U. et al.: Evolution of Helicobacter pylori positivity in infants born from positive mothers. J. Pediatr. Gastroenterol. Nutr. 1994, 19:87-90. 29. Blecker U. et al.: The prevalence of Helicobacter pylori positivity in a symptom-free population, aged 1 to 40 years. J. Clin. Epidemiol. 1994, 47:1095-1098. 30. Hornemann F. et al.: Seroprevalence of Helicobacter pylori in German infants and children. Helicobacter 1997, 2:176-179. 31. Gościniak G. i wsp.: Przeciwciała IgA anty-Helicobacter pylori w surowicy i ślinie chorych ze schorzeniami górnego odcinka przewodu pokarmowego. Gastroenterol. Ped. 1996, 3:119-124. 32. Gościniak G.: Przeciwciała w zakażeniach Helicobacter pylori, praca habilitacyjna, AM, Wrocław 2000. 33. Bąk-Romaniszyn L. i wsp.: Badania nad przenoszeniem zakażenia Helicobacter pylori matka-dziecko. Ped. Pol. 1999, supl. 6:354. 34. Przybyszewska K. i wsp.: Częstość występowania zakażenia Helicobacter pylori u dzieci zdrowych poniżej czwartego roku życia – doniesienie wstępne. Ped. Współ. 2000, 2:39-42. 35. Drum B., Koletzko B., Oderda G.: Helicobacter pylori infection in children: a consensus statement. J. Ped. Gastroenterol. Nutr. 2000, 30:207-213.

