© Borgis - Nowa Pediatria 1/2009, s. 3-18
*Helena Ziółkowska
Ostra niewydolność nerek u dzieci
Acute renal failure in children
Katedra i Klinika Pediatrii i Nefrologii Warszawskiego Uniwersytetu Medycznego
Kierownik Kliniki: prof. dr hab. n. med. Maria Roszkowska-Blaim
Streszczenie
Acute kidney injury (AKI, previously acute renal failure) is characterized by a reversible increase in the blood concentration of nitrogenous waste products and by inability of the kidney to regulate homeostasis. Renal failure can be divided into prerenal failure, intrinsic renal disease and obstructive uropathies. Over the past two decades the etiology of AKI in children has changed. Historically, hemolytic uremic syndrome was the major cause of pediatric AKI. Single center studies published more recently show, that AKI is now seen most frequently in association with surgery for congenital heart disease, sepsis and multi-organ dysfunction. In current clinical practice, AKI is typically diagnosed by a rise in serum creatinine and decrease urine output (RIFLE criteria). Unfortunately, creatinine is and unreliable indicator during acute changes in kidney function, especially in neonates. Early biomarkers of AKI need to be explored in critically ill children. The most promising AKI biomarkers include neutrophil gelatinase-associated lipocalin (NGAL), IL-18, kidney injury molecule-1 (KIM-1). The basic principles of management of AKI are avoidance of life-threatening complications, maintenance of fluid and electrolyte balance, and nutritional support. Many children with AKI will need renal replacement therapy (RRT). RRT may be provided by peritoneal dialysis, intermittent hemodialysis or continuous renal replacement therapy methods. The prognosis of AKI is highly dependent on the underlying etiology of the AKI. This review outlines the etiology, incidence, diagnosis, treatment-both dialytic and non-dialytic, and prognosis of pediatric AKI.

Ostrą niewydolnością nerek (ONN) określamy stan nagłego i najczęściej odwracalnego załamania funkcji nerek, który doprowadza do wzrostu stężenia w surowicy produktów przemiany azotowej i zaburzeń homeostazy ustrojowej. Obecnie w literaturze anglojęzycznej używa się szerszego określenia ostrego uszkodzenia nerek – acute kidney injury (AKI), rezerwując pojęcie ostrej niewydolności nerek – acute renal failure (ARF) tylko do stanów wymagających leczenia nerkozastępczego. Ponieważ w polskim piśmiennictwie określenie ostre uszkodzenie nerek (skrót – OUN?) nie zostało jeszcze powszechnie przyjęte, w tym artykule będzie używane nadal pojęcie ostrej niewydolności nerek.
W piśmiennictwie występuje ponad 35 różnych definicji określających ONN (1), co utrudnia rozpoznawanie i porozumienie między lekarzami. W 2004 roku międzynarodowa grupa ekspertów złożona z nefrologów i anestezjologów opublikowała kryteria rozpoznawania oraz klasyfikacji zejścia ONN. System ten o akronimie RIFLE, opiera się na ocenie stężenia kreatyniny w surowicy i ilości oddawanego moczu i kwalifikuje pacjentów do 3 różnych kategorii ciężkości uszkodzenia nerek (1). Do klasyfikacji przyjmuje się to kryterium, które kwalifikuje go do cięższej kategorii. System został opracowany z myślą o pacjentach będących w stanie krytycznym, przebywających w OIT, ale jest ostatnio coraz szerzej stosowany. W tabeli 1 przedstawiono kryteria RIFLE. W 2007 r. grupa badaczy zaproponowała, aby posługiwać się następującymi określeniami w rozpoznawaniu ONN: stadium 1 – łagodna (odpowiednik R w kryteriach RIFLE), stadium 2 – umiarkowana (odpowiednik I) i stadium 3 – ciężka (odpowiednik F) ONN (2). Akcan-Arikan i wsp. (3) zaproponowali pediatryczną modyfikację kryteriów RIFLE opartą na ocenie kalkulowanego klirensu kreatyniny wg wzoru Schwartza (tab. 2). Dostosowanie kryteriów diagnostycznych dla potrzeb pediatry nie usunęło jednak wszystkich trudności, szczególnie jeśli chodzi o dzieci najmłodsze (4). Wątpliwości dotyczą szczególnie noworodków, u których:
– w pierwszych 2 dniach życia stężenie kreatyniny jest odbiciem funkcji nerek matki,
– przesączanie kłębuszkowe (glomerular filtration rate – GFR) zwiększa się istotnie w pierwszym miesiącu życia,
– bilirubina, często podwyższona w pierwszych dniach życia interferuje z oznaczaniem stężenia kreatyniny metodą Jaffe.
Tabela 1. Kryteria RIFLE (1, 2).
| Kryteria GFR | Kryteria diurezy |
| R - risk (ryzyko dysfunkcji nerek) |
Skrea x 1,5
lub
Ż GFR > 25% | D < 0,5 ml/kg/godz. x 6 godzin |
| I - injury (uszkodzenie nerek) | Skrea x 2
lub
Ż
GFR > 50% | D < 0,5 ml/kg/godz. x 12 godzin |
| F - failure (niewydolność nerek) | Skrea x 3
lub
Ż FR >
75%
lub
Skrea ł 4 mg/dl
Szybki wzrost o min. 0,5 mg/dl | Oliguria
D < 0,3 ml/kg/godz. x 24 godzin
lub anuria x 12 godzin |
| |
| L - loss (utrata, przedłużajaca się ONN)* |
| E - end-stage renal disease (schyłkowa niewydolność nerek)** |
*L – przedłużająca się NN, jest rozpoznawana, gdy istnieje konieczność stosowania leczenia nerkozastępczego dłużej niż 4 tygodnie
**E – schyłkowa niewydolność nerek jest rozpoznawana, gdy istnieje konieczność stosowania dializ dłużej niż 3 miesiące
GFR – glomerular filtration rate, przesączanie kłębuszkowe oceniane na podstawie obliczenia klirensu kreatyniny endogennej
Skrea – stężenie kreatyniny w surowicy
D – diureza
Tabela 2. Pediatryczna modyfikacja kryteriów RIFLE (3).
| Kryteria GFR | Kryteria diurezy |
| R - risk (ryzyko dysfunkcji nerek) | Ż kClkr o 25% | D < 0,5 ml/kg/godz. x 8 godzin |
| I - injury (uszkodzenie nerek) | Ż kClkr o 50% | D < 0,5 ml/kg/godz. x 16 godzin |
| F - failure (niewydolność nerek) | Ż kClkr o 75%
lub kClkr < 35 ml/min/1,73
m2 | D < 0,3 ml/kg/godz. x 24 godzlub anuria x 12 godzin |
| |
| L - loss (utrata, przedłużajaca się ONN)* |
| E - end-stage renal disease (schyłkowa niewydolność nerek)** |
kClkr – kalkulowany klirens kreatyniny (wg wzoru Szwartza)
*L – przedłużająca się NN, jest rozpoznawana, gdy istnieje konieczność stosowania leczenia nerkozastępczego dłużej niż 4 tygodnie
** E – schyłkowa niewydolność nerek jest rozpoznawana gdy istnieje konieczność stosowania dializ dłużej niż 3 miesiące
Epidemiologia ostrej niewydolności nerek
Nie prowadzono badań dotyczących częstości występowania ONN na dużych grupach dzieci. U ludzi dorosłych przeprowadzono takie badania, stwierdzając, że częstość występowania ONN wynosi 209/milion populacji (5). U dzieci w ciągu 8-letniej obserwacji w ośrodku 3. stopnia referencyjności stwierdzono występowanie ONN wymagającej dializ z częstością 0,8/100 000 populacji (6). W korelacji z wiekiem ONN najczęściej rozwija się u noworodków (6), u noworodków z innymi chorobami ONN występuje z częstością 8-24% (7).
Przyczyny ostrej niewydolności nerek
Zależnie od mechanizmu wywołującego zaburzenie funkcji nerek mówimy o przednerkowej, nerkowej i zanerkowej ONN.
Przednerkowa ONN, inaczej skąpomocz czynnościowy – wywołana jest spadkiem przepływu krwi przez nerki, nie jest związana z uszkodzeniem komórek.
Nerkowa ONN – występuje, gdy uszkodzeniu ulega jakakolwiek ze struktur budujących nerkę – naczynia, kłębuszek, cewka lub śródmiąższ.
Zanerkowa ONN – spowodowana jest zamknięciem dróg wyprowadzających mocz.
Przyczyny ONN przedstawiono na rycinie 1.
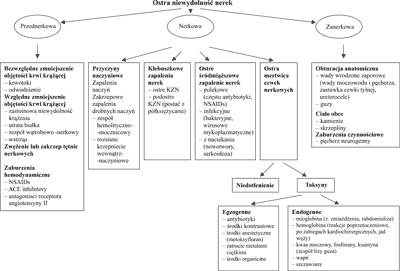
Ryc. 1. Przyczyny ostrej niewydolności nerek u dzieci (8, 18, 19).
Częstość występowania poszczególnych przyczyn ONN różni się w zależności od wieku, ale również od obszaru geograficznego, na którym są zbierane dane. Dlatego dla ustalenia rzeczywistej częstości poszczególnych przyczyn ONN u dzieci najbardziej obiektywne byłyby badania wieloośrodkowe.
Przyczyny ONN w zależności od wieku
Noworodki i niemowlęta
Najczęściej: przyczyny przednerkowe
Przednerkowa ONN:
– krwawienia okołoporodowe (przedwczesne odklejenie łożyska, skrwawienie do drugiego płodu, traumatyczny poród);
– krwawienia okresu noworodkowego (ciężkie krwawienia dokomorowe, krwawienia do nadnerczy);
– niedotlenienie okołoporodowe i zespół błon szklistych;
– niewydolność lewokomorowa.
Nerkowa ONN:
– ostra martwica cewek nerkowych (ATN – acute tubular necrosis) jako następstwo przednerkowej niewydolności nerek. Może również wystąpić na skutek stosowania leków przez matkę w okresie okołoporodowym (leki niesterydowe przeciwzapalne – NSAIDs, aminoglikozydy);
– inhibitory konwertazy angiotensyny (ACE inhibitory) przechodzą przez łożysko i mogą powodować ONN na podłożu zaburzeń hemodynamiki;
– martwica kory (w następstwie niedotlenienia okołoporodowego);
– zakrzep żył nerkowych;
– wady wrodzone nerek (dysplazja, torbielowatość nerek);
– kłębuszkowe zapalenia nerek występują w tym okresie bardzo rzadko, mogą być następstwem przechodzenia przez łożysko przeciwciał skierowanych przeciwko kłębuszkom płodu lub czynników infekcyjnych (kiła, wirus cytomegalii).
Zanerkowa ONN:
– należy brać pod uwagę przede wszystkim wady wrodzone układu moczowego (zastawka cewki tylnej, obustronna niedrożność moczowodów, pęcherz neurogenny).
Dzieci powyżej 12. miesiąca zycia
Najczęściej: przyczyny przednerkowe
Przednerkowa ONN:
– najczęstszą przyczyną hipowolemii w tym wieku są ostre choroby przewodu pokarmowego przebiegające z biegunką i wymiotami;
– przyczyną zmniejszonej perfuzji przez nerki są również wrodzone i nabyte choroby serca (również po operacjach).
Nerkowa ONN:
– zespół hemolityczno-mocznicowy (ZHM) – często wymieniany jako najczęstsza przyczyna ONN u dzieci poniżej 3 r.ż.;
– ostra martwica cewek nerkowych;
– ostre kłębuszkowe zapalenie nerek;
– ostre śródmiąższowe zapalenie nerek (infekcyjne, polekowe).
Zanerkowa ONN:
– wady wrodzone,
– kamica układu moczowego,
– ciała obce,
– nowotwory uciskające drogi wyprowadzające mocz.
Jak wspomniano na wstępie częstość występowania poszczególnych przyczyn ONN jest różna zależnie od miejsca zbierania danych. W 2005 r. opublikowano dane z Houston w Teksasie (10), w których analizowano przyczyny ONN u dzieci hospitalizowanych. Niedotlenienie było przyczyną ONN w 21%, środki farmakologiczne w 16%, posocznica w 11%, pierwotne choroby nerek tylko w 7% przypadków. U noworodków najczęstszą przyczyną ONN było niedotlenienie związane z operacjami kardiochirurgicznymi.
Podobnie, Bunchman (11) analizował przyczyny ONN u 226 dzieci leczonych nerkozastępczo w latach 1992-1998. Najczęstszymi przyczynami ONN w tej grupie były: wrodzone wady serca (w tym poddawane operacjom kardiochirurgicznym), ostra martwica cewek i posocznica. Wg danych z Leeds w Wielkiej Brytanii (12) najczęstszą przyczyną ONN u dzieci był ZHM, który powodował 45% wszystkich przypadków. W tym zestawieniu, podobnie jak w Houston (10), ONN u noworodków występowała najczęściej po operacjach kardiochirurgicznych. W krajach rozwijających się najczęstszą przyczyną ONN są choroby infekcyjne przebiegające z biegunką oraz malaria (13).
Na podstawie doniesień wydaje się, że główne przyczyny ONN u dzieci zmieniły się w ostatnich latach, przechodząc od dominujących w latach 80-tych pierwotnych chorób nerek do przyczyn wtórnych, będących konsekwencją chorób wielonarządowych oraz ich leczenia (10, 11, 12).
Patofizjologia
Przednerkowa ONN
Przepływ krwi przez nerki wynosi 25% rzutu serca. Większość przepływającej krwi kierowana jest do kory. W stanach hipowolemii, prowadzącej do obniżenia ciśnienia tętniczego zostają uruchomione mechanizmy neurohormonalne, mające na celu utrzymanie przepływu przez ważne dla życia narządy tj. serce i mózg. Zmniejszony przepływ krwi przez nerki uruchamia mechanizmy chroniące przesączanie kłebuszkowe:
– stopniowe rozszerzanie tętniczek doprowadząjących przez prostacyklinę (PGI2) (uruchamianą przez angiotensynę) oraz tlenek azotu;
– zwężenie tętniczki odprowadzajacej przez angiotensynę II.
Powoduje to przez pewien czas utrzymanie GFR w granicach normy. Jeśli czynniki powodujące zaburzony przepływ nie zostaną usunięte i hipoperfuzja nerek będzie się utrzymywać, dojdzie do skurczu naczynia doprowadzającego, skąpomoczu, a następnie rozwoju niedotlenieniowej martwicy cewek nerkowych.
Należy pamiętać, że stosowanie leków zaburzających autoregulację przepływu nerkowego, w sytuacji zmniejszonego przepływu może powodować szybszy rozwój martwicy cewek. Do leków tych należą:
– leki hamujące cyklooksygenazę (I i II) – (NSAIDs),
– ACE inhibitory i blokery receptora dla angiotensyny II (8, 14, 15).
Zanerkowa ONN
Mechaniczne zatkanie dróg wyprowadzających mocz powoduje wyrównanie ciśnień po obu stronach błony podstawnej kłębuszków i ustanie filtracji. Charakterystyczną cechą kliniczną stwierdzaną w zanerkowej niewydolności nerek jest pojawienie się wielomoczu po odblokowaniu dróg moczowych oraz występowanie hiperkaliemicznej nerkowej kwasicy cewkowej. Wielomocz występuje dopiero po pełnym odblokowaniu nerek i w niektórych przypadkach jest bardzo nasilony (u dorosłych do 20 l/dobę), i wymaga intensywnego nawadniania. Kwasica cewkowa hiperkaliemiczna rozwija się powoli w przebiegu zanerkowej ONN, ale ma tendencje do utrzymywania się po przywróceniu drożności dróg moczowych. Pacjenci po przebytej zanerkowej ONN z utrzymującą się hiperkaliemią wymagają wykonania badań w kierunku kwasicy cewkowej.
Martwica cewek nerkowych
Najbardziej charakterystyczną zmianą morfologiczną dla ostrej nerkowej niewydolności nerek (ONNN) jest martwica cewek nerkowych (acute tubular necrosis – ATN).
Najistotniejsze są dwa czynniki powodujące ostre zmniejszenie GFR w przypadku ATN:
1. Czynnik naczyniowy:
– skurcz naczyń doprowadzających ze spadkiem ciśnienia filtracyjnego. W ONNN dochodzi do utraty fizjologicznej autoregulacji, która polega na rozszerzeniu tętniczki doprowadzającej w przypadku zmniejszonego ciśnienia przepływającej krwi;
– przekrwienie zewnętrznej części rdzenia nerki;
– aktywacja cewkowo-kłębuszkowego sprzężenia zwrotnego.
2. Czynnik cewkowy
– uszkodzenie komórek cewkowych, zaburzenie apoptozy i procesów naprawczych;
– zatkanie światła cewek;
– przechodzenie przesączu pierwotnego do śródmiąższu;
– rozwój procesów zapalnych w obrębie śródmiąższu.
Redystrybucja krwi w obrębie nerki w okresie niedotlenienia powoduje przekrwienie zewnętrznych części rdzenia nerki. W trwającej ostrej martwicy cewek, nerkowy przepływ krwi jest zmniejszony o 30-50% i szczególnie dotyczy zewnętrznej części rdzenia. W warunkach fizjologicznych przez obszar ten przepływa mniejsza ilość krwi niż przez korę. W tym obszarze znajdują się segment S3 kanalika proksymalnego (końcowy odcinek) oraz gruba część zstępującego ramienia pętli Henlego, w których znajdują się komórki o dużej aktywności metabolicznej (zawierające Na/K ATP-azę), a więc zużywające dużą ilość tlenu i ulegające szczególnie łatwo uszkodzeniu w warunkach hipoksji.
Niedotlenienie nerki powoduje utratę integralności cytoszkieletu komórek, zaburzenie polarności komórek, odłączanie się rąbka szczoteczkowego cewek proksymalnych, przemieszczenie cząsteczek adhezyjnych oraz innych białek, apoptozę i śmierć komórek.
Charakterystycznymi cechami ATN są zaburzenia regulacji wydalania Na+ oraz wydalanie wraz z moczem komórek nabłonka cewek nerkowych. Zwiększone wydalanie Na+ wiąże się z przemieszczeniem Na/K ATP-azy z części podstawno-bocznej komórki do części wierzchołkowej. To przemieszczenie może tłumaczyć zmniejszony proces reabsorpcji sodu stwierdzany w martwicy cewek. Zmniejszony proces wchłaniania zwrotnego sodu w cewce proksymalnej zwiększa stężenie chlorku sodu w okolicy plamki gęstej.
W ciężkim uszkodzeniu dochodzi do złuszczania komórek cewek zarówno martwych, jak i zdolnych jeszcze do życia (około 30-70%). Oznacza to, że niedotlenienie nie powoduje śmierci wszystkich komórek cewek, ale znacząco zaburza ich strukturę komórkową.
Złuszczenie komórek cewek powoduje, że jedyną barierą oddzielającą przesącz pierwotny od śródmiąższu znajdującego się wokół cewek jest błona podstawna cewek. Dochodzi do bardzo charakterystycznego dla uszkodzenia cewek przechodzenia przesączu pierwotnego do śródmiąższu („moczenie nerki do nerki”). Obrzęk śródmiąższu powoduje ucisk na naczynia i stanowi dodatkowy czynnik pogarszający ukrwienie tkanek nerkowych. Nasilenie procesu „moczenia nerki do nerki” zależy od wzrostu ciśnienia wewnątrzcewkowego, zależnego od zatkania ich światła. Do zatykania światła cewek dochodzi zarówno przez komórki cewek, jak i przez „wysalające się” wałeczki. Wałeczki wewnątrz cewek nerkowych występujące w ostrej niewydolności nerek składają się głównie z białka Tamma-Horsfalla produkowanego w grubym odcinku pętli zstępującej. Białko Tamma-Horsfalla w dystalnych częściach nefronów, w obecności podwyższonego stężenia Na+ tworzy materiał podobny do żelu. W tworzeniu wałeczków poza białkiem Tamma-Horsfalla biorą udział komórki nabłonka cewek nerkowych zdolne do życia, a także obumarłe, błony rąbka szczoteczkowego oraz zewnątrzkomórkowej macierzy.
Ciężkie uszkodzenie komórek cewkowych powoduje szereg konsekwencji metabolicznych. Do najistotniejszych należą:
– nagłe zmniejszenie substancji wysokoenergetycznych (ATP). Skutkiem rozpadu ATP jest dysfunkcja komórek, a także wzrost stężenia adenozyny, która nasila skurcz naczyń i hipoksantyny, która sprzyja powstawaniu wolnych rodników w okresie reperfuzji,
– wzrost stężenia wolnych jonów Ca2+,
– wzrost stężenia wolnych rodników tlenowych,
– wzrost aktywności fosfolipazy A (przez wolne Ca2+),
– uwalnianie proteaz z komórek rąbka szczoteczkowego,
– przemieszczenie integryn z części podstawno-bocznych do wierzchołkowych, co przyczynia się do złuszczania komórek. Receptory integryn na częściach wierzchołkowych komórek powodują adhezję złuszczonych komórek do komórek pozostających na błonie podstawnej i po połączeniu się z sekwencją Arg-Gly-Asp (RGD – arginina, glicyna, kwas asparaginowy) białka Tamma-Horsfalla przyczyniają się do tworzenia wałeczków i zatkania światła cewek dystalnych.
Bezpośrednio po niedotlenieniu w cewkach proksymalnych wzrasta stężenie lipokaliny związanej z żelatynazą neutrofilów (NGAL – neutrophil gelatinase-associated lipocalin). NGAL pełni funkcje ochronne dla uszkodzonej komórki, wpływając na apoptozę, przyspieszając procesy naprawcze.
Istotny udział w patofizjologii ONN mają również procesy zapalne. W odpowiedzi zapalnej biorą udział komórki śródbłonkowe i nabłonkowe oraz leukocyty. Komórki uwalniając chemokiny i cytokiny (TNF-α, IL-18) uruchamiają kaskadę odpowiedzi zapalnej. Ostrej martwicy cewek nerkowych towarzyszy aktywacja dopełniacza na drodze alternatywnej.
Tlenek azotu gra podwójną rolę w patogenezie niedotlenieniowej niewydolności nerek. Ostre niedotlenienie powoduje wzrost ekspresji indukowalnej syntazy tlenku azotu (iNOS), zwiększona ilość tlenku azotu może przyczyniać się do uszkodzenia cewek. Efekty naczyniowe wywierane przez śródbłonkową syntazę tlenku azotu (eNOS) w tętniczkach doprowadzających chronią kłębuszek przed uszkodzeniem, to działanie może mieć w sumie większe znaczenie w momencie uszkodzenia nerki. NO zmniejsza wytwarzanie eNOS i indukuje syntezę oksygenazy hemu typu pierwszego, który działa cytoprotekcyjnie w momencie uszkodzenia (8, 14, 15).
Nie do końca poznane są mechanizmy powodujące zmniejszenie przesączania kłębuszkowego w odpowiedzi na uszkodzenie cewek nerkowych. Na spadek GFR wpływają na pewno:
– zwiększenie stężenia Na+ w okolicy plamki gęstej i w wyniku tego skurcz tętniczki doprowadzającej,
– zmniejszenie ciśnienia filtracyjnego w kłębuszku nerkowym na skutek wzrostu ciśnienia w świetle cewek, co jest skutkiem tworzenia się trudno usuwalnych wałeczków,
– obrzęk tkanki śródmiąższowej i wzrost ciśnienia śródcewkowego na skutek „moczenia się nerki do nerki”.
Procesy naprawcze
W warunkach eksperymentalnych wkrótce po indukcji ATN wiele komórek pozostających w fazie spoczynkowej rozpoczyna cykl komórkowy. Mogą one wejść na drogę przemian rozpoczynających procesy naprawcze, albo przyspieszających śmierć komórki.
Decyzja o drodze obranej przez komórkę w cyklu komórkowym jest ściśle regulowana, ważną rolę w tej regulacji odgrywają inhibitory kinaz, szczególnie p21.
Pierwszą fazą naprawy jest infiltracja granulocytów obojętnochłonnych i monocytów, która następuje na skutek działania czynników wzrostu. W drugiej fazie główną rolę grają słabo zróżnicowane komórki nabłonkowe, które reprezentują populację komórek macierzystych w obrębie nerek. W trzecim, ostatnim, stadium naprawy, w którym również istotną rolę grają czynniki wzrostowe stwierdza się wzrost proliferacji żywych komórek cewek proksymalnych. Komórki cewek odzyskują swój prawidłowy zróżnicowany charakter.
Procesy regeneracyjne trwają około 6 tygodni, reabsorpcja Na+ ulega normalizacji po 10 dniach, glukozy po około 17.
Podsumowując, wiedza na temat zmian w komórkach cewek nerkowych pod wpływem niedotlenienia jest coraz szersza i wzbogaca się systematycznie dzięki pracom doświadczalnym na zwierzętach. Nadal jednak nie ma spójnej teorii powstających zmian, a zwłaszcza brak przełożenia poznanych już faktów patofizjologicznych na język kliniki, co pozwoliłoby na skuteczniejsze leczenie (8, 14, 15).
Objawy i rozpoznawanie ONN u dzieci
U dziecka z ONN występuje:
– Zmniejszenie lub ustanie oddawania moczu.
Skąpomocz (oliguria)
– u dzieci <0,5 ml/kg/godz.
– u niemowląt <1,0 ml/kg/godz.
U starszych dzieci oliguria <400 ml/m2/dobę, bezmocz <100 ml/m2/dobę.
– Retencja wody i produktów przemiany azotowej
– Nadciśnienie tętnicze
– Zaburzenia elektrolitowe
– Kwasica metaboliczna
Poza ww. objawami u dziecka występują objawy typowe dla danej przyczyny ONN.
Diureza
Ilość oddawanego moczu generalnie słabo koreluje z przyczyną ONN. Można jednak zwrócić uwagę na to, że:
– anuria – występuje w zanerkowej ONN, przy całkowitym zamknięciu dróg wyprowadzających mocz, w zakrzepie tętnic nerkowych, gwałtownie postępującym kłębuszkowym zapaleniu nerek,
– oliguria – jest sytuacją występującą najczęściej w ONN, stąd mało różnicującą,
– brak zmian w ilości oddawanego moczu (postacie nieoliguryczne ONN)– główna postać ONN u noworodków. Występuje też w ostrym śródmiąższowym zapaleniu nerek, ONN spowodowanej środkami kontrastowymi, rabdomiolizie, zanerkowej ONN z niepełną okluzją dróg wyprowadzających mocz.
Badanie podmiotowe
W wywiadzie należy uwzględnić przebycie chorób poprzedzających wystąpienie ONN: anginy lub innej infekcji dróg oddechowych ok. 2 tygodnie przed zachorowaniem, infekcyjnych zmian skórnych ok. 3 tyg. przed zachorowaniem, biegunki (ważny charakter oddawanych stolców, czy nie było domieszki krwi), sytuacji, mogących spowodować przednerkową ONN. Bardzo istotne jest przeprowadzenie wywiadu w kierunku możliwości kontaktu z ewentualnymi toksynami (farby, lakiery) oraz stosowanymi lekami.
Badanie przedmiotowe
Biorąc pod uwagę wysoką śmiertelność, ONN należy traktować jak stan zagrożenia życia. W badaniu przedmiotowym należy w pierwszym rzędzie ocenić czy u dziecka w danym momencie nie występują groźne dla życia objawy.
1. Ocenić stopień nawodnienia: czy dziecko jest istotnie odwodnione, czy masywnie przewodnione. Równocześnie ocenić kolor skóry (znaczna bladość – niedokrwistość, żółtaczka – hiperbilirubinemia) i ewentualne zmiany skórne (wybroczyny, wylewy krwawe mogą świadczyć o skazie krwotocznej).
2. Osłuchiwaniem klatki piersiowej należy stwierdzić czy dziecku nie zagraża niebezpieczeństwo wystąpienia obrzęku płuc. Równocześnie należy ocenić sposób oddychania (cechy niewydolności oddechowej, oddech Kussmaula).
3. Ocenić akcję serca: bradykardia – hiperkaliemia, tachycardia – hipowolemia, zagrażający wstrząs, znacznego stopnia niedokrwistość. Zaburzenia rytmu serca mogą sugerować znacznego stopnia zaburzenia elektrolitowe.
4. Zmierzyć ciśnienie tętnicze: bardzo niskie ciśnienie – zagrażający wstrząs, wysokie ciśnienie tętnicze – zagrożenie przełomem nadciśnieniowym.
Stwierdzenie któregokolwiek z objawów zagrażających życiu powoduje wdrożenie leczenia przed ukończeniem diagnostyki. Po wykluczeniu objawów groźnych dla życia należy starannie zebrać wywiad i dokończyć badanie przedmiotowe.
W badaniu przedmiotowym poza oceną ważnych dla życia objawów należy zwrócić uwagę na zmiany mogące przybliżyć przyczynę wystąpienia ONN. Obrzęki stawów, zmiany skórne mogą sugerować choroby układowe, uogólnione zapalenia naczyń. Cechy kliniczne niewydolności wątroby (żółtaczka, obrzęki, hepatomegalia) mogą sugerować wystąpienie zespołu wątrobowo-nerkowego.
Badania laboratoryjne u dziecka z ONN
W większości przypadków dziecko z ONN wymaga założenia cewnika Foley´a w celu pobrania próbki moczu do badania oraz możliwości starannego monitorowania ilości oddawanego moczu. Dziecku z ONN należy pobrać mocz i krew na badania laboratoryjne. Mocz wysyłamy na badanie ogólne, określenie stężenia Na, kreatyniny i posiew.
Krew pobieramy na oznaczenie: morfologii krwi obwodowej, stężenia mocznika, kreatyniny, bilirubiny, cukru, białka całkowitego, albumin, elektrolitów (Na, K, Ca, P), aktywności transaminaz, gazometrii oraz markera stanu zapalnego (OB, CRP).
Interpretacja badania moczu w ONN
Badanie mikroskopowe osadu moczu:
– prawidłowe – przednerkowa i zanerkowa ONN;
– leukocyturia, wałeczki granulocytarne, leukocytarne – ostra martwica cewek, kłębuszkowe zapalenia nerek, ostre śródmiąższowe zapalenie nerek, odmiedniczkowe zapalenie nerek;
– erytrocyturia, wałeczki eytrocytarne – kłębuszkowe zapalenie nerek, ZHM;
– eozynofiluria – ostre alergiczne śródmiąższowe zapalenie nerek;
– krystaluria – acyklovir, sulfonamidy, metotrexat, zatrucie glikolem etylenowym, środki kontrastowe.
Na podstawie oznaczenia stężenia Na i kreatyniny w moczu i w surowicy należy wyliczyć frakcjonowane wydalanie przefiltrowanego w kłębuszkach Na (FENa):
Na w moczu x kreatynina w osoczu
---------------- X 100
Na w osoczu x kreatynina w moczu
Klinicznie czasem trudno stwierdzić, czy mamy do czynienia z przednerkową ONN, czy doszło już do martwicy cewek nerkowych. W różnicowaniu należy uwzględnić parametry zestawione w tabeli 3.
Tabela 3. Różnicowanie przednerkowej ONN (skąpomoczu czynnościowego) i martwicy cewek.
| Przednerkowa ONN | Martwica cewek |
| Ciężar właściwy moczu | > 1018 | < 1012 |
| Osmolalność moczu (mOsm/kg) | > 500 | < 500 |
| Na w moczu (mmol/l) | < 20 | > 40 |
| FENA* | < 1 | > 1 |
| Mocznik w moczu/mocznik w surowicy | > 10 | < 10 |
| FE mocznika** | < 35 | > 35 |
| Osad moczu | prawidłowy, czasem wałeczki szklistei ziarniste | komórki nabłonkowe cewek nerkowych, wałeczki ziarniste, wałeczki typu "muddy brown" |
*u noworodków FENa> 2,5% wskazuje na martwicę cewek, u wcześniaków <32 Hbd współczynnik FENa jest nieprzydatny w różnicowaniu ONN, ponieważ jest zwykle wyższy niż 2,5%.
**parametr przydatny u pacjentów, u których stosowano leki moczopędne. Utrzymywanie się FE mocznika <35 wskazuje na zachowaną funkcję cewek.
Interpretacja wyników innych badań laboratoryjnych
Stężenie kreatyniny jest podstawowym parametrem w rozpoznawaniu ONN. Należy pamiętać, że sprawnie działające cewki nerkowe wydalają kreatyninę w sytuacji niewydolności nerek, stąd w przednerkowych postaciach (również w zespole nerczycowym) stężenie kreatyniny nie jest bardzo wysokie. Oznaczenie stężenia kreatyniny pozwala na obliczenie wartości GFR za pomocą wzoru Schwartza (16, 17):
GFR (ml/min/1,73 m2) = K x wzrost w cm/stężenie kreatyniny w mg/dl,
gdzie współczynnik K = 0,33 – niemowlęta z małą masą urodzeniową,
0,45 – niemowlęta z prawidłową masą urodzeniową,
0,55 – dzieci 2-12 lat,
0,55 – dziewczynki od 13 r.ż.,
0,70 – chłopcy od 13 r.ż.
Stężenie mocznika zależy nie tylko od GFR, ale również od generacji wątrobowej i od poziomu katabolizmu (poziom mocznika jest obniżony w ciężkiej niewydolności wątrobowej lub niedożywieniu).
W morfologii krwi obwodowej należy zwrócić uwagę na poziom hematokrytu (wysoki w odwodnieniu, niski w przewodnieniu i niedokrwistości), hemoglobiny (może być bardzo niski w zespole hemolityczno-mocznicowym), liczbę leukocytów (leukocytoza jest obserwowana często w ONN, wysokie wartości świadczą o infekcji; leukopenia może występować w toczniu uogólnionym), płytek krwi (trombocytopenia zawsze w ZHM, często w posocznicy), liczbę granulocytów kwasochłonnych (eozynofilia sugeruje śródmiąższowe zapalenie nerek, guzkowe zapalenie tętnic).
Wzrost aktywności transaminaz sugeruje uszkodzenie komórki wątrobowej, podwyższony poziom bilirubiny występuje w ZHM.
Charakterystyczne dla ONN zaburzenia jonowe to hiponatremia, hipokalcemia i hiperkaliemia. W dłużej utrzymującej się ONN może wystąpić hiperfosfatemia. Hiponatremia przede wszystkim wynika z przewodnienia, ale należy pamiętać, że przy uszkodzeniu cewek dochodzi do rzeczywistej utraty sodu. Hipokalcemia przede wszystkim zależy od towarzyszącej hipoproteinemii, z czasem rozwija się rzeczywisty niedobór wapnia, wynikający z niedoboru aktywnego metabolitu witaminy D. Hiperkaliemia jest najgroźniejszym zaburzeniem jonowym w ONN i wynika z zaburzonego wydalania przez uszkodzone cewki.
Stałym objawem ONN jest kwasica metaboliczna, która jest wynikiem zaburzonych mechanizmów alkalizujących nerek.
Badania obrazowe u dziecka z ONN
Niezbędne jest wykonanie badania USG jamy brzusznej, na podstawie którego można wykluczyć obecność guza czy wady układu moczowego. USG jest również przydatne dla różnicowania czy mamy do czynienia z ONN czy zaostrzeniem przewlekłej choroby nerek (PChN). W ONN (nerkowej) nerki są duże, często z zaburzonym zróżnicowaniem korowo-rdzeniowym. W PChN nerki są małe lub zawierają torbiele.
Badanie radiologiczne klatki piersiowej pozwala na wykluczenie znacznego stopnia przewodnienia, w tym obrzęku płuc. Zdjęcie klatki piersiowej musi być również wykonane dla wykluczenia zmian typowych dla ziarniniaka Wegenera czy zespołu Goodpasture´a.
Dalsze badania obrazowe jak tomografia komputerowa, urografia czy cystografia wykonywane są tylko w wybranych przypadkach, szczególnie przy podejrzeniu wady układu moczowego.
Biopsja nerki wykonywana jest w ONN rzadko. Tylko sytuacje niejasne klinicznie mogą wymagać mikroskopowego badania wycinka nerki. Wykonanie biopsji jest natomiast niezbędne, jeśli u dziecka trzeba przeprowadzić różnicowanie między ostrym i podostrym (gwałtownie postępującym, z półksiężycami) kłębuszkowym zapaleniem nerek.
W tabeli 4. przedstawiono różnicowanie różnych postaci ONN, najczęściej spotykanych u dzieci.
Tabela 4. Różnicowanie ONN (18, 19).
| Przednerkowa ONN | Ostra martwica cewek | Kłębuszkowe zapalenie nerek | Zespół hemolityczno--mocznicowy | Śródmiąższowe zapalenie nerek |
| Diureza | oliguria | oliguria, rzadziej postacie nieoliguryczne | oliguria,w gwałtownie postępującym KZN może być anuria | oliguria lub anuria | zwykle postacie nieoliguryczne |
| Badanieogólne moczu | prawidłowe | nabłonki, wałeczki | białkomocz, krwinkomocz, abakteryjna leukocyturia, wałeczki | krwinkomocz, białkomocz, często elementy ostrej martwicy cewek, czyli liczne nabłonki | eozynofiluria, leukocyturia, niewielki białkomocz, glikozuria |
| FENA | < 1 | > 1 | < 1 | jeśli towarzysząca martwica cewek > 1,jeśli nie < 1 | > 1 |
| Na w moczu (mmol/l) | < 20 | > 40 | < 20 | jeśli towarzysząca martwica cewek > 40 | > 40 |
| Inne objawy | w wywiadzie różne sytuacje mogące doprowadzić do zmniejszeniaobjętości śródnaczyniowej | jak w przednerkowej ONN | poprzedzająca infekcja, ASO +
Ż C3w OKZN, przeciwciałaanty GBM, przeciwjądrowe, ANCA | poprzedzająca biegunka, często krwotoczna w typowym ZHM, trombocytopenia+ niedokrwistość hemolityczna | infekcje poprzedzające, często rzadkie, również pasozytnicze, pierwotniakowe, leki, eozynofilia |
Markery ONN
Trwają poszukiwania markerów, które mogłyby posłużyć do wczesnego rozpoznawania ONN. Oznaczanie substancji, których stężenie we krwi lub moczu rośnie wcześniej niż stwierdza się wzrost stężenia kreatyniny jest szczególnie istotne u pacjentów narażonych na wystąpienie ONN, czyli u pacjentów w OIT lub po przeszczepieniu nerki.
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
24 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
59 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
119 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 28 zł
Piśmiennictwo
1. Bellomo R et al.: Palevsky and the ADQI workgroup. Acute renal failure - definition, outcome measures, animal models, fluid therapy and information technology needs: the Second International Consensus of the Acute Dialysis Quality Initiative (ADQI) Group. Critical Care 2004; 8: R204-R212. 2. Mehta RL et al.: Acute Kidney Injury Network (AKIN): report of an initiative to improve outcomes in acute kidney injury. Cri Care 2007; 11: R31. 3. Akcan-Arikan A et al.: Modified RIFLE criteria in critically ill children with acute kidney injury. Kidney Int 2007; 71: 1028-1035. 4. Askenazi DJ, Ambalavanan N, Goldstein SL: Acute kidney injury in critically ill newborn: What do we know? What do we need to learn? Pediatr Nephrol 2009; 24: 265-274. 5. Liano F, Pascual J, Madrid Acute Renal Failure Study Group: Epidemiology of acute renal failure: a prospective, multicenter study community-based study. Kidney Int 1996; 50: 811-818. 6. Moghal NE, Brocklebank JT, Meadow SR: A review of acute renal failure in children: incidence, etiology and outcome. Clin Nephrol 1998; 49: 91-95. 7. Andreoli SP: Acute renal failure in the newborn. Semin Perinatol. 2004; 8: 112-123. 8. Lameire N, Van Biesen W, Vanholder R: Acute renal failure. Lancet 2005; 365: 417-430. 9. Sieniawska M, Roszkowska-Blaim M: Ostra niewydolność nerek. Nefrologia dziecięca pod red. M. Sieniawskiej i T. Wyszyńskiej. OINPHARMA. Warszawa 2004; 11-26. 10. Hui-Sticle S, Brewer ED, Goldstein SL: Pediatric ARF epidemiology at a tertiary care center from 1999 to 2001. Am J Kidney Dis. 2005; 45: 96-101. 11. Bunchman TE et al.: Pediatric acute renal failure: outcome by modality and disease. Pediatr Nephrol. 2001; 16(12): 1067-1071. 12. Moghal NE, Brocklebank JT, Meadow SR: A review of acute renal failure in children: incidence, etiology and outcome. Clin Nephrol 1998; 49: 91-95. 13. Cerdá J et al.: The contrasting characteristics of acute kidney injury in developed and developing countries. Nat Clin Pract Nephrol 2008; 4(3): 138-153. 14. Liu KD, Brakeman PR: Renal repair and recovery. Crit Care Med 2008; 36(4): S187-S192. 15. Andreoli S.P. Acute kidney injury in children. Pediatr Nephrol 2009; 24: 253-263. 16. Schwartz GJ et al.: A simple estimate of glomerular filtration rate in children derived from body length and plasma creatinine. Pediatrics 1976; 58(2): 259-263. 17. Bassam AA, Dabbagh SS, Gruskin AB: Ocena czynności nerek u dzieci. Pediatrics in Review (wydanie polskie) 1997; 1(5): 19-28. 18. Laine J: Acute renal failure: presentation w European Society for Paediatric Nephrology Handbook. ESPN 2002, redakcja P. Cochat. str 322-324. 19. Sieniawska M, Roszkowska-Blaim M: Ostra niewydolność nerek. Nefrologia dziecięca pod red. M. Sieniawskiej i T. Wyszyńskiej. OINPHARMA. Warszawa 2004; 11-26. 20. Devarajan P: Emerging urinary biomarkers in the diagnosis of acute kidney injury. Expert Opin Med Diagn. 2008; 2(4): 387-398. 21. Buyan N, Latta Et:Management of acute renal failure w European Society for Paediatric Nephrology Handbook pod red. P. Cochat ESPN 2002; 325-328. 22. Grzywna W: Nieprawidłowości w gospodarce elektrolitowej noworodka. [W:] Świetliński J, Grzywna W: Zaburzenia homeostazy u noworodka.a-medica press. Bielsko-Biala 1998; 95-134. 23. Friedman PA: Czynniki wpływające na homeostazę mineralną i metabolizm kości. Farmakologia Goodmana & Gilmana pod red. Brunton LL, Lazo JS, Parker KL. Czelej Lublin 2007; tom II 1767-1800. 24. Grenda R: Leczenie nerkozastępcze u dzieci. Wybrane zagadnienia z nefrologii dziecięcej pod red. R. Grendy Wydawnictwo Lekarskie PZWL. Warszawa 2003; 178-204. 25. Bagshaw SM, Bellomo R, Kellum JA: Oliguria, volume overload, and loop diuretics. Crit Care Med 2008; 36(4): S172-S178. 26. Bellomo R et al.: Low-dose dopamine in patients with early renal dysfunction: a placebo-controlled randomized trial. Australian and New Zealand Intensive Care Society (ANZICS) Clinical Trials Group. Lancet 2000; 356(9248): 2139-2143. 27. Lauschke A et al.: ?Low-dose´ dopamine worsens renal perfusion in patients with acute renal failure. Kidney Int 2006; 69(9): 1669-1674. 28. Landoni G et al.: Beneficial impact of fenoldopam in critically ill patients with or at risk for acute renal failure: a meta-analysis of randomized clinical trials. Am J Kidney Dis 2007; 49(1): 56-68. 29. Knoderer CA et al.: Fenoldopam for acute kidney injury in children. Pediatr Nephrol. 2008; 23(3): 495-498. 30. Moffett BS et al.: Renal effects of fenoldopam in critically ill pediatric patients: A retrospective review. Pediatr Crit Care Med 2008; 9(4): 403-406. 31. McClure RJ, Prasad VK, Brocklebank JT: Treatment of hyperkalaemia using intravenous and nebulised salbutamol. Arch Dis Child 1994; 70(2): 126-128. 32. Bagshaw SM et al.: Continuous versus intermittent renal replacement therapy for critically ill patients with acute kidney injury: A meta-analysis. Crit Care Med 2008; 36(2): 610-617. 33. Symons JM et al.: Demographic Characteristics of Pediatric Continuous Renal Replacement Therapy: A Report of the Prospective Pediatric Continuous Renal Replacement Therapy Registry. Clin J Am Soc Nephrol 2007; 2: 732-738. 34. Van Biesen W, Lameire N, Vanholder R: A tantalizing question: Ferrari or Rolls Royce? A meta-analysis on the ideal renal replacement modality for acute kidney injury at the intensive care unit. Crit Care Med 2008; 36(2): 649-650. 35. Goldstein SL et al.: "Mild" renal insufficiency is associated with poor outcome in children with acute decompensated heart failure: evidence for a pediatric cardio-renal syndrome. J Am Soc Nephrol 2005; 16: 534A. 36. Feltes CM, Van Eyk J, Rabb H: Distant-organ changes after acute kidney injury. Nephron Physiol 2008; 109(4): p80-p84. 37. Bresolin N et al.: Prognosis for children with acute kidney injury in the intensive care unit. Pediatr Nephrol 2009; 24: 537-544. 38. Askenazi DJ et al.: 3-5 year longitudinal follow-up of pediatric patients after acute renal failure. Kidney Int 2006; 69: 184-189. 39. Abitbol CL et al.: Long-term follow-up of extremely low birth weight infants with neonatal renal failure. Pediatr Nephrol 2003; 18: 887-893.

