© Borgis - Postępy Nauk Medycznych 3/2009, s. 214-224
*Adam Kiciak, Katarzyna Borycka, Krzysztof Bielecki
Pooperacyjne zaburzenia motoryki górnego odcinka przewodu pokarmowego na modelu zwierzęcym
Postoperative upper gut motility disorders in animal model
Klinika Chirurgii Ogólnej i Przewodu Pokarmowego Centrum Medycznego Kształcenia Podyplomowego w Warszawie
Kierownik Kliniki: prof. dr hab. med. Krzysztof Bielecki**
Streszczenie
Na modelu zwierzęcym badano aktywność mioelektryczną i liczbę śródmiąższowych komórek Cajala (ICC) w górnym odcinku przewodu pokarmowego po dwóch grupach procedur chirurgicznych: wytworzeniu pętli Roux-en-Y i „un-cut”Roux oraz pankreatoduodenektomii sposobami Whipple´a i Longmire-Traverso, w odniesieniu do wyników klinicznych mierzonych zmianami masy ciała i występowaniem objawów opóźnionego pasażu żołądkowego.
Materiał i metody: U dwudziestu czterech świń rasy wielkiej białej polskiej (10-13 kg) w znieczuleniu ogólnym z zastosowaniem halotanu, wykonano po dwie operacje: pierwszą wszczepienia elektrod bipolarnych i implantów do pomiarów telemetrycznych pozwalających na ciągły zapis aktywności mioelektrycznej, a po tygodniu, drugą – odpowiednio wytworzenia pętli Roux-en-Y (n=6) i „un-cut”Roux oraz pankreatoduodenektomii sposobami Whipple´a (n=6) i Longmire-Traverso (n=6). Po dwu-, trzytygodniowym okresie pooperacyjnej obserwacji i po zakończeniu protokołu pomiarów, od zabitych zwierząt pobierano próbki tkanek do znakowania komórek Cajala.
Wyniki: Regularne MMC (wędrujący kompleks mioelektryczny) powróciły średnio po 10,5 godzinach u świń w grupie „un-cut”Roux i po średnio 37 godzinach w grupie Roux-en-Y (p=0,02) oraz średnio po 68 h i 27 h odpowiednio w grupach Whipple i Longmire-Traverso (p=0,002). Świnie z grupy „un-cut”Roux zwiększyły swoją masę ciała średnio o 18,0% w odniesieniu do wagi wstępnej mierzonej przed operacją wobec średnio 7,3% wzrostu w grupie Roux-en-Y po dwóch tygodniach obserwacji (p≤0,05); w grupach zwierząt po pankreatodudenectomiach nie obserwowano istotnych różnic w odniesieniu do masy ciała. Stwierdzono bezpośrednią pozytywną zależność między ilością komórek Cajala zlokalizowanych w obrębie splotu Auerbacha i powrotem regularnego MMC w obrębie poszczególnych grup. Wykazano, że im większa gęstość występowania wspomnianych komórek, co zaobserwowano w grupie „un-cut”Roux, tym mniejsza ilość pooperacyjnych zrostów wewnątrz jamy brzusznej po upływie dwóch tygodni od operacji. Co więcej, sieć komórek Cajala w okolicy zespolenia i dystalnie od niego była bardziej zniszczona po operacji Whipple´a w porównaniu z operacją Longmire-Traverso.
Wnioski: Zachowanie ciągłości przewodu pokarmowego i sieci komórek Cajala może mieć istotne znaczenie w pooperacyjnym powrocie do zdrowia, na modelu zwierzęcym.
Summary
We designed a conscious pig model to investigate myoelectric activity and number of interstitial cells of Cajal (ICC) in the proximal jejunum following two groups of surgical procedures: Roux-en-Y and "un-cut”Roux loop creation and Whipple and Longmire-Traverso pancreatoduodenectomies in relation to clinical outcomes measured by body weight changes and presence of delayed gastric emptying symptoms.
Materials and Method s: Twenty four male Polish White pigs (10-13 kg) were operated under general halothane anesthesia first to implant bipolar electrodes and telemetry transmitters for continuous electromyography recordings and then, after one week recovery, to create Roux-en-Y (n=6) and "un-cut”Roux (n=6) loops and Whipple (n=6) and Longmire-Traverso (n=6) pancreatoduodenectomies. Upper gut tissue specimens were taken for an anti-human CD-117 staining procedure to quantitatively identify the presence of interstitial cells of Cajal.
Results: The intestinal migrating motor complex (MMC) was restored within 10.5 h and 37 h in "un-cut”Roux and Roux-en-Y pigs, respectively (p=0.02) and within 68 h in Whipple and 27 h in Longmire-Traverso pigs, respectively (p=0.002). During two weeks, the "un-cut”Roux piglets increased their body weight by 18.0%, whereas the Roux-en-Y piglets, by 7.3% (p≤0.05); no statistically significant change in body weight between Whipple and Longmire-Traverso group was observed. Two weeks after surgery, the number of ICC located in the region of Auerbach´s plexus was higher and adhesions in the abdominal cavity lower in the "un-cut”Roux group; it was noticed that Cajal cells net in the vicinity of anastomosis and distally from it presented greater destruction after Whipple operation in relation to Longmire-Traverso one. A direct positive relation between the amount of ICC located in the region of Auerbach´s plexus and restoration of regular MMC cycle among the same group and between the groups of animal were noted.
Conclusions: In the pig model, preservation of smooth muscle and ICC network continuity in the proximal jejunum may play an important role in early post-surgical recovery.

Wstęp
Motoryka przewodu pokarmowego jest przedmiotem intensywnych badań, w trakcie których wykorzystywany jest fakt, że aktywność elektryczna mięśni gładkich dobrze odzwierciedla motorykę i może służyć do jej oceny. Sama motoryka przewodu pokarmowego odgrywa ważną rolę w procesie trawienia poprzez kontrolowanie pasażu pokarmu w górnym odcinku przewodu pokarmowego, co zapewnia optymalne warunki dla enzymatycznego trawienia w żołądku i jelicie cienkim. Jednakże żaden potencjał czynnościowy i w konsekwencji skurcz mięśni nie może zostać wyzwolony bez obecności elektrycznego rytmu podstawowego (1, 2). Ten ostatni jest wytwarzany przez śródmiąższowe komórki Cajala, które uważane są za komórki rozrusznikowe dla elektrycznych fal wolnych (3). Morfologiczne i elektrofizjologiczne badania komórek Cajala wykazały, że są one zarówno ściśle związane ze sobą, jak i pobudzającymi i hamującymi gałązkami nerwowymi w obrębie przewodu pokarmowego. Funkcjonalnie, działając jako sieć, służą jako elektryczny rozrusznik odpowiedzialny za generowanie i propagację fal wolnych. Znakiem dobrostanu przewodu pokarmowego jest wędrujący kompleks mioelektryczny (MMC) – wzorzec motoryki jelit szeroko obecny w okresie głodzenia i żywienia tak u ludzi, jak i u zwierząt (4, 5). W badaniach na psach (6, 7, 8, 9, 10) wykazano, że okolica rozrusznikowa żołądka zlokalizowana jest na krzywiźnie większej żołądka w górnej 1/3 trzonu, zajmując 20% jego obwodu i generuje fale wolne z częstością 3-4/minutę. Koncepcja istnienia „rozrusznika dwunastniczego” powstała w wyniku obserwacji Diamanta i Bortoffa (11) częstotliwości potencjałów rozrusznikowych jelita cienkiego. Koncepcja ta została potwierdzona identyfikacją nadrzędnej okolicy rozrusznikowej (12, 13) w opuszce dwunastnicy, w odległości około 5-6 mm od odźwiernika. Wykazano, że w warunkach fizjologicznych większa częstość generowanych dwunastniczych potencjałów rozrusznikowych zapewnia propagację tych potencjałów wzdłuż jelita, od okolicy rozrusznikowej w kierunku dystalnym, co koordynując czynność motoryczną jelita czyni ją skuteczną siłą oczyszczającą jelito z resztek pokarmowych.
W ostatnich latach pojawiły się doniesienia o roli komórek Cajala w patogenezie zaburzeń motorycznych. Uszkodzenie sieci komórek Cajala powoduje zaburzenia w generowaniu i przewodzeniu impulsów elektrycznych (BER) w górnym odcinku przewodu pokarmowego, a w konsekwencji – zaburzenia motoryki przewodu pokarmowego (14). Operacyjne przecięcie jelita, przerywające ciągłość sieci komórek Cajala, zaburza potencjały rozrusznikowe przez przerwanie propagacji i zmniejszenie ich częstości w jelicie czczym (15). Poniżej zespolenia uaktywniają się ekotopowe ośrodki rozrusznikowe. Wstecznie rozchodzące się potencjały rozrusznikowe i wywołane przez nie wsteczne fale perystaltyczne upośledzają pasaż treści jelitowej i czynią niewydolnym mechanizm odbioru jelitowego wspomagający opróżnianie żołądkowe (16, 17).
Operacyjne wytworzenie pętli Roux wymaga przecięcia jelita cienkiego i przerwania ciągłości sieci komórek Cajala, co w konsekwencji prowadzi do zaburzeń przewodzenia potencjałów rozrusznikowych przerywając ich propagację i zmniejszając częstotliwość w pętli Roux. Następnie, ektopiczne rozruszniki rozwijają się w pętli Roux, a dogłowowa propagacja potencjałów rozrusznikowych i jako jej konsekwencja, dogłowowa propagacja skurczów skutkuje w wolniejszym przemieszczaniu się treści w wytworzonej pętli (16, 17). Prowadzi to do powstania zespołu pętli Roux (uczucie pełności w nadbrzuszu, ból brzucha, nudności, wymioty) (18, 19).
Aby zapobiec powstawaniu zespołu pętli Roux, zaprojektowano zespolenie żołądkowo-jelitowe sposobem „un-cut”Roux. „Un-cut”Roux jest wytwarzane przez zespolenie pętli jelita cienkiego z żołądkiem i zamknięcie pętli doprowadzającej za pomocą staplera poprzecznego. Zamknięcie staplerem zapobiega refluksowi żółciowemu i, według teorii, umożliwia niezmienioną migrację potencjałów rozrusznikowych (20). W badaniach na psach, operacja sposobem „un-cut”Roux zapobiegała powstawaniu ektopicznych rozruszników w pętli Roux i przyspieszała opóźnione opróżnianie opisywane w konwencjonalnym zespoleniu żołądkowo-jelitowym sposobem Roux (14).
Aktualnie, najczęściej wykonywanymi sposobami pankreatoduodenektomii są procedury Whipple´a i Longmire-Traverso. Mimo licznych sprzecznych doniesień w literaturze, wśród klinicystów utrzymuje się pogląd o przewadze operacji oszczędzającej nad standardową. Argumentami są: łatwiejsza technika operacyjna, niższy odsetek powikłań i mniejsza śmiertelność w przebiegu pooperacyjnym. Uważa się też, że zachowanie nienaruszonej czynnościowej jednostki motorycznej (odźwiernika i początkowego odcinka dwunastnicy) zapewnia lepsze opróżnianie żołądkowe, dzięki czemu po operacji obserwuje się mniej zaburzeń motoryki przewodu pokarmowego, refluksu żołądkowo-jelitowego i objawów zespołu poposiłkowego ( dumping syndrom). Z ostatnich badań (21, 22, 23) wynika jednak, że obie metody – oszczędzająca i standardowa – wiążą się z porównywalnym odsetkiem śmiertelności i powikłań pooperacyjnych, są jednakowo skuteczne w leczeniu przewlekłego zapalenia trzustki i nowotworów okolicy okołobańkowej oraz mają jednakowe przeżycia w obserwacji długoterminowej.
Aktualnie pankreatoduodenektomia wykonywana jest z odsetkiem śmiertelności poniżej 5%, a w najlepszych ośrodkach – poniżej 2% i liczbą powikłań okołooperacyjnych od 10 do 15%. W większości ośrodków jednak, ogólny odsetek powikłań pooperacyjnych wciąż szacuje się na 20-50% (Hoshal [24] 28%). Do najczęstszych powikłań należy opóźnione opróżnianie żołądkowe (5-50%), a do najpoważniejszych – przecieki i przetoki trzustkowe, żółciowe i okolicy zespolenia jelitowego, ropnie wewnątrzbrzuszne, krwawienia lub niedokrwienie jelita cienkiego (25, 26, 27, 28, 29).
W opisywanym projekcie badano zasadnicze mechanizmy zaburzeń motoryki górnego odcinka przewodu pokarmowego po wykonaniu dwóch grup procedur chirurgicznych – wytworzenia pętli Roux-en-Y i „un-cut”Roux oraz pankreatoduodenektomii sposobami Whipple´a i Longmire-Traverso, przez porównanie ich w odniesieniu do długoterminowych telemetrycznych rejestracji czynności mioelektrycznej, obserwacji klinicznej od pierwszych chwil po operacji, a także rozmieszczenia i gęstości występowania komórek Cajala w obrębie przewodu pokarmowego z oceną ich przewidywanego wpływu na szybkość powrotu czynności mioelektrycznej górnego odcinka przewodu pokarmowego.
Materiał i metody
Dla celów projektu utworzono cztery grupy zwierząt odpowiednio dla wytworzenia pętli sposobami Roux-en-Y i „un-cut”Roux oraz wykonania pankreatoduodenektomii sposobami Whipple´a i Longmire-Traverso. Wszystkie wdrożone procedury były analogiczne do tych rutynowo stosowanych u pacjentów leczonych w oddziałach chirurgicznych i zwierały między innymi: profilaktykę antybiotykową, odpowiednie wyposażenie bloku operacyjnego i techniki operacyjne, pooperacyjne żywienie pozajelitowe. Wprowadzenie telemetrycznej techniki rejestracji umożliwiło pomiar czynności mioelektrycznej u swobodnie poruszających się świń. Po dwu-, trzytygodniowym okresie pooperacyjnej obserwacji i po zakończeniu protokołu pomiarów, od zabitych zwierząt były pobierane próbki tkanek do znakowania komórek Cajala.
Do badania wykorzystano 24 świnie rasy wielkiej białej polskiej o wadze wyjściowej od 10 do 13 kg, pochodzących z prywatnej hodowli. Badania prowadzono zgodnie z uregulowaniami Unii Europejskiej dotyczącymi dobrostanu zwierząt eksperymentalnych i zasadami protokołu pozytywnie zaopiniowanego przez Lokalną Komisję Etyczną. Doświadczenia na zwierzętach prowadzono w Zakładzie Fizjologii Przewodu Pokarmowego Instytutu Fizjologii i Żywienia Zwierząt im. Kielanowskiego PAN w Jabłonnie.
Po tygodniowej adaptacji w warunkach laboratoryjnych, świnie poddawano krótkiemu zabiegowi operacyjnemu, przeprowadzanemu w znieczuleniu ogólnym, obejmującemu:
– wszczepienie cewnika do żyły szyjnej zewnętrznej służącego do pobierania próbek krwi w okresie okołooperacyjnym, wlewów dożylnych, podawania całkowitego żywienia pozajelitowego oraz
– naszycie elektrod oraz implantu telemetrycznego, umożliwiających rejestrację czynności mioelektrycznej jelit.
Cięciem w linii białej otwierano jamę otrzewnej. Po kontroli narządów wewnętrznych, lokalizowano więzadło Treitza, a następnie 5, 15 i 45 cm poniżej więzadła na surowicówkę jelita czczego naszywano trzy elektrody. Elektrody układano wzdłuż przebiegu mięśniówki okrężnej i każdą mocowano ośmioma pojedynczymi, jedwabnymi szwami (Silk 4,0). Po pozostawieniu luźnej pętli kabli w jamie otrzewnej wyprowadzano implant na zewnątrz z oddzielnego cięcia otrzewnej w prawym podbrzuszu. Następnie, po wytworzeniu między mięśniami prawego podbrzusza kieszonki o średnicy 8 cm x 8 cm, umieszczano w niej implant wraz z nadmiarem kabli i kablem uziemiającym z nierdzewnej stali, który mocowano do włókien mięśni szkieletowych. Obie rany w linii białej i w prawym podbrzuszu zamykano rutynowo – trzema warstwami szwów. 3-kanałowy implant telemetryczny (D70EEE, DIS, Oregon, MN, USA) o masie całkowitej 40 g emituje w postaci fali radiowej sygnały mioelektryczne rejestrowane przez dwubiegunowe elektrody. Sygnały te są zbierane poprzez specjalną antenę umieszczoną w zasięgu fal (np. 1,5 m).
Po kolejnych siedmiu dniach, przeprowadzano właściwą procedurę operacyjną, zgodnie z obowiązującymi w chirurgii ludzkiej zasadami. Schematy wykonanych operacji, wraz z zaznaczonymi miejscami ostatecznej lokalizacji elektrod I, II, III, przedstawia rycina 1.
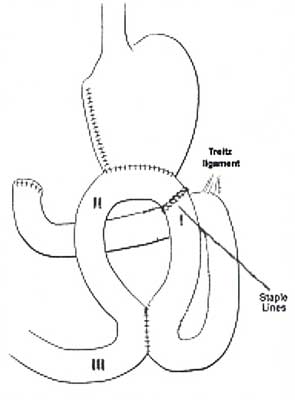
Schemat operacji „un-cut”Roux
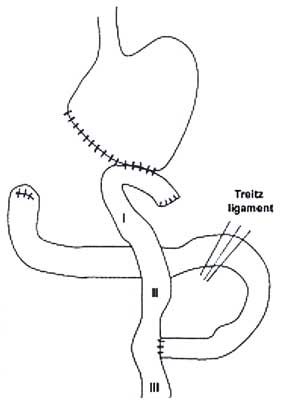
Schemat operacji Roux-en-Y

Schemat operacji Whipple´a
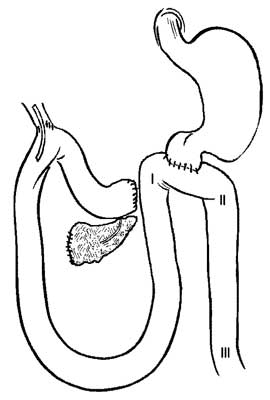
Schemat operacji Longmire-Traverso
Ryc. 1. Schematy procedur chirurgicznych.
W czasie operacji zwierzętom podawano pojedynczą, profilaktyczną dawkę antybiotyku (Clamoxyl 1mg/kg i.m.). W okresie pooperacyjnym zwierzęta dostawały jeszcze:
– pojedynczą dawkę profilaktyczną antybiotyku (po 48 godzinach) (Clamoxyl 1mg/kg i.m.) przy braku dodatkowych czynników ryzyka lub
– regularne leczenie antybiotykiem (Clamoxyl 1mg/kg i.m. co 48 godzin przez 8 dni), gdy istniały czynniki ryzyka zakażenia jak: czas operacji powyżej 3 godzin bądź znaczna kontaminacja pola operacyjnego żółcią lub treścią jelitową.
Czas trwania operacji wynosił średnio 180 minut (140-220).
Po zabiegu zwierzęta umieszczano w klatkach pod promiennikiem podczerwieni, uruchamiano ciągły, 24-godzinny zapis czynności mioelektrycznej jelit i podawano pierwszą dawkę żywienia pozajelitowego: 150 ml preparatu Kabiven Peripheral i 100 ml 0,9% roztworu soli fizjologicznej, na zakończenie wypełniając cewnik dożylny roztworem heparyny.
Zapis czynności mioelektrycznej rozpoczynano zaraz po przeniesieniu zwierzęcia ze stołu operacyjnego do klatki i kontynuowano nieprzerwanie przez 14-21 dni. Sygnały elektromiograficzne były odbierane i przekształcane przez implant na fale radiowe, a następnie odbierane przez antenę odbiorczą (RMC-1, DSI, Oregon, MN, USA) umieszczoną pod klatką. Odbiornik był połączony z analogowym przetwarzaczem (DL10, DSI, Oregon, MN, USA); sygnał z każdego z trzech kanałów był filtrowany poprzez odcięcie sygnałów wysokich częstotliwości>50 Hz i sygnałów niskich częstotliwości <10 Hz, a następnie wzmacniany (BioAmp, ADInstruments, Melbourne, Australia) zgodnie z opisem metody Gacsalyi i wsp. (30). Do zapisywania, przechowywania i analizy danych używano komputera PC z oprogramowaniem Chart 4.2 (ADInstruments, Melbourne, Australia).
Do znakowania markerów komórkowych w komórkach Cajala stosowano poliklonalne przeciwciała królicze CD117, c-kit (Sigma, St. Louis, MO, USA). Preparaty analizowano przy użyciu mikroskopu konfokalnego LSM5 PASCAL (Zeiss, Niemcy).
Wyniki opracowywano w arkuszu kalkulacyjnym Excel(r) 2000 (Microsoft Corp, CA, USA) i poddano analizie statystycznej w programie GraphPad Prism v.4.1 (GraphPad Software, San Diego, CA, USA), z wykorzystaniem testu t-studenta, testu nieparametrycznego Mann-Whitneya, jednoczynnikowej analizy wariancji (ANOVA) dla zmiennych niepołączonych popartej post-hoc testem Tukeya lub testu Kruskal-Wallisa popartego testem post-hoc Dunna, których używano do wykazania statystycznych różnic między zapisami kontrolnymi i pooperacyjnymi. Wyniki wyrażano w postaci średnich arytmetycznych i odchyleń średnich (średnia ± SEM). We wszystkich analizach p<0,05 uznawano za poziom istotności statystycznej.
Ilościowej analizy statystycznej komórek Cajala dokonano za pomocą oprogramowania mikroskopu konfokalnego Axion Vision Release 4.3 (Zeiss, Niemcy).
Wyniki
Świnie z grupy „un-cut”Roux zwiększyły swoją masę ciała średnio o 18,0% w odniesieniu do wagi wstępnej mierzonej przed operacją. W odróżnieniu od nich, świnie z grupy Roux-en-Y po dwóch tygodniach obserwacji oscylowały wokół wagi wyjściowej (średnio 7,3% wzrostu), a dwie z nich nawet spadły na wadze. Te wyniki odzwierciedlały obserwację kliniczną. Świnie z grupy „un-cut”Roux: wcześniej wracały do normalnej aktywności ruchowej, wcześniej czuły głód i szukały jedzenia, a pierwsze wypróżnienie miały przynajmniej jeden dzień wcześniej w porównaniu ze świniami z grupy Roux-en-Y. W oparciu o objawy kliniczne zauważono także, że u trzech świń z grupy Roux-en-Y pojawił się zespół pętli Roux, podczas gdy u zwierząt z grupy „un-cut”Roux nie obserwowano tego zjawiska.
W grupie Longmire-Traverso po przebytej pankreatoduodenektomii oszczędzającej już w ciągu pierwszego tygodnia zaobserwowano przybieranie na wadze, a po 3-tygodniowym okresie obserwacji wszystkie zwierzęta wykazywały statystycznie znamienny przyrost masy ciała średnio o 19,8% w stosunku do masy sprzed operacji (p=0,002). W grupie Whipple´a w ciągu 7 pierwszych dni po operacji zwierzęta straciły na wadze średnio 1,4 kg. W dalszej obserwacji pięć świń zaczęło przybierać na wadze powoli ale regularnie, zwiększając ostatecznie swoją masę wyjściową o średnio 15,2%. Oceniając dynamikę zmiany masy ciała zwierząt między grupami, należy stwierdzić, że najważniejszą różnicą był ujemny przyrost masy ciała zwierząt obserwowany w 7 dniu po operacji Whipple´a, przy jednocześnie dodatnim przyroście u zwierząt po operacji Longmire-Traverso; jednak w 21 dniu obserwacji przyrosty były już w obu grupach dodatnie, choć utrzymała się tendencja do słabszych przyrostów w grupie Whipple´a.
Po przeprowadzonych operacjach, zaraz po umieszczeniu zwierzęcia w klatce uruchamiano zapis EMG (około 30 minut po operacji). Początkowo u wszystkich zwierząt zapis wykazywał całkowity zanik aktywności potencjałów czynnościowych (ERA). Pierwszą manifestacją powracającej czynności elektrycznej jelita były pojedyncze potencjały czynnościowe, które pojawiły się w obu grupach badanych już 1-2 godziny po operacji. Pojedyncze zniekształcone ERA po kilku godzinach stawały się bardziej regularne, a po kilku następnych zaczęły grupować się w salwy pobudzeń przypominające fazę III prawidłowego wzorca MMC. Regularne MMC powróciły średnio po 10,5 godzinach u świń „un-cut”Roux i dopiero po średnio 37 godzinach w grupie Roux-en-Y (p=0,02). U wszystkich zwierząt po operacji Longmire-Traverso wzorzec MMC pojawiał się na powrót już w pierwszej dobie pooperacyjnej, średnio po 27,8±5,1 godzinach od zakończenia operacji. W zapisach EMG zwierząt po operacji Whipple´a, po 2-3 dniach skąpej aktywności mioelektrycznej, migrujące na kolejne elektrody MMC pojawiały się średnio po 68,2±12,9 godzinach od operacji. Pierwsze izolowane MMC często widoczne były już wcześniej (średnio po 39 godzinach) głównie na elektrodzie III, jednak nie obserwowano bardzo długo aktywności MMC i migracji w bliższej okolicy zespolenia. Tak więc, również w grupach zwierząt po pankreatoduodenektomii obserwowano statystycznie znamienną różnicę w czasie powrotu pooperacyjnych wzorców MMC między badanymi grupami (p=0,002).
Najbardziej charakterystycznym zjawiskiem obserwowanym w zapisach zwierząt z grupy Longmire-Traverso była migracja fazy III rozpoczynającej się na elektrodzie II, na elektrodę III i jednocześnie wstecznie na elektrodę I, a następnie jej „powrót” z elektrody I kolejno na elektrodę II i III. W ten sposób jeden wzorzec MMC miał dwie fazy III na elektrodach II i III, a tylko jedną na elektrodzie I (zjawisko podobne do re-entry obserwowanego w mięśniu sercowym).
Z kolei, charakterystycznym zjawiskiem w grupie "un-cut”Roux było statystycznie istotne spowolnienie migracji impulsów wyładowań elektrycznych wzdłuż jelita [cm/s] między elektrodami I i II, w porównaniu z kontrolą. Zgodnie z procedurą chirurgiczną w tej grupie zwierząt, linia zszywek staplera znajdowała się między wspomnianymi elektrodami. W odniesieniu do grupy kontrolnej, gdzie średnia prędkość wynosiła 4,7±0,7 cm/s, opóźnienie w grupie badanej utrzymywało się w trzeciej, siódmej i czternastej dobie pooperacyjnej – prędkość wynosiła odpowiednio 3,25±0,5 ( P<0,0001), 3,21±0,45 ( P<0,0001), i 3,27±0,5 cm/s ( P<0,0001).
W przeprowadzonej analizie pooperacyjnej sieci komórek Cajala w grupach Roux-en-Y i „un-cut”Roux stwierdzono bezpośrednią pozytywną zależność pomiędzy ilością komórek Cajala zlokalizowanych w obrębie splotu Auerbacha i powrotem regularnego MMC w obrębie poszczególnych grup. Zaobserwowano także, że im większa gęstość występowania wspomnianych komórek tym mniejsza ilość pooperacyjnych zrostów (ocenianych według makroskopowej skali) wewnątrz jamy brzusznej po upływie dwóch tygodni od operacji.
W analogicznej analizie komórek Cajala w grupach Whipple´a i Longmire-Traverso wykazano, że liczba ICC w preparatach zwierząt po operacji Whipple´a obserwowanych w okolicach poszczególnych elektrod jest znamiennie mniejsza w porównaniu z preparatami zwierząt po operacji Longmire-Traverso i kontrolnymi. W preparatach z okolicy ślepej pętli stwierdzono znikomą liczbę ICC, zarówno w grupie Whipple´a jak i w grupie Longmire-Traverso. Zaobserwowano pewne tendencje wskazujące na istnienie zależności między liczbą komórek Cajala i szybkością powrotu regularnych wzorców MMC – im szybciej po operacji pojawiała się regularna aktywność mioelektryczna w postaci MMC, tym większą liczbę komórek Cajala stwierdzano w preparatach jelitowych danego zwierzęcia.
Dyskusja
Gatunek Sus scofa od dawna był i nadal jest wykorzystywany jako model eksperymentalny w licznych badaniach nad fizjologią przewodu pokarmowego (32, 33, 34, 35). Świnia jest zwierzęciem osiągającym już w młodym wieku rozmiary wystarczające do przeprowadzenia operacji brzusznej i wszczepienia implantu telemetrycznego w powłoki. Ponieważ jest wszystkożerna, procesy fizjologiczne odbywające się w przewodzie pokarmowym są zbliżone do procesów fizjologicznych u człowieka. Ma też podobne wymagania pokarmowe do człowieka, co umożliwia zaadoptowanie i odtworzenie w eksperymencie wszystkich procedur okresu pooperacyjnego stosowanych u pacjentów po tego typu procedurach chirurgicznych. Podobna podatność na choroby przewodu pokarmowego zapewnia analogiczną reaktywność organizmu na uraz okołooperacyjny.
Świnia ma podobną do człowieka budowę anatomiczną górnego odcinka przewodu pokarmowego, co umożliwia przeprowadzenie skomplikowanej procedury chirurgicznej zgodnie z regułami sztuki chirurgicznej stosowanej w medycynie człowieka.
Zjawiska elektrofizjologiczne zachodzące w przewodzie pokarmowym świni doskonale odpowiadają potrzebom modelu eksperymentalnego na potrzeby gastroenterologii ludzkiej. Są analogiczne do tych u człowieka, ale trwają krócej, co ułatwia obserwację i pozwala na uzyskanie wyników w krótszym czasie. Częstotliwość fal wolnych (BER) w dwunastnicy u świni wynosi 17-18/min (33, 35) u człowieka 10-13/min i w obu przypadkach, zmniejsza się dystalnie. Z badań Gronera (36) wynika, że częstość fal wolnych w żołądku i dwunastnicy u małych 14-28-dniowych świń jest podobna do ich częstości u dorosłego człowieka. Czas trwania pojedynczych potencjałów czynnościowych u świni wynosi 1,0-1,5 s, a szybkość ich migracji 4,2-4,7 cm/s jest podobna jak u człowieka (37, 38). Czas trwania międzyposiłkowego wzorca MMC u świni jest nieco krótszy (60-90 min) niż u człowieka (90-110 min). Zaburzenia MMC przez posiłek również trwają krócej – regularne MMC powracają już po 2-3 godzinach. Czyni to świnię lepszym modelem obserwacyjnym od psa, u którego zaburzony pokarmem wzorzec MMC powraca dopiero po kilkunastu godzinach. Cykle MMC u psa trwają dłużej niż u człowieka, a treść pokarmowa transportowana jest przez jelito znacznie szybciej. Dieta psa zawiera mniej białek roślinnych niż ludzka czy świńska, a odmienne schematy zachowań i mechanizmy regulacyjne czynności przewodu pokarmowego sprawiają, że właściwa wielkość zwierzęcia jest niewystarczająca, żeby stał się odpowiednim modelem eksperymentalnym dla potrzeb gastroenterologii. Z kolei niewielkie rozmiary innych zwierząt eksperymentalnych, jak myszy czy szczurów, stanowią zasadniczą przeszkodę do wykonywania u nich procedur operacyjnych w górnym piętrze przewodu pokarmowego i wszczepienia implantu do telemetrycznej rejestracji czynności mioelektrycznej. Poza tym, cykl MMC u szczurów trwa zaledwie 15 min, co znacznie odbiega od czasu trwania ludzkiego wzorca i sprawia, że obserwacje zaburzeń aktywności mioelektrycznej prowadzone u szczurów trudno byłoby odnieść do człowieka.
Niewielki spadek masy ciała zwierząt w okresie adaptacyjnym był efektem reakcji stresowej związanej z transportem, nowym miejscem pobytu, obsługą, np. można to uznać za normalne zjawisko towarzyszące wprowadzaniu zwierząt w nowe środowisko. W prezentowanej pracy, przy tej samej średniej masie wyjściowej, warunkach operacji i opieki pooperacyjnej, różnica w pooperacyjnych przyrostach masy ciała między badanymi grupami była wyraźna i przemawiała na niekorzyść operacji z wytworzeniem pętli Roux-en-Y. Przy braku innych parametrów, pooperacyjna masa ciała uznana została za najlepszy miernik stanu odżywienia zwierząt. Oceniając stan operowanych zwierząt na jej podstawie, wykazano przewagę operacji z wytworzeniem pętli „un-cut”Roux nad operacją Roux-en-Y i nie wykazano przewagi metody oszczędzającej nad klasyczną (39, 40, 41).
Obserwowane różnice w stanie odżywienia zwierząt we wczesnym okresie pooperacyjnym po pankreatoduodenektomii, mogą mieć związek ze stanem zapalnym i obrzękiem okolicy zespolenia, obecnością pooperacyjnych zaburzeń motoryki przewodu pokarmowego bądź innymi czynnikami, których obecność lub brak wynika z różnic w technice operacyjnej.
Znaczny uraz chirurgiczny, jakim jest resekcja w górnym odcinku przewodu pokarmowego, manipulacje w obrębie jelita oraz endotoksemia indukują rozwój procesu zapalnego. Wiadomo, że stopień aktywacji makrofagów i wzrost napływu neutrofilów do warstwy mięśniowej jelita jest wprost proporcjonalny do stopnia manipulacji w obrębie ściany przewodu pokarmowego (42). Być może, większy zakres operacji Whipple´a i związany z tym większy uraz okołooperacyjny skutkują bardziej nasiloną odpowiedzią zapalną, obrzękiem okolicy zespolenia żołądkowo-jelitowego i w konsekwencji – zaburzeniami stanu odżywienia.
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
24 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
59 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
119 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 28 zł
Piśmiennictwo
1. Otterson MF, Sarr MG: Normal physiology of small intestinal motility Surg Clin North Am 1993 73(6), 1173-92.
2. Zenilman ME: Origin and control of gastrointestinal motility. Surg Clin North Am. 1993: 73(6); 1081-99.
3. Suzuki N, Prosser CL, Dahms V: Boundary cells between ejunadinal and circular layers: essential for electrical slow waves in cat intestine. Am. J. Physiol. 1986: 250; G287-G294.
4. Code CF, Marlett JA: The interdigestive myo-electric complex of the stomach and small bowel of dogs. J Physiol 1975: 246(2), 289-309.
5. Szurszewski JH: A 100-year perspective on gastrointestinal motility. Am J Physiol 1998: 274(3 Pt 1); G447-53.
6. Kelly KA, Code CF, Elveback LR: Patterns of canine gastric electrical activity. Am J Physiol. 1969: 217; 461-470.
7. Weber J, Kohatsu S: Pacemaker localization and electrical conduction patterns in the canine stomach. Gastroenterology 1970: 59, 5; 717-725.
8. Sarna S, Daniel EE, Kingma YJ: Stimulation of the electric-control activity of the stomach by an array of relaxation oscillators. Am J Dig Dis. 1972: 17; 299-310.
9. Sarna S et al.: Intrinsic nervous control of migrating mioelectric complexes. Am J Physiol. 1981: 241, 1; G16-G23.
10. Sarna S: Cyclic motor activity, migrating motor complex. Gastroenterology. 1985: 89, 4; 894-913.
11. Diamant NE, Bortoff A: Nature of the intestinal low-wave frequency gradient. Am J Physiol. 1969: 216(2); 301-307.
12. Bunker CE, Johnson LP, Nelsen TS. Chronic in situ studies of the electrical activity of the small intestine. Arch Surg. 1967: 95; 259-268.
13. Hermon-Taylor J, Code C: Localization of the duodenal pacemaker and its role in the organization of duodenal myoelectric activity. Gut. 1971: 12; 40-47.
14. Miedema BW, Kelly KA: The Roux stasis syndrome. Treatment by pacing and prevention by use of an "uncut”Roux limb. Arch. Surg. 1992: 127; 295-300.
15. Kiciak A i wsp.: Roux-en-Y 127or "un-cut”Roux procedure? Relation of intestinal migrating motor complex recovery to the preservation of the network of interstitial cells of Cayal in pigs. Exp Physiol. 2007: 92, 2; 399-408.
16. Karlstrom L, Kelly KA: Ectopic jejunal pacemakers and gastric emptying after Roux gastrectomy: Effect of intestinal pacing. Surgery. 1989: 106; 486-495.
17. Vantrappen G et al.: Inversion of the slow-wave frequency gradient in symptomatic patients with Roux-en-Y anastomoses. Gastroenterology. 1991: 101; 1282-1288.
18. Mathias JR et al.: Nausea, vomiting and abdominal pain after Roux-en-Y anastomosis: motility of the jejunal limb. Gastroenterology. 1985: 88; 101-107.
19. Gustavsson S et al.: Roux-en-Y stasis syndrome after gastrectomy. Am J Surg. 1988: 155; 490-494.
20. Van Stiegmann G, Gott JS: An Alternative to Roux-en-Y for treatment of bile reflux gastritis. Surg. Gynecol. Obstet. 1988: 166; 69-70.
21. Greve JWG et al.: Pylorus Preserving Pancreaticoduodenectomy versus Standard Whipple Procedure: a prospective, randomized, multicenter analysis of 170 Patients with pancreatic and periampullary tumors. Ann Surg. 2004: 240(5); 738-745.
22. Ohtsuka T, Yamaguchi K: Comparison of quality of life after pylorus-preserving pancreatoduodenectomy and Whipple resection. Hepatogastroenterology. 2003: 50(51); 846-50.
23. Hashimoto N et al.: Comparison of the functional and morphological changes in the pancreatic remnant between pylorus-preserving pancreatoduodenectomy and pancreatoduodenectomy. Hepatogastroenterology. 2003: 50(54); 2229-2232.
24. Hoshal VL, Benedict MB: Personal experience with the Whipple operation. Am Surg. 2004: 70(2); 121-126.
25. Adam U, Makowiec F, Ridiger H. Risk factors for complications after pancreatic head resection. Am J Surg. 2004: 187(2); 201-8.
26. Behrman SW, Rush BT, Dilawari RA: A modern analysis of morbidity after pancreatic resection. Am Surg 2004: 70(8); 675-83.
27. Camp ER, Vogel SB: Blind Whipple resection for periampullary and pancreatic lesions. Am Surg. 2004: 70(1); 6-12.
28. Morel P, Mathey P, Corboud H: Pylorus-preserving duodenopancreatectomy: long-term complications and comparison with the Whipple procedure. World J Surg. 1990: 14; 642-646
29. Niedergethmann M, Farag Soliman MP: Postoperative complications of pancreatic cancer surgery. Minerva Chir. 2004: 59(2); 175-83.
30. Gacsalyi U, Zabielski R, Pierzynowski SG: Telemetry facilitates long-term recording of gastrointestinal myoelectrical activity in pigs. Exp Physiol. 2008: 5(2); 239-41.
31. Ruckebusch Y, Bueno L: The effect of feeding on the motility of the stomach and small intestine in the pig. Br J Nutr. 1976: 35; 397.
32. Abello J, Laplace J, Corring T: Biliary and pancreatic secretory component of the migrating motor complex in the pig. Effect on intraduodenal pH. Reprod Nutr Develop. 1988: 28(4A); 953-967.
33. Burrows CF, Merritt AM, Tash J: Jejunal myoelectrical activity in the conscious neonatal pig. J Physiol. 1986: 374; 349-357.
34. Yao G et al.: Daily changes in antroduodenal myoelectric activity in weaned pigs. Anim Sci. 2003: 76; 273-281.
35. Jimenez M et al.: Slow waves in circular muscle of porcine ileum: structural and electrophysiological studies. Am J Physiol. 1999: 276 (2Pt1); G393-406.
36. Groner JI, Altschuler SM, Ziegler MM: The newborn piglets: a model of neonatal gastrointestinal motility. J Pediatr Surg. 1990: 25(3); 315-318.
37. Kiciak A: Mechanisms of upper gut motility disorders following Roux-en-Y and un-cut Roux constructions in pig. The role of pacemaker cells. Ph.D. thesis. Warsaw 2004.
38. Yao G: Gut myoelectrical activity in the conscious weaned pigs: daily variability, cholinergic regulation aand the influence of E. coli enterotoxins. Ph.D. thesis. Jabłonna 2003.
39. Jimenez RE, Fernandez-Del Castillo C, Rattner DW: Outcome of pancreaticoduodenectomy with pylorus preservation or with antrectomy in the treatment of chronic pancreatitis. Ann Surg. 2000: 231; 293-300.
40. Kozuschek W, Reith HB, Waleczek H: A comparison of long term results of the standard Whipple procedure and the pylorus preserving pancreatoduodenectomy. J Am Coll Surg. 1994: 178; 443-453.
41. McLeod RS, Taylor BR, O´Connor BI: Quality of life, nutritional status and gastrointestinal hormone profile following the Whipple procedure. Am J Surg. 1995: 169; 179-185.
42. Kalff JC et al.: Surgical manipulation of the gut elicits an intestinal muscularis inflammatory response resulting in postsurgical ileus. Ann Surg. 1998: 228; 652-663.
43. Schönfeld J, Evans DF, Wingate DL: Daytime and night time motor activity of the small bowel after solid meals of different caloric value in humans. Gut. 1997: 40, 614-618.
44. Dardillat, C. Analyse electromyographique et debimetrique du transit alimentaire chez le veau nouveau-ne. Journal of Physiology (Paris). 1977: 73; 925-944.
45. Dardillat, C, Marrero E: Etude de l´electromyogramme global chronique de la parov intestinale du veau preruminant: migration des phases d´activite reguliere et relation avec le transit. Annales de Biologie Animale Biochimie Biophysique 1977: 17; 523-550.
46. Romański KW, Rudnicki J, Sławuta P: The mioelectric activity of ileum in fasted and fed young pigs. J Physiol Pharmacol. 2001: 52; 851-861.
47. Klabunde RE: Cardiovascular Physiology Concepts. Rozdz. 1. Arrythmias, Lippincott Williams&Wilkins, 2004.
48. Richardson WS et al.: Teflon buttress inhibits recanalization of uncut stapled bowel. J Gastrointest Surg. 2004: (4); 424-9.
49. Ohwada S et al.: Low-dose erythromycin reduces delayed gastric emptying and improves gastric motility after Billroth I pylorus-preserving pancreaticoduodenectomy. Ann Surg. 2001: 234(5); 668-674.
50. Furgała A et al.: The effect of transcutaneus nerve stimulation (TENS) on gastric electrical activity. J Physiol Pharmacol. 2001: 52(4Pt1); 680-686.
51. Królczyk G et al.: Effects of continuous microchip (MC) vagal neuromodulation on gastrointestinal function in rats. J Physiol Pharmacol. 2001: 52(4); 705-715.
52. Closset J, Gelin M: Delayed gastric emptying after pancreatoduodenectomy. Acta Chir Belg. 2003: 103(3); 338-9.
53. Takayama I et al.: The interstitial cells of Cajal and a gastroenteric pacemaker system. Arch Histol Cytol. 2002: 65(1); 1-26.
54. Herold G: Medycyna wewnętrzna. Rozdz: Gastroenterologia. Zespoły upośledzonego wchłaniania. Wydawnictwo Lekarskie PZWL, Warszawa 2000: 498-499.




