© Borgis - Postępy Nauk Medycznych 5/2010, s. 391-407
*Tomasz Sikorski, Ewa Marcinowska-Suchowierska
Problemy hematologiczne u ciężarnych w praktyce lekarza rodzinnego
Haematogical problems in pregnant women at a general practitioner's practice
Klinika Medycyny Rodzinnej i Chorób Wewnętrznych Centrum Medycznego Kształcenia Podyplomowego w Warszawie
Kierownik Kliniki: prof. dr hab. med. Ewa Marcinowska-Suchowierska
Streszczenie
W prawidłowej ciąży występują zmiany w krwi obwodowej oraz w układzie krzepnięcia i fibrynolizy. Najważniejsze z nich to fizjologiczna niedokrwistość z rozcieńczenia, łagodna leukocytoza neutrofilowa, łagodna małopłytkowość, pobudzenie krzepnięcia i zahamowanie fibrynolizy. Ich znajomość jest niezbędna dla lekarza rodzinnego, aby mógł właściwie rozpoznawać niedokrwistości i małopłytkowości, najczęstsze zaburzenia hematologiczne u ciężarnych. Jako kryterium niedokrwistości w ciąży przyjmuje się najczęściej stężenie hemoglobiny <11,0 g/dL w 1. i 3. trymestrze i <10,5 g/dL w 2. trymestrze oraz <10,0 g/dL po porodzie. Przyczyną niedokrwistości u ciężarnych jest przede wszystkim niedobór żelaza, utrata krwi w połogu, a rzadko niedobór kwasu foliowego. Najlepszym sposobem suplementacji żelaza w ciąży jest droga doustna, zwłaszcza, że wzrasta absorpcja żelaza w przewodzie pokarmowym, ale problemem może być zła tolerancja preparatów doustnych. Jednakże droga parenteralna daje szybszą odpowiedź niż doustna. Dostępność coraz bezpieczniejszych kompleksów żelaza z sacharozą i karboksymaltozą zliberalizowała wskazania do dożylnego podawania żelaza w ciąży, które praktycznie jest stosowane już w umiarkowanej niedokrwistości z niedoboru żelaza z hemoglobiną <10 g/dL w 2. i 3. trymestrze ciąży i po porodzie. Najczęstszą przyczyną małopłytkowości w ciąży jest łagodna incydentalna małopłytkowość, dalej małopłytkowość towarzysząca powikłaniom ciąży przebiegającym z nadciśnieniem tętniczym i małopłytkowość immunologiczna, które odpowiadają odpowiednio za 74, 21 i 4% przypadków. Kryterium ilościowym rozpoznania małopłytkowości immunologicznej jest liczba płytek krwi <100 x 109/L. Oprócz niedokrwistości i małopłytkowości zwrócono również uwagę na zakrzepową plamicę małopłytkową, rozsiane wykrzepianie wewnątrznaczyniowe, wrodzone skazy osoczowe oraz nowotwór mieloproliferacyjny.
Summary
In normal pregnancy there are changes in a peripheral blood and coagulation and fibrinolysis systems. Of these, the most important are physiological dilutional anaemia, benign neutrophilic leucocytosis, benign thrombocytopenia, coagulation activation and fibrinolysis inhibition. A general practitioner must be familiar with these changes to diagnose correctly anaemia and thrombocytopenia, the two most common haematological abnormalities in pregnancy. As a criterion for anaemia in pregnancy, haemoglobin of <11.0 g/dL in the first and third trimester, and <10.5 g/dL in the second trimester, and <10.0 g/dL after parturition are commonly used. Anaemia in pregnant women is mainly due to iron deficiency, an acute blood loss in the puerperium, and infrequently folate deficiency. Given increased alimentary iron absorption, oral iron supplementation is the most convenient, but its poor tolerance may be a problem. However, parenteral iron brings about a faster response. An availability of more and more safe iron complexes with sucrose and carboxymaltose allowed to use easier intravenous iron in pregnancy, practically even in moderate iron deficiency anaemia with haemoglobin of <10 g/dL in the second and third trimester and the puerperium. Of thrombocytopenias in pregnancy, the most common is benign incidental thrombocytopenia, then thrombocytopenia associated with hypertensive complications of pregnancy and immunologic thrombocytopenia, which account for 74, 21 and 4% of cases, respectively. Platelet count of <100 x 109/L is a quantitative criterion for diagnosing immunologic thrombocytopenia. Besides anaemia and thrombocytopenia, we also consider thrombotic thrombocytopenic purpura, disseminated intravascular coagulation, congenital disorders of plasma coagulation, and myeloproliferative neoplasm.

ZMIANY FIZJOLOGICZNE WE KRWI W CIĄŻY PRAWIDŁOWEJ
Ciąża prawidłowa wywołuje w organizmie matki zmiany adaptacyjne we wszystkich układach, w tym również we krwi, będące odpowiedzią na pojawienie się płodu i łożyska, i zwiększone zapotrzebowanie jednostki płodowo-łożyskowej na tlen i substancje odżywcze. Najważniejsze zmiany hematologiczne w ciąży to fizjologiczna niedokrwistość z rozcieńczenia, łagodna leukocytoza neutrofilowa, łagodna małopłytkowość, wzrost stężenia czynników krzepnięcia i spadek aktywności fibrynolizy (tab. 1).
Tabela 1. Zmiany fizjologiczne we krwi w ciąży.
| ? "Niedokrwistość" z rozcieńczenia |
| ? Łagodna leukocytoza neutrofilowa |
| ? Łagodna małopłytkowość |
| ? Zwiększenie aktywności krzepnięcia |
| ? Zmniejszenie aktywności fibrynolizy |
W ciąży wzrasta przede wszystkim objętość osocza, w mniejszym stopniu masa krwinek czerwonych (1). Objętość osocza wzrasta o 10-15% już między 6. a 12. tygodniem ciąży i rośnie szybko aż do 30-34 tygodnia ciąży. Całkowity wzrost objętości osocza do porodu wynosi 1100-1600 ml, co daje 30-50% wzrost w porównaniu z objętością osocza u kobiet nieciężarnych. W ciąży obserwuje się wzrost aktywności reninowej osocza i spadek poziomu natriuretycznego peptydu przedsionkowego, co sugeruje, że wzrost objętości osocza jest wywołany systemową wazodilatacją. Masa krwinek czerwonych zaczyna wzrastać od 8-10 tygodnia ciąży i stopniowo rośnie do porodu o 250-450 ml u ciężarnych przyjmujących suplementację żelaza, co daje 20-30% wzrost w porównaniu z wartościami u kobiet nieciężarnych. U ciężarnych bez suplementacji żelaza całkowity wzrost masy erytrocytów jest mniejszy i wynosi tylko 15-20% w porównaniu do wartości sprzed ciąży. Za wzrost masy erytrocytów w ciąży odpowiada zwiększona produkcja erytropoetyny, której stężenie w surowicy wzrasta od 50 do 90% (2). Wzrost stężenia erytropoetyny w surowicy ma charakter kompensacyjny i koreluje z odsetkiem hipochromicznych erytrocytów i zawartością hemoglobiny w retikulocytach (3). Po porodzie stężenie erytropoetyny w surowicy wraca do normy. Czas życia erytrocytów w ciąży jest skrócony. W następstwie tych zmian wzrasta również objętość krwi średnio o 48% (zakres od 20 do 100%) w porównaniu do wartości u nieciężarnej i przy porodzie wynosi 100 ml/kg, a spada hematokryt, osiągając swój nadir między 24. a 26. tygodniem ciąży. We krwi obwodowej daje to obraz „fizjologicznej niedokrwistości” z normocytozą i normochromią erytrocytów, przy czym stężenie hemoglobiny nie powinno być niższe od 11 g/dL w 1. trymestrze i od 10 g/dL w 2. i 3. trymestrze (1). W godzinę po porodzie siłami natury utrata objętości krwi wynosi 10,2% (ok. 600 ml), a po cięciu cesarskim 17,4% (ok. 1000 ml), przy czym w pierwszym przypadku objętość krwi stopniowo obniża się do 3 dnia, a w drugim pozostaje stabilna do 5 dnia po porodzie (4). Chociaż w obu grupach rodzących 3 dnia po porodzie spadek objętości krwi był podobny (o 16,2%), to towarzyszył mu wzrost hematokrytu po porodzie siłami natury o 5,2%, a spadek po cięciu cesarskim o 5,8% (4). W prawidłowej ciąży wzrasta średnia objętość erytrocytów ( mean corpuscular volume, MCV), dlatego normocytoza nie wyklucza niedoboru żelaza, a niewielka makrocytoza nie wskazuje na niedobór kwasu foliowego (1).
W ciąży dochodzi również do zmian stężenia żelaza i witamin krwiotwórczych w surowicy. Stężenia żelaza i ferrytyny w surowicy spadają, a całkowita zdolność wiązania żelaza w surowicy ( total iron binding capacity, TIBC) będąca miarą stężenia transferyny i stężenie wolnego receptora dla transferyny w surowicy ( serum transferrin receptor, sTfR) wzrastają z postępem ciąży (1). Wzrost stężenia sTfR, podobnie jak wolnej protoporfiryny w surowicy, w prawidłowej ciąży wynika raczej z pobudzenia matczynej erytropoezy niż z niedoboru żelaza i wraca do normy po porodzie. Stężenie w surowicy witaminy B12 może obniżyć się w czasie ciąży o 30-50% wskutek wzrastającej objętości osocza i zwiększonego zapotrzebowania u matki oraz przechodzenia do płodu (1). U ciężarnych bez suplementacji kwasu foliowego występuje postępujący spadek stężenia folanów w surowicy, natomiast zawartość folanów w erytrocytach wzrasta lub nie zmienia się (1). Stężenie homocysteiny w osoczu w prawidłowej ciąży spada i nie jest to spowodowane suplementacją kwasu foliowego, hemodilucją, czy spadkiem stężenia albumin, a prawdopodobnie ma podłoże hormonalne (5), a w czasie porodu wzrasta (6). Stężenie witaminy B6 w surowicy spada w ciąży, ale nie wiadomo, czy pojawia się jej niedobór i jakie są jego ewentualne implikacje kliniczne (1).
Prawidłowa ciąża przebiega ze stopniowym wzrostem leukocytozy, zwykle łagodnym poniżej 15 x 109/L, ale liczba leukocytów może nierzadko wynosić 15-20 x 109/L (1, 7). Wzrost leukocytozy zależy przede wszystkim od zwiększenia bezwzględnej liczby neutrofili, ale w 3. trymestrze wzrasta również bezwzględna liczba monocytów (7). Bezwzględna liczba eozynofili nie ulega zmianie, natomiast liczba bazofili spada przejściowo w 2. trymestrze. W rozmazie krwi obwodowej spotyka się młodsze postaci granulocytów – pałki i mielocyty. W ciąży nieznacznie wzrasta bezwzględna liczba limfocytów T, ale nie obserwuje się zmian w subpopulacjach CD8+ i CD4+. W czasie samego porodu wzrost leukocytozy jest jeszcze wyraźniejszy i tym wyższy, im dłużej trwa poród. Wysokość leukocytozy w czasie porodu nie wskazuje na możliwość powikłań. Wzrost leukocytozy z neutrofilią przebiega ze wzrostem stężenia w osoczu czynnika stymulującego kolonie granulocytarne i makrofagowe ( granulocyte-macrophage colony stimulating factor, GM-CSF) i laktoferyny w czasie całej ciąży, a w 1. trymestrze również elastazy w porównaniu z kobietami nieciężarnymi (8). Ponieważ laktoferyna i elastaza są markerami aktywacji neutrofili, w ciąży występuje zwiększone zużycie i wytwarzanie neutrofili (zwiększony obrót) podobnie jak w reakcji zapalnej. Stężenie CRP w surowicy zachowuje się zmiennie, ale jest wyższe niż u nieciężarnych (8). Czasami neutrofilia jest wywołana podaniem glikokortykosteroidu w celu przyspieszenia dojrzewania płuc u płodu.
Średnia liczba płytek krwi jest niższa u kobiet ciężarnych niż nieciężarnych, ale u części ciężarnych (co najmniej 5%), zwłaszcza pod koniec ciąży, liczba płytek krwi spada poniżej 150 x 109/L, czyli dolnej wartości referencyjnej dla nieciężarnych (1, 9). Liczba płytek utrzymuje się zwykle w zakresie 80-100 x 109/L i nie towarzyszą jej objawy skazy krwotocznej. Stan ten określa się małopłytkowością towarzyszącą ciąży lub łagodną małopłytkowością ciężarnych. Przyczyną małopłytkowości ciężarnych jest zwiększenie objętości osocza prowadzące do rozcieńczenia krwi oraz wzrost aktywacji i zużycia płytek, zwłaszcza w krążeniu łożyskowym kompensowany częściowo ich zwiększonym wytwarzaniem (zwiększony obrót płytek krwi u matki). Za zwiększoną aktywacją i obrotem płytek krwi u ciężarnej przemawia wzrost średniej objętości płytek krwi ( mean platelet volume, MPV) i stężenia w osoczu β-tromboglobuliny, czynnika płytkowego 4 oraz metabolitów tromboksanu A2 uwalnianych z płytek. Po porodzie liczba płytek krwi wzrasta. Zmiany ilościowe elementów morfotycznych i czynników krwiotwórczych we krwi obwodowej w prawidłowej ciąży przedstawia tabela 2.
Tabela 2. Zmiany we krwi obwodowej i czynników krwiotwórczych w ciąży prawidłowej (1).
| Parametr | Zmiana |
| Stężenie Hb | Ż (> 11/10 g/dL) |
| MCV | Bez zmian lub |
| Liczba płytek krwi | Ż (> 80 x 109/L) |
| Liczba neutrofili | (młode formy) |
| Stężenie witaminy B12 | Ż
<50% |
| Stężenie kwasu foliowego | Ż
<30% |
| Kwas foliowy w erytrocytach |
<20% lub bez zmian |
| Stężenie homocysteiny | Bez zmian lub Ż |
| Stężenie witaminy B6 | Ż <20% |
| Stężenie żelaza | Ż |
| TIBC | |
| Stężenie ferrytyny | Ż |
| Stężenie receptora transferyny | |
W ciąży dochodzi do istotnych zmian w układzie hemostazy z pobudzeniem krzepnięcia i zmniejszeniem aktywności fibrynolizy. Zwiększone wytwarzanie trombiny u ciężarnej jest fizjologiczną adaptacją do zbliżającego się porodu i zależy od wzrastającego stężenia estrogenów. Mikrocząsteczki uwalniane z matczynych komórek śródbłonka i płytek krwi oraz z trofoblastu łożyska mają działanie prokoagulacyjne. Stężenia w osoczu fibrynogenu, czynnika VII, VIII, X, XII i czynnika von Willebranda ( von Willebrand factor, vWF) wzrastają stopniowo w czasie ciąży i osiągają maksymalne poziomy przed porodem, czynnika V i IX pozostają niezmienione, natomiast stężenie czynnika XI może się zmniejszyć (1, 10). Czynnik XIII po początkowym wzroście stopniowo spada do końca ciąży do połowy wartości u nieciężarnych (10). Ciąża charakteryzuje się więc stanem prozakrzepowym, o czym świadczą wyraźnie zwiększone stężenia fragmentu protrombiny 1+2 ( prothrombin fragment, PF1+2), kompleksów trombina-antytrombina ( thrombin-antithrombin complexes, TAT), fibrynopeptydu A, rozpuszczalnej fibryny i D-dimeru (1, 10). Jednocześnie aktywność i/lub całkowity poziom antygenu inhibitorów krzepnięcia białka C i antytrombiny nie ulega zmianie, a białka S istotnie spada (10). Inhibitor szlaku czynnika tkankowego ( tissue factor pathway inhibitor, TFPI) i trombomodulina w czasie ciąży wzrastają. Doniesienia o zachowaniu się w ciąży białka Z, będącego kofaktorem osoczowej proteazy ( protein Z-dependent protease inhibitor, ZPI) hamującej aktywny czynnik X są niejednoznaczne. Opisywano zarówno wzrost, jak i spadek białka Z w ciąży prawidłowej (11), natomiast niedobór tego białka (<1 mg/L) prowadzi do wczesnej i późnej utraty płodu. W ciąży pojawia się również nabyta oporność na aktywne białko C ( activated protein C resistance, aPCR) (10).
W badaniach koagulologicznych zmiany te objawiają się niewielkim skróceniem czasu częściowej tromboplastyny po aktywacji ( activated partial thromboplastin time, aPTT) i skróceniem czasu protrombinowego ze znormalizowanym wskaźnikiem protrombiny ( international normalized ratio, INR) poniżej 0,9 (10). Czas krwawienia w czasie ciąży nie zmienia się.
W czasie ciąży wzrasta stężenie inhibitora aktywatora plazminogenu-1 ( plasminogen activator inhibitor, PAI-1) i inhibitora aktywatora plazminogenu-2 (PAI-2) dodatkowo wytwarzanego przez łożysko (1, 10, 12). Aktywność tkankowego aktywatora plazminogenu ( tissue plasminogen activator, tPA) w czasie ciąży spada (10). Stężenia we krwi tPA i urokinazy spadają w 1. trymestrze, ale rosną w 3. (12). Jednak uwalnianie tPA z komórek śródbłonka pod wpływem bradykininy jest w 3. trymestrze ciąży mniejsze o 36% w porównaniu z nieciężarnymi (13). Stężenie aktywowalnego trombiną inhibitora fibrynolizy ( thrombin-activatable fibrinolysis inhibitor, TAFI) w ciąży wzrasta (14). Zmiany te prowadzą do zmniejszenia aktywności fibrynolizy w ciąży, ale wzrastające stężenie D-dimeru uwalnianego z polimerów fibryny przez plazminę świadczy o odpowiedzi układu fibrynolizy na pobudzenie krzepnięcia. Zmiany w układzie krzepnięcia i fibrynolizy normalizują się do 6 tygodni po porodzie (12). Stężenia PAI-1 i PAI-2 szybko spadają po porodzie, ale PAI-2 był wykrywany nawet do 8 tygodni. Zmiany w układach krzepnięcia i fibrynolizy przedstawia tabela 3.
Tabela 3. Zmiany w układach krzepnięcia i fibrynolizy od 1. do 3. trymestru ciąży prawidłowej (1, 10-14).
| Parametr | Zmiana (%) | Parametr | Zmiana (%) |
| Układ krzepnięcia: | | Inhibitory krzepnięcia: | |
| Fibrynogen | 31 | Białko C | 0 |
| Protrombina | 0 | Antytrombina | 0 |
| Czynnik V | 0 | Białko S całkowite | Ż 15 |
| Czynnik VII | 42 | Białko S wolne | Ż 46 |
| Czynnik VIII | 62 | Białko Z | 20 (Ż 18) |
| Czynnik IX | 0 | Trombomodulina |
41 |
| Czynnik X | 20 | aPCR |
20 |
| Czynnik XI | Ż 5 | | |
| Czynnik XII | 14 | Układ fibrynolizy: | |
| Czynnik XIII | Ż 50 | Plazminogen | |
| vWF | 96 | t-PA | Ż
|
| TAT | 128 | u-PA | Ż
|
| PF1+2 | 140 | PAI-1 | 150-400 |
| Fibrynopeptyd A | 80 | PAI-2 | 400-1200 |
| D-dimer | 180 | Antyplazmina | 0 |
| Rozpuszczalna fibryna | 45 | TAFI | 45 |
NIEDOKRWISTOŚCI U CIĘŻARNYCH
Niedokrwistość rozpoznaje się zwykle, gdy stężenie hemoglobiny lub hematokryt jest poniżej 5 percentyla rozkładu ich wartości w zdrowej referencyjnej populacji. Ponieważ w ciąży prawidłowej fizjologicznie spada stężenie hemoglobiny we krwi i hematokryt, osiągając nadir w 2 trymestrze, tj. w 20-24 tygodniu (15), nie można rozpoznawać niedokrwistości u ciężarnych na podstawie kryteriów dla kobiet nieciężarnych. Dla kobiet rasy kaukaskiej w wieku prokreacyjnym (20-49 lat) kryterium niedokrwistości jest stężenie hemoglobiny poniżej 12,0 g/dL wg raportu WHO z 1968 r. lub poniżej 12,2 g/dL w oparciu o 5 percentyl prawidłowych wartości z rejestru Scripps-Kaiser w USA (16). Dla kobiet ciężarnych raport WHO przyjmował jako kryterium niedokrwistości stężenie hemoglobiny <11 g/dL, ale Centra Kontroli i Zapobiegania Chorób ( Centers for Disease Control and Prevention, CDC) w USA rekomendują stężenia <11,0 g/dL dla 1. i 3. trymestru i <10,5 g/dL dla 2. trymestru ciąży u kobiet z dostateczną suplementacją żelaza (17). Badania u zdrowych ciężarnych w Danii sugerują przyjęcie stężenia hemoglobiny <11,0 g/dL dla 1. trymestru i <10,5 g/dL dla 2. i 3. trymestru ciąży (5 percentyl prawidłowych wartości) jako kryterium niedokrwistości u kobiet z suplementacją żelaza (18). U ciężarnych nie stosujących suplementacji żelaza należy się spodziewać jednak niższych stężeń hemoglobiny nawet do 10,0 g/dL zwłaszcza w 2. i 3. trymestrze ciąży (18). Najczęściej jako kryterium niedokrwistości przyjmuje się stężenia hemoglobiny <11,0 g/dL w 1. i 3. trymestrze i <10,5 g/dL w 2. trymestrze ciąży oraz <10,0 g/dL po porodzie (19, 20).
Kryteria niedokrwistości przedstawia tabela 4. Niedokrwistość zwiększa ryzyko powikłań i śmiertelność u matek, która przy ciężkiej niedokrwistości (stężęnie hemoglobiny poniżej 5 g/dL) może być nawet 3,5-krotnie większa oraz zwiększa ryzyko porodu martwego płodu, porodu przedwczesnego i urodzenia noworodka z niską masą ciała (19). Niekorzystnie na płód wpływa zwłaszcza ciężka niedokrwistość u matek (stężenie hemoglobiny <6 g/dL). Optymalny dla ciąży, z najmniejszym ryzykiem powikłań, zakres stężeń hemoglobiny u matki jest wąski i wynosi 11-13 g/dL. Podawano nawet najmniejszą częstość porodu przedwczesnego i urodzenia noworodka z niską masą ciała przy stężeniach hemoglobiny u matek poniżej 10 g/dL, a więc poniżej progu dla niedokrwistości. Niekorzystny wpływ ma bowiem również za wysokie stężenie hemoglobiny i przy hemoglobinie powyżej 14,4-14,5 g/dL wzrasta ryzyko porodu martwego płodu, porodu przedwczesnego i urodzenia noworodka z niską masą ciała (19).
Tabela 4. Najczęściej stosowane kryteria niedokrwistości w ciąży (17, 19, 20).
| Grupa kobiet | Stężenie Hb (g/dL) |
| ? Kobiety w wieku rozrodczym | < 12,0 |
| ? Ciężarne w 1. trymestrze | < 11,0 |
| ? Ciężarne w 2. trymestrze | < 10,5 |
| ? Ciężarne w 3. trymestrze | < 11,0 |
| ? Po porodzie | < 10,0 |
| ? W połogu | < 12,0 |
Częstość niedokrwistości u ciężarnych w 3. trymestrze jest szacowana w USA na około 20% wśród kobiet rasy kaukaskiej (15). W Europie częstość niedokrwistości w 2.-3. trymestrze ciąży u kobiet przyjmujących placebo wynosiła 14-52%, a u stosujących suplementację żelaza 0-25% (20). Spośród kobiet z prawidłowymi wartościami hematokrytu> 33% w 1. trymestrze ciąży u 16,2% wystąpiła niedokrwistość w 3. trymestrze ciąży. Wystąpieniu niedokrwistości w ciąży sprzyjają pewne czynniki socjodemograficzne (wiek, rasa, stan materialny), położnicze (mnoga ciąża), medyczne (cukrzyca, nadciśnienie tętnicze, choroby nerek i serca) i tryb życia (palenie, używanie alkoholu). Najczęstsze przyczyny niedokrwistości w ciąży to niedobór żelaza, utrata krwi po porodzie i niedobór kwasu foliowego (tab. 5). Diagnostyka niedokrwistości u ciężarnych przebiega podobnie jak u kobiet nieciężarnych (21) z uwzględnieniem fizjologicznych zmian we krwi zachodzących w ciąży i najczęstszych przyczyn niedokrwistości w ciąży. Ponieważ w ciąży wzrasta MCV zarówno w niedokrwistości mikrocytowej, jak i normocytowej przede wszystkim poszukujemy niedoboru żelaza jako czynnika etiologicznego. Występujące w ciąży obniżenie stężenia żelaza w surowicy, wzrost TIBC i stężenia TfR są identycznie jak przy niedoborze żelaza, dlatego powinno się w pierwszej kolejności dla potwierdzenia niedoboru żelaza oznaczać stężenie ferrytyny w surowicy. Niedokrwistość makrocytowa nie zawsze wskazuje na niedobór kwasu foliowego, zwłaszcza przy nieznacznej makrocytozie. W diagnostyce niedoboru kwasu foliowego przydaje się oznaczenie stężenia całkowitej homocysteiny ( total homocystein, tHcyst) w surowicy, która w ciąży obniża się. Nie należy oznaczać stężenia kwasu foliowego w surowicy, gdyż w ciąży obniża się, ale zawartość folanów w krwinkach czerwonych. Wzrost retikulocytozy w niedokrwistości makrocytowej i normocytowej zwłaszcza w okresie okołoporodowym wskazuje na utratę krwi jako przyczynę niedokrwistości. Na rycinach 1, 2 i 3 przedstawiono zmodyfikowane algorytmy diagnostyczne w przypadku niedokrwistości mikro-, normo- i makrocytowej w ciąży.
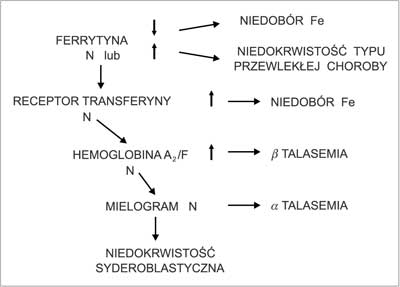
Ryc. 1. Diagnostyka niedokrwistości mikrocytowej w ciąży.
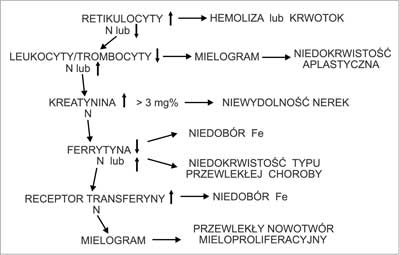
Ryc. 2. Diagnostyka niedokrwistości normocytowej w ciąży.
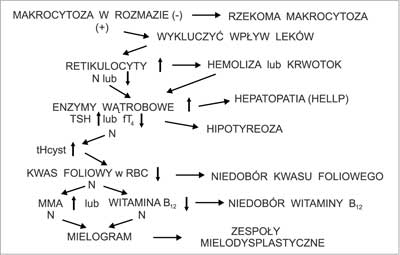
Ryc. 3. Diagnostyka niedokrwistości makrocytowej w ciąży.
Tabela 5. Najczęstsze przyczyny niedokrwistości w ciąży.
| ? Niedobór żelaza |
| ? Utrata krwi |
| ? Niedobór kwasu foliowego |
Niedokrwistość z niedoboru żelaza jest najczęstszą niedokrwistością u ciężarnych. Niedobór żelaza odpowiada za od 75 (19) do 98% (20) wszystkich przypadków niedokrwistości w ciąży. Niedokrwistość z niedoboru żelaza występuje nawet u 37% ciężarnych bez suplementacji żelaza, a niedobór żelaza nawet u 50% ciężarnych z suplementacją żelaza (15). Tak wysoka częstość niedokrwistości z niedoboru żelaza w ciąży wynika z wysokiej częstości niedoboru żelaza i niedokrwistości syderopenicznej w populacji kobiet w wieku rozrodczym i wzrastającego zapotrzebowania na żelazo w ciąży.
CDC szacuje częstość niedoboru żelaza u amerykańskich kobiet w wieku rozrodczym na 11-12%, a niedokrwistości z niedoboru żelaza na 4-5% (17). Zalecanego dziennego spożycia ( recommended dietary allowance, RDA) żelaza w ilości 15 mg przestrzega tylko 1/4 kobiet w wieku rozrodczym. Dorosły człowiek traci przeciętnie 1 mg żelaza dziennie ze stolcem i złuszczonymi komórkami nabłonkowymi skóry i błon śluzowych, a miesiączkująca kobieta dodatkowo do 0,5 mg dziennie. U kobiet w wieku rozrodczym dodatkowym czynnikiem ryzyka rozwoju niedoboru żelaza są obfite miesiączki (≥ 80 ml utraty krwi na miesiąc), które mogą występować u 10% (17). W ciąży wzrasta zapotrzebowanie na żelazo średnio o 3 mg dziennie przez 280 dni ciąży (700-1400 mg na całą ciążę) z powodu rosnącego płodu i łożyska, powiększającej się macicy i wzrastającej masy krwinek czerwonych u matki i utraty krwi w czasie porodu. Zapotrzebowanie na żelazo wzrasta 3-krotnie w 2. i zwłaszcza 3. trymestrze ciąży nawet do 5-8 mg dziennie (15, 17, 20). U kobiet w wieku rozrodczym absorpcja żelaza pokarmowego wynosi przeciętnie 13% i chociaż wzrasta w ciąży kilkukrotnie nawet do 60%, może nie kompensować zwiększonego zapotrzebowania przy małej podaży w diecie. Według WHO zalecane dzienne spożycie ( recommended nutrient intake, RNI) żelaza zależnie od jego biodostępności w diecie (od 15 do 5%) u kobiet w wieku rozrodczym wynosi od 19,6 do 58,8 mg, a w połogu od 10 do 30 mg (22). Z powodu trudności w ocenie metabolizmu żelaza w ciąży WHO w ogóle nie podaje RNI dla kobiet w ciąży i zaleca suplementację żelaza w tabletkach u wszystkich ciężarnych, a w drugiej połowie ciąży w dawce 100 mg dziennie przy braku niedokrwistości. Niedokrwistość z niedoboru żelaza, ale raczej ciężka <8,0 g/dL, ma negatywny wpływ na przebieg ciąży i może zwiększać 2-krotnie ryzyko porodu przedwczesnego i 3-krotnie ryzyko urodzenia noworodka z niską masą ciała (17). Sam niedobór żelaza bez niedokrwistości jest niekorzystny dla kobiet nieciężarnych i prawdopodobnie ciężarnych przynajmniej zwiększając ryzyko wystąpienia niedokrwistości z niedoboru żelaza. Chociaż może być potencjalnie niekorzystny dla płodu, brak dowodów na jego wpływ na ryzyko porodu przedwczesnego i urodzenia noworodka z niską masą ciała. U matek z czynnościowym niedoborem żelaza w postaci wzrostu odsetka hipochromicznych erytrocytów ciąża trwała nawet dłużej a noworodki miały większą masę ciała. W USA u kobiet ciężarnych o niskich dochodach częstość niedokrwistości z niedoboru żelaza szacowana była na 9, 14 i 37%, odpowiednio w 1., 2. i 3. trymestrze ciąży (17). W Europie częstość niedokrwistości z niedoboru żelaza w 2.-3. trymestrze ciąży u kobiet przyjmujących placebo wynosiła 12-17%, a u stosujących suplementację żelaza 0-3% (20).
Częstymi objawami niedokrwistości z niedoboru żelaza w ciąży są uczucie zmęczenia i senność, mogą występować bóle głowy, parestezje, pieczenie języka i spaczone łaknienie czyli jedzenie dziwnych rzeczy bez wartości odżywczej ( pica) (19). Objawami niedoboru żelaza mogą być zapalenie języka, bladość, zajady, rzadziej wklęsłość płytek paznokciowych ( koilonychia). W ciężkiej niedokrwistości z hemoglobiną poniżej 6 g/dL występuje tachykardia, tachypnoe, zapalenie spojówek, wylewy do siatkówki i splenomegalia. Rozpoznanie niedokrwistości z niedoboru żelaza wymaga potwierdzenia laboratoryjnego – oceny morfologicznej krwi obwodowej i biochemicznych markerów metabolizmu żelaza. W tabeli 6 przedstawiono testy biochemiczne i hematologiczne, ich zachowanie się w ciąży i punkty odcięcia wykorzystywane w diagnostyce niedoboru żelaza i niedokrwistości syderopenicznej. Testy biochemiczne wcześniej wykrywają zmiany w metabolizmie żelaza niż testy hematologiczne. CDC definiują niedobór żelaza jako brak żelaza zapasowego w szpiku, wzrost stężenia hemoglobiny o ≥ 1 g/dL w czasie leczenia żelazem lub nieprawidłowe wyniki testów biochemicznych oceniających metabolizm żelaza (17). Według wytycznych CDC niedobór żelaza rozpoznaje się na podstawie nieprawidłowych wyników co najmniej 2 z 3 testów: stężenie protoporfiryny w erytrocytach, stężenie ferrytyny w surowicy i wysycenie transferyny (17). W niedokrwistości z niedoboru żelaza niedoborowi żelaza towarzyszy obniżone stężenie hemoglobiny. W polskich warunkach warte wykorzystania w diagnostyce niedoboru żelaza w ciąży jest stężenie ferrytyny w surowicy i ewentualnie wysycenie transferyny. Prawidłowe stężenie ferrytyny w ciąży pozostaje w granicach 55-70 ?g/l, a jej obniżenie poniżej 35 ?g/l wskazuje na niedobór żelaza. Z nowszych testów hematologicznych dla rozpoznania niedoboru żelaza w ciąży godne polecenia są zawartość hemoglobiny w retikulocytach ( reticulocyte hemoglobin content, CHr) <28,8 pg i odsetek hipochromicznych erytrocytów ( percentage of hypochromic mature red blood cells, %HYPOm)> 3,4% (23). Szersze zastosowanie nowej generacji automatycznych analizatorów hematologicznych pozwoli na łatwe i szybkie rozpoznanie niedoboru żelaza u ciężarnych na podstawie obniżonego CHr i/lub podwyższonego %HYPOm. Punkcja szpiku dla rozpoznania niedoboru żelaza w ciąży praktycznie nie ma zastosowania. Dopuszcza się również rozpoczęcie leczenia żelazem w przypadku niedokrwistości u ciężarnej z hemoglobiną nie niższą niż 9,0 g/dL i dopiero przy braku poprawy po 4-tygodniowym leczeniu preparatem żelaza (ustąpienie niedokrwistości lub wzrost stężenia hemoglobiny ≥ 1,0 g/dL lub hematokrytu ≥ 3%) dalszą diagnostykę niedokrwistości (17).
Tabela 6. Testy biochemiczne i hematologiczne w diagnostyce niedoboru żelaza w ciąży (17, 23).
| Test | Zmiana w ciąży | Punkt odcięcia |
| Stężenie ferrytyny w surowicy | Ż | < 11 ?g/L |
| Wysycenie transferyny | Ż | < 11% |
| Stężęnie protoporfiryny w erytrocytach | | > 70 ?g/dL |
| Stężenie receptora dla transferyny w surowicy | | > 1,8 mg/L |
| Stężenie hemoglobiny we krwi | Ż | < 10,0 g/dL |
| MCV | | < 80 fL |
| Odsetek hipochromicznych erytrocytów | | > 2% |
| Zawartość hemoglobiny w retikulocytach | Ż | < 30,5 pg |
Leczenie niedoboru żelaza i niedokrwistości z niedoboru żelaza polega na suplementacji tego pierwiastka. Najlepszym sposobem jest droga doustna, pamiętając zwłaszcza o wzroście absorpcji żelaza w przewodzie pokarmowym w ciąży. Zalecana dawka doustna żelaza elementarnego lecznicza to 200-300 mg/d, a podtrzymująca 30-60 mg/d, podawana najlepiej 3-4 razy dziennie (19). CDC zalecają leczenie niedokrwistości z niedoboru żelaza w ciąży dawką 60-120 mg/d doustnie, ale kładą nacisk na modyfikację diety ze zwiększeniem pokarmów bogatych w żelazo i zwiększających absorpcję żelaza (17). Skuteczne są również mniejsze dawki żelaza 20-80 mg/d przyjmowane między posiłkami, które rzadziej dają objawy uboczne ze strony przewodu pokarmowego, ale efekt zależy od dawki (20). Wzrost retikulocytozy występuje zwykle po 10 dniach od rozpoczęcia leczenia żelazem, ale udaje się go udokumentować raczej w ciężkiej niż lekkiej niedokrwistości (15). Wzrost stężenia hemoglobiny> 0,5-1,0 g/dL w ciągu 2 tygodni leczenia żelazem oznacza odpowiedź na leczenie, a w przeciwnym wypadku definiuje brak odpowiedzi (20). W ocenie odpowiedzi na leczenie żelazem mogą być przydatne %HYPOm i CHr. Doustny preparat żelaza może wywoływać nudności, wymioty, biegunkę lub zaparcie, lepiej tolerowane są preparaty o powolnym uwalnianiu żelaza. Parenteralne (domięśniowe lub dożylne) podawanie żelaza ma przewagę nad drogą doustną, jeśli chodzi o szybkość odpowiedzi na leczenie (20), ale zagraża wystąpieniem odczynu anafilaktycznego natychmiastowego lub opóźnionego, zwłaszcza przy jednoczesnym przyjmowaniu doustnym (19). Zalecane jest podanie próbnej dawki żelaza (25 mg) przed rozpoczęciem leczenia parenteralnego. Wskazaniami do parenteralnego leczenia żelazem są całkowita nietolerancja preparatów doustnych (po ich przerwaniu), brak odpowiedzi na suplementację doustną, ciężka niedokrwistość syderopeniczna z hemoglobiną <9 g/dL i niedokrwistość syderopeniczna w 3 trymestrze ciąży, a zwłaszcza na 2 tygodnie przed terminem porodu (tab. 7) (19, 20). Dwa ostatnio wymienione wskazania wynikają z konieczności szybkiego uzupełnienia niedoboru żelaza. Z preparatów parenteralnych żelaza zastosowanie znajdują kompleksy żelaza z dekstranem lub dekstryną (okres półtrwania w osoczu 3-4 dni), sacharozą (okres półtrwania 6 godzin) (20, 24) i karboksymaltozą (okres półtrwania 16 godzin) (25). Należna dawka żelaza potrzebna do podniesienia stężenia hemoglobiny do zakładanej wartości (w ciąży zwykle 10,5 g/dL) może być obliczona na podstawie wzoru Ganzoni z 1970 r. uwzględniającego, że objętość krwi stanowi 7% masy ciała, a zawartość żelaza 0,34% masy hemoglobiny: całkowity niedobór żelaza elementarnego w mg = 2,4 x masa ciała w kg x niedobór stężenia hemoglobiny w g/dL (różnica między docelowym a aktualnym stężeniem hemoglobiny) i powinna być zwiększona o 500 mg na odbudowanie zapasów żelaza (25). Dożylne leczenie żelazem jest bezpieczne w 2 i 3 trymestrze ciąży, w 1 trymestrze doświadczenie jest niewielkie i powinno być stosowane dopiero po 14 tygodniu ciąży (20). Żelazo może być podawane dożylnie ambulatoryjnie, o ile dostępna jest aparatura do resuscytacji krążeniowo-oddechowej (20). Uboczne objawy suplementacji parenteralnej to najczęściej dyskomfort w miejscu wstrzyknięcia, przebarwienie skóry, osłabienie, czy smak metaliczny. Umiarkowane objawy uboczne typu gorączki, limfadenopatii i zapalenia żyły zdarzają się w 1-2% przypadków, natomiast anafilaksja tylko w 0,5% przypadków i zwykle po kompleksach żelaza z dekstranem lub dekstryną (19, 20, 24). Podanie próbnej dawki żelaza (25 mg w 15-minutowej infuzji dożylnej z obserwacją do 60 minut) jest zalecane przed rozpoczęciem leczenia kompleksem żelaza z dekstranem, ale nie jest wskazane przed rozpoczęciem leczenia kompleksem żelaza z sacharozą lub karboksymaltozą. Dostępność coraz bezpieczniejszych kompleksów żelaza z sacharozą (Venofer(r)) i karboksymaltozą (Ferinject(r)) zliberalizowała wskazania do dożylnego podawania żelaza w ciąży, które praktycznie jest stosowane już w umiarkowanej niedokrwistości z niedoboru żelaza z hemoglobiną <10 g/dL w 2 i 3 trymestrze ciąży i po porodzie (20, 24). Dodatkową zaletą jest możliwość podania całkowitej obliczonej należnej dawki żelaza jednorazowo w postaci kompleksu z dekstranem lub karboksymaltozą (do 1000 mg) w infuzji dożylnej. Wzrost retikulocytozy obserwowano już po 8 dniach od podania kompleksu żelaza z karboksymaltozą (25). Kompleks żelaza z sacharozą (Venofer(r)) podawany w dawkach podzielonych 200 mg/d w 60 minutowej infuzji dożylnej był skuteczniejszy w niedokrwistości syderopenicznej w ciąży w porównaniu z doustnym siarczanem żelaza w dawce 180 mg/d dając większą i 2-krotnie szybszą odpowiedź przy braku istotnych objawów ubocznych (24). Leczenie kompleksem żelaza z karboksymaltozą (Ferinject(r)) było skuteczniejsze niż siarczanem żelaza podawanym doustnie w dawce 3 x 65 mg lub 2 x 100 mg na dobę u położnic z niedokrwistością syderopeniczną po porodzie dając o 25% większy odsetek odpowiedzi (91,4 i 64,6%) i 2-krotnie szybszą odpowiedź (po 7 i 14 dniach) (25). W ciężkiej niedokrwistości (hemoglobina <9,0 g/dL) z niedoboru żelaza lub przy braku odpowiedzi na leczenie można dołączyć do parenteralnego żelaza rekombinowaną ludzką erytropoetynę w dawce 10 000 U lub 20 000 U podskórnie 2 razy tygodniowo (20, 26). Wzrost stężenia hemoglobiny do ≥ 10,5 g/dL wymaga zmniejszenia dawki doustnego żelaza lub przejścia z parenteralnej na suplementację doustną w dawce 80-100 mg/d (20). CDC zalecają nawet zmniejszenie dawki żelaza do 30 mg/d po wzroście stężenia hemoglobiny do wartości należnej dla danego okresu ciąży (17). Przy leczeniu żelazem korzystne jest dołączenie małej dawki (0,37 mg) kwasu folinowego doustnie (27).
Tabela 7. Wskazania do parenteralnego leczenia niedokrwistości z niedoboru żelaza w ciąży (20, 24).
| ? Nietolerancja doustnego żelaza w dawce leczniczej |
| ? Brak odpowiedzi na doustne żelazo po 2 tygodniach |
| ? Ciężka niedokrwistość z hemoglobiną < 9,0 g/dL |
| ? Niedokrwistość w 3 trymestrze lub po porodzie |
| ? Przewlekła utrata krwi > możliwość suplementacji doustnej |
| ? Leczenie kombinowane z erytropoetyną |
| ? Przeciwwskazania do transfuzji krwinek czerwonych |
Suplementacja żelaza w ciąży przebiegającej bez niedoboru żelaza i bez niedokrwistości syderopenicznej budzi kontrowersje. Na pewno zapobiega wystąpieniu niedokrwistości z niedoboru żelaza u ciężarnej (20). Korzystny wpływ suplementacji żelaza na przebieg ciąży i redukcję wczesnej śmiertelności noworodków wykazano tylko w populacjach kobiet w krajach rozwijających się. Pierwotna prewencja niedoboru żelaza w ciąży może być realizowana przez modyfikację diety ze zwiększeniem podaży produktów bogatych w żelazo i zwiększających absorpcję żelaza lub suplementację doustną żelaza (17). W diecie ciężarnej powinno być więcej żelaza hemowego (zawartego w mięsie, drobiu i rybach) 2-3-krotnie lepiej wchłanialnego w przewodzie pokarmowym niż żelaza niehemowego (zawartego w produktach roślinnych i wzbogacanych w żelazo). Przyswajalność żelaza niehemowego zależy od składu posiłku: żelazo hemowe (w mięsie, drobiu, rybach) i witamina C zwiększają jego absorpcję, natomiast polifenole (w warzywach), taniny (w herbacie), fityniany (w otrębach) i wapń (w produktach mlecznych) zmniejszają jego absorpcję.
Ponieważ większość kobiet w wieku rozrodczym przyjmuje w diecie żelazo poniżej RDA – w USA 75% kobiet poniżej 15 mg/d (17), a w Europie (Dania) nawet> 90% kobiet poniżej 18 mg/d – i ich dieta nie ulega zmianie w ciąży, konieczna jest suplementacja żelaza w 2 i 3 trymestrze ciąży (20). Jako profilaktykę niedoboru żelaza u ciężarnych CDC w USA zalecają małą dawkę żelaza 30 mg doustnie od wczesnej ciąży (17), a w krajach europejskich zaleca się 30-40 mg żelaza doustnie przed spaniem lub między posiłkami (20). Oznaczenie stężenia ferrytyny w surowicy u ciężarnych pozwala zindywidualizować profilaktykę niedoboru żelaza: przy stężeniu ferrytyny> 70 ?g/L nie jest potrzebna suplementacja żelaza, stężenie ferrytyny 30-70 ?g/L wymaga suplementacji 30-40 mg żelaza, a stężenie <30 ?g/L suplementacji 80-100 mg żelaza dziennie (20). Indywidualna profilaktyka niedoboru żelaza w ciąży pozwala zminimalizować ryzyko dla płodu związane z suplementacją żelaza. Ponieważ w okresie organogenezy żelazo może wpływać teratogennie na płód, suplementację można bezpiecznie włączyć dopiero po 8 tygodniu ciąży. Nie zaleca się suplementacji żelaza u ciężarnych bez niedokrwistości, tj. z hemoglobiną> 11 g/dL w 1 i 3 trymestrze i> 10,5 g/dL w 2 trymestrze.
Niedokrwistość z powodu utraty krwi po porodzie jest drugą pod względem częstości niedokrwistością w ciąży. Niedokrwistość poporodowa ma cechy ostrej niedokrwistości pokrwotocznej, ale przyczynia się do jej wystąpienia również niedokrwistość z niedoboru żelaza obecna w 3 trymestrze. Częstość niedokrwistości poporodowej wynosi 27% u kobiet w USA, a w grupie o niskich dochodach nawet 48% (28). Spośród ciężarnych z prawidłowym stężeniem hemoglobiny w 3 trymestrze u 21% występuje niedokrwistość poporodowa. Krwotok poporodowy definiowany jako utrata> 500 mL krwi w czasie porodu zdarza się w 18%, a krwotok ciężki z utratą> 1000-1500 ml krwi w 3% porodów (29). Jego przyczyną jest najczęściej atonia macicy (70%), rzadziej uraz porodowy (20%), łożysko zatrzymane lub inwazyjne, zaburzenia krzepnięcia (29). Zapobieganie, rozpoznanie i postępowanie w krwotoku poporodowym należy do położnika i będzie tutaj tylko zasygnalizowane.
Najlepszym sposobem zapobiegania krwotokowi poporodowemu jest aktywne prowadzenie 3 okresu porodu i profilaktyczne podanie oksytocyny (29). Atonia macicy wymaga masażu macicy i podania leków obkurczających macicę (oksytocyna, alkaloidy sporyszu, prostaglandyny). Poza czynnościami resuscytacyjnymi u matki (dostęp do 2 żył, wlew elektrolitów i koloidów, tlen podawany przez maskę, monitorowanie ciśnienia tętniczego, częstości serca i diurezy) zwłaszcza w ciężkim krwotoku konieczne będzie przetoczenie koncentratu krwinek czerwonych. O ile przetoczenie koncentratu krwinek czerwonych w ciężkim krwotoku poporodowym jest uzasadnione, to transfuzja w każdym krwotoku, a zwłaszcza w każdej niedokrwistości poporodowej, budzi wątpliwości, jeśli prawidłowe postępowanie położnicze usunęło przyczynę krwawienia. Szacuje się, że nawet ponad 30% przetoczonych jednostek krwi w okresie okołoporodowym może być niepotrzebna. Przyjęcie jako wskazania do transfuzji po porodzie podobnych kryteriów jak w populacji ogólnej w tym samym wieku (stężenie hemoglobiny 6,4 g/dL przy niemasywnym krwotoku i stężenie hemoglobiny 8,1 g/dL przy masywnym krwotoku) wykazało, że w Holandii u 68% pacjentek przetoczenie co najmniej 1 jednostki krwi mogło nie być potrzebne, co pozwoliłoby zaoszczędzić aż 46% jednostek krwi (30). Agresywne leczenie preparatami żelaza, zwłaszcza parenteralnymi, niedokrwistości poporodowej pozwala zmniejszyć częstość transfuzji. Z preparatów dożylnych skuteczne są kompleksy żelaza z sacharozą (24) i karboksymaltozą (25), które dają szybszą odpowiedź i są lepiej tolerowane niż siarczan żelaza podawany doustnie. Kompleks żelaza z sacharozą podawany dożylnie był skuteczny w leczeniu niedokrwistości pokrwotocznej poporodowej ze stężeniem hemoglobiny od 6,5 do 8,5 g/dL. Kompleks żelaza z sacharozą podawany był w jednorazowej dawce 200 mg, a kompleks żelaza z karboksymaltozą w dawce jednorazowej maksymalnie 1000 mg, a dawka całkowita zależała od obliczonego niedoboru żelaza elementarnego. Rekombinowana ludzka erytropoetyna była stosowana w niedokrwistości poporodowej w połączeniu z doustnym lub dożylnym żelazem (31). O ile w połączeniu z doustnym preparatem żelaza erytropoetyna w dawce 200 U/kg/d podskórnie dała wzrost stężenia hemoglobiny już od 5 dnia, to w połączeniu z dożylnym kompleksem żelaza z sacharozą nie obserwowano jej korzystnego efektu w całkowitej dawce 20 000 lub 40 000 U (31). Wyniki 2 metaanaliz nie wykazały istotnego wpływu erytropoetyny na zmniejszenie częstości transfuzji w niedokrwistości poporodowej, chociaż obserwowano szybszą poprawę hematologiczną i brak objawów ubocznych.
Niedobór żelaza jest istotną przyczyną niedokrwistości poporodowej. Występuje nawet u 30% kobiet o niskich dochodach w okresie do 6 miesięcy po porodzie, z których 1/3 ma niedokrwistość z niedoboru żelaza (28). Czynnikami ryzyka niedokrwistości z niedoboru żelaza po porodzie są: BMI sprzed ciąży> 24 kg/m2, krwotok porodowy, urodzenie dużego noworodka, brak suplementacji żelaza przed porodem, niedokrwistość w 2. i 3. trymestrze ciąży, mnogi poród, brak lub krótki okres karmienia piersią. U kobiet z niedokrwistością od 3. trymestru ciąży, nadmierną utrata krwi w czasie porodu i porodem mnogim zaleca się po porodzie suplementację doustną żelaza w dawce 60-120 mg/d (28).
Niedokrwistość z niedoboru kwasu foliowego jest 3 najczęstszą przyczyną niedokrwistości w ciąży, a niedobór kwasu foliowego drugim po niedoborze żelaza najczęściej występującym niedoborem w ciąży. Fortyfikacja żywności w kwas foliowy i powszechna suplementacja kwasu foliowego w krajach rozwiniętych u kobiet w ciąży zmniejszyła częstość jego niedoboru i niedokrwistości z nim związanej. Przed wprowadzeniem suplementacji w badaniach wykonanych w latach 60. i 70. ubiegłego wieku częstość niedoboru kwasu foliowego w ciąży oceniana na podstawie obecności zmian megaloblastycznych w rozmazach szpiku kostnego wynosiła od 25% w krajach rozwiniętych do 60% w krajach rozwijających się, a częstość niedokrwistości megaloblastycznej, odpowiednio, od 2,8 do 24% (15). U kobiet w wieku rozrodczym (25-44 lat) w Iranie stwierdzano nawet obniżone stężenie kwasu foliowego w 98%, mimo średniego dziennego spożycia 270 ?g. Ostatnie badania w krajach rozwijających się podają zdecydowanie niższą częstość, np. tylko u 14,3% kobiet irańskich w wieku rozrodczym stwierdzono niedobór kwasu foliowego na podstawie obniżonego jego stężenia w surowicy (32). Częstość niedokrwistości megaloblastycznej u kobiet w ciąży w Wielkiej Brytanii obecnie wynosi 0,2-5% i zależy od stanu odżywienia i zamożności (33). Według WHO RNI dla kwasu foliowego u kobiet w wieku rozrodczym wynosi 400 ?g, w ciąży wzrasta do 600 ?g, a w połogu do 500 ?g (22). Czynnikami predysponującymi do wystąpienia niedokrwistości z niedoboru kwasu foliowego w ciąży są (tab. 8): dieta uboga w folany, mnoga ciąża, współistniejąca niedokrwistość hemolityczna, zakażenie układu moczowego, leki interferujące w metabolizm kwasu foliowego (trimetoprim, dwufenylohydantoina, nitrofurantoina, barbiturany, sulfasalazyna, doustne leki antykoncepcyjne), spożywanie alkoholu, pora roku (mniejsza dostępność świeżych warzyw w zimie w naszym rejonie geograficznym) (15, 34). Zapasy kwasu foliowego w organizmie są rzędu 5-10 mg, czyli relatywnie małe w porównaniu z RNI, i wystarczają co najwyżej na 2-3 miesiące (34). Niedobór kwasu foliowego upośledza syntezę DNA i metioniny, prowadząc do wzrostu stężenia homocysteiny w surowicy. Podwyższone stężenie homocysteiny w ciąży jest związane z wystąpieniem powikłań położniczych: stanu przedrzucawkowego, przedwczesnego oddzielenia się łożyska, porodu przedwczesnego i poronienia. Przy negatywnym bilansie kwasu foliowego po 7-11 tygodniach pojawiają się zmiany we krwi obwodowej w postaci makrocytozy i hipersegmentacji granulocytów obojętnochłonnych (wzrost do 6 liczby płatów jąder w granulocytach), a po 17-19 tygodniach występuje niedokrwistość makrocytowa z odnową megaloblastyczną w szpiku.
Tabela 8. Czynniki ryzyka niedokrwistości z niedoboru folanów w ciąży (15).
| ? Dieta uboga w folany |
| ? Ciąża mnoga |
| ? Niedokrwistość hemolityczna |
| ? Zakażenie układu moczowego |
| ? Leki wpływające na metabolizm folanów |
| ? Alkohol |
| ? Pora roku z mniejszą dostępnością świeżych warzyw |
Również w ciąży niedobór kwasu foliowego może być przyczyną małopłytkowości i pancytopenii. Niedobór kwasu foliowego u matki w okresie przed zapłodnieniem i we wczesnej ciąży może prowadzić do urodzenia noworodka o niskiej masie ciała i wystąpienia u płodu wad cewy nerwowej (bezmózgowie, rozszczep kręgosłupa, przepuklina mózgowa). Występowanie wad cewy nerwowej u płodu związane jest z hiperhomocysteinemią i mutacją genu dla reduktazy metylenotetrahydrofolanowej. Po wprowadzeniu fortyfikacji żywności i suplementacji kwasu foliowego w niektórych krajach częstość wad cewy nerwowej u noworodków zdecydowanie spadła, nawet o 92% (35). Zmniejszyła się również częstość innych wad wrodzonych, m.in. układu krążenia i moczowego.
We wtórnej prewencji wad wrodzonych u płodu kobietom planującym ciążę zaleca się w okresie 3 miesięcy poprzedzających zapłodnienie i w okresie pierwszych 12 tygodni ciąży stosowanie diety bogatej w folany oraz suplementację kwasu foliowego w dawce 5 mg/d, a od 12 tygodnia ciąży do połogu w dawce 0,4-1,0 mg/d (36). W pierwotnej prewencji zaleca się w okresie 3 miesięcy poprzedzających zapłodnienie i w okresie ciąży i połogu stosowanie diety bogatej w folany oraz suplementację kwasu foliowego w dawce od 0,4-1,0 mg/d przy małym ryzyku do 5 mg/d przy dużym ryzyku wystąpienia wad wrodzonych u płodu (36). Źródłem kwasu foliowego w diecie są świeże zielone, zwłaszcza liściaste, warzywa i owoce. Gotowanie warzyw może zmniejszyć biodostępność folanów nawet o 50-90% (34).
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
24 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
59 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
119 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 28 zł
Piśmiennictwo
1. Clark P, Greer IA: Hematology measurements in pregnancy. In: Clark P, Greer IA. Practical obstetric hematology. Abingdon: Taylor & Francis Group; 2006; p. 1-14.
2. McMullin MF, White R, Lappin T et al.: Haemoglobin during pregnancy: relationship to erythropoietin and haematinic status. Eur J Haematol 2003; 71: 44-50.
3. Ervasti M, Kotisaari S, Heinonen S et al.: Elevated serum erythropoietin concentration is associated with coordinated changes in red blood cell and reticulocyte indices of pregnant women at term. Scand J Clin Lab Invest 2008; 68: 160-5.
4. Ueland K: Maternal cardiovascular dynamics. VII. Intrapartum blood volume changes. Am J Obstet Gynecol 1976; 126(6): 671-7.
5. Murphy MM, Scott JM, McPartlin JM et al.: The pregnancy-related decrease in fasting plasma homocysteine is not explained by folic acid supplementation, hemodilution, or a decrease in albumin in a longitudinal study. Am J Clin Nutr 2002; 76: 614-9.
6. Murphy MM, Scott JM, Arija V et al.: Maternal homocysteine before conception and throughout pregnancy predicts fetal homocysteine and birth weight. Clin Chem 2004; 50: 1406-12.
7. Lurie S, Rahamim E, Piper I et al.: Total and differential leukocyte counts percentiles in normal pregnancy. Eur J Obstet Gynecol Reprod Biol 2008;136: 16-9.
8. Belo L, Santos-Silva A, Rocha S et al.: Fluctuations in C-reactive protein concentration and neutrophil activation during normal human pregnancy. Eur J Obstet Gynecol Reprod Biol 2005; 123: 46-51.
9. Verdy E, Bessous V, Dreyfus M et al.: Longitudinal analysis of platelet count and volume in normal pregnancy. Thromb Haemost 1997; 77: 806-7.
10. Bremme KA: Haemostatic changes in pregnancy. Best Pract Res Clin Haematol 2003; 16: 153-68.
11. Paidas MJ, Ku DH, Lee MJ et al.: Protein Z, protein S levels are lower in patients with thrombophilia and subsequent pregnancy complications. J Thromb Haemost 2005; 3: 497-501.
12. Coolman M, de Groot CJ, Steegers EA et al.: Concentrations of plasminogen activators and their inhibitors in blood preconceptionally, during and after pregnancy. Eur J Obstet Gynecol Reprod Biol 2006; 128: 22-8.
13. Robb AO, Mills NL, Din JN et al.: Acute endothelial tissue plasminogen activator release in pregnancy. J Thromb Haemost 2009; 7: 138-42.
14. Mousa HA, Downey C, Alfirevic Z et al.: Thrombin activatable fibrinolysis inhibitor and its fibrinolytic effect in normal pregnancy. Thromb Haemost 2004; 92: 1025-31.
15. Williams MD, Wheby MS: Anemia in pregnancy. Med Clin North Am 1992; 76: 631-47.
16. Beutler E, Waalen J: The definition of anemia: what is the lower limit of normal of the blood hemoglobin concentration? Blood 2006; 107: 1747-50.
17. Recommendations to prevent and control iron deficiency in the United States. Centers for Disease Control and Prevention. MMWR Recomm Rep 1998; 47(RR-3): 1-29.
18. Milman N, Byg KE, Agger AO: Hemoglobin and erythrocyte indices during normal pregnancy and postpartum in 206 women with and without iron supplementation. Acta Obstet Gynecol Scand 2000; 79: 89-98.
19. Sifakis S, Pharmakides G: Anemia in pregnancy. Ann N Y Acad Sci 2000; 900: 125-36.
20. Milman N: Prepartum anaemia: prevention and treatment. Ann Hematol 2008; 87: 949-59.
21. Sikorski T, Marcinowska-Suchowierska E: Interpretacja wyników badań hematologicznych w praktyce lekarza rodzinnego. Post Nauk Med 2007; 20: 112-8.
22. World Health Organization, Food and Agriculture Organization of the United Nations. Vitamin and mineral requirements in human nutrition. 2nd ed. Geneva: World Health Organization; Rome: Food and Agriculture Organization of the United Nations; 2004. p. 246-302.
23. Ervasti M, Kotisaari S, Heinonen S et al.: Use of advanced red blood cell and reticulocyte indices improves the accuracy in diagnosing iron deficiency in pregnant women at term. Eur J Haematol 2007; 79: 539-45.
24. Perewusnyk G, Huch R, Huch A et al.: Parenteral iron therapy in obstetrics: 8 years experience with iron-sucrose complex. Br J Nutr 2002; 88: 3-10.
25. Lyseng-Williamson KA, Keating GM: Ferric carboxymaltose: a review of its use in iron-deficiency anaemia. Drugs 2009; 69: 739-56.
26. Krafft A, Bencaiova G, Breymann C: Selective use of recombinant human erythropoietin in pregnant patients with severe anemia or nonresponsive to iron sucrose alone. Fetal Diagn Ther 2009; 25: 239-45.
27. Juarez-Vazquez J, Bonizzoni E, Scotti A: Iron plus folate is more effective than iron alone in the treatment of iron deficiency anaemia in pregnancy: a randomised, double blind clinical trial. BJOG 2002; 109: 1009-14.
28. Bodnar LM, Cogswell ME, McDonald T: Have we forgotten the significance of postpartum iron deficiency? Am J Obstet Gynecol 2005; 193: 36-44.
29. Anderson JM, Etches D: Prevention and management of postpartum hemorrhage. Am Fam Physician 2007; 75: 875-82.
30. So-Osman C, Cicilia J, Brand A et al.: Triggers and appropriateness of red blood cell transfusions in the postpartum patient-a retrospective audit. Vox Sang 2010; 98: 65-9.
31. Wĺgström E, Akesson A, Van Rooijen M et al.: Erythropoietin and intravenous iron therapy in postpartum anaemia. Acta Obstet Gynecol Scand 2007; 86: 957-62.
32. Abdollahi Z, Elmadfa I, Djazayeri A et al.: Folate, vitamin B12 and homocysteine status in women of childbearing age: baseline data of folic acid wheat flour fortification in Iran. Ann Nutr Metab 2008; 53: 143-50.
33. Burton R, Kelion Z, Costello C: Severe folate deficiency in pregnancy with normal red cell folate level. Clin Lab Haematol 2006; 28: 66-8.
34. Snow CF: Laboratory diagnosis of vitamin B12 and folate deficiency: a guide for the primary care physician. Arch Intern Med 1999; 159: 1289-98.
35. Czeizel AE, Dudás I: Prevention of the first occurrence of neural-tube defects by periconceptional vitamin supplementation. N Engl J Med 1992; 327: 1832-5.
36. Wilson RD, Johnson JA, Wyatt P et al.: Pre-conceptional vitamin/folic acid supplementation 2007: the use of folic acid in combination with a multivitamin supplement for the prevention of neural tube defects and other congenital anomalies. J Obstet Gynaecol Can 2007; 29: 1003-26.
37. Selhub J, Jacques PF, Dallal G et al.: The use of blood concentrations of vitamins and their respective functional indicators to define folate and vitamin B12 status. Food Nutr Bull 2008; 29(2 Suppl): S67-73.
38. McMullin MF, Young PB, Bailie KE et al.: Homocysteine and methylmalonic acid as indicators of folate and vitamin B12 deficiency in pregnancy. Clin Lab Haematol 2001; 23: 161-5.
39. Gill KK, Kelton JG: Management of idiopathic thrombocytopenic purpura in pregnancy. Sem Hematol 2000; 37: 275-89.
40. British Committee for Standards in Haematology General Haematology Task Force. Guidelines for the investigation and management of idiopathic thrombocytopenic purpura in adults, children and in pregnancy. Br J Haematol 2003; 120: 574-96.
41. McCrae KR, Cines DB. Thrombotic microangiopathy during pregnancy. Sem Hematol 1997; 34: 148-58.
42. Provan D, Stasi R, Newland AC et al.: International consensus report on the investigation and management of primary immune thrombocytopenia. Blood 2010; 115: 168-86.
43. Rodeghiero F, Stasi R, Gernsheimer T et al.: Standardization of terminology, definitions and outcome criteria in immune thrombocytopenic purpura of adults and children: report from an international working group. Blood 2009; 113: 2386-93.
44. Page LK, Psaila B, Provan D et al.: The immune thrombocytopenic purpura (ITP) bleeding score: assessment of bleeding in patients with ITP. Br J Haematol 2007; 138: 245-8.
45. Allford SL, Hunt BJ, Rose P et al.: Guidelines on the diagnosis and management of the thrombotic microangiopathic haemolytic anaemias. Br J Haematol 2003; 120: 556-73.
46. Mannucci PM, Canciani MT, Forza I et al.: Changes in health and disease of the metalloprotease that cleaves von Willebrand factor. Blood 2001; 98: 2730-5.
47. Bick RL, Hoppensteadt D: Disseminated intravascular coagulation in obstetrics, pregnancy, and gynecology: Criteria for diagnosis and management. In: Bick RL, editor. Hematological complications in obstetrics, pregnancy, and gynecology. Cambridge: University Press; 2006. p. 1-54.
48. Levi M, Toh CH, Thachil J et al.: Guidelines for the diagnosis and management of disseminated intravascular coagulation. British Committee for Standards in Haematology. Br J Haematol 2009; 145: 24-33.
49. Windyga J, Chojnowski K, Klukowska A et al.: Polskie zalecenia postępowania we wrodzonych skazach krwotocznych na tle niedoboru czynników krzepnięcia. Część I: Zasady postępowania w hemofilii A I B. Acta Haematol Pol 2008; 39: 537-64.
50. Apperley J: CML in pregnancy and childhood. Best Practice Res Clin Haematol 2009; 22: 455-74.



