© Borgis - Postępy Nauk Medycznych 8/2010, s. 595-599
*Michał Rabijewski, Jarosław Kozakowski, Wojciech Zgliczyński
Związek stężeń testosteronu, estradiolu i siarczanu dehydroepiandrosteronu z zaburzeniami wzwodu u zdrowych mężczyzn w starszym wieku
The relationship of serum testosterone, estradiol and dehydroepiandrosterone sulfate to erectile dysfunction in healthy, aging male
Klinika Endokrynologii Centrum Medycznego Kształcenia Podyplomowego, Szpital Bielański
Kierownik Kliniki: prof. dr hab. med. Wojciech Zgliczyński
Streszczenie
Cel pracy: Celem pracy była ocena stężeń testosteronu, siarczanu dehydroepiandrosteronu (DHEAS) oraz estradiolu u zdrowych, starszych mężczyzn oraz ocena częstości zaburzeń wzwodu (ED). U 179 mężczyzn w średnim wieku 61,4 lat oceniono funkcje erekcyjne na podstawie kwestionariusza International Index of Erectile Function (IIEF). Badanych zakwalifikowano do 5 kategorii według uzyskanych wyników. Oceniano poranne stężenia testosteronu całkowitego, DHEAS oraz estradiolu. Częstość ED w całej badanej grupie wynosiła 53,6%. W zależności od wieku ED występowały u 29,2% mężczyzn w wieku 40-49 lat, 39,3% w wieku 50-59, 54,3% w wieku 60-69, 72,7% w wieku powyżej 70 lat. Średnie stężenie testosteronu oraz DHEAS statystycznie istotnie zmniejszało się z wiekiem (p<0,05) i było istotnie niższe u pacjentów z umiarkowanymi i ciężkimi objawami ED według IIEF-5 w porównaniu ze zdrowymi oraz tymi z niewielkimi i niewielkimi do umiarkowanych ED. Wykazano istotną ujemną korelację pomiędzy punktacją IIEF-5 a stężeniami testosteronu całkowitego (r=-0,34, p<0,05), stężenia estradiolu i DHEAS nie korelowały ze wskaźnikiem IIEF-5.
Wnioski: częstość zaburzeń wzwodu wzrasta z wiekiem natomiast obniżają się stężenia testosteronu i DHEAS, Mężczyźni z nasilonymi zaburzeniami wzwodu mają istotnie niższe stężenia testosteronu i DHEAS. Stężenia testosteronu wykazują istotną ujemną korelacje z nasileniem zaburzeń wzwodu według IIEF-5.
Summary
The aim of this study was to evaluate serum testosterone, dehydroepiandrosterone sulfate (DHEAS) and estradiol levels in normal aging men and these relationship with erectile function. In a study 179 men completed questionnaire International Index of Erectile Function (IIEF-5), as a diagnostic tool for erectile dysfunction (ED). Patients were classified into 5 categories based on the scores. Serum total testosterone, DHEAS and estradiol was measured morning in all men. Mean age was 61.4 years. In these patients the prevalence of erectile dysfunction was estimated to be 53.6%. According to age the erectile dysfunction rate was 29.2% in the 40 to 49, 39.3% in the 50 to 59, 54.3% in the 60 to 69, 72.7% in the above 70 years group (p<0.05). The mean serum total testosterone and DHEAS significantly decreased with age (p<0.05) and were statistical significant lower in men with moderate and severe erectile dysfunctions according IIEF when compared with those without erectile dysfunction and with mild and mild to moderate. There was negative correlation between IIEF-5 score and testosterone levels (r=-0.34, p<0.05), estradiol and DHEAS levels did not correlate with IIEF-5 score.
Conclusions: erectile dysfunctions decreased with aging ehilr testosterone and DHEAS levels decreased with aging. Men with erectile dysfunctions have lower testosterone and DHEAS levels. Testosterone levels showed a statistical significant negative correlation with erectile dysfunctions according IIEF-5.

Wstęp
Starzenie się mężczyzn jest procesem złożonym, w którym istotne znaczenie odgrywa stopniowe obniżanie się stężenia testosteronu objawiające się zmniejszeniem masy i siły mięśni, wzrostem masy tkanki tłuszczowej, osteoporozą, pogorszeniem jakości życia, depresją oraz obniżeniem libido i zaburzeniami wzwodu (1-4). Zmniejszeniu stężenia testosteronu całkowitego towarzyszy stopniowy wzrost stężenia globuliny wiążącej hormony płciowe (SHBG), co pogłębia niedobór biodostępnego testosteronu (5). Zjawisko postępującego wraz z wiekiem niedoboru testosteronu dotyczy wszystkich mężczyzn, ale jego tempo jest indywidualne (6). Prawidłowe funkcje seksualne u mężczyzn zależą od złożonego mechanizmu, w którym znaczenie mają czynniki psychiczne, neurologiczne, naczyniowe i endokrynne (7). Nie jest jasne, który z tych czynników odgrywa wiodącą rolę w uzyskaniu i utrzymaniu erekcji, dotyczy to zwłaszcza roli androgenów, testosteronu i siarczanu dehydroepiandrosteronu (DHEAS) (7, 8). W wielu pracach wykazano, że starzenie związane jest ze stopniowym zmniejszeniem aktywności seksualnej, a zwłaszcza wzrostem częstości zaburzeń wzwodu (9, 10). Androgeny regulują libido i aktywność seksualną, ale ich wpływ na mechanizm erekcji pozostaje niejasny (11). Jednakże najnowsze dane wskazują, że testosteron ma dobroczynny wpływ na funkcje seksualne (12). Nie wiadomo również, czy tylko testosteron, czy także estradiol oraz DHEAS mają znaczenie w mechanizmie erekcji (8, 13). Celem pracy była ocena stężeń testosteronu, DHEAS i estradiolu u zdrowych starszych mężczyzn i ich wpływ na zaburzenia wzwodu.
Materiał i metody
Materiał stanowiło 179 mężczyzn w średnim wieku 61,4 lat, rekrutowanych spośród pacjentów Poradni Endokrynologicznej zgłaszających się z powodu zaburzeń nie mających związku z zaburzeniami gospodarki androgenowej ani potencją. Pacjenci wypełniali kwestionariusz International Index of Erectile Function w jego zmodyfikowanej formie, zawierającej 5 pytań dotyczących funkcji erekcyjnej (IIEF-5) (13, 14). Odpowiedzi na pytania udziela się w 5-stopniowej skali, gdzie 1 punkt oznacza całkowity brak funkcji erekcyjnej, a 5 punktów oznacza prawidłową funkcję erekcyjną. Wyniki mieszczą się w zakresie od 1 do 25 punktów. Wynik powyżej 21 punktów oznacza prawidłowe funkcje erekcyjne, a wynik ≤ 21 punktów oznacza zaburzenia wzwodu. Zaburzenia podzielono na 4 stopnie: ciężkie – 1 do 7 punktów, umiarkowane – 8 do 11 punktów, niewielkie do umiarkowanych – 12 do 16, niewielkie – 17 do 21 punktów i brak – 22 do 25 punktów. Krew do oznaczeń hormonalnych pobierano na czczo w godzinach 8.00-9.00. Testosteron oznaczano metodą RIA, norma: 2,5-12,0 ng/ml, siarczan dehydroepiandrosteronu (DHEAS) metodą RIA, norma: 2000-3750 ng/ml, estradiol oznaczano metodą chemiluminescencyjną, norma estradiolu – do 53 pg/ml.
Z badania wykluczono mężczyzn z chorobami układu podwzgórzowo-przysadkowo-gonadowego, cukrzycą i innymi chorobami przewlekłymi oraz zaburzeniami wzwodu wcześniej zdiagnozowanymi i leczonymi inhibitorami PDE5 oraz mężczyzn, którzy nie przejawiali aktywności seksualnej w ciągu ostatnich 6 miesięcy, a także przyjmujących leki mogące wpływać na stężenia hormonów lub potencję. W analizie statystycznej zastosowano analizę wariancji (ANOVA) oraz obliczano wskaźnik korelacji Pearsona, uważając p<0,05 za znamienne statystycznie.
Wyniki
Średni wiek mężczyzn wynosił 61,4 lat (od 47 do 72 lat). W całej badanej grupie mężczyzn częstość zaburzeń wzwodu wynosiła 53,6%, z czego niewielkie zaburzenia obserwowano u 21,8% mężczyzn, niewielkie do umiarkowanych u 13,9%, umiarkowane u 6,1% oraz ciężkie u 11,7% – tabela 1. W zależności od wieku ED występowały u 29,2% mężczyzn w wieku 40-49 lat, 39,3% w wieku 50-59 lat, 54,3% w wieku 60-69 lat oraz 72,7% w wieku powyżej 70 lat. Wykazano statystycznie istotne różnice pomiędzy badanymi grupami (p<0,05), z wyjątkiem grup 40-49 lat oraz 50-59 lat (ryc. 1).
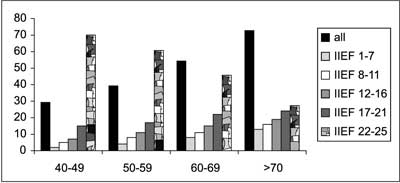
Ryc. 1. Częstość zaburzeń wzwodu w poszczególnych grupach wiekowych, słupek czarny pokazuje całkowitą częstość zaburzeń wzwodu w danej grupie wiekowej. Istotna statystycznie różnica pomiędzy grupami z wyjątkiem grup 40-49 i 50-59 lat (test ANOVA; p<0,05).
Tabela 1. Częstość zaburzeń wzwodu w badanej populacji według IIEF-5.
| Funkcje erekcyjne | N (%) |
| Zdrowi | 83 (46,1) |
| ED wg IIEF-5 | 96 (53,6) |
| IIEF-5 1-7 | 21 (11,7) |
| IIEF-5 8-11 | 11 (6,1) |
| IIEF-5 12-16 | 25 (13,9) |
| IIEF-5 17-21 | 39 (21,8) |
Średnie stężenia testosteronu, DHEAS i estradiolu przedstawiono w tabeli 2. Wykazano istotnie niższe stężenia testosteronu całkowitego w grupie mężczyzn w wieku 60-69 lat, 70-79 lat i>70. roku życia w stosunku do grupy 40-49 lat i 50-59 lat (p<0,02). Nie obserwowano istotnych statystycznie różnic stężeń testosteronu pomiędzy grupami 40-49 lat oraz 50-59 lat (p=0,07). Stężenia DHEAS obniżały się istotnie statystycznie wraz z wiekiem w badanych grupach, natomiast stężenia estradiolu nie zmieniały się istotnie wraz z wiekiem, z wyjątkiem grupy 50-59 lat, gdzie były istotnie wyższe w stosunku do pozostałych grup (p<0,02).
Tabela 2. Średnie stężenia testosteronu całkowitego, siarczanu dehydroepiandrosteronu (DHEAS) i estradiolu w badanych grupach (*p<0,05 oraz **p<0,02 vs. grupy 40-49 oraz 50-50 lat, #p<0,02 vs. pozostałe grupy).
| Grupa wiekowa | Testosteron (ng/ml ? SD) | DHEAS (ng/ml ? SD) | Estradiol (pg/ml ? SD) |
| 40-49 lat | 6,56 ? 1,56 | 2 450 ? 543 | 28,2 ? 5,4 |
| 50-59 lat | 5,74 ? 1,43 | 2 329 ? 493 | 29,8 ? 6,2 |
| 60-69 lat | 4,38 ? 1,39* | 2 042 ? 562** | 38,5 ? 5,9# |
| >70 lat | 4,11 ? 1,65* | 1 945 ? 633** | 33,2 ? 6,3 |
Wraz z wiekiem wzrastał procentowy udział mężczyzn ze stężeniami testosteronu całkowitego poniżej 3,5 ng/ml, a więc poniżej przyjętej dolnej normy i wynosił w grupie 40-49 lat – 4,7%, w grupie 50-59 lat – 7,3%, w grupie 60-69 lat – 15,3% oraz>70 lat – 33,3%.
Średnie stężenie testosteronu było istotnie niższe u mężczyzn z umiarkowanymi i ciężkimi zaburzeniami wzwodu według IIEF-5 w stosunku do grupy zdrowej oraz pozostałych 2 grup mężczyzn z ED (p<0,02 vs, zdrowi oraz grupa z zaburzeniami niewielkimi i niewielkimi do umiarkowanych wg IIEF-5) – rycina 2. Podobnie stężenia DHEAS były istotnie niższe tylko u mężczyzn w grupach z zaawansowanymi ED w stosunku do grupy zdrowej i pozostałych 2 grup (p<0,05 vs. zdrowi oraz grupa z zaburzeniami niewielkimi i niewielkimi do umiarkowanych wg IIEF-5). Stężenia estradiolu nie różniły się istotnie pomiędzy mężczyznami zdrowymi i z ED (według IIEF-5).
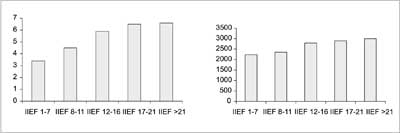
Ryc. 2. Stężenia testosteronu i DHEAS u pacjentów z zaburzeniami wzwodu według IIEF-5 (*p<0,02, **p<0,05 vs. pozostałe grupy).
Wykazano istotną ujemną korelację pomiędzy punktacją IIEF-5 a stężeniami testosteronu całkowitego (r=-0,34, p<0,05) w całej grupie mężczyzn z zaburzeniami wzwodu według IIEF-5 (≤ 21 punktów), stężenia DHEAS i estradiolu nie korelowały ze wskaźnikiem IIEF-5.
Dyskusja
Uzyskane wyniki badań wskazują, że częstość zaburzeń wzwodu wzrasta z wiekiem, natomiast obniżają się stężenia testosteronu i DHEAS. Mężczyźni z nasilonymi zaburzeniami wzwodu mają istotnie niższe stężenia testosteronu i DHEAS w porównaniu ze zdrowymi i stężenia testosteronu i DHEAS wykazują istotną ujemną korelacje z nasileniem zaburzeń wzwodu definiowanym według IIEF-5. Należy podkreślić, że badana grupa nie była całkowicie reprezentatywna dla populacji zdrowych mężczyzn, ponieważ byli oni rekrutowani spośród osób zgłaszających się do poradni endokrynologicznej. Jednak z badań wykluczono mężczyzn z patologiami mogącymi istotnie wpływać na metabolizm i działanie androgenów lub powodować bezpośrednio luib pośrednio zaburzenia wzwodu.
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
24 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
59 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
119 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 28 zł
Piśmiennictwo
1. Vermeulen A: Some reflections on the endocrinology of the aging male. The Aging Male 1998; 1: 163-168.
2. Nieschlag E, Swerdloff R, Behre HM et al.: ISA, ISSAM, EAU, EAA and ASA recommendations: investigation, treatment and monitoring of late-onset hypogonadism in males. THe Aging Male 2009; 12 (10): 5-12.
3. Kaufmann JM, Vermeulen A: The decline of androgens levels in elderly men and its clinical and therapeutic implications. Endocr Review 2005; 26: 833-876.
4. Rabijewski M, Jakiel G, Zgliczyński W: Zespół niedoboru testosteronu. Medycyna po Dyplomie 2008; 7: 77-79.
5. Feldman HA, Longcope C, Derby C et al.: Age trends in the level of serum testosterone and other hormones in middle-aged men: longitudinal results from Massachusetts Male Aging Study. J Clin Endocrinol Metab 2002; 87: 589-598.
6. Harman SM, Metter EJ, Tobin JD et al.: Longitudinal effects of aging on serum total and free testosterone levels in healthy men: Baltimore Longitudinal Study of Aging. J Clin Endocrinol Metab 2001; 86: 724-731.
7. Buvat J, Bou Jaoude G: Significance of hypogonadism in erectile dysfunction. World J Urol 2006; 24: 657-667.
8. Roumequere T: Rationale for androgens and erectile dysfunction in 2006. Eur Urol 2006; 50: 898-900.
9. Gooren, LJG: The age-related decline of androgen levels in men: clinically significant? Br J Urol 1996; 78: 763-768.
10. Feldman HA, Goldstein I, Hatzichristou DG et al.: Impotence and its medical and psychosocial correlates: results of the Massachusetts Male Aging Study J Urol 1994; 151: 54-61.
11. Mikhail N: Does testosterone have a role in erectile function? Am J Med 2006; 139: 373-382.
12. Mulhall J, Valenzuela R, Aiv N et al.: Effect of testosterone supplementation on sexual function in hypogonadal men with erectile dysfunction. Urology 2004; 63: 348-353.
13. Reiter W, Pycha A, Schatzl G et al.: Serum dehydroepiandrosterone sulfate concentraytions in men with erectile dysfunction. Urology 2000; 55: 755-758.
14. Rosen RC, Cappelleri JC, Smith MD et al.: Development and evaluation of (an) abridged, 5-item version of the International Index of Erectile Function (IIEF-5) as a diagnostic tool for erectile dysfunction. Int J Impot Res 1999; 11: 319-327.
15. Rosen RC, Riley A, Wagner G et al.: The International Index of Erectile Function (IIEF): a multidimensional scale for assessment of erectile dysfunction. Urology 1997; 49: 822-828.
16. Stief C: Testosterone and erection: practical management for the patient with erectile dysfunction. Eur Urol 2007; supl. 6: 868-873.
17. Morgentaler A. Male impotence. Lancet 1999; 354: 1713-1718.
18. Guay AT: Testosterone and erectile physiology. Aging Male 2006; 9 (4): 201-206.
19. Vermulen A, Kaufman JM: Aging of the hypothalamo-pituitary-testicular axis in men. Horm Res 1995; 43: 25-32.
20. Deslypere JP, Vermulen A: Leydig cell function in normal men: effects of aging, life-style, residence, diet, and activity. J Clin Endocrinol Metab 1984; 59: 95-101.
21. Joahannes CB, Araujo AB, Feldman H A et al.: Incidence of erectile dysfunction in men 40 to 69 years old: longitudinal results from the Massachusetts Male Aging Study. J Urol 2000; 163: 460-467.
22. Zitzmann M, Faber S, Nieschlag E: Association of specific symptoms and metabolic risks with serum testosterone in older men. J Clin Endocrinol Metab 2006; 91: 4335-4343.
23. Tserotas K, Merino G: Andropause and the aging male. Arch Androl 1998; 40: 87-93.
24. Korenman SG, Morley JE, Mooradian AD et al.: Secondary hypogonadism in older men: its relation to impotence. J Clin Endocr Metab 1990; 71: 963-969.
25. Nieschlag E, Lammers U, Freischem C et al.: Reproductive function in young fathers and grandfathers. J Clin Endocr Metab 1982; 55: 676-681.
26. Davidson JM, Chen JJ, Crapo L et al.: Hormonal changes and sexual function in aging men. J Clin Endocr Metab 1983; 37: 71-76.
27. Tsitouras RD, Martin FE, Harman SM: Relationship of serum testosterone to sexual activity in eldery men. J Gerontol 1982; 37: 288-293.
28. Gray A, Feldman A, McKinlay JB et al.: Age disease, and changing sex hormone levels in middle-aged men: results of the Massachusetts Male Aging Study. J Clin Endocrinol Metab1991; 73: 1016-1023.
29. Morales A, Johnston B, Heaton JP et al.: Testosterone supplementation for hypogonadal impotence: assessment of biochemical measures and therapeutic outcomes. J Urol 1997; 157: 849-855.
30. Becker AJ, Uckert S, Stief CG et al.: Cavernous and systemic testosterone levels in different phases of human penile erection. Urology 2000; 56: 125-131.
31. Rabijewski M, Kubuj M, Zgliczyński S: Skuteczność i bezpieczeństwo hormonalnego leczenia zastępczego (HLZ) testosteronem u starszych mężczyzn z hipogonadyzmem. Endokrynol Pol 2003; 3 (54): 293-300.
32. Reiter WJ, Pycha A, Schatzl G et al.: Dehydroepiandrosterone in the treatment of erectile dysfunction: a prospective, double-blind, randomized, placebo-controlled study. Urology 1999; 53: 590-595.


