© Borgis - Postępy Nauk Medycznych 8/2010, s. 616-623
*Leszek Majecki1, Marek Dąbrowski1,2
Całkowite zamknięcie tętnicy wieńcowej w ostrym zespole wieńcowym bez uniesienia odcinka ST – analiza danych klinicznych i elektrokardiograficznych
Total occlusion of coronary artery in non-ST segment elevation acute coronary syndrome – analysis of electrocardiographic and clinical data
1Kliniczny Oddział Kardiologiczny w Szpitalu Bielańskim
Ordynator Oddziału: dr hab. med. Marek Dąbrowski
2III Klinika Chorób Wewnętrznych i Kardiologii II Wydziału Lekarskiego Warszawskiego Uniwersytetu Medycznego
Kierownik Kliniki: prof. dr hab. med. Artur Mamcarz
Streszczenie
Wstęp: W przeciwieństwie do zawału mięśnia sercowego przebiegającego z przetrwałym uniesieniem odcinka ST (STEMI), w którym zaleca się jak najszybsze udrożnienie tętnicy wieńcowej odpowiedzialnej za obraz kliniczny, podejście do chorych z zawałem serca przebiegającym bez uniesienia odcinka ST (NSTEMI) jest bardziej liberalne. Zalecenia towarzystw naukowych zakładają, iż angioplastykę należy wykonać najpóźniej do 72 godzin w zależności od oszacowanego wyjściowo ryzyka.
Cel: Ocena przebiegu choroby w grupie chorych, u których na podstawie wyjściowego elektrokardiogramu ostatecznie rozpoznano OZW bez uniesienia odcinka ST, natomiast w koronarografii stwierdzono ostrą niedrożność tętnicy wieńcowej odpowiedzialnej za bieżący incydent kardiologiczny.
Materiał i metody: Badanie ma charakter retrospektywny. Obserwacji poddano kolejnych 206 pacjentów, którzy byli hospitalizowani z powodu NSTE ACS w Pododdziale Intensywnego Nadzoru Kardiologicznego oraz w Oddziale Kardiologicznym Szpitala Bielańskiego w okresie od 01.08.2007 do 30.04.2008 (okres rekrutacji – 9 m-cy). Jedynym kryterium wykluczającym z badania było rozpoznanie w wyjściowym ekg OZW z uniesieniem odcinka ST. Następnie spośród tej grupy pacjentów wyodrębniono 39 osób (19%), u których w wykonanej koronarografii z powodu NSTE ACS stwierdzono ostrą niedrożność tętnicy wieńcowej (TIMI 0). Średni czas obserwacji po wypisie ze szpitala wyniósł 26 m-cy (do 31.12.2009).
Wyniki: Poziom śmiertelności wewnątrzszpitalnej (2,56%) jest porównywalny z liczbą wczesnych zgonów dużych rejestrów kardiologicznych zarówno u pacjentów z NSTEMI, jak i ze STEMI. Natomiast rokowanie odległe w tej grupie pacjentów jest poważne i zbliżone do śmiertelności odległej u pacjentów ze STEMI. Prawie 18% pacjentów z grupy docelowej, miało ponowny ostry zespół wieńcowy lub wymagało przezskórnej interwencji wieńcowej z powodu zaostrzenia choroby niedokrwiennej serca na skutek restenozy w stencie. Taki sam odsetek pacjentów w przeciągu średnio 2 lat od kwalifikującego do obserwacji incydentu kardiologicznego doznaje ponownego epizodu niedokrwienia mięśnia serca zakończonego zgonem.
Wnioski: Charakterystyka tej grupy pacjentów przypomina raczej grupę z OZW z uniesieniem odcinka ST. Zaskakująco duży odsetek pacjentów z OZW bez uniesienia odcinka ST ma niedrożną GPZ/GD. Elektrokardiogram nie decyduje o ciężkości przebiegu OZW, raczej należy kierować się przesłankami klinicznymi. Nie do zaakceptowania jest duże opóźnienie pain/door to balloon. Pacjenci z tej grupy powinni zostać objęci pilnymi wskazaniami do leczenia interwencyjnego, zbliżonymi do wytycznych dla pacjentów ze STEMI.
Summary
Introduction: In contrast to myocardial infarction with persistent ST-segment elevation (STEMI), which is recommended for emergent coronary reperfusion of the artery responsible for the cardiac incident, the approach to patients with myocardial infarction that runs without ST segment elevation (NSTEMI) is more liberal. The up-to-date recommendations of scientific societies assume that angioplasty should be performed not later than 72 hours since the onset of chest pain depending on the estimated baseline risk.
A im: The assessment and outcome of disease in patients in whom on the basis of the baseline electrocardiogram the ACS without ST-segment elevation was finally diagnosed, whereas the acute coronary occlusion responsible for the current cardiac incident was observed.
M ethods: The study is retrospective. 206 consecutive patients hospitalized for NSTE ACS in the Cardiac Intensive Care and the Department of Cardiology of the Bielanski Hospital in the period from 01.08.2007 to 30.04.2008 (recruitment period – 9 months) were observed. The only exclusion criterion from the study was the presence of ST-segment elevation in baseline electrocardiogram. Then, in this group 39 patients (19%) were selected in whom coronary angiography revealed the acute coronary artery occlusion (TIMI 0). The mean follow-up after discharge from hospital was 26 months (till 31.12.2009).
R esults: The level of in-hospital mortality (2.56%) is comparable with the number of early deaths in large cardiac registries, both in patients with NSTEMI and STEMI. However, long-term prognosis in these patients is severe and similar to long-term mortality in patients with STEMI. Almost 18% of patients in the target group, suffered from the recurrent coronary syndrome or required percutaneous coronary intervention due to the exacerbation of ischemic heart disease as a result of in-stent restenosis. In the same proportion of patients within an average 2-year follow-up fatal recurrent myocardial ischemia occurred.
C onclusions: The characteristics of this group resembles rather the group of patients with STE-ACS. A surprisingly large percentage of patients with NSTE-ACS has LAD or diagonal branch occluded. Electrocardiogram did not indicate the severity of ACS. Physicians should be guided rather by the clinical premises. There is an unacceptable long pain/door-to-balloon delay. Patients in this group should be subjected to urgent interventional treatment, similarly to patients with STEMI.

Wstęp
Pomimo dotychczasowego znacznego postępu, jaki dokonał się w kardiologii zarówno w zakresie diagnostyki, jak i leczenia zawału serca, pozostaje on nadal statystycznie jedną z najczęstszych przyczyn hospitalizacji i nagłej śmierci sercowej (SCD). Ostry zespół wieńcowy (OZW) występuje rocznie u ponad 200 000 osób w Polsce (1). Nieco ponad jedna trzecia zachorowań przypada na zawał serca z przetrwałym uniesieniem odcinka ST (STEMI), natomiast prawie 70% pozostałych stanowi OZW bez uniesienia odcinka ST (NSTE ACS), który ostatecznie jest definiowany jako niestabilna dusznica bolesna (UA) lub zawał serca bez uniesienia odcinka ST (NSTEMI). Zarówno w STEMI, jak i NSTEMI dochodzi do martwicy komórek mięśnia sercowego, o czym świadczy dynamika stężeń tzw. markerów martwicy mięśnia serca uwalnianych do krwi na skutek uszkodzenia kardiomiocytów przedłużającym się niedokrwieniem. Wzrost troponin (cTnT lub cTnI) i/lub kinazy kreatynowej (CK) i jej izoformy MB (CK-MB) w surowicy powyżej 99 centyla zakresu referencyjnego jest bardzo czułym biomarkerem uszkodzenia kardiomiocytów – a zatem to conditio sine qua non dla rozpoznania zawału mięśnia sercowego. Jednakże nie jest on wyłącznie patognomoniczny dla ostrego niedokrwienia, gdyż istnieje wiele stanów klinicznych, którym również towarzyszy znamienny wzrost poziomu we krwi ww. białek.
Pozawałowa martwica miokardium oraz wiążąca się z tym nierozerwalnie niewydolność serca należy obecnie do jednej z najtrudniej poddających się leczeniu jednostek chorobowych, doprowadzając stopniowo do pogorszenia jakości życia oraz niewydolności wielonarządowej pacjentów. Najlepszą metodą, zapobiegającą temu niekorzystnemu „efektowi domina”, jest szybkie, właściwe i kompleksowe leczenie pacjentów z ostrym zespołem wieńcowym.
W 2000 r. na skutek napływu wielu nowych danych klinicznych – zwłaszcza w zakresie patofizjologii OZW – oraz dynamicznego rozwoju technologii dotyczących wizualizacji kurczliwości i ukrwienia mięśnia sercowego, towarzystwa kardiologiczne zostały zmuszone do weryfikacji ówczesnych poglądów na temat definicji i podziału ostrych zespołów wieńcowych (2, 3). Zdecydowano, iż czynnikiem odróżniającym jest obecność lub brak przetrwałego uniesienia odcinka ST w wyjściowym elektrokardiogramie (ekg), na podstawie którego w stosunku do pacjenta wdrażany jest ex definitione dalszy algorytm postępowania diagnostyczno-terapeutycznego. Fala Pardee widoczna przynajmniej w 2 sąsiadujących odprowadzeniach w elektrokardiogramie prawie ze 100% prawdopodobieństwem odpowiada za ostre uszkodzenie integralności kardiomiocytów jako wynik nagłej niedrożności tętnicy wieńcowej (STEMI). W tej sytuacji zarówno amerykańskie (ACC/AHA), jak i europejskie Towarzystwa Kardiologiczne (ESC) są zgodne co do wykonania pierwotnej PCI w ciągu 90 minut od pierwszego kontaktu z lekarzem (klasa zaleceń IA). Zgoła inaczej traktowany jest pacjent bez uniesienia odcinka ST w elektrokardiogramie, gdyż w tym wypadku nie ma elektrokardiograficznie pewnych cech sugerujących ostry incydent wieńcowy wynikający z istotnego hemodynamicznie zwężenia światła tętnicy nasierdziowej. Aż u około 5-6% pacjentów z NSTE ACS wyjściowo rejestrowany jest prawidłowy elektrokardiogram. Duża heterogenność tej grupy oraz brak jednoznacznych dla tego typu niedokrwienia zmian odcinka ST w ekg w OZW (w przeciwieństwie do STEMI) skutkują wdrażaniem bardziej „liberalnej” i zachowawczej terapii względem pacjentów (4).
Dane z rejestru Polish Registry of Acute Coronary Syndrome z 2007 r. (PL-ACS) są jednoznaczne – u chorych z NSTEMI w porównaniu z pacjentami ze STEMI ponad dwukrotnie rzadziej wykonywano koronarografię i PCI (5). Fakt ten wynika zapewne również z powszechnego przekonania, iż NSTEMI w swoim klinicznym przebiegu i rokowaniu jest bardziej zbliżony do UA niż do STEMI, wobec czego nie jest konieczne zastosowanie natychmiastowego leczenia reperfuzyjnego (6). Obydwie te grupy charakteryzuje wzrost wartości enzymów wskaźnikowych świadczący o uszkodzeniu miokardium. Trzecią grupę stanowią chorzy z niestabilną chorobą wieńcową (UA), klinicznie zbliżoną do chorych z NSTEMI, jednak bez wzrostu enzymów przemawiających za uszkodzeniem kardiomiocytów (7).
Na podstawie wielu dotychczas przeprowadzonych badań (np. OPERA, GRACE, PL-ACS) można wnioskować, iż rokowanie odległe u pacjentów po NSTEMI jest przynajmniej tak samo poważne, jak u chorych po przebytym STEMI (8). Co więcej, niektóre z rejestrów zwracają uwagę na znaczny wzrost odsetka zgonów w obserwacji długoterminowej w grupie pacjentów z NSTEMI. Dotyczy to zwłaszcza pacjentów poddanych leczeniu zachowawczemu.
Metodyka
Celem niniejszej obserwacji jest ocena przebiegu choroby w grupie chorych, u których na podstawie wyjściowego ekg ostatecznie rozpoznano OZW bez uniesienia odcinka ST, natomiast w koronarografii stwierdzono ostrą niedrożność tętnicy wieńcowej odpowiedzialnej za bieżący incydent kardiologiczny (czyli angiograficznie obraz charakterystyczny dla pacjentów ze STEMI, ale bez fali Pardee w ekg).
Badanie ma charakter retrospektywny, potrzebne informacje pozyskiwano z dokumentacji źródłowej (historii chorób pacjentów) oraz dostępnych w Szpitalu Bielańskim komputerowych baz danych (Hipokrates, Kroton, Echopack). Wstępnie obserwacji poddano wszystkich kolejnych pacjentów, którzy byli hospitalizowani z powodu NSTE ACS w Pododdziale Intensywnego Nadzoru Kardiologicznego oraz w Oddziale Kardiologicznym Szpitala Bielańskiego w okresie od 01.08.2007 do 30.04.2008 (okres rekrutacji – 9 m-cy). Jedynym kryterium wykluczającym z badania było rozpoznanie w wyjściowym ekg OZW z uniesieniem odcinka ST. Ogólna liczba pacjentów, która została w ten sposób wyszczególniona, wyniosła 206 chorych.Następnie spośród tej grupy pacjentów wyodrębniono 39 osób (19%), u których w koronarografii z powodu NSTE ACS stwierdzono ostrą niedrożność tętnicy wieńcowej. Brak przepływu w takim naczyniu oceniano na podstawie skali Thrombolysis In Myocardial Infarction jako TIMI 0. Średni czas obserwacji po wypisie ze szpitala wyniósł 26 m-cy (do 31.12.2009).
W okresie 2-letniej obserwacji w obrębie tej grupy oceniano częstość następujących punktów końcowych: zgonów z powodów sercowo-naczyniowych, ponownego zawału serca leczonego zachowawczo, ponownego zawału serca leczonego angioplastyką wieńcową z implantacją stentu oraz restenozy w uprzednio implantowanym stencie (Target Lesion Restenosis) poddaną następczej przezskórnej angioplastyce – Target Lesion Revascularisation.
Wyniki
Charakterystyka grupy badanej
W każdym przypadku głównym powodem kontaktu z lekarzem był epizod silnego bólu w klp, trwający nieprzerwanie przynajmniej około 30 min, najczęściej z towarzyszącą dusznością spoczynkową, wysiłkową oraz uczuciem lęku. Prawie 2/3 pacjentów (24 chorych) zostało przywiezionych do szpitala karetką pogotowia (wezwanie do domu lub przez lekarza pierwszego kontaktu z przychodni), 13 osób dotarło transportem własnym, dla 2 pacjentów – brak jednoznacznych informacji. Brak precyzyjnych danych w dokumentacji źródłowej nie pozwolił na określenie opóźnienia od momentu pojawienia się bólu do czasu kontaktu z wykwalifikowanym personelem medycznym. Wszyscy pacjenci po przyjęciu do szpitala i rozpoznaniu NSTE ACS otrzymali kwas acetylosalicylowy (ASA) w dawce 300 mg oraz dawkę nasycającą klopidogrelu 300-600 mg, jeżeli tych leków nie podano wcześniej. Zakres wieku pacjentów wahał się w dość szerokich granicach: 39-86 lat. Średnia wieku wyniosła 65,4 lat, natomiast dla mężczyzn (M), którzy stanowili 54% badanych i kobiet (K) odpowiednio: 59,7 i 72,0 lat.
Prawie 90% pacjentów z grupy docelowej przy przyjęciu do szpitala było w dobrym stanie ogólnym (I klasa wg klasyfikacji Killipa-Kimballa), żadna z 39 osób nie miała cech wstrząsu kardiogennego. Również w ocenie prawdopodobieństwa wystąpienia 14-dniowego punktu końcowego, tj.: zgonu/zawału serca/potrzeby wczesnej rewaskularyzacji – oszacowanego na podstawie skali Antmana (9) – ponad 75% chorych plasowało się w grupie małego i średniego ryzyka. Wartość punktowa TIMI risk score w tej grupie chorych wyniosła 0-4.
Na rycinach 1 i 2 zestawiono czynniki ryzyka choroby wieńcowej w grupie docelowej (TIMI 0) w porównaniu z pozostałymi pacjentami z NSTE ACS (N – 167), u których angiograficznie stwierdzono w różnym stopniu zachowany przepływ w tętnicy wieńcowej (w zakresie TIMI 1-3) odpowiedzialnej za ostry incydent wieńcowy. Uwagę zwraca fakt, iż wśród pacjentów z niedrożną tętnicą wieńcową znacznie częściej stwierdza się obniżony poziom cholesterolu HDL (44% vs 22%), więcej pacjentów jest aktywnymi palaczami tytoniu (44% vs 24%). Natomiast niższy jest odsetek chorych ze współistniejącym nadciśnieniem tętniczym (77% vs 86%), znamiennie niższy tych, którzy przynajmniej w okresie 7 dni przed hospitalizacją stosowali ASA (44% vs 59%) oraz pacjentów z cukrzycą (26% vs 39,5%).
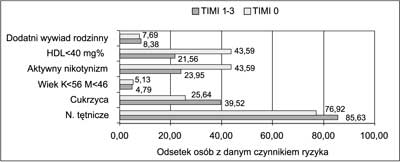
Ryc. 1. Czynniki ryzyka choroby wieńcowej.
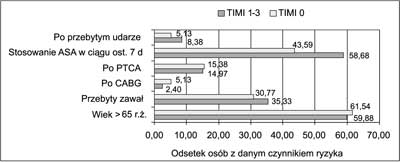
Ryc. 2. Inne czynniki ryzyka choroby wieńcowej.
Rodzaj zmian w wyjściowym elektrokardiogramie, na podstawie którego pacjenci byli klasyfikowani przez kardiologa interwencyjnego do grupy NSTE ACS, ilustruje rycina 3. Aż 7,7% chorych nie miało żadnych zmian sugerujących OZW (1), u kolejnych około 8% były to zmiany mało charakterystyczne (np. blok prawej odnogi pęczka Hisa). Typowe dla niedokrwienia serca, aczkolwiek nie patognomoniczne, zmiany odcinka ST pod postacią jego obniżenia przynajmniej o 1 mm w 2 sąsiadujących odprowadzeniach oraz symetryczne, ujemne załamki T łącznie występowały u ponad 70% badanych. Natomiast współistnienie obu ww. zmian mogących sugerować OZW dotyczyło jedynie jednej piątej chorych.
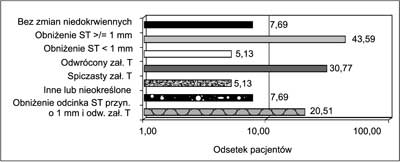
Ryc. 3. EKG przy przyjęciu.
W każdym przypadku decyzję o wykonaniu koronarografii w trakcie bieżącej hospitalizacji podejmował lekarz dyżurny Pracowni Hemodynamicznej w oparciu o uzyskane dane kliniczne i ewentualnie wyniki badań dodatkowych od lekarza prowadzącego z SOR (Szpitalny Oddział Ratunkowy) Szpitala Bielańskiego. Koronarografię wykonano u wszystkich 39 pacjentów, u 38 z dostępu transradialnego, a u 1 z dostępu od tętnicy udowej. Decyzję o ewentualnym wykonaniu następczej angioplastyki i jej zakresie – w tym także o potencjalnym podaniu inhibitora płytkowego receptora GP IIb/IIIa – każdorazowo podejmował lekarz wykonujący zabieg. U 38 pacjentów w trakcie hospitalizacji wykonano badanie echokardiograficzne, 1 pacjent miał wykonane badanie wcześniej w szpitalu, z którego został przeniesiony.
Sposób i wyniki leczenia
Czas pain-to-balloon (czyli od pojawienia się bólu do rozprężenia balonu w tętnicy wieńcowej) u ponad 50% badanych wyniósł> 24 h, z czego u około 2/3 oscylował wokół 72 h od początku bólu. Zaledwie 10% pacjentów zostało skierowanych pilnie do Pracowni Hemodynamicznej (w czasie <6 h).
W ponad 50% przypadków niedrożną tętnicą odpowiedzialną za OZW była gałąź okalająca (GO) lub jej odgałęzienia, następnie prawa tętnica wieńcowa (PTW) – 25,5% i u około 18% pacjentów zamkniętą tętnicą była gałąź przednia zstępująca (GPZ) lub odchodzące od niej gałęzie diagonalne, w 2,5% była to gałąź pośrednia (GP).
Wyniki leczenia interwencyjnego były następujące:
– u około 60% chorych implantowano stent metalowy do tętnicy wieńcowej, średnica naczynia docelowego wynosiła min. 2,5 mm,
– około jedna piąta pacjentów została zakwalifikowana do dalszego leczenia zachowawczego choroby wieńcowej, głównie z powodu czasu pain-to-balloon oscylującego w granicach od 24 do 72 h ze współistniejącym stabilnym klinicznie i hemodynamicznie stanem pacjenta oraz angiograficznymi cechami tworzenia się krążenia obocznego do strefy niedokrwienia),
– około 10% chorych poddano jedynie angioplastyce balonowej (techniczne problemy z dostarczeniem stentu w miejsce istotnego zwężenia po udrożnieniu tętnicy wieńcowej z uwagi na jej silnie uwapniony lub kręty przebieg w proksymalnym odcinku),
– około 10% badanych zakwalifikowano do elektywnej operacji pomostowania aortalno-wieńcowego (nieskuteczna angioplastyka lub choroba wielonaczyniowa).
U 3 pacjentów kardiolog interwencyjny zdecydował o podaniu abciksimabu w okresie okołozabiegowym. U około 13% pacjentów w badaniu echokardiograficznym stwierdzono znaczne upośledzenie kurczliwości mięśnia serca (EF<35%), natomiast umiarkowaną dysfunkcję (EF w granicach 35-50%) oraz zachowaną globalną kurczliwość mięśnia serca uwidoczniono odpowiednio u 41 i 44% badanych.
Na rycinie 4 oraz w tabeli 1 przedstawiono wyniki częstości wystąpienia punktów końcowych. W sumie u około 36% pacjentów w okresie 2-letniej obserwacji wystąpił ponowny OZW lub zaostrzenie choroby wieńcowej, co w połowie przypadków wymagało pilnej hospitalizacji i ewentualnego leczenia inwazyjnego, natomiast u pozostałych 50% chorych taki incydent kardiologiczny zakończył się zgonem.
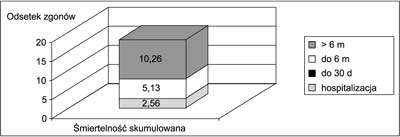
Ryc. 4. Całkowita śmiertelność – 17,95%.
Tabela 1. Zestawienie punktów końcowych u pacjentów z zawałem serca bez uniesienia odcinka ST z niedrożną tętnicą odpowiedzialną za dany incydent wieńcowy w okresie obserwacji wynoszącej średnio 26 miesięcy.
| Incydent | Śmiertelność | Ponowny OZW leczony zachowawczo | Ponowny OZW leczony PTCA | PCI z powodu restenozy |
| Okres obserwacji |
| Bieżąca hospitalizacja | 2,56% | | | |
| Do 30 dni po wypisie | | 2,56% | | |
| Do 6 m-cy po wypisie | 5,13% | | 2,56% | 2,56% |
| > 6 m-cy po wypisie | | 5,13% | 5,13% | |
| Wartość skumulowana | 10,26% | 7,69% | 7,69% | 2,56% |
Omówienie
Podstawowe wnioski, jakie można sformułować, analizując wyniki niniejszego badania, są następujące:
1) nie do zaakceptowania jest duże opóźnienie pain/door to balloon;
Dobry stan kliniczny pacjentów, brak jakichkolwiek lub jednoznacznych dla NSTE ACS zmian niedokrwiennych w ekg zapewne w dużej mierze przesądzał o odroczeniu w czasie diagnostyki inwazyjnej, która często była wdrażana z dużym opóźnieniem dopiero po stwierdzeniu znamiennego wzrostu stężenia lub swoistej dynamiki markerów martwicy mięśnia serca w surowicy albo w wypadku pojawienia się cech niestabilności hemodynamicznej, niewydolności krążenia lub groźnej arytmii.
2) EKG nie decyduje o ciężkości przebiegu OZW, raczej należy kierować się przesłankami klinicznymi;
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
24 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
59 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
119 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 28 zł
Piśmiennictwo
1. http://www.rejestrozw.pl/.
2. Alpert JS, Thygesen K, Antman E, Bassand JP: Myocardial infarction redefined – a consensus document of the Joint European Society of Cardiology/American College of Cardiology/Committee for the redefinition of myocardial infarction. Eur Heart J 2000; 21: 1502-1513.
3. Scull GS, Martin JS, Weaver D, Etery NR: For the MITI Investigators. Early angiography versus conservative treatment in patients with non-ST elevation acute myocardial infarction. J Am Coll Cardiol 2000; 35: 895-902.
4. Braunwald E: Application of current guidelines to the management of unstable angina and non-ST-elevation myocardial infarction. Circulation 2003; 108 (16 Suppl 1): III 28-37.
5. Poloński L, Gąsior M, Gierlotka M et al.: Characteristisc, treatment and outcomes of patients with acute coronary syndromes in Poland. Kardiologia Polska 2007; 65: 861-872.
6. Koyama Y, Hansen PS, Hanratty CG, Nelson G, Rasmussen HH: Prevalence of coronary occlusion and outcome of an immediate invasive strategy in suspected acute myocardial infarction with and without ST-segment elevation. Am J Cardiol 2002; 90: 579-584.
7. Moliterno PR, Granger CB: Differences between unstable angina and acute myocardialn infartion: the pathophysiological and clinical spectrum. [W:] Topol EJ (red.): Acute coronary syndromes. Basel Marcel Dekker Inc New York 2001; 139-144.
8. Montalescot G, Dallongeville J, Van Belle E et al.: STEMI and NSTEMI: Are they so different? 1-year outcomes in acute myocardial infarction as defined by the ESC/AC definition (the OPERA registry). Eur Hart J 2007; 28: 1409-1417.
9. Elliott M, Antman MD, Marc Cohen MD et al.: The TIMI Risk Score for Unstable Angina/Non-ST Elevation MI. A Method for Prognostication and Therapeutic Decision Making. JAMA 2000; 284: 835-842.
10. The Euro Heart Survey on diabetes and the heart. Eur Heart J 2004; 25: 1880-90.
11. Bassand JP, Hamm CW, Jr Ardissino D i wsp.: Guidelines for diagnosis and treatment of no-ST-segment elevation acute coronary syndromes. The task force for diagnosis and treatment of non-ST-segment elevation acute coronary syndromes of ESC. Eur Heart J 2007; 28: 1598-1660.
12. Neuman FJ, Kastrati A, Pogatsa-Murray G et al.: Evaluation of prolonged antithrombotic pretreatment ("cooling-off” strategy) before intervention in patients with unstable coronary syndromes: a randomized controlled trial JAMA 2003; 290: 1593-1599.
13. Tricoci P, Lokhnygina Y, Berdan LG et al.: Time to coronary angiography and outcomes among patients with high-risk non-ST-segment elevation acute coronary syndromes. Results from the SYNERGY trial. Circulation 2007; 116: 2669-2677.
14. Mehta SR, Granger CB, Boden WE et al.: Early versus delayed invasive intervention in acute coronary syndromes. N Engl J Med 2009; 360: 2165-2175.
15. Sorajja P, Bernard J, Gersh, David A Cox et al.: Impact of delay to angioplasty in patients with acute coronary syndromes undergoing invasive management: Analysis from the ACUITY (Acute Catheterization and Urgent Intervention Triage strategY) trial. J Am Coll Cardiol 2010; 55 (14): 1414-1424.
16. Van de Werf F, Ardissino D, Betriu A et al.: Management of acute myocardial infarction in patients presenting with ST-segment elevation. Eur Heart J 2008; 29: 2909-2945.




