© Borgis - Postępy Fitoterapii 2/2010, s. 97-100
*Edyta Kwiatkowska
Luteina – źródła w diecie i potencjalna rola prozdrowotna
Lutein – diet source and potential disease prevention
Instytut Turystyki i Rekreacji, Akademia Wychowania Fizycznego im. Józefa Piłsudskiego w Warszawie
Kierownik Instytut Turystyki i Rekreacji: dr hab. Ludwik Mazurkiewicz, prof. AWF
Summary
Lutein belong to the xanthophyll family of carotenoids. It has two hydroxyl groups one on each side of the molecule. In the diet it is found in highest concentrations in dark green, leafy vegetables (spinach, kale, collard greens), corn, and egg yolks. Cooking of lutein containing foods may increase bioavailability by disrupting the cellular matrix and the carotenoid – protein complexes. Some observational studies have shown these xanthophylls may help reduce the risk of certain types of cancer, particularly those of the breast. Studies suggest a potential contribution of lutein to the prevention of heart disease and stroke. Epidemiologic studies indicating an inverse relationship between xanthophylls intake can play a protective role in the eye. The evidence for a role of lutein in disease prevention continues to evolve.

Wstęp
Luteina, podobnie jak likopen, należy do karotenoidów. Karotenoidy są jedną z najważniejszych grup naturalnych barwników. Obecnie zidentyfikowano ponad 50 tych związków, które występują w żywności pochodzenia roślinnego. Jednak tylko nieliczne z nich, około 10%, ulegają przekształceniu do witaminy A. Karotenoidy dzielą się na karoteny będące węglowodorami izoprenu i ksantofile. Do ksantofili należą: luteina, zeaksantyna, kryptoksantyna. Większość karotenoidów ma silne właściwości antyoksydacyjne i między innymi takie właściwości ma luteina (1, 2). Pod względem chemicznym luteina jest nienasyconym węglowodorem polienowym, zbudowanym z ośmiu reszt izoprenowych, tworzących łańcuch węglowy o 40 atomach węgla i dwóch grupach – OH w pierścieniach β-jononowych. Ze względu na obecność w cząsteczce grup hydroksylowych w pierścieniu węglowym, wykazuje większą polarność niż pozostałe karotenoidy. Sumaryczny wzór luteiny ma postać C40H54O2. Luteina dobrze rozpuszcza się w tłuszczach i rozpuszczalnikach organicznych oraz alkoholach. Ze względu na te właściwości korzystne jest spożywanie produktów będących źródłem luteiny z posiłkami zawierającymi tłuszcz, gdyż zwiększa się wtedy biodostępność luteiny (3, 4). Na rycinie 1 przedstawiono budowę strukturalną luteiny.
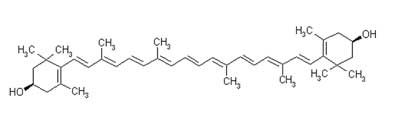
Ryc. 1. Budowa strukturalna luteiny.
Zawartość w żywności i źródła w diecie
Luteina jest wyłącznie syntetyzowana przez rośliny i występuje w zielonych liściach warzyw oraz żółtych i pomarańczowych warzywach, ale również w owocach. Zawartość luteiny w warzywach jest bardzo różna i wynosi od 0,01 do 40 mg/100 g (tab. 1). Najwyższą zawartość luteiny ma jarmuż (około 39 mg/100 g) oraz szpinak (około 11,9 mg/100 g). Oprócz produktów spożywczych przedstawionych w tabeli 1 luteina występuje w natce pietruszki, w cukinii, papryce. Warzywa są lepszym źródłem tego składnika niż owoce. Najwyższe zawartości luteiny w owocach odnotowano w nektarynkach, jeżynach, agreście, awokado, kiwi, malinach, porzeczkach czarnych. Z badań wynika, że jeżyny zawierają średnio 0,54 mg/100 g luteiny (5). Zawartość luteiny w warzywach i owocach zależy od wielu czynników, włączając w to metody uprawy, miejsce uprawy – region geograficzny oraz procesy technologiczne. Luteina koncentruje się najczęściej w skórce i w miąższu owoców i warzyw. Substancja ta występuje również w żółtku jaja kurzego (6). Obecność luteiny w żółtkach jaj jest konsekwencją skarmiania kur produktami roślinnymi. Z uwagi na rodzaj hodowli i sposób karmienia kur, zawartość luteiny w żółtkach jaj może być różna. Z badań wynika, że zawartość luteiny w żółtku jaja wynosi 1723 ± 690 μg/100 g (6).
Tabela 1. Zawartość luteiny w produktach spożywczych (5, 7).
| Produkt spożywczy | Luteina/zeaksantyna (mg/100 g) | Średnia zawartość luteiny (mg/100 g) |
| Jarmuż | 39,55 | - |
| Jarmuż gotowany | 15,79 | |
| Szpinak surowy | 11,93 | 8,95 |
| Szpinak gotowany | 7,04 | - |
| Sałata | 2,63 | 0,41-1,65 |
| Brokuły | 2,44 | 1,97 |
| Cukinia ze skórką | 2,12 | - |
| Dynia | 2,12 | 2,82 |
| Brukselka | 1,59 | 0,51 |
| Groszek zielony (w puszce) | 1,35 | 2,23 |
| Kukurydza (w puszce) | 0,88 | 0,41 |
| Fasolka szparagowa | 0,64 | 0,29 |
| Marchew | 0,35 | 0,30 |
| Kapusta | 0,31 | 6,89 |
| Melon | 0,04 | 0,03 |
Przeciętne dzienne spożycie luteiny w USA oceniane jest na 1,7 mg dziennie, a w Europie na 2,2 mg dziennie (8). Nie zostały jeszcze ustalone normy żywieniowe uwzględniające wysokość spożywania luteiny. Spożycie luteiny w pięciu krajach europejskich w zależności od źródła pochodzenia przedstawia tabela 2.
Tabela 2. Najlepsze źródła luteiny w diecie w pięciu krajach Europy (w %) (9).
| Hiszpania (n=70) | Francja (n=76) | UK (n=71) | Irlandia (n=76) | Holandia (n=75) |
| Szpinak (34) | Szpinak (31) | Brzoskwinie (36) | Brzoskwinie (19) | Szpinak (30) |
| Sałata (16) | Sałata (8) | Brokuły (8) | Brokuły (16) | Brokuły (16) |
| Pomarańcze (7) | Jaja (8) | Jaja (8) | Jaja (10) | Brzoskwinie (9) |
| Jaja (7) | Miks warzyw (6) | Słodka kukurydza (7) | Marchew (9) | Cykoria (8) |
| Brokuły (6) | Ogórki (6) | Sałata (6) | Pomidory (8) | Sałata (4) |
Metabolizm i biodostępność
Pomimo że z wielu badań wynika istnienie ścisłego związku między spożywaniem luteiny wraz z żywnością a ograniczeniem skutków wielu stanów chorobowych, to nadal stosunkowo niewiele wiadomo na temat jej wchłaniania i przemian w organizmie człowieka, ponieważ mechanizmy te nie zostały do końca wyjaśnione. Luteina ulega w organizmie podobnym przemianom jak lipidy (10, 11). Pobrana z dietą po strawieniu w żołądku oraz dwunastnicy tworzy wraz z monoglicerydami i wolnymi kwasami tłuszczowymi, w obecności soli kwasów żółciowych, kompleksy umożliwiające utrzymanie ich w wodzie w postaci roztworu miceralnego (12). Za pośrednictwem chylomikronów tworzących się w enterocytach, związki te są wydzielane do naczyń chłonnych i transportowane za pośrednictwem krwi do wątroby. Następnie krew transportuje te związki w postaci lipoprotein z wątroby do tkanek w zależności od potrzeb organizmu. Luteina gromadzi się głównie w soczewce oka i centralnej części siatkówki – plamce żółtej, gdyż wykazuje szczególne powinowactwo do gałki ocznej (13).
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
24 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
59 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
119 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 28 zł
Piśmiennictwo
1. Bates C. Vitamin A. Lancet 1995; 345:31-5. 2. Handelman GJ. The evolving role of carotenoids in human biochemistry. Nutrition 2001; 17:818-22. 3. Castenmiller JJ, West CE, Linssen JP i wsp. The food matrix of spinach is a limiting factor in determining the bioavailability of beta-carotene and to a lesser extent of lutein in humans. J Nutr 1999; 129:394-455. 4. Van het Hof KH, Brouwer IA, West CE i wsp. Bioavailability of lutein from vegetables is 5 times higher than that of β-carotene. Am J Clin Nutr 1999; 70:261-8. 5. Hamułka J, Wawrzyniak A. Likopen i luteina – rola prozdrowotna i ich zawartość w produktach. Wyd. SGGW, Warszawa 2004; 41. 6. Handelman GJ, Nightingale ZD, Lichtenstein AH i wsp. Lutein and zeaxanthin concentrations in plasma after dietary supplementation with egg yolk. Am J Clin Nutr 1999; 70:247-51. 7. Holden JM, Eldridge AL, Beecher GR i wsp. Carotenoid content of U.S. foods: an update of the database. J Food Com Anal 1999; 12:169-96. 8. Alves-Rodriques A, Shao A. The science behind lutein. Toxicol Left 2004; 150:57. 9. O'Neil ME, Carroll Y, Corridan B i wsp. A European carotenoid database to assess carotenoid intakes and its use in a five-country comparative study. Br J Nutr 2001; 85:499-507. 10. Hernandez M, Montenergro J, Steiner M i wsp. Intestinal absorption of cholesterol is mediated by a saturable inhibitable transporter. Biochim Biophys Acta 2000; 1486:232-42. 11. Schaffer JE. Fatty acid transport: the roads taken. A J Physiol (Endocrinol Metab) 2002; 282:E239-46. 12. Borel P, Grolier P, Armand M i wsp. Carotenoids in biological emulsions: solubility, surface-to-core distribution, and release from lipid droplets. J Lipid Res 1996; 37:250-61. 13. Granado F, Olmedilla B, Blanco I. Nutritional and clinical relevance of lutein in human health. Br J Nutr 2003; 90:487-502. 14. Castenmiller JJM, West CE, Linseen JPH i wsp. The food matrix of spinach is a li-miting factor in determining the bioavailability of â-carotene and to a lesser extent of lutein in humans. J Nutr 1999; 129:349-55. 15. O'Neil ME, Thurnham DI. Intestinal absorption of beta-carotene, lycopene and lutein in men and women following a standard meal: response curves in the tracylglycerol-rich lipoprotein fraction. Br J Nutr 1998; 79:149-59. 16. Mares-Perlman JA, Fisher A, Klein R i wsp. Lutein and zeaxanthin in the diet and serum and their relation to age-related maculopathy in the Third National Health and Nutrition Examination Survey. Am J Epidemiol 2001; 153:424-32. 17. Hamułka J. Badania nad wpływem wybranych frakcji włókna pokarmowego na wykorzystanie luteiny w warunkach in vitro i in vivo. Wyd. SGGW, Warszawa 2009; 1. 18. Riedl J, Linseisen J, Hoffmann J i wsp. Some dietary fibers reduce the absorption of carotenoids in women. J Nutr 1999; 129:2170-6. 19. Szostak WB, Szostak-Węgierek D. Żywienie w profilaktyce zwyrodnienia plamki żółtej. Przegl Lek 2008; 65:6-8. 20. Bartz J, Brecht J. Postharvest physiology and pathology of vegetables. Marcel Deker Inc. New York 2003: cyt. za Niewczas J, Szweda D, Mitek M. Zawartość wybranych składników prozdrowotnych w owocach dyni olbrzymiej ( Cucurbita Maxima). Żywność Nauka Technologia Jakość 2005; 2:147-55. 21. Fraser P, Bramley P. The biosynthesis and nutritional uses of carotenoids. Progress Lipid Res 2004; 43:228-65. 22. Perrone S, Longini M, Marzocchi B i wsp. Effects of lutein on oxidative stress in the term newborn: A pilot study. Neonatology 2010; 97:36-40. 23. Panasenko OM, Sharov VS, Briviba K i wsp. Interaction of peroxynitrite with carotenoids in human low density lipoproteins. Arch Biochem Biophys 2000; 373:302-5. 24. Iribarren C, Folsom AR, Jacobs DR i wsp. Associatian of serum vitamin levels, LDL susceptibility to oxidation and autoantibodies against MDA – LDL with carotid atherosclerosis. Arterioscler Thromb Vasc Biol 1997; 17:1171-7. 25. Dwyer JH, Navab M, Dwyer KM i wsp. Oxygenated carotenoid lutein and progression of early atherosclerosis: the Los Angeles atherosclerosis study. Circulation 2001; 103:2922-7. 26. Ribaya-Mercado JD, Blumberg JB. Lutein and zeaxanthin and their potential roles in disease prevention. J Am Coll Nutr 2004; 23:567-87. 27. Howard AN, Williams NR, Palmer CR i wsp. Do hydroxyl-carotenoids prevent coronary heart diseases? A comparison between Belfast and Toulouse. Int Vit Nutr Res 1996; 66:113-24. 28. Michaud DS, Feskanich D, Rimm EB. Intake of specific carotenoids and risk of lung cancer in 2 prospective US cohorts. Am J Clin NutR 2000; 72:990-97. 29. Voorrips LE, Goldbohm RA, Brants HA i wsp. A prospective cohort study on antioxidant and folate intake and male lung cancer risk. Cancer Epidemiol Biomarkers Prev 2000; 9:357-65. 30. Slattery ML, Benson J, Curtin K i wsp. Carotenoids and colon cancer. Am J Clin Nutr 2000; 71:575-82. 31. Zeegers MP, Goldholm RA, van den Brandt P. Are retinol, vitamin C, vitamin E., folate and carotenoids intake associated with bladder cancer risk? Results from the Netherlands cohort study. Br J Cancer 2001; 85:977-83. 32. Mares-Perlman JA, Millen AE, Ficek TL. The body of evidence to support a protective role for lutein and zeaxanthin in delaying chronic disease. Overview J Nutr 2002; 132:518-21. 33. Van Leeuwen R, Boekhoorn S, Vingerling JR i wsp. Dietary intake of antioxidants and risk of age-related macular degeneration. JAMA 2005; 294:3101-7. 34. Cho E, Hankinson SE, Rosner B i wsp. Prospective study of lutein/zeaxanthin intake and risk of age-related macular degeneration. Am J Clin Nutr 2008; 87:1837-3. 35. Bernstein PS, Khachik F, Carvalho LS i wsp. Identification and quantification of carotenoids and their metabolites in the tissues of the human eye. Exp Eye Res 2001; 72:215-23. 36. Khachik F. Distribution and metabolism of dietary carotenoids in humans as a criterion for development of nutritional supplements. Pure Appl Chem 2006; 78:1551-7.

