© Borgis - Postępy Nauk Medycznych 4/2011, s. 274-285
*Katarzyna Lewandowska
Alergiczne zapalenie pęcherzyków płucnych
Extrinsic allergic alveolitis (hypersensitivity pneumonitis)
I Klinika Chorób Płuc Instytutu Gruźlicy i Chorób Płuc w Warszawie
Kierownik Kliniki: prof. dr hab. med. Jan Kuś
Streszczenie
Alergiczne zapalenie pęcherzyków płucnych (AZPP) jest chorobą zapalną miąższu płuc i oskrzelików, związaną z powtarzanym narażeniem na wziewne antygeny środowiskowe, którymi są białka bakterii, grzybów, roślin i zwierząt lub też cząstki nieorganiczne. Zapalenie to ma charakter reakcji nadwrażliwości typu III (kompleksy immunologiczne) i typu IV (reakcja komórkowa typu późnego). W badaniu mikroskopowym bioptatów płuca obserwuje się nacieki komórkowe z przewagą limfocytów, słabo uformowane ziarniniaki oraz cechy zapalenia oskrzelików i śródmiąższowego włóknienia. W płynie z płukania oskrzelowo-pęcherzykowego przeważają limfocyty, które mogą stanowić ponad 50% składu komórkowego płynu. Klinicznie wyróżnia się AZPP o przebiegu ostrym, podostrym i przewlekłym. W postaci ostrej dominują objawy pseudogrypowe z suchym kaszlem, dusznością, gorączką z dreszczami i bólami kostno-mięśniowymi. Postać podostra i przewlekła charakteryzują się postępującą dusznością i pogorszeniem tolerancji wysiłku. W badaniu przedmiotowym stwierdza się trzeszczenia nad dolnymi polami płuc, palce pałeczkowate występują rzadko. W surowicy niektórych osób narażonych można wykazać obecność przeciwciał precypitujących przeciwko danym antygenom, ich wykrycie nie stanowi jednak warunku koniecznego do rozpoznania. W badaniu radiologicznym klatki piersiowej widoczne są zmiany o charakterze drobnoplamistym i drobnoguzkowym, a w tomografii komputerowej wysokiej rozdzielczości wewnątrzzrazikowe guzki zlewające się w obraz matowej szyby, mozaikowatość perfuzji oraz cechy włóknienia płuc. W badaniach czynnościowych układu oddechowego obserwuje się restrykcję i obniżenie pojemności dyfuzyjnej płuc, a także hipoksemię powysiłkową. Najskuteczniejszym sposobem leczenia jest zaprzestanie ekspozycji na wywołujący chorobę antygen. W ciężkich i przewlekłych przypadkach stosuje się kortykosteroidy systemowe. Rokowanie jest dobre w postaci ostrej i podostrej, postać przewlekła może doprowadzić do zwłóknienia płuc i inwalidztwa oddechowego.
Summary
Extrinsic allergic alveolitis (EAA, also: hypersensitivity pneumonitis – HP) is an inflammatory lung disease caused by environmental antigens of different source: bacterial, fungal, animal or chemical. It is characterized as type III (immune complexes) and type IV (delayed cellular infiltrates) hypersensitivity reaction. Histologically, lymphocytic infiltrates, poorly defined granulomas, bronchiolitis and fibrotic pattern are present. Lymphocytes predominate in broncho-alveolar lavage fluid and they may constitute over 50% of cell count. EAA is traditionally divided on clinical grounds into acute, subacute and chronic stages. In acute stage flu – like symptoms are present: fever, chills, dry cough, dyspnoea, bone and muscle pain. Subacute and chronic stages are characterized by progressive dyspnoea and exercise intolerance. On examination bilateral basal crepitations are present, clubbing is rare. In some patients precipitins against causative antigens may be found, but diagnosis does not relay on positive test. Patchy and nodular opacities are found on plain chest X-ray and high resolution computed tomography shows centrilobular nodules, diffuse ground glass opacities and fibrosis. Pulmonary function tests reveal restrictive pattern with decreased diffusion capacity of the lungs and hypoxemia on exertion. The most effective treatment is avoiding antigen exposure. In some severe and chronic cases systemic steroids may be useful. Prognosis is good in most cases of acute and subacute stages, but chronic HP may produce lung fibrosis and respiratory failure.

Wprowadzenie
Alergiczne zapalenie pęcherzyków płucnych jest trzecią co do częstości chorobą śródmiąższową płuc w Polsce, jej częstość występowania szacuje się na ok. 10/100 tys. (1).
Pierwsza wzmianka o „ostrych objawach występujących po pracy przy sianie” pochodzi z 1932 r. – JM Campbell opisał 3 rolników, którzy skarżyli się na duszność, gorączkę i suchy kaszel, a w badaniu radiologicznym klatki piersiowej stwierdzano u nich rozsiane zmiany drobnoguzkowe w płucach. Nie wykryto obecności prątków gruźlicy w plwocinie chorych, a objawy, jak również obraz radiologiczny uległy poprawie po zaprzestaniu pracy (2). Ze względu na obecność objawów u rolników chorobę nazwano „płucem rolnika”. W kolejnych latach opisywano podobne objawy u osób mających kontakt z innymi cząstkami organicznymi, np. odchodami gołębi („płuco hodowców ptaków”), pracujących przy zbiorze bawełny („płuco zbierających bawełnę”), w przemyśle drewnianym („płuco odkorowujących klony”), a w ostatnich latach również w przemyśle metalowym oraz u osób korzystających z parków wodnych, basenów i jacuzzi (hot tub lung) (3).
Definicja
Alergiczne zapalenie pęcherzyków płucnych (AZPP) jest chorobą zapalną miąższu płuc i oskrzelików, związaną z powtarzanym narażeniem na wziewne antygeny środowiskowe (cząstki organiczne i nieograniczne), na które osoba została wcześniej uczulona. Zapalenie ma charakter głównie limfocytarny i ziarniniakowy (4).
Antygeny wywołujące reakcję immunologiczną mogą pochodzić z bakterii lub grzybów, mogą to być białka roślinne lub zwierzęce, a także cząstki nieorganiczne, które stanowią hapteny i po połączeniu z ludzką albuminą tworzą pełnowartościowe antygeny (3, 5). Coraz częściej spotyka się w literaturze również opisy przypadków AZPP wywołanego przez leki, np. lenalidomid (6), leflunomid (7), temozolomid (8), rituximab (9), a nawet dopęcherzowo podawane prątki kwasooporne szczepu BCG (10). Oprócz najczęściej opisywanego narażenia zawodowego lub związanego z działalnością hobbystyczną, AZPP może wystąpić również w wyniku ekspozycji na grzyby obecne w środowisku domowym, jak w japońskim zapaleniu pęcherzyków płucnych typu letniego (11) oraz w kilku przypadkach pochodzących ze Stanów Zjednoczonych (12). Obecnie liczba znanych antygenów, które mogą wywołać AZPP zbliża się do 200 (1). Niektóre najczęściej spotykane i najlepiej poznane zawarto w tabeli 1 wraz z odpowiadającymi im typami AZPP.
Tabela 1. Czynniki wywołujące alergiczne zapalenie pęcherzyków płucnych (3, 4, 11).
| Antygen | Źródło | Choroba |
| Promieniowce termofilne, Saccharopolispora rectivirgula | Spleśniałe siano | Płuco rolnika |
| Micropolyspora faeni | Systemy nawilżające powietrze, klimatyzatory | Płuco nawilżaczowe |
| Trichosporon cutaneus | Środowisko domowe | Japońskie letnie zapalenie pęcherzyków płucnych |
| Penicillium sp. | Sery | Płuco serowarów |
| Mycobacterium avium | Woda w basenach, jaccuzi, itp. | hot tub lung |
| Mycobacterium species | Płyny stosowane do chłodzenia metalu w przemyśle metalowym | Płuco pracowników przemysłu metalowego |
| Białka surowicy, piór, odchodów ptaków | Surowica, pióra, odchody gołębi, papug, kaczek, indyków | Płuco hodowcy ptaków |
| Białka surowicy, skóry, sierści, odchodów zwierząt laboratoryjnych | Zwierzęta laboratoryjne | Płuco pracowników laboratoriów |
| Białko sierści zwierząt futerkowych | Futra | Płuco kuśnierzy |
| Pyrethrum | Pestycydy | AZPP wywołane środkami owadobójczymi |
| Izocyjaniany, cynk | Farby, plastik | Płuco pracowników przemysłu chemicznego |
Podłoże immunologiczne
Nawracająca ekspozycja na dany antygen powoduje uczulenie (sensytyzację) organizmu. Po pewnym czasie może dojść do reakcji immunologicznej wywołującej objawy ogólne i miejscowe.
Zapalenie w AZPP ma charakter reakcji nadwrażliwości typu III (kompleksy immunologiczne) i typu IV (reakcja komórkowa typu późnego) (13). Antygeny wywołujące AZPP są to cząstki o średnicy poniżej 5 μm, najczęściej ok. 1 μm (3). Dzięki małym rozmiarom docierają one do pęcherzyków płucnych. Uważa się, że mogą one przekraczać błonę pęcherzykowo-włośniczkową i dostawać się do krwi, gdzie łączą się z przeciwciałami, tworząc kompleksy immunologiczne (13). Kompleksy immunologiczne uruchamiają kaskadę dopełniacza. Zwiększenie stężenia fragmentu C3 dopełniacza powoduje aktywację makrofagów, które uwalniają mediatory zapalenia: interleukinę 8 (IL-8), makrofagowe białko hamujące (MIP-1), RANTES, IL-1, czynnik martwicy guza α (TNF-α) oraz IL-6. Te cytokiny i chemokiny stymulują napływ neutrofilów i makrofagów do tkanki śródmiąższowej w ciągu pierwszych 4-6 godzin od ekspozycji na antygen (14, 15). Znaczenie kompleksów immunologicznych nie jest jednak do końca wyjaśnione. Wyniki biopsji płuca wykonywanych u chorych na AZPP, nie wykazują obecności kompleksów immunologicznych w płucach, a jedynie nacieki z limfocytów i granulocytów (16). Z drugiej strony, ok. 50% osób narażonych na działanie danego antygenu ma stwierdzane w surowicy przeciwciała, choć nigdy nie rozwija się u nich jawna klinicznie choroba. Choruje jedynie 1 do 15% narażonych (14). Sugerowany jest wpływ genów układu zgodności tkankowej na skłonność do rozwoju reakcji zapalnej: u chorych na AZPP hodowców gołębi stwierdzano większą częstość alleli HLA – DRB1*1305 oraz HLA – DQB1*0501 (16). AZPP rzadziej występuje u osób palących papierosy, co prawdopodobnie wiąże się z immunosupresyjnym działaniem dymu tytoniowego, szczególnie jego wpływem na zwiększenie apoptozy makrofagów pęcherzykowych oraz zmniejszeniem odpowiedzi IgG na inhalowane antygeny (17). Z drugiej strony, jeżeli dojdzie do rozwoju choroby u osoby palącej, ma ona cięższy przebieg często prowadzący do niewydolności oddechowej w przebiegu włóknienia oraz rozedmy płuc. Objawy choroby u osób narażonych na działanie antygenów mogą zostać wyzwolone po infekcji wirusowej (np. RSV, wirus grypy A) lub po zadziałaniu dodatkowego czynnika uszkadzającego, np. pestycydów. Wydaje się, że rolę odgrywa tu uszkodzenie funkcji rzęsek, zwiększona ekspresja cząstek kostymulujących na makrofagach oraz zwiększone wytwarzanie chemokin powodujących napływ limfocytów do płuc (5, 15, 18).
W pierwszej fazie zapalenie ma charakter neutrofilowy – w popłuczynach oskrzelowo-pęcherzykowych (broncho-alveolar lavage fluid – BALF) obserwuje się zwiększony odsetek granulocytów obojętnochłonnych, którego szczyt przypada w ciągu 24 godzin od ekspozycji (13, 16). Kolejno narasta liczba makrofagów i limfocytów, które dominują w obrazie BALF nie tylko w czasie ostrych objawów, ale mogą utrzymywać się przez wiele lat, nawet po ustaniu ekspozycji, choć wówczas ich liczba stopniowo się zmniejsza (19). Limfocyty mogą stanowić od 60 do 90% składu komórkowego BALF. Jest to związane nie tylko z ich nadmiernym napływem do pęcherzyków płucnych, ale również z zahamowaniem apoptozy (19). Zasadniczo przeważają limfocyty o fenotypie CD8+, tak więc stosunek CD4+/CD8+ jest mniejszy od 1, tym niemniej w niektórych przypadkach obserwuje się również bardzo wysokie wartości indeksu CD4+/CD8+ (14, 20). Uważa się, że przewaga limfocytów CD8+ jest związana raczej z aktywną fazą choroby, podczas gdy przewaga CD4+ z przewlekłym włóknieniem. Tak więc fenotyp limfocytów może być zależny od fazy choroby, rodzaju antygenu oraz czasu trwania narażenia (14).
Obraz histopatologiczny
W ostrym AZPP rzadko istnieje możliwość uwidocznienia zmian histopatologicznych. Opisywane są nacieki z eozynofilów i neutrofilów w przestrzeniach międzypęcherzykowych oraz zapalenie małych naczyń i obecność złogów immunoglobulin i dopełniacza w naczyniach.
Biopsja płuca najczęściej bywa wykonywana u chorych z podostrym i przewlekłym AZPP. Obraz histopatologiczny podostrej postaci choroby obejmuje zapalenie śródmiąższowe z przewagą limfocytów, słabo uformowane ziarniniaki bez tendencji do martwicy oraz zapalenie oskrzelików. Obecne mogą być także ogniska zarostowego zapalenia oskrzelików oraz włóknienie pęcherzykowe (21). Niekiedy oprócz ziarniniaków spotyka się izolowane komórki olbrzymie ze złogami cholesterolowymi i ciałka Schaumanna, będące pozostałością po ziarniniakach, które uległy rozpadowi. Sporadycznie widoczne są ogniska organizującego się zapalenia płuc (22). Zmiany mają lokalizację okołooskrzelikową i śródzrazikową. Obserwuje się również hiperplazję tkanki chłonnej związanej z oskrzelami i oskrzelikami (bronchus-associated limphoid tissue – BALT), która u osób zdrowych jest trudna do uwidocznienia (16, 21). W płucu hodowców gołębi można znaleźć piankowate makrofagi odpowiadające ogniskom wewnątrzpochodnego lipidowego zapalenia płuc (22). Zasadniczo nie stwierdza się obecności antygenu wywołującego chorobę w tkance. Niekiedy jednakże w przypadkach hot tub lung lub płuca pracowników przemysłu metalowego można uwidocznić, a nawet wyhodować mykobakterie (22, 23). Natomiast w płucu drwali odkorowujących klony znajduje się w płucach komórki grzyba, w korkowicy fragmenty korka, a w płucu kuśnierzy fragmenty włosia (5, 11, 22).
W przewlekłym alergicznym zapaleniu pęcherzyków płucnych dominuje obraz śródmiąższowego włóknienia płuc przypominające niespecyficzne śródmiąższowe zapalenie płuc (non-specific interstitial pneumonia – NSIP), typ włókniejący lub zwykłe śródmiąższowe zapalenie płuc (usual interstitial pneumonia – UIP) (21, 22, 24, 25). Wśród 25 chorych na przewlekłe AZPP Churg i wsp. stwierdzili obecność zmian podobnych do UIP w 72% przypadków, w większości z towarzyszeniem włóknienia okołooskrzelikowego, komórek olbrzymich i ziarniniaków. 16% chorych prezentowało obraz przypominający postać włókniejącą NSIP, również ze współistnieniem cech charakterystycznych dla podostrego AZPP. Tylko w 2 przypadkach zmian podobnych do UIP nie znaleziono żadnych innych obrazów histopatologicznych. U pozostałych 12% chorych obraz nie odbiegał od stwierdzanego w postaci podostrej (26).
Objawy i przebieg kliniczny
Alergiczne zapalenie pęcherzyków płucnych występuje w postaci ostrej, podostrej i przewlekłej w zależności od długości i intensywności narażenia. W postaci ostrej objawy pojawiają się kilka godzin (od 2 do 9) po masywnej ekspozycji. Pacjent ma gorączkę, dreszcze, suchy kaszel, duszność, bóle mięśniowe, poty, mogą też wystąpić nudności i ból głowy. Objawy przypominają ostre zakażenie dróg oddechowych (27). Najczęściej ustępują one w ciągu 24-48 godzin od zakończenia ekspozycji (4). Łatwa męczliwość może utrzymywać się przez kilka tygodni. Osłuchiwaniem najczęściej stwierdza się delikatne, symetryczne trzeszczenia u podstawy płuc i niekiedy pojedyncze świsty, które stopniowo zanikają po ustaniu ekspozycji (1, 5, 28).
Przy ciągłym, ale mniej intensywnym lub nawracającym narażeniu w ciągu kilku-kilkunastu tygodni rozwija się postać podostra. Dominuje suchy kaszel, niekiedy ze skąpym wykrztuszaniem, oraz postępująca duszność i ograniczenie tolerancji wysiłku (29). Często dochodzi do utraty apetytu i spadku masy ciała. W badaniu przedmiotowym stwierdza się obustronne trzeszczenia, zwykle u podstawy płuc, ale mogą występować także nad całymi polami płucnymi. W przebiegu choroby może dochodzić do ostrych epizodów w przypadku dodatkowej masywnej ekspozycji na antygen (19, 27, 28).
Przewlekłe AZPP objawia się postępującą dusznością i ograniczeniem czynności płuc prowadzącym do hipoksemii i inwalidztwa oddechowego. Rzadziej niż w samoistnym śródmiąższowym włóknieniu płuc występują palce pałeczkowate, jednak różnicowanie tych dwóch chorób może być trudne. Dominującym objawem osłuchowym są utrzymujące się stale trzeszczenia (15, 25, 27).
Obecnie klasyczny podział na ostrą, podostrą i przewlekłą postać AZPP coraz częściej jest krytykowany. Proponuje się wyróżnienie następujących typów choroby:
– ostrego postępującego, w którym po ekspozycji na antygen występują ciężkie objawy, niekiedy wymagające hospitalizacji, zaś każdy następny epizod powoduje ich jeszcze większe nasilenie;
– ostrego przerywanego, niepostępującego – kiedy objawy pojawiają się również wkrótce po ekspozycji, ale są znacznie mniej nasilone, a powtarzane narażenia mogą wywoływać nawet łagodniejszą reakcję; pomiędzy epizodami pacjent nie ma żadnych objawów, a badania czynnościowe pozostają w normie;
– przewlekłego postępującego, które jest efektem nawracających ostrych epizodów lub może rozpoczynać się skrycie, bez poprzedzających ostrych objawów; dominuje pogorszenie tolerancji wysiłku z narastającą dusznością wysiłkową, kaszel, brak apetytu i wyniszczenie, a ostatecznie dochodzi do zwłóknienia płuc i niewydolności oddechowej;
– subklinicznego, w przypadku osób narażonych na antygeny, u których występują przeciwciała, ale nie ma objawów; chorzy tacy nie zaprzestają ekspozycji, a w miarę narastania czasu ekspozycji może u nich dojść do rozwoju przewlekłej choroby (3).
Inny, proponowany przez Lacasse i wsp. (30) podział kliniczny obejmuje jedynie dwie grupy – chorobę odwracalną i nieodwracalną. W pierwszej znajdują się osoby z nawracającymi objawami ogólnymi i dusznością występującymi po ekspozycji na antygen, objawom tym nie zawsze towarzyszą trzeszczenia, a zdjęcie radiologiczne klatki piersiowej może być prawidłowe. Drugą grupę stanowią chorzy z zaawansowaną chorobą śródmiąższową, trzeszczeniami, zmianami restrykcyjnymi w badaniach czynnościowych, hypoksemią, a niekiedy również palcami pałeczkowatymi. W badaniu tomografii komputerowej wysokiej rozdzielczości widoczne są zmiany o charakterze włóknienia (30).
Z kolei Fink i wsp. wyróżniają AZPP ostre oraz przewlekłe nawracające i przewlekłe utajone (31).
Diagnostyka
Nie istnieje pojedyncze badanie diagnostyczne, które pozwalałoby na rozpoznanie alergicznego zapalenia pęcherzyków płucnych. Rozpoznanie powinno opierać się na kryteriach klinicznych, radiologicznych i czynnościowych, wspartych przez wyniki badania popłuczyn oskrzelowo-pęcherzykowych (broncho-alveolar lavage – BAL) i w rzadkich przypadkach badania histopatologicznego (27, 32).
Badania laboratoryjne
Badania laboratoryjne nie wnoszą wiele do rozpoznania, za wyjątkiem badania obecności specyficznych precypityn w surowicy. Swoiste IgG przeciwko antygenom wywołującym AZPP stwierdza się u 40-50% osób narażonych, które nie rozwijają objawów choroby (28), z kolei u chorych mogą one wystąpić w 75 do 100% przypadków płuca farmera, ale tylko w 30-50% przypadków płuca hodowców ptaków. Wśród chorych narażonych na rzadziej występujące antygeny testy wypadają ujemnie jeszcze częściej. Niska czułość badania jest związana z brakiem komercyjnie dostępnych testów obejmujących wszystkie możliwe antygeny wywołujące reakcję alergiczną w płucach – ich liczba i różnorodność (np. uzależniona od lokalizacji geograficznej) uniemożliwia opracowanie takich testów. Tak więc brak obecności precypityn nie wyklucza rozpoznania AZPP, a ich obecność nie może być jedynym kryterium diagnostycznym (27, 33). Poza tym z odchyleń w badaniach krwi można stwierdzić mierną leukocytozę z przesunięciem w kierunku form młodych, podwyższone stężenia immunoglobulin klasy G i M (IgG i IgM) i przyspieszenie opadania krwinek czerwonych, niekiedy obserwuje się obecność czynnika reumatoidalnego (RF), nieznacznie podwyższone stężenie białka C – reaktywnego i zwiększoną aktywność dehydrogenazy mleczanowej (LDH) (3, 18, 28).
W ramach badań naukowych istnieje możliwość wykonywania testów transformacji limfocytów pod wpływem swoistych antygenów. Nie jest to jednak procedura odpowiednio wystandaryzowana i dostępna w szerokim zakresie klinicznym (18, 27).
Badania obrazowe
Badanie radiologiczne klatki piersiowej jest pierwszym badaniem obrazowym wykonywanym u chorych z podejrzeniem AZPP. Obraz radiologiczny jest uzależniony od postaci klinicznej. W ostrym AZPP widoczne są obustronne zlewające się zagęszczenia drobnoplamiste, czasem guzkowe, o różnej lokalizacji, z przewagą jednak pól środkowych i dolnych (ryc. 1). Mogą one przypominać obrzęk płuc lub prosówkę. Zdjęcie przeglądowe może być prawidłowe nawet u 20% pacjentów. Zmiany znikają szybko po zaprzestaniu ekspozycji (1, 11, 18, 31).
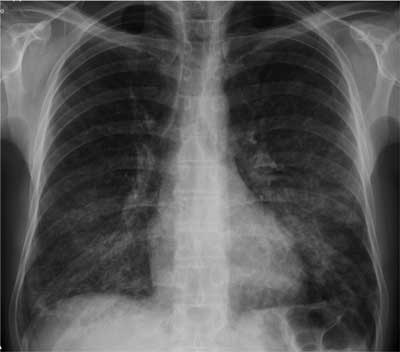
Ryc. 1. Zdjęcie radiologiczne klatki piersiowej w projekcji PA: Ostre AZPP. W obu płucach głównie w polach dolnych i w mniejszym stopniu w środkowych widoczne zacienienia o typie matowej szyby.
W postaci podostrej obraz radiologiczny jest podobny, mogą pojawić się zagęszczenia o charakterze siateczki, głównie w dolnych i środkowych polach płuc. Zmiany mają tendencję do utrzymywania się (ryc. 2) (5, 18).
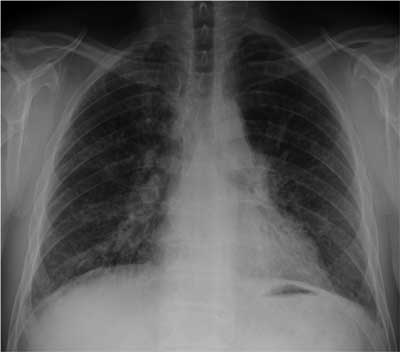
Ryc. 2. Zdjęcie radiologiczne klatki piersiowej w projekcji PA: Podostre AZPP. W obu płucach widoczne obszary matowej szyby i zmiany rozsiane o charakterze siateczkowatym i linijnym o nieregularnej dystrybucji.
Postać przewlekła charakteryzuje się dominacją utrwalonych zmian siateczkowych i o typie plastra miodu, często najbardziej nasilonych w górnych i środkowych polach płucnych (ryc. 3) (11, 18).

Ryc. 3. Zdjęcie radiologiczne klatki piersiowej w projekcji PA: Przewlekłe AZPP w fazie włóknienia płuc. Płuca o znacznie zmniejszonej objętości z obrazem zaawansowanego włóknienia – dystrybucja i lokalizacja zmian wskazują na włóknienie w przebiegu AZPP.
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
24 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
59 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
119 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 28 zł
Piśmiennictwo
1. Rowińska-Zakrzewska E, Bestry I: Alergiczne zapalenie pęcherzyków płucnych. [W:] Szczeklik A. (red.) Choroby Wewnętrzne Kraków 2005; 580-583.
2. Campbell JM: Acute symptoms following work with hay. Br Med J 1932; 2: 1143-1144.
3. Ismail T, Mcsharry C, Boyd G: Extrinsic allergic alveolitis. Respirology 2006; 11: 262-268.
4. Madison JM: Hpersensitivity pneumonitis clinical perspetives. Arch Patol Lab Med 2008; 132: 195-198.
5. Radzikowska E: Alergiczne zapalenie pęcherzyków płucnych. [W:] Rowińska-Zakrzewska E, Wiatr E, Pirożyński M (red.) Choroby śródmiąższowe płuc Bielsko-Biała 2001; 134-149.
6. Lerch E, Györik S, Feilchendfeld J et al.: A case of lenalidomide – induced hypersensitivity pneumonia. Onkologie 2010; 33: 249-252.
7. Martin N, Innes JA, Lambert CM: Hypersensitivity pneumonitis associated with leflunomide therapy. J Rheumatol 2007; 34: 1934-1937.
8. Kochel D, Handzhiev S, Leucht V et al.: Hypersensitivity pneumonitis associated with the use of temozolomide. Eur Resp J 2009; 33: 931-934.
9. Tonelli AR, Lottenberg R, Allan RW, Sriram PS: Rituximab – induced hypersensitivity pneumonitis. Respiration 2009; 78: 225-229.
10. Um SJ, Lee SK, Yang DK: Hypersensitivity pneumonitis following intravesical bacille Calmette-Guérin immunotherapy for superficial bladder cancer. J Investig Allergol Clin Immunol 2009; 19: 230-232.
11. Hirschmann JV, Pipavath SNJ, Godwin JD: Hypersensiticity pneumonitis: a historical, clinical and radiological review. Radio Graphics 209; 29: 1921-1938.
12. Apostolakos MJ, Rossmoore H, Beckett WS: Hypersensitivity pneumonitis from ordinary residual exposures. Envir Health Persp 2001; 109: 979-981.
13. Woda BA: Hypersensitivity pneumonitis an immunopathology review. Arch Patol Lab Med 2008; 132: 204-205.
14. Lacasse Y, Assayag E, Cormier Y: Myths and controversies in hypersensitivity pneumonitis. Semin Resp Crit Care Med 2008; 29: 631-642.
15. Patel AM, Ryu JH, Reed CE: Hypersensitivity pneumonitis: current concepts and future questions. J Allerg Clin Immunol 2001; 108: 661-670.
16. Mcsharry C, Anderson K, Bourke SJ, Boyd G: Takes your breath away – the immunology of allergic alveolitis. Clin Exp Immunol 2002; 128: 3-9.
17. Bourke SJ, Dalphin JC, Boyd G et al.: Hypersensitivity pneumonitis: current concepts. Eur Resp J 2001; 18 (Suppl 32): 81s-92s.
18. Selman M, Mejia M, Pardo A: Hypersensitivity pneumonitis. [W:] Lynch JP (red.) Intersitial pulmonary and bronchiolar disorders New York 2008; 267-288.
19. Girard M, Lacasse Y, Cormier Y: Hypersensitivity pneumonitis. Allergy 2009; 64: 322-334.
20. Hanak W, Kalra S, Aksamit TR et al.: Hot tub lung: presenting features and clinical course of 21 patients. Resp Med 2006; 100: 610-615.
21. Takemura T, Akashi T, Ohtani Y et al.: Pathology of hypersensitivity pneumonitis. Curr Opin Pulm Med 2008; 14: 440-454.
22. Barrios R: Hypersensitivity pneumonitis. Histopathology Arch Pathol Lab Med 2008; 132: 199-203.
23. Falkinham JO: Mycobacterial aerosols and respiratory disease. Emerg Infect Dis 2003; 9: 763-767.
24. Lima MS, Coletta ENAM, Ferreira RG et al.: Subacute and chronic hypersensitivity pneumonitis: histopathological patterns and survival. Resp Med 2009; 103: 508-515.
25. Hayakawa H, Shirai M, Sato A et al.: Clinicopathological features of chronic hypersensitivity pneumonitis. Respirology 2002; 7: 359-364.
26. Churg A, Muller NL, Flint J, Wright JL: Chronic hypersensitivity pneumonitis. Am J Surg Pathol 2006; 30: 20-208.
27. Richerson HB, Bernstein IL, Fink JN et al.: Guidlines for the clinical evaluation of hypersensitivity pneumonitis: report of the Subcomittee on Hypersensitivity Pneumonitis. J Alerg Clin Immunol 1989; 84: 839-844.
28. Fink JN: Hypersensitivity pneumonitis. J Alerg Clin Immunol 1984; 74: 1-9.
29. Hanak V, Golbin JM, Ryu JH: Causes and presenting features in 85 consecutive patients with hypersensitivity pneumonitis. Mayo Clin Proc 2007; 82: 812-816.
30. Lacasse Y, Selman M, Costabel U et al.: Classification of hypersensitivity penumonitis a hypothesis. Int Arch Allergy Immunol 2009; 149: 161-166.
31. Fink JN, Ortega HG, Reynolds HY: Needs and opportunities for research in hypersensitivity pneumonitis. Am J Resp Crit Care Med 2005; 171: 792-798.
32. Lacasse Y, Selamn M, Costabel U et al.: Clinical diagnosis f hypersensitivity pneumonitis. Am J Resp Crit Care Med 2003; 168: 952-958.
33. Diego C, Cullinan P: Extrinsic allergic alveolitis. [W:] Eur Respir Monography 2009; 46: 112-125.
34. Lynch DA, Rose CS, Way D, King TE: Hypersensitivity pmeumonitis: sensitivity of high – resolution CT In a population – based study. Am J Radiol 1992; 159: 469-472.
35. Hartman TE: The HRCT features of extrinsic allergic alveolitis. Sem Resp Crit Care Med 2003; 24: 419-425.
36. Hanak V, Golbin JM, Hartman TE, Ryu JH: High-resolution CT findings of parenchymal fibrosis correlate with prognosis in hypersensitivity pneumonitis. Chest 2008; 134: 133-138.
37. Churg A, Sin DD, Everest D et al.: Pathologic patterns and survival in chronic hypersensitivity pneumonitis. Am J Surg Pathol 2009; 33: 1765-1770.
38. Mróz RM, Korniluk M, Stasiak-Barmuta A, Chyczewska E: Upregulation of Th1 cytokine profile in bronchoalveolar lavage fluid of patients with hypersensitivity pneumonitis. J Physiol Pharm 2008; 59 (Suppl 6): 499-505.
39. Schuyler M, Cormier Y: The diagnosis of hypersensitivity pneumonitis. Chest 1997; 111: 534-536.
40. Kirkhorn SR, Garry VF: Agricultural Lung Diseases. Env Health Persp 2000; 108 (Suppl 4): 705-712.
41. Funke M, Fellrath JM: Hypersensitivity pneumonitis secondary to lovebirds: a new cause of bird fancier’s disease. Eur Resp J 2008; 32: 517-521.
42. Merget R, Sander I, Ewig S et al.: Consort hypersensitivity pneumonitis. Eur Resp J 2009; 33: 1223-1225.
43. Inase N, Ohtani Y, Sumi Y et al.: A clinical study of hypersensitivity pneumonitis presumably caused by feather duvets. Ann Allergy Asthma Immunol 2006; 96: 98-104.
44. Morell F, Roger A, Reyes L et al.: Bird fancier’s lung: a series of 86 patients. Medicine 2008; 87: 110-130.
45. Ohtani Y, Saiki S, Sumi Y et al.: Clinical features of recurrent and insidious chronic bird fancier’s lung. Ann Allergy Asthma Immunol 2003; 90: 604-610.
46. Beckett W, Kalla M, Sood A et al.: Hypersensitivity pneumonitis associated with environmental mycobacteria. Env Health Persp 2005; 113: 767-770.



