© Borgis - Postępy Nauk Medycznych 10/2011, s. 836-841
*Dagmara Borkowska1, Zofia Zwolska1, Beata Broniarek-Samson2, Dorota Michałowska-Mitczuk3, Ewa Augustynowicz-Kopeć1
Porównanie testów IGRA i próby tuberkulinowej w rozpoznaniu utajonego zakażenia prątkiem gruźlicy1)
The use of IGRAs and tuberculin skin test in the diagnosis of latent tuberculosis infection
1Zakład Mikrobiologii, Instytut Gruźlicy i Chorób Płuc w Warszawie
Kierownik Zakładu: prof. nadzw. dr hab. med. Ewa Augustynowicz-Kopeć
2Zakład Diagnostyki Laboratoryjnej, Instytut Gruźlicy i Chorób Płuc w Warszawie
Kierownik Zakładu: mgr Beata Broniarek-Samson
3Przychodnia Przykliniczna, Instytut Gruźlicy i Chorób Płuc w Warszawie
Kierownik Przychodni: dr med. Dorota Michałowska-Mitczuk
Streszczenie
Wstęp. Jedna trzecia ludności świata jest zakażona Mycobacterium tuberculosis. Tak duża populacja zakażonych osób stanowi poważną przeszkodę w nadzorze nad gruźlicą. Ze względu na ryzyko progresji od zakażenia utajonego do aktywnej choroby, identyfikacja osób z LTBI jest kluczowym elementem w programach nadzoru nad gruźlicą.
W Polsce, gdzie cała populacja jest szczepiona BCG istotne jest pytanie, czy dodatni wynik próby tuberkulinowej jest związany z wcześniejszym szczepieniem, czy z istniejącym zakażeniem M. tuberculosis. Dlatego poszukuje się nowych metod diagnozujących zakażenie prątkiem gruźlicy w stadium latencji jeszcze przed rozwojem choroby. Obecnie dostępne są dwa testy IGRA do szybkiej diagnostyki LTBI: QuantiFERON-Tb Gold i T-SPOT.TB.
Materiał i metody. Badaniem objęto 78 osób, 25 zdrowych pracowników ochrony zdrowia (grupa wysokiego ryzyka zakażeniem prątkiem gruźlicy) i 53 chorych Instytutu Gruźlicy i Chorób Płuc. Uczestnikom biorącym udział w badaniu wykonano dwa testy interferonowe: T-SPOT.TB, QuantiFERON-TbGold i próbę tuberkulinową TST.
Wyniki. Spośród 78 badanych, u 6 (7,7%) osób stwierdzono pozytywne wyniki wszystkich trzech testów T-SPOT.TB+/QFT-G+/TST+, co sugeruje że mogą być zakażeni prątkiem gruźlicy. W obu analizowanych grupach otrzymano 11 (14,1%) pozytywnych wyników testu T-SPOT.TB, 12 (15,4%) QuantiFERON-TB Gold i 22 (28,2%) TST. Przyjmując za punkt odcięcia średnicę odczynu tuberkulinowego 10 mm, zgodność wyników T-SPOT.TB i TST była wyższy w obu badanych grupach niż obserwowana dla QFT-G i TST. Zgodności pomiędzy testami IGRA była podobna, wynosiła 92% w grupie pracowników ochrony zdrowia HCWs i 88,5% w grupie pacjentów IGiChP.
Wnioski. Wyniki testów IGRA i TST mogą być niezgodne. Nie wszystkie przyczyny niezgodności testów są wytłumaczalne. Rozpoznanie zakażenia prątkiem gruźlicy nie może być oparte na pojedynczym wyniku testu T-SPOT.TB, QFT-G czy TST.
Summary
Introduction. One-third of the world’s population is infected with M. tuberculosis. This large pool of infected individuals poses a major hurdle of tuberculosis control. Due to the risk of progression from latent infection to active disease, identifying persons with latent TB infection is key component of disease elimination.
In Poland, where the entire population is BCG vaccinated, it is important to determine whether a positive tuberculin skin test result is associated with a prior BCG vaccination, or with an existing MTB infection. Therefore looking for new methods of diagnosing MTB infection in a stage of latency before the development of the disease. Currently, there are two interferon- gamma release assays for the rapid diagnosis of latent tuberculosis infection: QuantiFERON-TB Gold and T-SPOT.TB.
Material and methods. The study included 78 subjects, 25 health care workers (high risk of tuberculosis infection) and 53 patients from the Institute of Tuberculosis and Lung Disease. Of the participants studied performed both interferon-γ release assays: T-SPOT.TB, QuantiFERON-TbGold and a tuberculin skin test TST.
Results. Among 78 subjects, 6 (7.7%) were T-SPOT.TB+/QFT-G+/TST+, suggesting that they might in fact be infected with MTB. In the two analyzed groups showed 11 (14.1%) positive T-SPOT.TB results, 12 (15.4%) QuantiFERON-TB Gold and 22 (28.2%) positive TST results. Using 10 mm or more as a cut-off for TST, concordance between T-SPOT.TB and TST was higher in both study groups than that seen for QFT-G and TST. Concordance between interferon-γ release assays was similar in HCWs (92%) and in patients from the Institute of Tuberculosis and Lung Disease (88.5%).
Conclusions. The results of IGRAs and TST are discordant. Not all causes of discordances are explicable. The diagnosis of tuberculosis infection cannot be based on a single T-SPOT.TB, QFT-G or TST result.

Wstęp
Gruźlica wśród wielu chorób zakaźnych nadal pozostaje jedną z najczęstszych przyczyn zachorowań i zgonów na świecie (1). Szacuje się, że jedna trzecia ludności jest zakażona Mycobacterium tuberculosis, a większość tych zakażeń ma postać utajoną LTBI (Latent Tuberculosis Infection) (2). Szczególnie istotna w programach nadzoru nad gruźlicą jest identyfikacja osób z czynną gruźlicą, umożliwiająca wyleczenie chorego i zahamowanie rozprzestrzeniania się choroby. Śledzenie liczby osób z zakażeniem latentnym stanowi również ważny element tego nadzoru (1). Do chwili obecnej głównym narzędziem diagnostycznym w wykrywaniu zakażenia prątkiem gruźlicy była próba tuberkulinowa TST (Tuberculin Skin Test), której wyniki mogą być obarczone błędem (3). Niska specyficzność najstarszego z testów diagnostycznych wynika ze składu tuberkuliny, która jest mieszaniną antygenów wspólnych dla prątków chorobotwórczych, szczepu BCG i mykobakterii z grupy MOTT (Mycobacteria Other Than Tuberculosis). Do przyczyn niskiej czułości TST zalicza się upośledzenie odpowiedzi immunologicznej typu komórkowego i brak reakcji na tuberkulinę wynikającą z wieku pacjenta i złego stanu jego zdrowia (3, 4). W diagnostyce zakażenia M. tuberculosis coraz powszechniej stosuje się testy interferonowe oparte na antygenach ESAT-6 (Early Secretory Antigen Target 6) i CFP 10 (Culture Filtrated Potein 10 kDa) (2, 5, 6). Oba białka kodowane są w regionie RD1 genomu M. tuberculosis, region ten jest nieobecny u M. bovis BCG i prątków środowiskowych, dzięki czemu możliwe jest zmniejszenie liczby wyników fałszywie dodatnich w populacjach szczepionych BCG lub zakażonych większością prątków niegruźliczych za wyjątkiem M. kansasi, M. szulgai, M. marinum (7, 8, 9). W Polsce obecnie są dostępne dwa testy IGRA wykrywające zakażenie M. tuberculosis z krwi obwodowej badanego: QuantiFERON-Tb Gold (Cellestis, Australia) i T-SPOT.TB (Oxford Immunotec, Wielka Brytania). Zasada działania testów opiera się na ocenie ilości IFN-γ wytwarzanego przez limfocyty T na skutek ich stymulacji antygenami ESAT-6 i CFP 10 metodą ELISA (enzyme-linked immunosorbent assay) – test QuantiFERON-Tb Gold lub metodą ELISpot (enzym linked immuno-spot assay) – test T-SPOT.TB (8, 10, 11).
Cel pracy
Celem pracy, było porównanie wyników badań w kierunku rozpoznania latentnego zakażenia prątkiem gruźlicy przy użyciu dwóch komercyjnych testów IGRA (interferon-γ release assay): T-SPOT.TB, QuantiFERON-Tb Gold i próby tuberkulinowej TST.
Materiał i metody
Badaniem objęto 78 osób, które podzielono na dwie grupy: I. 25 zdrowych pracowników ochrony zdrowia – HCWs (Health Care Workers) i II. 53 chorych hospitalizowanych w Instytucie Gruźlicy i Chorób Płuc, u których wykluczono aktywną postać gruźlicy na podstawie ujemnych wyników badań mikrobiologicznych.
W analizowanej grupie były 42 kobiety i 36 mężczyzn w wieku od 12 do 70 lat (1 dziecko i 77 dorosłych). Wszyscy szczepieni BCG (tab. 1). Osobom biorącym udział w badaniu wykonano równocześnie testy T-SPOT.TB, QuantiFERON-Tb Gold i próbę tuberkulinową TST. W celu wykonania testów IGRA wszystkim badanym pobrano krew obwodową do odpowiednich probówek zgodnie z zaleceniami producentów testów IGRA i założono próbę tuberkulinową. Za wynik pozytywny testu T-SPOT.TB uznawano co najmniej 6 plam „spots”, czyli 6 limfocytów T wydzielających IFN-γ. Za wynik pozytywny testu QuantiFERON-Tb Gold uznawano poziom IFN-γ ≥ 0,35 IU/Ml. Próbę tuberkulinową wykonano stosując odmianę tuberkuliny PPD (purfied protein derivative) – tuberkulinę RT 23 (renset tuberculin, 23. seria). Wprowadzono ją śródskórnie w dłoniową powierzchnię przedramienia w ilości dwóch jednostek. Wynik odczytano po upływie 48-72 godzin, mierząc średnicę utworzonego nacieku poprzecznie do długiej osi przedramienia. Za wynik dodatni uznawano naciek większy bądź równy 10 mm, zgodnie z europejskimi rekomendacjami. Dla wszystkich 78 osób test TST wykonano w IGiChP. Za wykonanie próby tuberkulinowej i odczyt była odpowiedzialna ta sama osoba. Wśród 53 pacjentów hospitalizowanych w IGiChP, 46 miało podejrzenie gruźlicy i wykonane badania mikrobiologiczne (bakterioskopia, posiew, badanie genetyczne), u pozostałych 7 chorych prowadzono diagnostykę różnicową zmian płucnych. Na badania uzyskano zgodę Komisji Etycznej przy Instytucie Gruźlicy i Chorób Płuc nr KE-63/2005.
Tabela 1. Charakterystyka analizowanych grup badawczych.
| Pracownicy ochrony zdrowia (HCWs)/wysokie ryzyko zakażenia prątkiem gruźlicy | Chorzy leczeni w IGiChP |
| n = 78 | 25 | 53 |
| wiek w latach | 28-70 | 12-61 |
| dorośli | 25 | 52 |
| dzieci | 0 | 1 |
| K:M płeć | 25:0 | 17:36 |
| szczepienie BCG | 25 | 53 |
Wyniki
Wyniki TST przedstawiono w dwóch grupach, w zależności od wielkości średnicy nacieku. Wyniki ujemne < 10 mm stwierdzono u 56. Było to 15 (60%) pracowników ochrony zdrowia (HCWs) i 41 (77,3%) chorych hospitalizowanych w IGiChP. Wyniki pozytywne przy nacieku ≥ 10 mm stwierdzono u 22 osób. W grupie HCWs było to 10 (40%) osób, a w grupie chorych leczonych w IGiChP 12 (22,6%) (tab. 2).
Tabela 2. Wyniki testu TST w dwóch analizowanych grupach badawczych.
| TST (mm) | HCWs | Chorzy IGiChP |
| < 10 | 15 (60%) | 41(77,3%) |
| ≥ 10 | 10 (40%) | 12 (22,6%) |
| Razem | 25 | 53 |
W grupie 25 pracowników HCWs stwierdzono 5 (24%) pozytywnych wyników testu T-SPOT.TB, 6 (20%) QuantiFERON-TbGold i 10 (40%) próby tuberkulinowej. W grupie 53 chorych IGiChP było 6 (11,3%) pozytywnych wyników zarówno testu T-SPOT.TB i QuantiFERON-Tb Gold oraz 12 (22,6%) TST. Najwięcej pozytywnych wyników dla trzech porównywanych testów, przy uznaniu za punkt odcięcia nacieku o średnicy 10 mm, dawał test TST. W grupie 25 HCWs zaobserwowano więcej pozytywnych wyników testów IGRA i TST (ryc. 1).
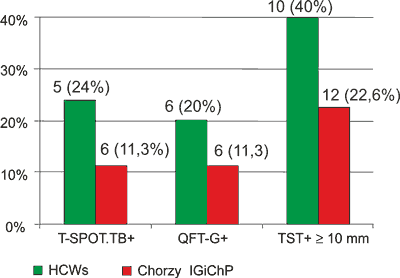
Ryc. 1. Rozkład pozytywnych wyników testów IGRA i TST w dwóch grupach badawczych.
Wśród 25 pracowników ochrony zdrowia (HCWs) u 2 osób wyniki testów IGRA były niezgodne. Niezgodności typu T.SPOT.TB-/QFT-G+ stwierdzono przy ujemnym wyniku TST, a niezgodność typu T.SPOT.TB+/QFT-G- zaobserwowano przy dodatnim wyniku TST. Wśród 4 (16%) osób z T.SPOT.TB+/QFT-G+, 1 (4%) osoba miała negatywny wynik TST, a pozostałe 3 (12%) miały pozytywny wynik TST. W badanej grupie 6 (24%) osób miało pozytywny wynik TST przy T.SPOT.TB-/QFT-G-. Ujemne wyniki wszystkich trzech testów stwierdzono dla 13 (52%) osób z grupy HCWs (tab. 3).
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
24 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
59 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
119 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 28 zł
Piśmiennictwo
1. Kang YA, Lee HW, Hwang SS et al.: Usefulness of whole-blood interferon-γ assay and interferon-γ enzyme-linked immunospot assay in the diagnosis of active pulmonary tuberculosis. Chest 2007; 132: 959-965.
2. Lee JY, Choi HJ, Park I-N et al.: Comparison of two commercial interferon-γ assays for diagnosing Mycobacterium tuberculosis infection. Eur Respir J 2006; 28: 24-30.
3. Bienek DR, Chang KG: Evaluation of a interferon-gamma release assay, T-SPOT.TB in a population with a low prevalence of tuberculosis. INT J Tuberc Lung Dis 2009; 13 (11): 1416-1421.
4. Ewer K, Deeks J, Alvarez L et al.: Comparison of T-cell-based assay with tuberculin skin test for diagnosis of Mycobacterium tuberculosis infection in a school tuberculosis outbreak. The Lancet 2003; 361: 1168-1173.
5. Demkow U: Diagnostyka immunologiczna zakażenia prątkiem gruźlicy u dzieci Ziołkowski J: Gruźlica dziecięca. Borgis, Warszawa 2010; 91-93.
6. Kim H-J, Yoon HJ, Park KU et al.: The impact of previous tuberculosis history on T-SPOT.TB interferon-gamma release assay results. Int J Tuberc Lung Dis 2011; 15 (4): 510-516.
7. Pai M, Riley LW, Colford Jr JM: Interferon-g assay in the immunodiagnosis of tuberculosis: a systematic review. Lancet Infect Dis 2004; 4: 761-776.
8. Lalvani A: Counting antigen-specific T cells: a new approach for monitoring response to tuberculosis treatment? CID 2004; 38: 757-759.
9. van Pinxteren LAH, Ravn R, Agger EM et al.: Diagnosis of tuberculosis based on the two specific antigens ESAT-6 and CFP 10. Clin Diagn Lab Immunol 2000; 7 (2): 1550160.
10. van Leeuwen RML, Bossinka WJ, Thijsen SFT: Exclusion of active Mycobacterium tuberculosis complex infection with the T-SPOT.TB assay. Eur Respir J 2007; 29: 605-607.
11. Lalvani A: Diagnosing tuberculosis infection in the 21st century. New tools to tackle an old enemy. Chest 2007; 131: 1898-1906. Ferrara G, Losi M, Meacci M et al.: Routine hospital use of a new commercial whole blood interferon-g assay for the diagnosis of tuberculosis infection. Am J Respir Crit Care Med 2005; 172: 631-635.
12. Richeldi L: An update on the diagnosis of tuberculosis infection. Am J Respir Crit Care Med 2006; 174: 736-742.
13. Pai M, Kalantri S, Dheda K: New tools and emerging technologies for the diagnosis of tuberculosis: part I. Latent tuberculosis. Expert Rev Mol Diagn 2006; 3: 413-422.
14. Dominguez J, Ruiz-Manzano J, Souza-Galvao M et al.: Comparison of two commercially available gamma interferon blond tests for immunodiagnosis of tuberculosis. Clin Vaccine Immunol 2007; 15 (1): 168-171.
15. Barsegian V, Mathias KD, Wrighton-Smith P et al.: Prevalence of latent tuberculosis infection in German radiologists. J Hosp Infect 2008; 1-8.
16. Walsh MC, Camerlin AJ, Miles R et al.: The sensitivity of interferon-gamma release assays is not compromised in tuberculosis patients with diabetes. Int J Tuberc Lung Dis 2011; 15 (2): 179-184.
17. Ferrara G, Losi M, D’Amico R et al.: Use in routine clinical practice of two commercial blood tests for diagnosis of infection with Mycobacterium tuberculosis: a prospective study. The Lancet 2006; 367: 1328-1134.
18. Diel R, Loddenkemper R, Nienhaus A: Evidence-based comparison of commercial interferon-γ release assays for detecting active TB. A metaanalysis. Chest 2010; 137 (4): 952-968.
19. Mazurek GH, LoBue PA, Daley Ch.L et al.: Comparison of a whole-blood interferon-γ assay with tuberculin skin testing for detecting latent Mycobacterium tuberculosis infection. JAMA 2001; 286: 1740-1747.
20. Stefan DC, Dippenaar A, Detjen AK et al.: Interferon-gamma release assays for the detection of Mycobacterium tuberculosis infection in children with cancer. Int J Tuberc Lung Dis 2010; 6: 689-694.
21. Tissiot F, Zanetti G, Francioli P et al.: Influence of bacille Calmette-Guerin vaccination on size of tuberculin skin test reaction: to what size? Clin Infect Dis 2005; 40: 211-217.
22. Storla DG, Kristiansen I, Oftung F et al.: Use of interferon gamma-based assay to diagnose tuberculosis infection in health care workers after short term exposure. BMC Infect Dis 2009; 9: 60.
23. Borkowska D, Zwolska Z, Augustynowicz-Kopeć E et al.: Interferonowy test T-SPOT.TB w diagnostyce latentnego zakażenia prątkiem gruźlicy. Pneumonol Alergol Pol 2011; 79 (4): 264-271.
24. Cehovin A, Cliff JM, Hill PC et al.: Extended culture enhances sensitivity of a gamma interferon assay for latent Mycobacterium tuberculosis infection. Clin Vaccine Immunol 2007; 14 (6): 796-798.
25. Leung ChCh, Yam WCh, Yew WW et al.: T-SPOT.TB outperforms tuberculin skin test in predicting tuberculosis disease. AJRCCM 2010; 182: 834-840.
26. Nienhaus A, Schablon A, Diel R: Interferon-gamma release assay for the diagnosis of latent TB infection – analysis of discordant results when compared to the tuberculin skin test. PLoS One 2008; 7: e2665.
27. Weinfurter P, Blumberg HM, Goldbaum G et al.: Predictors of discordant tuberculin skin test and QuantiFERON-TB Gold In-Tube results in various high-risk groups. INT J Tuberc Lung Dis 2011; 15 (8): 1056-1061.

