© Borgis - Postępy Fitoterapii 1/2011, s. 41-47
Bogdan Kędzia
Działanie przeciwnowotworowe ekstraktów propolisowych
Anticancer activity of extracts from propolis
Instytut Włókien Naturalnych i Roślin Zielarskich w Poznaniu
Dyrektor Instytutu: prof. dr hab. Grzegorz Spychalski
Summary
The literature reviews show that the propolis extracts demonstrate the significant cytotoxic activity against many lines of animal tumor cells also human tumor cells. It has been documented by in vitro and in vivo studies.
The carried out studies show, that the main mechanism of activity of propolis extracts on cancer cells is the induction of apoptosis process (programmed cell death).

Działanie przeciwnowotworowe propolisu datuje się od połowy lat 60. ubiegłego stulecia. Jako pierwsi cytostatyczne właściwości ekstraktu etanolowego z propolisu stwierdzili badacze rumuńscy Derevici i Popescu (1) w połowie lat 60. ubiegłego wieku. Odnotowali oni, że ekstrakt ten hamował rozwój nowotworu puchliny wodnej Ehrlicha u szczurów.
W dziesięć lat później spostrzeżenia te zostały potwierdzone w trakcie leczenia nowotworów u zwierząt doświadczalnych przez naukowców litewskich Valaviczju i wsp. (2).
Duże zasługi w tym zakresie mają badacze polscy. Hładoń i wsp. (3) wykazali działanie ekstraktów z propolisu krajowego na hodowle komórkowe nowotworów ludzkich Hela i KB (tab. 1). Najwyższą aktywność cytostatyczną ED50 (stężenie hamujące w 50% biosyntezę białek w hodowlach tych nowotworów) wykazywał ekstrakt eterowy z propolisu w odniesieniu do hodowli tkankowej nowotworu HeLa (ED50 = 3,9 μg/ml). Jeszcze większą aktywnością cytostatyczną odznaczały się frakcja butanolowa i frakcja octanu etylowego, które otrzymano z ekstraktu eterowego. Ich ED50 wobec hodowli komórkowej nowotworu Hela wynosiły odpowiednio 2,6 i 3,3 μg/ml, a wobec hodowli nowotworu KB odpowiednio 2,9 i 3,4 μg/ml. Dla porównania ED50 dla substancji standardowej, jaką jest arabinozyd cytozyny, wynosiło 0,89 μg/ml.
Tabela 1. Działanie cytotoksyczne ekstraktów z propolisu polskiego na hodowle tkankowe nowotworów (3).
| Ekstrakty propolisowe |
Hodowle tkankowe nowotworów (ED50)* |
| Hela (μg/ml) |
KB (μg/ml) |
Ekstrakt eteru naftowego
Ekstrakt chloroformowy
Ekstrakt metanolowy
Ekstrakt wodny
Ekstrakt eterowy (EE)
Frakcja chloroformowa z EE
Frakcja octanu etylowego z EE
Frakcja butanolowa z EE
Frakcja etanolowa z EE
Arabinozyd cytozyny (standard) | 510,0
200,0
580,0
> 1000,0
3,9
4,6
3,3
2,6
13,2
0,89 | –
–
–
–
–
4,8
3,4
2,9
12,1 |
| *ED50 – Stężenie ekstraktu (μg/ml) hamujące w 50% biosyntezę białek w hodowli tkankowej nowotworu |
Ban i wsp. (4), naukowcy serbscy, odnotowali wysoką aktywność ekstraktu etanolowego z propolisu krajowego. Stwierdzili oni, że ED50 ekstraktu w odniesieniu do hodowli komórek nowotworowych Hela wynosi 10 μg/ml (ryc. 1). Ponadto po 24 godz. ekstrakt ten odznaczał się wysoką aktywnością przeciwnowotworową nie tylko wobec komórek znajdujących się w trakcie namnażania, ale także będących w fazie spoczynkowej.
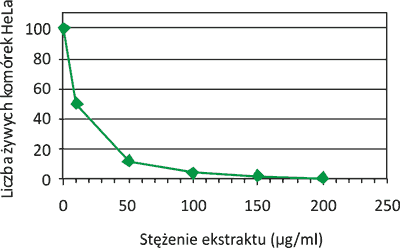
Ryc. 1. Działanie ekstraktu etanolowego z propolisu serbskiego na hodowlę tkankową komórek nowotworowych Hela (4).
Następnie Bašić i wsp. (5) badali u myszy działanie ekstraktu wodnego z propolisu chorwackiego w kontekście zapobiegania przerzutom do płuc przeszczepialnego nowotworu piersi (TBK) o słabej immunogenności. Zarówno komórki przeszczepialne nowotworu w liczbie 103/zwierzę, jak i ekstrakt propolisowy w ilości 0,5 mg/kg podawano drogą dożylną. Zauważono, że podanie ekstraktu propolisowego na 7 dni przed zakażeniem powodowało znaczne zmniejszenie przerzutów nowotworu do płuc, natomiast jeśli zakażenie zwierząt wykonywano równocześnie z podaniem ekstraktu lub ekstrakt podawano po 7 dniach od zakażenia, nie miało to wpływu na liczbę przerzutów do płuc.
Banskota i wsp. (6) zajęli się działaniem ekstraktów otrzymanych z propolisu brazylijskiego na hodowle komórkowe nowotworu włókniakomięsaka ludzkiego HT-1080 i nowotworu mysiego okrężnicy L5-26. Ekstrakty z propolisu otrzymywano w następujący sposób: najpierw surowiec ekstrahowano wodą, następnie pozostałość ekstrahowano kolejno alkoholem metylowym i chloroformem. Ekstrakt metanolowy frakcjonowano z kolei za pomocą octanu etylu na frakcję rozpuszczalną i nierozpuszczalną w tym rozpuszczalniku. Cytotoksyczność otrzymanych ekstraktów podano w tabeli 2. Otrzymane wyniki wskazują, że ekstrakt wodny nie odznaczał się działaniem cytotoksycznym (ED50 > 100 μg/ml). Natomiast pozostałe ekstrakty i frakcje działały na hodowle komórkowe badanych nowotworów w granicach ED50 od 53,1 do 89,6 μg/ml.
Tabela 2. Działanie cytotoksyczne ekstraktów z propolisu brazylijskiego na hodowle komórkowe nowotworów (6).
| Ekstrakty propolisowe |
Hodowle komórkowe nowotworów (ED50) |
| HT-1080 (μg/ml) |
L5-26 (μg/ml) |
Ekstrakt wodny
Ekstrakt metanolowy
Ekstrakt chloroformowy
Frakcja octanu etylu rozpuszczalna
Frakcja octanu etylu nierozpuszczalna | >100,0
67,3
73,1
53,1
89,6 | >100,0
62,4
100,0
50,7
84,6 |
Ci sami autorzy (7) przebadali ekstrakty metanolowe, otrzymywane podobnie jak opisano powyżej, pochodzące z Brazylii, Peru, Chin i Holandii (tab. 3). Badania wykazały, że ekstrakty metanolowe z Chin i Holandii odznaczały się stosunkowo silnym działaniem cytotoksycznym wobec badanych hodowli komórek nowotworowych (ED50 = 3,5 i 3,9 μg/ml) w porównaniu do ekstraktów propolisowych pochodzących z Brazylii i Peru (ED50 = 12,5 i 65,5 μg/ml).
Tabela 3. Działanie cytotoksyczne ekstraktów metanolowych z propolisu pochodzących z różnych rejonów geograficznych na hodowle komórkowe nowotworów (7).
| Pochodzenie ekstraktów metanolowych z propolisu |
Liczba prób |
Hodowle komórkowe nowotworów (ED50) |
| HT-1080 (μg/ml) |
L5-26 (μg/ml) |
Brazylia
Peru
Chiny
Holandia | 6
1
1
1 | 14-3-56,4
51,1
3,9
3,5 | 12,5-65,5
76,4
N
N |
| N – Nie badano |
Kimoto i wsp. (8) wywoływali nowotwory nerek u myszy za pomocą nitrylotrioctanu żelazowego i leczyli je równocześnie za pomocą ekstraktu etanolowego z propolisu brazylijskiego. Zwierzęta otrzymywały dootrzewnowo wymieniony karcynogen w ilości 10 mg/dzień 2 razy w tygodniu przez 8 tygodni. Równocześnie otrzymywały one ekstrakt etanolowy z propolisu brazylijskiego w postaci 1% roztworu etanolowego dodawanego do wody do picia przez 5 tygodni. Zwierzęta kontrolne otrzymywały do picia 1% wodny roztwór etanolu. Zwierzęta, które przeżyły warunki doświadczenia, uśmiercano po roku od ostatniego podania roztworu propolisu i ich nerki badano histopatologicznie. Wyniki badań zamieszczone w tabeli 4 wskazują na wyraźne ochronne działanie ekstraktu propolisowego, zabezpieczające przed rozwojem nowotworu nerek. U zwierząt tych obserwowano co prawda powstawanie łagodnych torbieli, ale w żadnym przypadku nie przeistaczały się one w torbiele o charakterze przedrakowym, a następnie w formy nowotworowe, jak to miało miejsce u części zwierząt grupy nieleczonej.
Tabela 4. Działanie ochronne ekstraktu etanolowego z propolisu brazylijskiego przed rozwojem nowotworu nerek u myszy (8).
| Podawane substancje |
Liczba zwierząt |
Rozwój nowotworu nerek |
| poddanych badaniu |
przeżywających |
torbiel łagodna |
torbiel przedrakowa |
nowotwór nerek |
Etanol 1% (kontrola)
Ekstrakt etanolowy z propolisu – 1% roztwór etanolowy | 12
12 | 8
9 | 5
9 | 3
0 | 4
0 |
Badania kontynuowano z wywoływaniem nowotworu płuc u myszy za pomocą nitrylotrioctanu żelazowego i leczeniem zwierząt ekstraktem propolisu brazylijskiego (9). Wyniki badań zebrane w tabeli 5 dowodzą, że i w tym przypadku 1% roztwór etanolowy tego ekstraktu dodawany do wody do picia zwierzętom doświadczalnym w pełni zabezpieczał je przed powstaniem gruczolakoraka płuc w 50% przypadków.
Tabela 5. Działanie ochronne ekstraktu etanolowego z propolisu brazylijskiego przed rozwojem nowotworu płuc u myszy (9).
| Podawane substancje |
Liczba zwierząt |
Rozwój nowotworu płuc |
| poddanych badaniu | przeżywających |
gruczolak |
gruczolakorak |
Etanol 1% (kontrola)
Ekstrakt etanolowy z propolisu – 1% roztwór etanolowy | 12
12 | 8
9 | 1
1 | 4
0 |
Ekstrakt wodny z propolisu izraelskiego odznaczał się zdolnością hamowania przemiany komórek nowotworu NIH/3T3 w formę złośliwą pod wpływem wirusa raka mysiego Moloney MuSV-124 (10). Ekstrakt propolisowy działał najbardziej skutecznie, jeśli podawano go zwierzętom na 2 godz. przed zakażeniem wirusem lub w trakcie zakażania. Kiedy leczenie ekstraktem propolisowym kontynuowano przez 5-10 dni po zakażeniu, przemiana komórek nowotworowych w formę złośliwą cofała się całkowicie, a wirus MuSV-124 stawał się niechorobotwórczy. Przeprowadzone badania wskazują, że ekstrakt wodny z propolisu izraelskiego hamuje późniejszy stopień zakażenia wirusem, kiedy przenika on do genomu gospodarza. Świadczy o tym fakt, że ekstrakt propolisowy podany zwierzętom po zakażeniu ich wirusem także wyraźnie hamuje przemianę komórek nowotworu w formę złośliwą.
Z kolei Borelli i wsp. (11) oraz Bazo i wsp. (12) próbowali leczyć za pomocą ekstraktów etanolowych z propolisu nadżerki okrężnicy u szczurów o charakterze nowotworowym wywołane za pomocą substancji karcynogennych, takich jak azoksymetan i 1,2-dimetylohydrazyna. W pierwszym przypadku podawanie ekstraktu etanolowego w ilości 500 mg/kg m.c. drogą pokarmową nie przyniosło żadnych rezultatów, natomiast w drugim przypadku podawanie ekstraktu etanolowego z propolisu w ilości 30 mg/kg m.c. drogą jelitową obniżało zaledwie powstawanie nadżerek okrężnicy o ok. 8% w porównaniu do kontroli.
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
24 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
59 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
119 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 28 zł
Piśmiennictwo
1. Derevici A, Popescu A. Azione in vitro del propolis sulle cellule del tumore ascitico di Ehrlich. Riv Vet 1966; 15:175-182; wg Apicult Abstr 471/71. 2. Valaviczju JM, Neszukajtene KS, Valaviezene JV i wsp. Etude experimentale de l’action des preparations provenant des abeilles sur l’organism de rats porteurs de tumeurs. Liet. T.S.R. Mokslu Akad Darb CSSSR 1975; 3:105-10; wg BS 1976; 37:2995. 3. Hładoń B, Bylka W, Ellnain-Wojtaszek M i wsp. In vitro studies on the cytostatic activity of propolis extracts. Arzneim Forsch 1980; 30:1847-8. 4. Ban J, Popovic S, Maysinger D. Cytostatic effects of propolis in vitro. Acta Pharm Jugosl 1983; 33:254-5. 5. Bašić I, Čuvić S, Tadić Z i wsp. Antimetastase-Wirkung von Bienengift und wasserlőslichen Propolisderivaten bei Mäusen. Apimondia XXXIV Internationaler Bienenzűchterkongress, Lousanne 1995; 137-8. 6. Banskota AH, Tezuka Y, Prasain JK i wsp. Chemical constituents of Brazilian propolis and their cytotoxic activities. J Nat Prod 1998; 61:896-900. 7. Banskota AH, Tezuka Y, Adnyana IK i wsp. Cytotoxic, hepatoprotective and free radical scavenging effects of propolis from Brazil, Peru, the Netherland and China. J Ethnopharmacol 2000; 72:239-46. 8. Kimoto T, Koya S, Hino K i wsp. Renal carcinogenesis induced by ferric nitrilotriacetate in mice, and protection from it by Brazilian propolis and artepillin C. Pathol Int 2000; 50:679-89. 9. Kimoto T, Koya-Miyata S, Hino K i wsp. Pulmonary carcinogenesis induced by ferric nitrilotriacetate in mice, and protection from it by Brazilian propolis and artepillin C. Virchovs Arch 2001; 438:259-70. 10. Huleihel M, Ishano V. Effect of propolis extract on malignant cell transformation by Moloney murine sarcoma virus. Arch Virol 2001; 146:1517-26. 11. Borelli F, Izzo AA, di Carlo G i wsp. Effect of a propolis extract and caffeic acid phenethyl ester on formation of aberrant crypt foci and tumors in the rat colon. Fitoterapia 2002; 73 (Supp 1):S38-43. 12. Bazo AP, Marchesan-Rodrigues MA, Sforcin JM i wsp. Protective action of propolis on the rat colon carcinogenesis. Teratogen Carcinog Mutagen 2002; 22:183-94. 13. Banscota AH, Nagaoka T, Sumioka LY i wsp. Antiproliferative activity of the Netherlands propolis and its active principles in cancer cell lines. J Ethnopharmacol 2002; 80:67-73. 14. Oršolić N, Bašić I. Immunomodulation by water-soluble derivative of propolis; a factor of antitumor reactivity. J Ethnopharmacol 2003; 84:265-73. 15. Aso K, Kanno S-I, Tadano T i wsp. Inhibitory effect of propolis on the growth of human leukemia U937. Biol Pharm Bull 2004; 27:727-30. 16. Alencar SM, Oldoni TLC, Castro ML i wsp. Chemical composition and biological activity of a new type of Brazilian propolis: red propolis. J Ethnopharmacol 2007; 113:278-83. 17. B?falo MC, Candeias JM, Sforcin JM. In vitro cytotoxic effect of Brazilian green propolis on human laryngeal epidermoid carcinoma (HEp-2) cells. Evid-Bas Compl Alter Med 2009; 6:483-7. 18. Inoue K, Saito M, Kanai i wsp. Anti-tumor effects of water-soluble propolis on a mouse sarcoma cell line in vitro. Am J Chin Med 2008; 36:625-34. 19. Szliszka E, Czuba ZP, Domino M i wsp. Ethanolic extract of propolis (EEP) enhances the apoptosis-inducing potential TRAIL In cancer cells. Molecules 2009; 14:738-54. 20. Li F, Awale S, Zhang T i wsp. Chemical constituents of propolis from Myanmar and their preferential cytotoxicity against a human pancreatic cancer cell line. J Nat Prod 2009; 72:1283-7. 21. Vatansever HS, Sorkun K, Delilo?lu SI i wsp. Propolis from Turkey induces apoptosis through activating caspases in human breast carcinoma cell lines. Acta Histochim 2010; 112:546-56. 22. Chen C-N, Weng M-S, Wu C-L i wsp. Comparison of radical scavenging activity, cytotoxic effects and apoptosis induction in human melanoma cells by Taiwanese propolis from different sources. Evid-Bas Compl Alter Med 2004; 1:175-85. 23. Ishihara M, Naoi K, Nashita M i wsp. Growth inhibitory activity of ethanol extracts of Chinese and Brazilian propolis in four human colon carcinoma cell lines. Oncology Reports 2009; 22:249-54. 24. Eom HS, Lee EJ, Yoon BS i wsp. Propolis inhibits the proliferation of human leukemia HL-60 cells by inducing apoptosis through the mitochondrial pathway. Nat Prod Res 2010; 24:375-86.

