© Borgis - Medycyna Rodzinna 1/2012, s. 15-20
*Paweł Kowalczyk1, Dorota Dziuban2, Katarzyna Hulka3, Robert Sot1, Maciej Filocha1
Zastosowanie nowych innowacyjnych leków w leczeniu raka piersi
The application of new innovative drugs in breast cancer
1Interdyscyplinarne Centrum Modelowania Matematycznego i Komputerowego Uniwersytetu Warszawskiego
Dyrektor Centrum: prof. dr hab. Marek Niezgódka
2Zakład Biologii Molekularnej, Instytut Biochemii i Biofizyki Polskiej Akademii Nauk w Warszawie
Dyrektor Instytutu: prof. dr hab. Piotr Zielenkiewicz
3Wydział Biologii Uniwersytetu Warszawskiego
Dziekan Wydziału: prof. dr hab. Joanna Pijanowska
Summary
Treatment of breast cancer is a multistep process and requires assessment of the clinical staging of cancer. Depending on his selection is in the original investigation – operational, pre-operative treatment or palliative treatment. After any operation is evaluated pathological tumor stage, histological type of cancer and the occurrence of clinically important receptors – estrogen, progesterone (PgR), overexpression of the receptor for epidermal growth factor (HER2). The purpose of the original investigation and adjuvant therapy is complete remission (cure), or the total elimination of tumor foci. The effectiveness of treatment for breast cancer is increasing. Evidenced by the decline in mortality while increasing morbidity. We owe this new medication treatment strategies. Patients who reported at 0 degrees and I have more than 90% chance of durable remission (cure) in stage II 70% in the third about 40%. Not infrequently, manages to achieve long-term survival in patients with generalized malignancy. Using modern medicine acting on a specific cancer cells lead to targeted therapies. In the adjuvant used in the moment trastuzumab – a monoclonal antibody specifically binding to the receptor for epidermal growth factor (HER2), causing its inactivation. It is effective only in patients whose cancer cells show increased expression of HER2. It is given intravenously – either alone or in combination with chemotherapy. Lapatinib works more effectively. It is a drug with a relatively small molecule, and inactivating the receptor HER2. Another point handle targeted therapy may be vascular endothelial growth factor (VEGF). Bevacizumab is a drug blocking the activity of this factor. By this inhibits the formation of new blood vessels (angiogenesis) in tumors and attendant activation of a cascade of growth factors. Targeted therapies are very promising. They can be used concurrently with chemotherapy, hormone therapy and radiotherapy increasing their activity. Have few adverse reactions and side effects. Their only drawback is their terrific prices.

Wstęp
Choroba nie wybiera. To powszechnie znane stwierdzenie idealnie pasuje do chorób nowotworowych. Wiek, płeć, wykształcenie czy status społeczny nie odgrywają dla nich żadnej roli. Rak dotyka zarówno ludzi „anonimowych”, jak i tych znanych nam z gazet ze świata show-biznesu, nauki, polityki.
Na świecie co roku odnotowuje się 15-17 milionów przypadków raka (1). W Polsce nowotwory złośliwe piersi są najczęstszą przyczyną zgonu wśród kobiet w wieku poniżej 55 roku życia. Średnio na nowotwór złośliwy piersi zapada jedna na 12 Polek. Co roku rejestruje się niemal 11-15 tys. nowych zachorowań i liczba ta stale rośnie (2).
Co ważne, a o czym mówi się niewiele, około 1% zdiagnozowanych chorych na raka piersi to mężczyźni (2). Choć mają oni o wiele mniej tkanki sutków niż kobiety, może się w nich rozwinąć nowotwór. Niestety niska świadomość ryzyka zachorowania na raka piersi powoduje, że nowotwory u mężczyzn wykrywane są w zaawansowanym stanie choroby, co utrudnia leczenie.
Objawy raka piersi
Nowotwory nie pojawiają się spontanicznie. Są one chorobami, które rozwijają się długofalowo, do pewnego momentu wręcz niezauważalnie. Pierwszym symptomem raka piersi jest ból, obrzęk i tkliwość piersi. Kolejnym etapem (w różnej kolejności) jest spostrzeżenie przez chorego małego guzka w sutku. Najbardziej podejrzane są guzki występujące pojedynczo. Guzki mnogie mają charakter torbielowy lub są przejawem innych procesów degeneracyjnych. Do innych objawów należą także: podejrzana zmiana wyglądu lub kształtu piersi w zaawansowanym stadium choroby dochodzące do deformacji piersi (ryc. 1 A, B), ciemniejsza wydzielina lub krwawienie z brodawki, pomarszczona skóra nad guzem, sterczenie lub wciągnięcie brodawki, wysypka na brodawce sutkowej albo wokół niej, zmiany w kształcie sutka (nieregularność lub wklęsłość), zaczerwienienie i stwardnienie skóry, poszerzenie żył skóry piersi. U mężczyzn rzadko występuje ból w okolicach piersiowych. Pierwszymi widocznymi objawami rozwoju nowotworu są zmiany wielkości, kształtu oraz koloru piersi. Poza tym mogą pojawić się również owrzodzenie sutków oraz ropna lub krwawa wydzielina (ryc. 1 A, B).
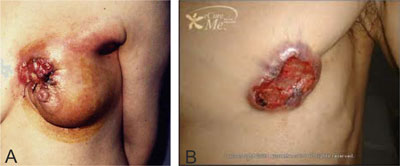
Ryc. 1. A. Rak piersi u kobiet, zaawansowane stadium choroby (źródło: http://shirleymedical.com/). B. Rak piersi u mężczyzn (źródło: http://shirleymedical.com/).
Możliwości terapeutyczne
Rak to nie wyrok. W dzisiejszym świecie, dynamiczny rozwój zaawansowanych technologii pozwala na stworzenie szczepionek i leków na raka, które powstają w wielu laboratoriach firm farmaceutycznych. Są one wynikiem nowego innowacyjnego podejścia do badań mających na celu odkrywanie nowych mechanizmów tworzenia się nowotworów i ich unieczynniania już na etapie dysplazji. Innowacyjne technologie obejmują m.in.:
– wytworzenie leków wpływających na przemiany metaboliczne komórek nowotworowych poprzez pozbawianie ich energii pochodzącej z glukozy;
– opracowanie leków pierwszego wyboru (podawane są one pacjentom w pierwszej kolejności, przed zastosowaniem jakichkolwiek innych metod leczenia). Leki te mają za zadanie zidentyfikować określone komórki nowotworowe i zniszczyć je, a następnie pobudzić do działania układ odpornościowy pacjenta, aby sam pokonał pozostałe komórki nowotworowe już w fazie dysplazji (ryc. 2);
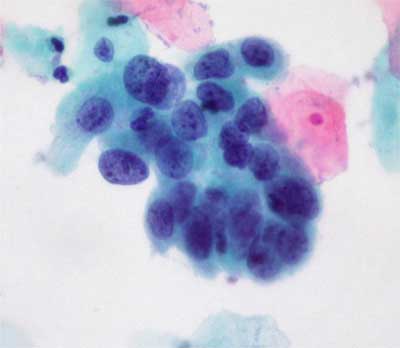
Ryc. 2. Dysplazja, czyli zmiana przedrakowa, to stadium między rozrostem a nowotworem, zmiany zachodzą w obrębie tkanek.
– nowe terapie badawcze wykorzystujące dziedziny nauki, takie jak: nanotechnologię, która ułatwia przyswajanie leku przez pacjenta, co pozwala na pokonanie ograniczeń związanych z istniejącymi tradycyjnymi metodami leczenia.
Potencjalni „pomocnicy”
Zaangażowanie potentatów farmaceutycznych, takich jak GlaxoSmithKline czy Roche oraz prowadzone przez nie prace badawcze przyniosły już znaczący postęp w walce z rakiem. Doprowadziło to do znacznego ograniczenia liczby zgonów spowodowanych przez choroby nowotworowe w ostatnich latach. Statystyki medyczne pokazują, że od 1993 do 2010 roku liczba śmiertelnych przypadków wśród chorych na nowotwory spadła około 30%. Średnio co roku umieralność na raka zmniejsza się o 2,3%. Pomimo to nowotwory, w tym rak piersi, pozostają nadal jedną z najczęstszych przyczyn zgonów kobiet w Europie.
W br. Komisja Europejska wydała warunkowe pozwolenie we wszystkich 27 państwach członkowskich Unii Europejskiej na dopuszczenie do obrotu dla preparatu Tyverb® (lapatynib), produkowanego przez firmę GlaxoSmithKline – jedną z najważniejszych firm branży farmaceutycznej i opieki zdrowotnej na świecie, prowadzącej badania mające na celu poprawę jakości życia ludzkiego, pozwalając ludziom robić więcej, czuć się lepiej i żyć dłużej. Firma GSK tworzy innowacyjne leki w leczeniu nowotworów, które odmienią życie pacjentów. Prowadzone przez nią prace badawcze na całym świecie obejmują współpracę z ponad 160 ośrodkami badania nowotworów. Firma GSK walczy z chorobą nowotworową przy pomocy nowoczesnych metod leczenia nowotworów, zapobiegania im, leczenia wspomagającego, chemioterapii oraz leczenia celowanego. Od dawna znana jest jego hormonowrażliwość i możliwość ingerencji w gospodarkę hormonalną pacjentek zmieniającej przebieg choroby. Ocena ekspresji receptorów estrogenowych i progesteronowych stanowi nieodłączny element standardowego badania histopatologicznego wchodzącego w skład postępowania diagnostycznego w przypadku raka piersi (3).
Lapatynib
Lek lapatynib cechuje się nowatorskim mechanizmem działania, który różni się od działania dostępnych już na rynku terapii celowanych, stosowanych w leczeniu pacjentek z zaawansowanym progresywnym (po wcześniejszej terapii z użyciem antracyklin i taksonów) lub przerzutowym rakiem piersi (po terapii trastuzumabem), u których występuje nadekspresja ErbB2 (HER2). Jest to pierwszy doustny, podwójnie celowany lek drobnocząsteczkowy, który w kombinacji z kapecytabiną przedostaje się do wnętrza komórki nowotworowej i hamuje dwa białka receptorowe – komponenty receptorów ErbB1 i ErbB2 o aktywności kinazy tyrozynowej. Sygnały wysyłane przez te receptory są odpowiedzialne za wzrost i proliferację guza oraz procesy naprawcze w komórkach ludzkich. Sama kapecytabina jest lekiem skutecznym, mało toksycznym i wygodnym w użyciu. Kapecytabina (nazwa handlowa Xeloda) w komórkach organizmu przekształca się w 5-FU (popularny cytostatyk). Ostatni etap przemiany w 5-FU (5-fluorouracil) odbywa się przy współudziale enzymu, który w wysokim stężeniu występuje w komórkach nowotworowych. I to właśnie tłumaczy wybiórczą aktywację substancji czynnej w komórkach guza i niewielką ekspozycję zdrowych tkanek na toksyczne działanie 5-FU.
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
29 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
69 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
129 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 78 zł
Piśmiennictwo
1. Statistical Yearbook of the Republic of Poland 2010. 2. Pharmindex – internetowy spis leków (pol.). UMB Medica Polska 2010. 3. Bange J, Zwick E, Ullrich A: Molecular targets for breast cancer therapy and prevention. Nature Medicine 2001; 7 (5), 548-552. 4. Kroep JR, Linn SC, Boven E et al.: Lapatinib: clinical benefit in patients with HER2-positive advanced breast cancer. Neth J Med 2010; 68 (9), 371-6. 5. Dębska S, Podemski P: Współczesna Onkologia. Termedia Wydawnictwa Medyczne, Poznań 2010; 14, 347-354. 6. Albanell J, Codony J, Rovira A et al.: Mechanism of action of anti-HER2 monoclonal antibodies: scientific update on trastuzumab and 2C4. Advances in Experimental Medicine and Biology 2003; 532, 253-268. 7. Wolff AC, Hammond ME: American Society of Clinical Oncology/College of American Pathologists guideline recommendations for human epidermal growth factor receptor 2 testing in breast cancer. J Clin Oncol 2007; 1 (25), 118-45. 8. Papouchado BG, Myles J: Silver in situ hybridization (SISH) for determination of HER2 gene status in breast carcinoma: comparison with FISH and assessment of interobserver reproducibility. Am J Surg Pathol 2010; 6 (34), 767-76. 9. García-Caballero T, Grabau D: Determination of HER2 amplification in primary breast cancer using dual-colour chromogenic in situ hybridization is comparable to fluorescence in situ hybridization: a European multicentre study involving 168 specimens. Histopathology 2010; 4 (56), 472-80. 10. Romond EH, Perez EA, Bryant J et al.: Trastuzumab plus adjuvant chemotherapy for operable HER2-positive breast cancer. New England Journal of Medicine 2005; 353 (16), 1673-1684. 11. Hudis CA: Trastuzumab – mechanism of action and use in clinical practice. N Engl J Med 2007; 357 (1), 39-51. 12. Piccart-Gebhart MJ, Procter M, Leyland-Jones B et al.: Trastuzumab after adjuvant chemotherapy in HER2-positive breast cancer. New England Journal of Medicine 2005; 353 (16), 1659-1672. 13. Meza-Junco J, Au HJ: Trastuzumab for gastric cancer. Expert Opin Biol Ther 2009; 12 (9), 1543-51. 14. Littlejohns P: Trastuzumab for early breast cancer: evolution or revolution? Lancet Oncology 2006; 7 (1), 22-3. 15. de Bono, Johann S, Bellmunt J et al.: Open-Label Phase II Study Evaluating the Efficacy and Safety of Two Doses of Pertuzumab in Castrate Chemotherapy-Naive Patients With Hormone-Refractory Prostate Cancer. Journal of Clinical Oncology 2007; 25 (3): 257-262. 16. Di Costanzo F, Mazzoni F, Micol M et al.: Bevacizumab in non-small cell lung cancer. Drugs 2008; 68 (6), 737-46. 17. Jinwoong K, Young MCh, Ki-Pung Y: Supercritical fluid extraction of alkaloids. [In:] Pelletier S William (red.): Alkaloids: chemical and biological perspectives. Vol. 15 S. 2011. 18. Gu L, Kelm M, Prior RL: Concentration of proanthocyanidins in common foods and estimation of normal consumpion. J Nutr 2004; 134, 3. 19. Foo LY, Lu Y: Isolation and identification of procyanidins in apple pomace. Food Chem 1999; 64, 511-518. 20. Andrew T, Chan MD, JoAnn MPH : Long-term Aspirin Use and Mortality in Women. Arch Intern Med 2007; 167 (6) 562-572. 21. Charles L, Campbell MD: Aspirin Dose for the Prevention of Cardiovascular Disease. JAMA 2007; 297 (18), 2018-2024. 22. Schlager N, Weisblatt J, Newton DE: Chemical Compounds. Thomson Gale 2006; 31-35.


