© Borgis - Postępy Fitoterapii 2/2012, s. 79-92
*Agnieszka Gryszczyńska1, Bogna Gryszczyńska2, Bogna Opala1, Zdzisław Łowicki1
Zastosowanie roślin leczniczych w menopauzie. Cz. I.
The use of medicinal plants in the menopause. Part I
1Instytut Włókien Naturalnych i Roślin Zielarskich w Poznaniu
Dyrektor Instytutu: prof. dr hab. Grzegorz Spychalski
2Zakład Chemii Ogólnej, Katedra Chemii i Biochemii Klinicznej, Uniwersytet Medyczny w Poznaniu
Kierownik Zakładu: dr hab. Maria Iskra prof. UM
Summary
A menopause usually affects women about 50 years old. The main reason for the formation of menopause is the lack of estrogen in the blood. An estrogen, in addition to the direct effect on the women menstrual cycle, is responsible for causing sever bone disease. It is the lack of estrogen is essential to the onset of menopausal women with osteoporosis. From several years, an hormone replace therapy are used an estrogen and/or progesterone to prevent certain diseases. Unfortunately, prolonged use of hormones adversely affects the health of women. Those hormones cause cancer including breast, endometrium, ovaries, blood clots and other serious diseases. Therefore of interest or researchers is to find a safe for the health of the medicinal product.

Wstęp
Stosowane od wieków rośliny lecznicze znalazły zastosowanie w różnych dziedzinach medycyny. Zioła wykorzystywane są zarówno w profilaktyce, jak również w leczeniu licznych chorób. Są one składnikami leków roślinnych i suplementów diety. Największy wzrost stosowania różnego rodzaju produktów medycyny tradycyjnej w krajach rozwiniętych zanotowano w Stanach Zjednoczonych. Prowadzone od lat badania rynku farmaceutycznego wskazują, że głównymi odbiorcami tego typu preparatów są kobiety (1). 80% kobiet w wieku 45-60 lat stosuje roślinne produkty lecznicze sprzedawane bez recepty w zwalczaniu symptomów menopauzy (2). Inicjatywa Zdrowia Kobiet (WHI) donosi również, że stosowanie tradycyjnych preparatów wypiera z rynku hormonalną terapię zastępczą (1). Przykładem krajów, w których medycyna alternatywna stosowana jest przez 22% kobiet są kraje północno-zachodniego Pacyfiku, w których od lat roślinne produkty wykorzystywane są w walce z objawami menopauzy (3). Dlatego też, w niniejszym opracowaniu, przedstawione zostaną rośliny, które wykorzystuje się w leczeniu chorób kobiecych, a w szczególności łagodzenia objawów menopauzy.
Do tej grupy roślin zaliczyć można: soję (Glycine Willd), pluskwicę groniastą (Cimicifuga racemosa), ostropest plamisty (Silybum marianum), niepokalanek pospolity (Vitex agnus-castus L.), chmiel zwyczajny (Humulus lupulus), koniczynę łąkową (Trifolium pratense L.), serdecznik pospolity (Leonurus cardiaca L.), wiesiołek dwuletni (Oenothera biennis L.), jak również rośliny charakterystyczne dla wschodnich i plemiennych tradycji ludowych tj. masha hari (Justicia pectoralis var. stenophylla).
Menopauza
Menopauza jest naturalnym następstwem zanikania pęcherzyków jajnikowych oraz syntezy estrogenów. Pierwsze objawy menopauzy dotykają kobiety po 50. roku życia. Na zachodzie średnio kobiety w wieku 53 lat przestają miesiączkować (4), a na przykład na Kostaryce – średnio w 50,6 roku (5). Początkowym symptomem menopauzy jest zmniejszenie aktywności jajników, co skutkuje nieregularną miesiączką, w konsekwencji prowadząc do jej ustania. Następstwem tego stanu jest ustanie zdolności rozrodczych kobiety (5). Do wczesnych objawów menopauzy zaliczyć można również wybuchy gorąca, suchość pochwy, nadmierną potliwość (6, 7). Objawy ze strony układu moczowo-płciowego są dość powszechne, cierpi na nie około 60-80% kobiet, a czas trwania i ich nasilanie może być długotrwałe (7). Dane statystyczne z Meksyku mówią, że 31-50% postmenopauzalnych kobiet ma objawy uderzenia gorąca i nocnego pocenia się (8).
Zaprzestanie miesiączkowania skutkuje obniżeniem stężenia progesteronu we krwi. Jedynym źródłem progesteronu w organizmie, uzyskanym na drodze aromatyzacji andostrenoidu, jest estron. Niestety, zawartość estronu we krwi jest zbyt niska, by skutecznie zahamować uwalnianie hormonów glikoproteinowych (gonadotropin) przez przysadkę mózgową. Do nich zalicza się hormon folikulotropowy (FSH) oraz hormon luteinizujący (LH). Wysokie stężenie tych dwóch hormonów we krwi charakteryzuje początkowy okres postmenopauzalny. Z okresem tym wiążą się dwie główne choroby – osteoporoza oraz zanikanie drugorzędowych cech płciowych (4).
Jedną z częstszych dolegliwości postmenopauzalnych kobiet jest ból pochwy, często wywoływany przez wzrastającą częstotliwość infekcji. Infekcje są wynikiem zmniejszającego się zakwaszenia środowiska spowodowanego przez brak estrogenu, w konsekwencji przyczyniając się do spadku aktywności seksualnej kobiet (9).
Naczynioruchowe wyrzuty gorąca u kobiet z menopauzą lub po owariektomii są wywoływane przez niski poziom estrogenu. Brak estrogenu zaburza mechanizm utraty ciepła poprzez podwyższenie perfuzji obwodowej oraz obniżenie temperatury ciała. Bezpośrednio przed wybuchem gorąca przewodnictwo cieplne skóry wzrasta, przepływ krwi oraz częstotliwość uderzeń serca przyspiesza, zwiększa się również poziom LH w surowicy, co w konsekwencji zwiększa potliwość. Po upływie 3-6 minut po wyrzucie gorąca obserwuje się podwyższone stężenie epinefryny (10).
Objawy te, jak również ich częstotliwość, zależne są od środowiska (miejsca zamieszkania), stanu zdrowia oraz uwarunkowania kulturowego w światopoglądzie zdrowia kobiety. Liczne badania prowadzone nad kobietami z menopauzą pochodzącymi z Ameryki Łacińskiej, w szczególności z Meksyku, sugerują że charakteryzują się one bardziej pozytywnym nastawieniem psychicznym niż kobiety w USA czy w Europie. Kobiety z plemienia Majów (n=78) z Jukatanu, pomimo wysokiego poziomu hormonów folikutropowego oraz luteinizującego we krwi porównywalnego z Amerykankami, nie miały zaburzeń naczynioruchowych powiązanych ze zmianami hormonalnymi. Inne badania (n=107) nad plemiennymi mieszkankami Jukatanu nie wykazały symptomatologicznego związku z menopauzą w przeciwieństwie do zaprzestania miesiączkowania. W obydwu przypadkach podanych wyżej, u latynoskich pacjentek zaobserwowano niższe ryzyko złamań kości niż u Amerykanek, które nie chorowały na osteoporozę. Pierwsze opublikowane badania nad menopauzą przeprowadzone na Gwatemalkach z plemion zamieszkujących Quiché, Tzutujili oraz na Majach sięgają 2003 roku. Eksperyment wykazał, że Gwatemalki, podobnie jak Meksykanki, wykazują bardziej pozytywne nastawienie do pojawiającej się u nich menopauzy. W przeciwieństwie do kobiet z plemienia Majów z Meksyku, gwatemalskie kobiety doświadczały takich samych objawów menopauzy, co Amerykanki, tj. wyrzuty gorąca, nocne pocenie się, zły humor oraz nieregularne miesiączki, jak również miały problemy z osteoporozą w okresie postmenopauzalnym (8).
Medycyna konwencjonalna stosuje w takich przypadkach hormonalną terapię zastępczą (HRT), w której wykorzystuje się estrogen lub/i progesteron (5, 8, 11). Estrogen jako HRT stosowany jest od ponad 30 lat, natomiast połączenie go z progesteronem od ponad 20 lat. Z wieloletnich badań nad HRT wynika, że terapia ta zmniejsza śmiertelność spowodowaną przez choroby sercowo-naczyniowe o ok. 35%, zmniejsza ryzyko wystąpienia osteoporozy o ok. 50% oraz zmniejsza występowanie innych symptomów menopauzy. Mniejsze badania pokazują również, że ma ona wpływ na zmniejszenie utraty pamięci, chorobę Alzheimera, utratę zębów i raka jelita grubego (12). Estrogen reguluje ekspresję genów poprzez wiązanie wewnątrzkomórkowych receptorów estrogenowych (ER), które odpowiadają za wzrost, różnicowanie oraz funkcjonowanie wielu komórek. Kiedy estrogen wiązany jest przez ER, następuje dimeryzacja receptora poprzez przyłączenie do receptora estrogenozależnego w DNA cząsteczki estrogenu, w konsekwencji czego powstaje kompleks ER-ERE. Kompleks ten odpowiada za modulację transkrypcji regulowanych przez estrogen genów, tj. receptora progesteronowego (PR) i preseneliny-2 (pS2) oraz pobudza wzrost i różnicowanie komórek. Różnice pomiędzy dwoma typami ERα i ERβ to podział komórek i specyfikacje ligandów. W środkowej fazie ciąży receptor ERα jest najbardziej rozpowszechniony w komórkach macicy płodu, w dużo mniejszym stopniu występuje w komórkach jajników, jąder, skórze i jelitach. Natomiast ERβ mRNA występuje w największej ilości w komórkach płodu w jajnikach, jądrach, nadnerczach i śledzionie (13).
Stosowanie HRT przynosi wyraźną ulgę naczynioruchową, zapobiega atrofii pochwy, zapobiega utracie gęstości kości (BMD) zmniejszając ryzyko złamań, w tym klinicznych złamań kręgów i kości udowej. Kobietom, którym nie usunięto macicy, podaje się najczęściej kombinację estrogenu i progesteronu, w celu zapobieżenia rozrostowi błony śluzowej macicy i rakowi endometrium (5). Według badań Inicjatywy Zdrowia Kobiet (WHI) u pacjentek przyjmujących estrogen i progesteron dłużej niż pięć lat, zwiększa się ryzyko wystąpienia raka: sutka, endometrium, jajników, zakrzepicy, czy chorób pęcherzyka żółciowego (5, 9, 14). Można również znaleźć informacje, że hormonalna terapia zastępcza powoduje chorobę niedokrwienną serca i udar mózgu u starszych kobiet. Jedynie krótkie stosowanie HRT jest w miarę bezpieczne (7). Narodowy Amerykański Instytut Zdrowia zakazał nawet prowadzenia badań klinicznych stosujących HRT u zdrowych postmenopauzalnych kobiet, ze względu na poważne powikłania, które wywołuje jej stosowanie (rak piersi, choroby układu krążenia, złamania szyjki kości udowej, rak jelita grubego) (11). Wyniki badań dotyczących syntetycznych hormonów żeńskich prowadzonych na zlecenie WHI mówią, że przyjmowanie przez kobiety syntetycznego estrogenu i progesteronu ma dużo bardziej szkodliwy wpływ niż stosowane w badaniach placebo. Dane kliniczne wskazują na zwiększenie prawdopodobieństwa wystąpienia chorób układu krążenia (29%), czy raka sutka (26%) (8).
Wiele kobiet ze względu na liczne poważne schorzenia, które są wynikiem stosowania hormonalnej terapii zastępczej, rezygnuje z niej na rzecz środków na bazie surowców roślinnych. Potwierdzają to liczne doniesienia naukowe, m.in. latynoski zamieszkujące USA można zaliczyć do grupy etnicznej, która nie korzysta z tradycyjnej terapii hormonalnej. W jednym z przeprowadzonych eksperymentów jedynie 5 nieoperowanych peri- i postmenopauzalnych kobiet stosowało HRT w grupie 130-osobowej składającej się z Meksykanek oraz Amerykanek (8). Z badań przeprowadzonych w USA wynika, że 29% kobiet w okresie menopauzy przyjmuje HRT, 16% HRT oraz suplementy diety, 32% jedynie suplementy diety, a 13% nie stosuje żadnych środków leczniczych. Rynek roślinnych środków leczniczych w 2002 roku w USA wart był 13,7 mld dolarów. Natomiast ze szwedzkich badań wynika, że jedynie ok. 4% kobiet w okresie menopauzy stosuje roślinne produkty lecznicze (15).
Można również znaleźć wzmianki w literaturze naukowej, że 65-80% kobiet zamieszkujących nieuprzemysłowione kraje, stosuje tradycyjną lub alternatywną medycynę jako część podstawowej, codziennej walki o zdrowie. Światowa Organizacja Zdrowia (WHO) i Pan-Amerykańska Organizacja Zdrowia (PAHO) rozpoczęły globalną inicjatywę, której celem jest zapewnienie bezpieczeństwa stosowania medycyny tradycyjnej, jak również zwiększenie jej dostępności, zachęcając tym samym do jej stosowania na podstawie potwierdzających ich skuteczność wyników licznych badań klinicznych (8). Do roślin, które rekomendowane są w zwalczaniu symptomów menopauzy należą: Caulophyllum thalictroides, pluskwica groniasta, olej z wiesiołka, niepokalanek pospolity i lukrecja (12).
Medycyna alternatywna stosuje w terapii surowce roślinne, które dzięki zawartym w nich związkom z grupy fitoestrogenów, zastępują estrogen. Co prawda terapia ta jest słabsza w porównaniu do konwencjonalnych preparatów, jednakże nie zwiększa prawdopodobieństwa wystąpienia raka piersi czy endometrium (16). Po raz pierwszy aktywność estrogenową fitoestrogenów zaobserwowano w 1926 roku. Ze względu na obecność w ich strukturze pierścienia fenylowego, wykazują one powinowactwo do receptorów estrogenowych, w szczególności ERβ. Ich aktywność jest jednak od 100 do 10 000 razy niższa niż estrogenów (12).
Fitoestrogeny wytwarzane są przez wiele dziko rosnących roślin. Badania z połowy XX wieku wskazują, że fitoestrogeny, w szczególności izoflawony, mają korzystny wpływ na bezpłodność zwierząt gospodarskich i gepardów żyjących w niewoli. Od tego czasu poznano ponad 300 roślin, które wykazują działanie estrogenne u zwierząt, dlatego naukowcy zaczęli prowadzić poszukiwania, mające na celu identyfikację tych związków w spożywanych zarówno przez ludzi, jak i zwierzęta produktach spożywczych. Fitoestrogeny obecne są w owocach i warzywach, jednak najbardziej rozpowszechnione są w roślinach strączkowych (17).
Do grupy związków, które mają działanie estrogenne zaliczyć można izoflawony (jest ich ponad 1000), kumestany (kumestrol), lignany oraz dihydroksychalkony. Do grupy wykazującej najwyższą aktywność zalicza się izoflawony (biochanina A, genisteina, daidzeina, formononetyna), związki charakterystyczne dla soi oraz koniczyny czerwonej (18). Oprócz izoflawonów za aktywność estrogenową mogą również odpowiadać takie flawonoidy, jak kwercetyna, kemferol czy kumestrol, które są aktywnymi związkami obecnymi w licznych nasionach i kiełkach roślin strączkowych. Natomiast siemię lniane bogate jest w lignany, tj. sekoizolarycirezynol i matairezynol (17).
W tabeli 1 przedstawione zostały typowe rośliny wykorzystywane w zwalczaniu symptomów menopauzy. Zawiera ona również informacje dotyczące pojawiających się skutków ubocznych oraz interakcji z innymi lekami.
Tabela 1. Zestawienie tradycyjnie stosowanych surowców roślinnych stosowanych w zwalczaniu symptomów menopauzy (wg 15).
| Nazwa rośliny | Składniki aktywne i sposób działania | Możliwe skutki uboczne i interakcje |
| Pluskwica groniasta (Cimicifuga racemosa) | – glikozydy triterpenowe, roślina standaryzowana jest na zawartość 27-deoksyacteiny
– początkowo sądzono, że roślina działa bezpośrednio na poziom estrogenów
– obecne badania mówią o odmiennym mechanizmie jej działania | – problemy z przewodem pokarmowym, niedociśnienie tętnicze, bóle głowy, zawroty głowy, nudności, reakcje alergiczne
– może reagować ze środkami na nadciśnienie |
| Dziurawiec zwyczajny (Hypericum perforatum) | – hiperycyna i hiperforyna
– łagodzenie depresji, prawdopodobnie aktywność tej rośliny polega na spowalnianiu wychwytu zwrotnego serotoniny, norepinefryny i dopaminy | – najczęściej są to problemy z przewodem pokarmowym, reakcje alergiczne, zmęczenie i niepokój
– w niektórych przypadkach wystąpiła mania oraz podostra toksyczna neuropatia
– możliwe wystąpienie nadwrażliwości na światło u osób z jasną karnacją skóry
– interakcje z inhibitorami wychwytu zwrotnego serotoniny, doustnymi środkami antykoncepcyjnymi, cyklosporynami, warfaryną, lekami przeciwdrgawkowymi, digoksyną, teofiliną, inhibitorami proteazy HIV |
| Koniczyna łąkowa (Trifolium pratense) | – prawdopodobnie izoflawony
– substancje o działaniu estrogennym łagodzące klimakterium | – tkliwość piersi, zmiany w cyklu menstruacyjnym, wzrost masy ciała
– prawdopodobnie mogą wystąpić interakcje z antykoagulantami i hormonami |
| Pieprz metystynowy, kava kava (Piper methysticum) | – kawapyron działający poprzez receptory A kwasu γ-aminomasłowego zakończeń nerwowych
– stymulacja hormonu folikulotropowego
– wykazuje działanie przeciwlękowe | – problemy żołądkowe, niepokój, rozszerzone źrenice, reakcje alergiczne skóry, zapalenie skóry, zapalenie wątroby
– nasilenie wpływu środków na układ nerwowy, tj. alkohol, benzodiazepiny, barbiturany |
| Arcydzięgiel chiński (Angelica sinensis) | – prawdopodobnie wykazuje aktywność estrogenną | – krwawienia, nadwrażliwość na światło
– interakcje z antykoagulantami |
| Łopian większy (Arctium lappa) | – prawdopodobnie wykazuje aktywność estrogenną | – potencjalne interakcje z lekami przeciwcukrzycowymi |
| Lukrecja gładka (Glycyrrhiza glabra) | – zawiera izoflawony i kwas glicyretynowy
– zawarty β-sitosterol prawdopodobnie wykazuje aktywność estrogenną | – niekorzystny wpływ, zgodny z działaniem adrenokortykotropowym |
| Serdecznik pospolity (Leonorus cardiaca) | – zawiera alkaloid leonurynę, która stymuluje aktywność macicy | – interakcje z glikozydami nasercowymi, lekami przeciwnadciśnieniowymi |
| Pochrzyn skrzydlaty (Dioscorea barbasco/Discorea willosa) | – glikozydy steroidowe, saponiny diosgeniny
– mechanizm działania nieznany | – brak poznanych skutków ubocznych i interakcji z innymi lekami |
| Olej z wiesiołka (Oenothera biennis) | – bogaty w kwas γ-linolowy powstały podczas częściowej przemiany do prostaglandyny E1 | – problemy z układem pokarmowym, bóle głowy
– prawdopodobne interakcje z lekami przeciwzapalnymi, kortykosteroidami, β-blokerami, lekami przeciwpsychotycznymi, antykoagulantami, lekami przeciwpadaczkowymi |
| Żeń-szeń (Panax ginseng) | – ginsenozydy (saponiny triterpenowe) podejrzewane są o działanie estrogenne | – bezsenność, biegunka, krwawienie z pochwy, bóle piersi, nabrzmiałe piersi, wzrost libido, epizody maniakalne, prawdopodobnie odpowiada za wywołanie syndromu Stevensa--Johnsona
– interakcje z monoaminowymi oksydazami, inhibitorami, tj. fenelzyna, zwiększa efekt leków hipoglikemizujących |
| Len zwyczajny (Linum usitatissimum) | – podejrzewa się efekt estrogenowy, antyestrogenny i steroidowy | – brak skutków ubocznych
– może mieć negatywny wpływ na wchłanianie innych leków |
| Pelargonia (Pelargonium graveolens) | – podejrzewa się efekt estrogenny | – brak danych |
| Szałwia lekarska (Salvia officinalis) | – zapobiega usuwaniu wody | – potencjalne interakcje z lekami przeciwnadciśnieniowymi i przeciwcukrzycowymi |
Postmenopauzalna osteoporoza
Osteoporoza u kobiet postmenopauzalnych jest najczęstszym powodem wystąpienia metabolicznych chorób kości, takich jak szybkie zmniejszenie zmineralizowania tkanek kostnych, zakłócenie ich struktury beleczkowatej oraz zmiany ich własności krystalicznych. W ich wyniku następuje brak zmineralizowania kości gąbczastej, kości bioder, kręgów i kości dystalnej przedramienia (19).
Za powstanie u kobiet osteoporozy odpowiedzialny jest estrogen (14). Niskie stężenie estrogenu przyczynia się do osłabienia układu kostnego, tj. zaburzenia równowagi pomiędzy resorpcją kości, a ich formowaniem, zmieniając kierunek równowagi w stronę zwiększonej resorpcji kości. W organizmie znajdują się dwa receptory estrogenowe (E2) ERα oraz ERβ. Za efekt przeciwosteoporozowy odpowiada ERα. Receptor E2 pośredniczy w regulowaniu przez estrogen czynnika wzrostu insuliny (IGF-I), transformującego czynnik wzrostu β-1 i osteoprotegeryny (OPG) (14). OPG, rozpuszczalny receptor należący do rodziny czynnika martwicy nowotworu, regulowany jest właśnie przez receptor E2. Główną funkcją OPG jest wiązanie, a tym samym inaktywacja czynnika różnicowania osteoklastów. Tak więc receptor E2 chroni organizm przed wystąpieniem i rozwojem osteoporozy na skutek owariektomii (20).
U postmenopauzalnych kobiet 17β-estradiol oraz sprzężony estrogen wykazują pożądany efekt antyosteoporozowy. Z wcześniejszych wzmianek wynika, że stosowanie zastępczej terapii hormonalnej przyczynia się do zmniejszenia gęstości kości. Z badań wynika, że stosowanie pluskwicy groniastej ma ochronny wpływ na kości, jednak nie jest poznany dokładny mechanizm tego procesu (9).
Poniżej opisane zostały dwa surowce zielarskie: pluskwica groniasta i soja, tradycyjnie wykorzystywane w menopauzie na całym świecie.
Pluskwica groniasta (Cimicifuga racemosa L.)
Pluskwica groniasta (ryc. 1) zwana jest również w Polsce świecznicą groniastą. Roślina ta pochodzi z Ameryki Północnej. Po raz pierwszy zastosowali ją jako surowiec leczniczy północnoamerykańscy Indianie dwa wieki temu (10, 21, 22). Rdzenni Amerykanie stosowali tę roślinę w leczeniu reumatyzmu, epilepsji, niestrawności, dolegliwościach wątroby, bolesnych miesiączkach i bólach porodowych (10, 23). W medycynie niekonwencjonalnej w łagodzeniu bólów miesiączkowych, bólów porodowych, uderzeń gorąca, drażliwości, wahaniu nastroju czy zaburzeniach snu wywołanych przez menopauzę, stosuje się jej korzenie oraz kłącza (22). Europejczycy poznali tę roślinę dopiero w XVII wieku (10). Z powodzeniem wykorzystywana jest od ponad 40 lat w różnego rodzaju ziołowych produktach leczniczych stosowanych w zastępczej terapii hormonalnej (22). W 2005 roku sprzedaż produktów zawierających w swym składzie pluskwicę groniastą osiągnęła w USA wartość 9,7 mln dolarów. W USA stosowana jest od lat 50. XX wieku, a produkty z jej udziałem od 2001 roku są rekomendowane przez American College of Obstetricians and Gynecologists w leczeniu objawów naczynioruchowych wywołanych przez menopauzę (1). Północnoamerykańskie Towarzystwo Menopauzy (NAMS) rekomenduje stosowanie preparatów z pluskwicą groniastą przez kobiety, u których występują łagodne objawy menopauzy (24).

Ryc. 1. Pluskwica groniasta.
Za działanie farmakologiczne tej rośliny odpowiadają liczne cykloartenolowe glikozydy triterpenowe, akteina, 27-deoksyakteina, cimicifugozyd, kwasy organiczne (kwas ferulowy, kwas izoferulowy, kwas kawowy), estry kwasu cynamonowego, alkaloidy (cytyzyna, metylocytyzyna), taniny, a przede wszystkim izoflawony (formononetyna). Substancja (wokół której toczą się spory nad jej obecnością w pluskwicy), która wiąże receptory estrogenowe, to formononetyna (1, 22, 23) (ryc. 2). Uważa się, że za możliwość wykorzystania tej rośliny w zwalczaniu objawów menopauzy odpowiadają glikozydy triterpenowe. Wyciąg z pluskwicy hamuje indukowany estradiolem wzrost komórek MCF-7, jak również wykazuje inne właściwości antyestrogenne (16, 25, 26). Badania in vitro na komórkach raka sutka MCF-7 potwierdziły jego aktywność (25, 27). Co prawda mechanizm działania jest jeszcze nieznany, ale podejrzewa się, że za tę właściwość odpowiadają związki, które wykazują zdolność wiązania receptorów estrogenowych (ER). Działanie przeciwrakowe pluskwicy musi być związane z jeszcze nie poznanymi receptorami ER lub mechanizm jej działania nie zależy od nich (26). Z drugiej strony, wyciąg z pluskwicy hamuje wzrost estrogenowego receptora T47D (25). W przeciwieństwie do estrogenu pluskwica nie stymuluje pojawienia się nowotworów sutka dimetylobenzantraceno-zależnych u szczurów po owariektomii (26).
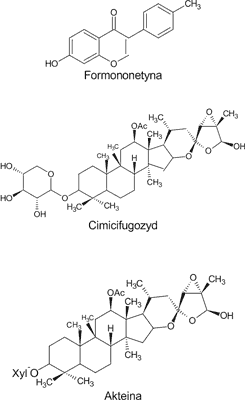
Ryc. 2. Przykłady budowy chemicznej głównych związków występujących w pluskwicy groniastej.
Stosowanie pluskwicy groniastej jest bezpieczne podczas ciąży, jak i w trakcie karmienia piersią. Można ją przyjmować nawet przez 6 miesięcy. W trakcie wieloletnich badań nie wykryto żadnych toksycznych metabolitów tej rośliny. Jednakże długotrwałe jej stosowanie, jak i spożywanie jej w dużych ilościach, może być niebezpieczne. Pacjentki z wysokim ciśnieniem krwi, dolegliwościami nerek i wątroby powinny konsultować przyjmowanie produktów leczniczych zawierających w swym składzie pluskwicę. Wysokie dawki pluskwicy mogą powodować zawroty głowy, zaburzenia widzenia, wymioty oraz problemy z krążeniem. Nie wykryto również żadnych niepokojących skutków ubocznych stosowania pluskwicy przez pacjentki ze zdiagnozowanym rakiem, przyjmujących inne leki o działaniu zwalczającym komórki nowotworowe (np. tamoxifen) (21).
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
24 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
59 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
119 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 28 zł
Piśmiennictwo
1. Borrelli F, Ernst E. Black cohosh (Cimicifuga racemosa): a systematic review of adverse events. Am J Obst Gynecol 2008; 199:455-66. 2. Chen LC, Wang BR, Chen IC i wsp. Use of Chinese herbal medicine among menopausal women in Taiwan. Int J Gynecol Obstet 2010; 109:63-6. 3. Newton KM, Reed SD, Grothaus L i wsp. Reprint of the herbal alternatives for menopauze (HALT) study: background and study design. Maturitas 2008; 61:181-93. 4. Murray RK, Granner DK, Mayes PA i wsp. Biochemia Harpera. PZWL Warszawa 1994; 667. 5. Lockler TD, Huang Y, Frasor J i wsp. Estrogenic and progestagenic effects of extracts of Justicia pectoralis Jacq, an herbal medicine from Costa Rica used for treatment of menopause and PMS. Maturitas 2010; 66:315-22. 6. Chen LC, Tson YT, Yen KY i wsp. A pilot study comparing the clinical effects of Jia-Wey Shiau-Yau San, a tradicional Chinese herbal prescription, and a continous combined hormone repacement therapy in postmenopausal women with climacteric symptoms. Maturitas 2003; 44:55-62. 7. Frei-Kleiner S, Schaffiner W, Rahlfs VW i wsp. Cimicifuga racemosa dried ethanolic extract in menopausal disorders: a double-blind placebo-controlled clinical trial. Maturitas 2005; 51:397-404. 8. Michel JL, Mahady GB, Veliz M i wsp. Symptoms, attitudes and treatment choices surrounding menopause among the Q`eqchi Maya of Livingston, Guatemala. Soc Sci Med 2006; 63:732-42. 9. Wuttke W, Seidlová-Wuttke D, Gorkow C. The Cimicifuga preparation BNO 1055 vs. conjugated estrogens in a double-blinde placebo-controlled study: effects on menopause symptoms and bone markers. Maturitas 2003; 44 (1):S67-S77. 10. Winterhoff H, Spengler B, Christoffel V i wsp. Cimicifuga extract BNO 1055; reduction of hot flushes and hints on antidepressant activity. Maturitas 2003; 44 (1):S51-8. 11. Seidlová-Wuttke D, Jarry H, Becker T i wsp. Pharmacology of Cimicifuga racemosa extract BNO 1055 in rats: bone, fat and uterus. Maturitas 2003; 44 (1):S39-S50. 12. Glazier MG, Bowman MA. A review of the evidence for the use of phytoestrogens as a replacement for traditional estrogen replacement therapy. Arch Intern Med 2001; 161:1161-72. 13. Liu J, Burdette JE, Xu H i wsp. Evaluation of estrogenic activity of plant extracts for the potential treatment of menopausal symptoms. J Agric Food Chem 2001; 49(5):2472-9. 14. El-Shitany NA, Hegazy S, El-desoky K. Evidences for antiosteoporotic and selective estrogen receptor modulator activity or silimarin compared with ethinylestradiol in ovariectomized rats. Phytomed 2010; 17:116-25. 15. Huntley AL, Ernst E. A systematic review of herbal medicinal products for the treatmenst of menopausal symptoms. Menopause 2003; 10(5):465-76. 16. Xu H, Fabricant DS, Piersen CE i wsp. A preliminary RAPD-PCR analysis of Cimicifuga species and other botanicals used for women`s health. Phytomed 2002; 9:757-62. 17. Boué SM, Wiese TE, Nehls S i wsp. Evaluation of the estrogenic effect of legume extracts containing phytoestrogens. J Agric Food Chem 2003; 51:2193-9. 18. Beck V, Unterrirder E, Krenn L i wsp. Comparison of hormonal activity (estrogen, androgen and progestin) of standardized plant extracts for large scale use in hormone replacenet therapy. J Stereo Biochem Mol Biol 2003; 84:259-68. 19. Zhang Y, Yu L, Ao M i wsp. Effect of ethanol of Lepidium meyenii Walp. on osteoporosis in ovariectomized rat. J Ethnopharmacol 2006; 105:274-9. 20. Seidlová-Wuttke D, Hesse O, Jarry H i wsp. Evidence for selective estrogen receptor modulator activity in a black cohosh (Cimicifuga racemosa) extract: comparison with estradiol-17β. Eur J Endocrinol 2003; 149:351-62. 21. González Stuart A. Black Cohosh Actaea racemosa L. (Cimicifuga racemosa L. (Nutt)), 2005. 22. Bolle P, Mastrangelo S, Perrone F i wsp. Estrogen-like effect of a Cimicifuga racemosa extract sub-fraction as assessed by in vivo, ex vivo and in vitro assays. J Stereo Biochem Mol Biol 2007; 107:262-9. 23. Gaube F, Wolfl S, Pusch L i wsp. Gene expression profiling reveals effects of Cimicifuga racemosa (L.) NUTT. (black cohosh) on the estrogen receptor positive human breast cancer cell line MCF-7 BMC Pharmacol 2007; 7:11. 24. Low Dog T. Menopause: a review of botanical supplements. Am J Med 2005; 118(12B):98S-108S. 25. Zierau O, Bodinet C, Kolba S i wsp. Antiestrogenic activities of Cimicifuga racemosa extracts. J Steroid Biochem Mol Biol 2002; 80:125-30. 26. Bodinet C, Freudenstein J. Influence of marketed herbal menopause preparations on MCF-& cell proliferation. Menopause 2004; 11(3):281-9. 27. Jarry H, Thelen P, Christoffel V i wsp. Cimicifuga racemosa extract BNO 1055 inhibits proliferation of the human prostate cancer cell line LNCaP. Phytomed 2005; 12:178-82. 28. Wuttke W, Jarry H, Seidlová-Wuttke D. Cimicifuga racemosa extract for the treatment of climacteric complaints. J Endocrinol Reprod 2006; 10(2):106-10. 29. Hostanska K, Nisslein T, Freudenstein J i wsp. Inhibitory effect of an isopropanolic extract of black cohosh on the invasiveness of MDA-MB 231 human breast cancer cells. In vivo 2007; 21:349-56. 30. Cassiedy A, Bingham S, Setchell KDR. Biological effects of a diet of soy protein rich in isoflavones on the menstrual cycle of premenopausal women. Am J Clin Nutr 1994; 60:333-40. 31. Petrakis NL, Barnes S, King EB i wsp. Stimulatory influence of soy protein isolate on breast secretion in pre- and postmenopausal women. Cancer Biomark Prev 1996; 5:785-94. 32. Potter SM, Baum JA, Teng H i wsp. Soy protein and isoflavones: their effects on blood lipids and bone density in postmenopausal women. Am J Clin Nutr 1998; 68:1375S-1379S.


