© Borgis - Postępy Fitoterapii 3/2012, s. 173-183
*Agnieszka Gryszczyńska1, Bogna Gryszczyńska2, Bogna Opala1, Zdzisław Łowicki1
Zastosowanie roślin leczniczych w menopauzie. Cz. II
The use of medicinal plants in the menopause. Part II
1Instytut Włókien Naturalnych i Roślin Zielarskich w Poznaniu
Dyrektor Instytutu: prof. dr hab. Grzegorz Spychalski
2Zakład Chemii Ogólnej, Katedra Chemii i Biochemii Klinicznej, Uniwersytet Medyczny w Poznaniu
Kierownik Zakładu: dr hab. Maria Iskra prof. UM
Summary
This article is a second part of article about herbs which are used in menopause symptoms treatment. This article contains information about current research on herbs such as soy, maca and clover grass in combating outbreaks include hot flashes, mood swings, herbs impact the hormonal balance that is disturbed during menopause, as well as reducing the prevalence of breast cancer and endometrial cancer. Article consists informations about main bioactive compounds for example isoflavons or flavonolignans which are responsible for the protective effect on the human body.

Poniżej przedstawione zostaną kolejne rośliny, które znajdują zastosowanie w leczeniu chorób kobiecych.
Koniczyna łąkowa – koniczyna czerwona (Trifolium pratense L.)
Do głównych związków czynnych zawartych w koniczynie łąkowej (ryc. 1) zaliczyć można następujące fitoestrogeny: genisteinę, daidzeinę, biochaninę A i formononetynę (ryc. 2) (1, 2). Koniczyna łąkowa zawiera najwyższą zawartość fitoestrogenów ze wszystkich roślin z gatunku Trifolium (1). Izoflawony w koniczynie wiązane są tylko przez malonylo-β-glikozydy, w przeciwieństwie do izoflawonów pochodzących z soi, które wiązane są jeszcze przez inne cukry. Związane izoflawony nie wykazują działania estrogennego.

Ryc. 1. Koniczyna łąkowa (Trifolium pratense L.).
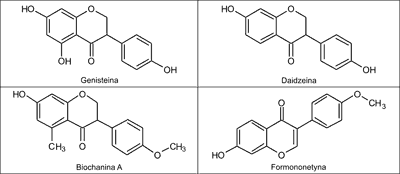
Ryc. 2. Struktury podstawowych substancji czynnych zawartych w koniczynie łąkowej.
Biochanina A metabolizowana jest w układzie pokarmowym do genisteiny, natomiast formononetyna do daidzeiny, z kolei ta do 4’,7-izoflawandiolu. Metabolizm tych związków zależny jest od indywidualnych zdolności organizmu ludzkiego. Sprzężone izoflawony nie są aktywne chemiczne, a ich metabolizm zachodzi w jelitach (3).
Podejrzewa się, że wpływ koniczyny czerwonej na endometrium wynika z jej zdolności antyproliferacyjnej. Wyciągi z tej rośliny wykazują słabe działanie estrogenne na szczury po owariektomii, ale nie stymulują proliferacji komórek gruczołu sutkowego. Z kolei inne doniesienia naukowe mówią, że u zdrowych kobiet można zauważyć wpływ izoflawonów nie tylko na receptory estrogenowe, ale również na oś podwzgórzowo-przysadkowo-gonadową (3).
Z badań in vitro wynika, że daidzeina reguluje różnicowanie osteoklastów poprzez interferencję apoptozy i szlaku kapsazy-3. Izoflawony oraz ich metabolity oddziałują na 17β-oksydoreduktazę hydroksysteroidową, aromatazę oraz sulfotransferazę (3).
Baber i wsp. (4) w 1999 roku badali wpływ stosowania preparatu z koniczyny czerwonej na 51 kobietach. Pacjentki przyjmowały Promensil w dawce 40 mg/dobę oraz placebo przez 12 tygodni. Przed rozpoczęciem badań przez 1 miesiąc wszystkie kobiety przyjmowały placebo. W badaniach nie zaobserwowano statystycznie istotnych zmian pomiędzy grupami w przypadku częstotliwości uderzeń gorąca. Zanotowano jednak zmianę poziomu izoflawonów w moczu u pacjentek z grupy placebo po zakończeniu eksperymentu. Nasuwają się pytania dotyczące wpływu stosowania diety na skład moczu.
Liu i wsp. (5) w 2001 roku opublikowali wyniki swoich badań prowadzonych na 8 ze 150 roślin o działaniu estrogennym i progestagennym. W badaniach wykorzystane zostały metanolowe wyciągi z arcydzięgla chińskiego, koniczyny czerwonej, pluskwicy groniastej, niepokalanka pospolitego, lukrecji, chmielu oraz żeń-szenia azjatyckiego i północnoamerykańskiego. Wyciągi badane były pod kątem aktywności (IC50) wobec receptorów ERα i ERβ. Potencjał wiązania receptorów przez najaktywniejsze wyciągi można uszeregować w następującej kolejności: koniczyna czerwona >> chmiel > niepokalanek pospolity. Dodatkowo różnice powinowactwa tych wyciągów do ERα i ERβ nie były statystycznie istotne. Arcydzięgiel oraz lukrecja wykazywały słabą aktywność, natomiast żeń-szeń azjatycki i północnoamerykański oraz pluskwica groniasta nie wykazywały żadnej zdolności wiązania tych receptorów (< 20% przy stężeniu 200 μg/ml).
Przebadano również substancje porównawcze z grupy izoflawonów zawartych w koniczynie czerwonej wobec receptorów ERα i ERβ. Efektywność konkurencyjnego potencjału wiązania uszeregować można w następujący sposób: genisteina > daidzeina > biochanina A > formononetyna. Wszystkie te izoflawony wykazują wyższą aktywność wobec receptorów ERβ niż ERα. Podjęto dodatkowe badania mające na celu wyjaśnienie wyższej aktywności substancji porównawczych izoflawonów niż wyciągu z koniczyny łąkowej. Dlatego przeprowadzono próbę rozfrakcjonowania wyciągu z koniczyny i weryfikację substancji najbardziej aktywnych. Wykorzystano takie rozpuszczalniki, jak chloroform, eter naftowy, butanol i wodę. Najlepszym wyciągiem pod względem aktywności wobec receptorów ERβ, w skład którego wchodzą genisteina, daidzeina i biochanina A, był wyciąg chloroformowy. W eksperymencie z fosfatazą alkaliczną wyciąg z koniczyny łąkowej wykazał zdolność indukcji IC50 przy stężeniu 1 μg/ml. Frakcje chloroformowe również wykazywały taką zdolność wobec komórek Ishikawy.
Wyciąg z chmielu wykazał silne właściwości cytotoksyczne, efekt estrogenny IC50 widoczny był przy stężeniu 13,1 μg/ml. Niepokalanek pospolity odznaczał się słabą aktywnością (40%) przy stężeniu 20 μg/ml. Pozostałe wyciągi były nieaktywne. Ekspresja receptora progesteronowego (PR) była znamienna w przypadku wyciągu z koniczyny czerwonej. W odniesieniu do arcydzięgla i lukrecji zanotowano słabą aktywność wobec omawianego receptora przy zastosowaniu takiego samego stężenia. W przypadku obu gatunków żeń-szenia i pluskwicy groniastej nie zanotowano aktywności wobec receptora PR. Wyciąg chloroformowy z koniczyny łąkowej, który wykazywał najwyższą aktywność wobec receptora ER, był też najaktywniejszy wobec receptora PR. W kolejnym etapie badań sprawdzany był wpływ wyciągów na ekspresję receptora pS2 estrogenowego linii komórek raka sutka MCF-7.
Na podstawie uzyskanych wyników można stwierdzić, że wszystkie wyciągi, z wyjątkiem pluskwicy groniastej, indukują ekspresję pS2 przy stężeniu 20 μg/ml. Co istotne, żeń-szeń azjatycki i północnoamerykański nie wykazywały aktywności w trzech wymienionych testach (test komórek Ishikawy, stymulacja receptora PR mRNA i receptora pS2 mRNA). Reasumując, w 4 różnych modelach badań in vitro najwyższą aktywność wykazywał wyciąg z koniczyny łąkowej. Chmiel również cechuje aktywność estrogenna, jednak wykazuje on także działanie cytotoksyczne wobec komórek Ishikawy. Najbardziej aktywnym związkiem w stosunku do receptora ERβ z koniczyny czerwonej była genisteina, która może być również odpowiedzialna za indukcję fosfatazy alkalicznej oraz za ekspresję receptorów pS2 i PR (5).
Tice i wsp. w 2003 roku (4) prowadzili badania na 252 kobietach, u których tygodniowo występowało minimum 35 uderzeń gorąca. W eksperymencie pacjentki przyjmowały dwa preparaty izoflawonowe z koniczyny czerwonej: Promensil (82 mg/dobę) oraz Rimostil (57 mg/dobę), trzecia grupa pacjentek przyjmowała placebo. Doświadczenie prowadzone było przez 12 tygodni. Nie zauważono różnic w liczbie wyrzutów gorąca w przypadku stosowania preparatów w porównaniu do placebo. U pacjentek przyjmujących Promensil początkowo zaobserwowano gwałtowny spadek liczby wyrzutów gorąca w porównaniu do pozostałych grup. Jednak po upływie 12 tygodni redukcja wyrzutów gorąca była na podobnym poziomie: 41% Promensil, 34% Rimostil, a w przypadku placebo – 36% (4).
Nie zaobserwowano też żadnych poważnych skutków ubocznych stosowania preparatów zawierających wyciąg z liści koniczyny czerwonej. W 12-miesięcznych badaniach prowadzonych przez Atkinson i wsp. (cyt. za 4) na kobietach stosujących Promensil (43,5 mg/dobę) w wieku 49-65 lat oraz placebo, nie zanotowano zmiany gęstości tkankowej gruczołów piersiowych. Nie zaobserwowano również statystycznie istotnego efektu estradiolowego czy zmiany zawartości enzymów FSH i LH. W innych badaniach prowadzonych przez zespół Clifton-Blight (cyt. za 4), po 6 miesiącach stosowania izoflawonów w ilości 85,5 mg/dobę, nie zanotowano wzrostu grubości endometrium. Zespół Baber (cyt. za 4) nie znalazł statystycznie istotnej różnicy w poziomie estradiolu w surowicy, enzymu FSH, globulin wiążących hormony płciowe, cytologii oraz grubości endometrium po 3-miesięcznym stosowaniu preparatu Promensil. Koniczyna czerwona ma zdolność spowalniania metabolizmu leków przez oddziaływanie na cytochrom P450, enzymy CYP1A1, CYP1B1 i CYP2C9, jednak nie zaobserwowano oddziaływania pomiędzy koniczyną czerwoną a lekami (4).
Maca (Lepidium meyenii Walp.) (ryc. 3)

Ryc. 3. Maca (Lepidium meyenii Walp.).
Jedną z częściej wykorzystywanych roślin w leczeniu symptomów menopauzy w Australii jest maca. Wzmianki o pierwszych hodowcach tej rośliny w Andach sięgają ok. 2000 r. p.n.e., a w czasach kolonizacji przez Hiszpanów była uznawana za walutę (6). Pochodzi ona z wysokich partii Andów Peruwiańskich (powyżej 4000 m n.p.m.) (7-10). Plemiona peruwiańskie spożywają jej hipokotyle w ilościach większych od 20 g/dzień; świeżo zebrane części są gotowane przed konsumpcją, ponieważ inaczej mogą wywołać skutki uboczne. Z badań na 600 pacjentach wynika, że zagotowanie nie powoduje żadnych skutków ubocznych, nawet po zjedzeniu ok. 17 g wysuszonych hipokotyli/kg (8).
W Peru maca tradycyjnie stosowana jest jako roślina zwiększająca płodność oraz jako afrodyzjak (7-9). Można odnaleźć doniesienia naukowe, które potwierdzają zwiększenie płodności mężczyzn po zażywaniu tej rośliny (8). Maca stosowana jest do zwalczania wyrzutów gorąca, drażliwości gruczołów piersiowych, wysuszenia pochwy czy osteoporozy (7). Jej wodne wyciągi często testowane są w licznych badaniach dotyczących spermatogenezy, płodności, nastroju, pamięci, metabolizmu czy różnego rodzaju nowotworów (9). Badania prowadzone na szczurach po owariektomii sugerują, że spożywanie tego produktu zwiększa masę kości oraz przywraca strukturę beleczkowatą w odcinku lędźwiowym kręgosłupa, zmniejszając prawdopodobieństwo wystąpienia osteoporozy. Badania te dają dużą szansę na skuteczne wykorzystywanie jej w zwalczaniu groźnych objawów menopauzy u kobiet (8). Najlepszymi właściwościami wśród różnych odmian charakteryzuje się czarna maca. Jedną z jej właściwości jest obniżenie aktywności enzymu acetylocholinesterazy oraz brak aktywności wobec enzymu oksydazy monoaminowej u samców myszy; tak więc może wpływać na proces uczenia się i zapamiętywanie u myszy po owariektomii (10).
Za działanie fitoestrogene tej rośliny odpowiada β-sitosterol. Można odnaleźć wzmianki, które mówią o wpływie wyciągu z maca na proliferację komórek MCF-7. Alkaloidy, izocyjaniany oraz glukozynolaty zawarte w maca mają również wpływ na jej aktywność (8). Izotiocyjaniany redukują ryzyko wystąpienia raka sutka, żołądka czy wątroby (6). Niektórzy naukowcy sugerują, że wyciąg z tej rośliny działa endokrynologiczne nie za sprawą hormonów roślinnych czy fitoestrogenów, ale za sprawą alkaloidów oddziałujących na oś podwzgórzowo-przysadkową i nadnercza. Jeden z obecnych w maca glukozynolatów – glukobrassyicyna, wykazuje aktywność androgenną; w procesach enzymatycznych hydrolizowany jest do 3,3-diindolilometanu – antagonisty receptora androgenowego. Jak dotąd jest to jedyna poznana roślina, która wykazuje taką właściwość (8). Skład chemiczny maca prawdopodobnie odpowiada za jej aktywność afrodyzjakalną, adaptogenną, anaboliczną, immunostymulacyjną oraz równowagę hormonalną (2, 7). Oprócz organicznych związków można znaleźć w maca takie pierwiastki, jak wapń, żelazo, miedź, cynk oraz potas (9). Struktury podstawowych substancji wykazujących właściwości fitoestrogenne ilustruje rycina 4.
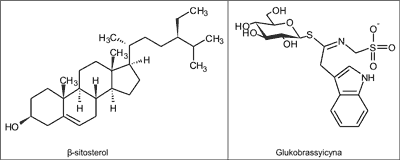
Ryc. 4. Podstawowe substancje zawarte w maca wykazujące właściwości fitoestrogenne.
Zhang i wsp. (7) sprawdzali działanie etanolowego wyciągu z maca na osteoporozę u szczurów po owariektomii przez 28 tygodni. Badaniom poddano 40 szczurów, które podzielono na 4 grupy po 10 osobników. Pierwszą grupą były szczury, u których wykonano operację Shama, tzw. operację rzekomą (mającą na celu manipulację chirurgiczną polegającą na rozcięciu skóry, warstwy mięśniowej i otrzewnej), drugą – szczury po owariektomii (grupa kontrolna OVX), trzecią i czwartą – szczury po owariektomii otrzymujące etanolowy wyciąg z maca w różnych dawkach (0,096 g/kg oraz 0,24 g/kg). Z badań wynika, że długotrwałe pozbawienie dojrzałych samic szczurów jajników wpływa na spadek zawartości wapnia w kości udowej, pomimo stosowania diety zawierającej wapń. Stosowanie wyciągu maca 0,24 g/kg spowodowało wzrost gęstości mineralnej kości (BDM) odcinka lędźwiowego, natomiast BDM trzonu kości udowej nieznacznie zmieniła się w stosunku do kontroli. Zależność ta wskazuje, że maca ma wpływ na kości gąbczaste, a nie na kości korowe. Zastosowanie maca w ilości 0,24 g/kg spowodowało zmniejszenie redukcji zawartości wapnia, czyli miało wpływ na absorpcję wapnia w kościach. Wyciąg z maca wykazuje właściwości przeciwosteoporozowe bez statystycznej zmiany masy macicy. Własność ta wyróżnia maca od hormonalnej terapii zastępczej, wykazując mniejsze ryzyko proliferacji endometrium. W badaniach wyciąg z maca nie wykazywał również statystycznej zmiany składu markerów osteoporozy w surowicy krwi i innych jej składników biochemicznych. Istnieje więc prawdopodobieństwo, że wyciąg nie bierze udziału w metabolizmie kości (7).
Brooks i wsp. (8) prowadzili badania na 14 postmenopauzalnych kobietach (w wieku 50-60 lat), u których określono poziom hormonów płciowych (LS i FSH), poziom globulin wiążących hormony płciowe (SHBG) oraz skalę Greene (GCS) przed rozpoczęciem badań (t = 0) oraz po 6 i 12 tyg. eksperymentu. Kobiety zostały podzielone na dwie grupy po 7 osób. Pierwsza grupa przyjmowała najpierw przez 6 tyg. metanolowy wyciąg z maca (3,5 g/dzień), potem przez kolejne 6 tygodni badań placebo, w drugiej grupie zastosowano odwrotną kolejność podawania preparatów. Na przestrzeni prowadzonych badań nie zanotowano statystycznie istotnych zmian składu hormonalnego surowicy. Tak więc nie potwierdzono w tym badaniu aktywności estrogennej ani androgennej maca. Wynik ten może byś spowodowany słabą wchłanialnością substancji czynnych przez organizm. Z kolei w badaniach GCS, w grupie rozpoczynającej przyjmowanie preparatów od maca zanotowano 30% redukcję wartości GCS w stosunku do badania w dniu rozpoczęcia eksperymentu (t = 0) oraz 27% spadek po przyjmowaniu placebo (w stosunku do t = 0). Skalę GCS można podzielić na 2 podskale: charakteryzujące niepokój oraz depresję. W skali niepokoju zanotowano znamienne 30,8% obniżenie wartości w grupie pierwszej w stosunku do t = 0 oraz 27,3% dla placebo w porównaniu do t = 0. Natomiast w skali opisującej depresję statystycznie istotny spadek wartości odnotowano dla grupy pierwszej w stosunku do t = 0 (28,9%) i dla placebo w stosunku do t = 0 (26,8%). Zanotowano również zmniejszenie problemów seksualnych w przypadku maca o 22,9% w porównaniu do t = 0 i o 34,6% w stosunku do placebo. Podsumowując, maca spowodowała redukcję skali GCS o 18% w stosunku do t = 0 oraz 17,3% w stosunku do placebo, nie zanotowano jednak wpływu tego produktu na somatyczne i naczynioruchowe symptomy podczas eksperymentu (8).
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
24 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
59 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
119 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 28 zł
Piśmiennictwo
1. Xu H, Fabricant DS, Piersen CE i wsp. A preliminary RAPD-PCR analysis of Cimicifuga species and other botanicals used for women's health. Phytomed 2002; 9:757-62. 2. Khaosaad T, Krenn L, Medjakovic S i wsp. Effect of mycorrhization on the isoflavone content and the phytoestrogen activity of red clover. J Plant Physiol 2008; 165:1161-7. 3. Beck V, Unterrirder E, Krenn L i wsp. Comparison of hormonal activity (estrogen, androgen and progestin) of standarized plant extracts for large scale use in hormone replacenet therapy. J Stereo Biochem Mol Biol 2003; 84:259-68. 4. Dog TL. Menopause: a review of botanical supplements. Am J Med 2005; 118(12B):98S-108. 5. Liu J, Burdette JE, Xu H i wsp. Evaluation of estrogenic activity of plant extracts for the potential treatment of menopausal symptoms. J Agric Food Chem 2001; 49(5):2472-9. 6. Valentová K, Ulrichová J. Smallanthus sonchifolius and Lepidium meyenii – prospective Andean crops for the prevention of chronic diseases. Bomed Papers 2003; 147(3):119-30. 7. Zhang Y, Yu L, Ao M i wsp. Effect of ethanol of Lepidium meyenii Walp. on osteoporosis in ovariectomized rat. J Ethnopharmacol 2006; 105:274-9. 8. Brooks NA, Wilcox G, Walkar KZ i wsp. Beneficial effect of Lepidium meyenii (Maca) on physiological symptoms and measures of sexual dysfunction in postmenopausal women are not related to estrogen or androgen content. Menopause 2008; 15(6):1157-62. 9. Gonzales GF. Ethnobiology and ethnopharmacology of Lepidium meyenii (Maca), a plant from the Peruvian highlands. Hindawi Publ Corpor Vol. 2012; ID193496:10. 10. Roubio J, Qiong W, Liu X i wsp. Aqueous extracts of black maca (Lepidium meyenii) on memory impairment induced by ovariectomy in mice. Hindawi Publ Corpor Vol. 2011; ID 253958:7. 11. Dog TL, Mahady R, Gardiner P i wsp. Assessing safety of herbal products for complaints: an international perspective. Maturitas 2010; 66:355-62. 12. El-Shitany NA, Hegazy S, El-Desoky K. Evidences for antiosteoporotic and selective estrogen receptor modulator activity or silymarin compared with ethinylestradiol in ovariectomized rats. Phytomed 2010; 17:116-25. 13. HuntleyAL, Ernst E. A systematic review of herbal medicinal products for the treatmenst of menopausal symptoms. Menopause 2003; 10(5):465-76. 14. Boué SM, Wiese TE, Nehls S i wsp. Evaluation of the estrogenic effect of legume extracts containing phytoestrogens. J Agric Food Chem 2003; 51:2193-9. 15. Lockler TD, Huang Y, Frasor J i wsp. Estrogenic and progestagenic effects of extracts of Justicia pectoralis Jacq., an herbal medicine from Costa Rica used for treatment of menopause and PMS. Maturitas 2010; 66:315-22.




