© Borgis - Postępy Fitoterapii 4/2012, s. 226-229
*Bogdan Kędzia, Elżbieta Hołderna-Kędzia
Działanie terpenów roślinnych na drobnoustroje
The microbiological activity of plant terpenes
Instytut Włókien Naturalnych i Roślin Zielarskich w Poznaniu
Dyrektor Instytutu: prof. dr hab. Grzegorz Spychalski
Summary
The studies inculded the activity on bacteria and yeast fungi of 32 acyclic, monocyclic and dicyclic monoterpenes sesquiterpenes, diterpenes and triterpenes of plant origin.
It was stated that on such human pathogenic microbes like: Staphylococcus aureus, Escherichia coli and Candida albicans the strong activity showed acyclic monoterpenes – geraniol and citronelol, monocyclic monoterpene – menthol, dicyclic monoterpenes – camphen, borneol, camphor and thujon and acyclic sesquiterpenes – β-caryophylen, α-bisabolol and chamazulen.
Their inhibited the growth of investigated microorganisms in the concentration limits 75-750 μg/ml. The above studies are the possibility of use of mentioned plant terpenes in the medical practice.

Wstęp
Nazwą terpenów (izoprenoidów) określa się dużą grupę substancji naturalnych, które są pochodnymi tzw. aktywnego izoprenu – izopentenylodifosforanu lub jego izomeru dimetyloallilodifosforanu (ryc. 1). Wymienione związki przez połączenie w dwie lub więcej jednostek tworzą cząsteczki, w których liczba atomów węgla jest podzielna przez 5, a mianowicie: monoterpeny (C10), seskwiterpeny (C15), diterpeny (C20) i triterpeny (C30). Z kolei wśród monoterpenów wyróżniamy związki acykliczne, monocykliczne i dicykliczne (1).
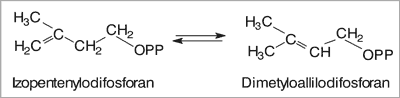
Ryc. 1. Terpeny (izopreny) jako pochodne aktywnego izoprenu i jego izomeru (wg 1).
Celem pracy była ocena działania przeciwdrobnoustrojowego terpenów roślinnych z punktu widzenia poznawczego oraz ewentualnego zastosowania w praktyce medycznej. W opracowaniu wykorzystane zostały wyniki badań własnych wykonanych w latach 1976-2010.
Materiał i metody
Badane substancje
W badaniach użyto 32 terpenów, które pochodziły z następujących firm: Aldrich – geraniol, octan geranylu, cytronelal, cytral, limonen, mentol, p-cymen, α-terpineol, α-pinen, β-pinen, kamfen, borneol, izoborneol, kamfora, fenchon, farnezol, farnezal; Dragoco – linalol, octan bornylu; Riedel – cytronelol; Sigma – β-myrcen; Fluka – 1,8-cyneol, α-felandren; Phytolab – chamazulen i Roth – β-kariofylen, kwas abietynowy, kwas β-ursolowy, kwas oleanolowy, hederasaponina, prymulina (chlorek), tujon, α-bisabolol.
Drobnoustroje
W badaniach wykorzystano szczepy wzorcowe z następujących kolekcji mikrobiologicznych: ATCC (American Type Culture Collection), CNCTC (Czechoslovak National Collection of Type Cultures) oraz PZH (Państwowy Zakład Higieny). Poza tym w badaniach użyto szczepy drobnoustrojów wyizolowane z materiału szpitalnego (S) oraz z produktów żywnościowych (P).
Określanie aktywności przeciwdrobnoustrojowej
Badane terpeny rozpuszczano w DMSO (firmy Serva) w stężeniu 100 mg/ml i sporządzano z nich rozcieńczenia w podłożach płynnych dla bakterii – Antibiotic Broth i dla grzybów Sabouraud Broth (oba podłoża firmy Merck). Oznaczenia prowadzono w granicach stężeń 1-1500 μg/ml. Do poszczególnych rozcieńczeń badanych terpenów o objętości 1 ml dodawano po 0,1 ml 24-48 godz. hodowli bakterii lub grzybów drożdżoidalnych. Inokulum badanych drobnoustrojów mieściło się w granicach 105-106 komórek w 1 ml. Próbki inkubowano przez 24-48 godz. w temp 37°C (bakterie i grzyby drożdżoidalne chorobotwórcze dla człowieka) oraz w temp. 25°C (grzyby drożdżoidalne izolowane z produktów żywnościowych). Następnie określano najmniejsze stężenie hamujące (MIC – Minimal Inhibitory Concentration) badanych terpenów.
Wyniki
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
24 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
59 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
119 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 28 zł
Piśmiennictwo
1. Kohlmünzer S. Farmakognozja. Wyd Lek PZWL, Warszawa 2000; 277-337. 2. Kędzia B, Hołderna-Kędzia E, Grabowska H. Poszukiwanie antybiotycznych substancji roślinnych. Dokumentacja tematu statutowego nr 24/91/Y. Inst Rośl Przetw Ziel, Poznań 1994. 3. Kędzia B, Krzyżaniak M, Hołderna-Kędzia E i wsp. Skład i właściwości przeciwdrobnoustrojowe Ol. Melissae i jego składników. Herba Pol 1994; 40:5-11. 4. Hołderna-Kędzia E. Działanie substancji olejkowych na bakterie i grzyby. Post Fitoter 2010; 1:3-8. 5. Kędzia B, Hołderna-Kędzia E. Działanie antybiotyczne substancji roślinnych na drobnoustroje. Badania wykonane w latach 1976-2010. Dane nieopublikowane. 6. Olechnowicz-Stępień W, Lamer-Zarawska E, Kędzia B. Poszukiwanie związków przeciwbakteryjnyh w krajowych balsamach. Cz. I. Izolacja substancji o działaniu przeciwbakteryjnym z kalafonii sosnowej (Pinus sylvestris L.). Herba Pol 1981; 27:273-82.

