© Borgis - Postępy Nauk Medycznych 5/2014, s. 328-333
*Paweł Krzęczko1, Kamil Radzikowski1, Radosław Chutkowski1, Bartłomiej Wódarski1, Marek Molski2, Łukasz Ulatowski2, Małgorzata Malec-Milewska1
Znieczulenie złożone podpajęczynówkowe w odcinku lędźwiowym oraz ciągłe zewnątrzoponowe w odcinku piersiowym do zabiegów rekonstrukcji piersi metodą wolnego płata (DIEP lub SIEA) – doświadczenia własne
Combined anesthesia – spinal and thoracic continuous epidural, in free flap breast reconstruction surgery (DIEP or SIEA) – our experience
1Klinika Anestezjologii i Intensywnej Terapii, Centrum Medyczne Kształcenia Podyplomowego, Warszawa
p.o. Kierownika Kliniki: dr med. Małgorzata Malec-Milewska
2Klinika Chirurgii Plastycznej, Centrum Medyczne Kształcenia Podyplomowego, Warszawa
Kierownik Kliniki: dr hab. med. Bartłomiej Noszczyk
Streszczenie
Wstęp. Rak piersi jest najczęstszym nowotworem złośliwym u kobiet. Podstawową metodą leczenia jest mastektomia i leczenie uzupełniające. Leczenie operacyjne pozostawia pacjentki z poczuciem okaleczenia zarówno fizycznego, jak i psychicznego, znacząco wpływając na ich samopoczucie. Dlatego coraz częściej wykonuje się operacje rekonstrukcyjne piersi, w tym rekonstrukcje piersi metodą wolnego płata tkankami z podbrzusza (ang. deep interior epigastric perforator – DIEP lub ang. superficial inferior epigastric artery – SIEA). Są to zabiegi czasochłonne, obejmujące swoim zasięgiem powłoki brzuszne i ścianę klatki piersiowej.
Cel pracy. Zastosowanie złożonego znieczulenia podpajęczynówkowego w odcinku lędźwiowym i zewnątrzoponowego ciągłego w odcinku piersiowym ma szansę wyeliminować większość powikłań i trudności związanych z długotrwałym znieczuleniem ogólnym. Ze względu na zakres blokady (ściana klatki piersiowej i powłoki brzuszne) wykonano w dolnej części odcinka piersiowego znieczulenie zewnątrzoponowe ciągłe z użyciem Ropiwakainy (Ropimol Molteni).
Materiał i metody. Przedstawiamy opis zastosowania tej metody na grupie sześciu pacjentek operowanych w Klinice Chirurgii Plastycznej Centrum Medycznego Kształcenia Podyplomowego w latach 2011-2012.
Wyniki i wnioski. Uważamy, że zastosowana technika znieczulenia jest bezpieczna i komfortowa zarówno dla pacjentek, jak i operatora. Zapewnia również skuteczne leczenie przeciwbólowe w okresie pooperacyjnym i umożliwia wczesne rozpoczęcie rehabilitacji.
Summary
Introduction. Breast cancer is the most common cancer in women. Primary method of treatment is mastectomy and adjuvant therapy. Surgical treatment leaves patients with a sense of both physical and mental damage, significantly affecting their well-being. This is the reason why more and more breast reconstruction surgeries are performed. From among them, free flap method (deep interior epigastric perforator – DIEP or superficial inferior epigastric artery – SIEA) is one of the most feasible ones. These are long lasting operations, covering abdomen and chest.
Aim. Use of combined spinal anesthesia – spinal and thoracic continuous epidural – gives a chance to eliminate majority of difficulties and complications that are linked to long-term general anesthesia. Due to the neuroaxial blockade range we decided to use Ropivacaine.
Material and metods. We report an application of this method in a group of six patients operated in Plastic Surgery Department of the Medical Center of Postgraduate Education in years 2011-2012.
Results and conclusion. We believe that the technique we used is safe and comfortable both for patient and surgeon. It also provides effective postoperative analgesia and early rehabilitation.

Wstęp
Zabieg rekonstrukcji piersi z użyciem wolnego płata (DIEP lub SIEA) jest mikrochirurgicznym sposobem odtworzenia piersi z użyciem tkanek własnych pacjentki (1). Jest to bardzo rozległa i bolesna operacja trwająca kilkanaście godzin. Efekt kosmetyczny, a co za tym idzie poprawa samopoczucia psychicznego i wzrost samooceny pacjentki są jednak lepsze niż w alternatywnych metodach, takich jak wszczepienie endoprotezy pod mięsień piersiowy (ryc. 1, 2). Należy pamiętać, jak duże znaczenie, szczególnie w grupie pacjentek onkologicznych, ma odtworzenie piersi po okaleczającym zabiegu mastektomii (2).
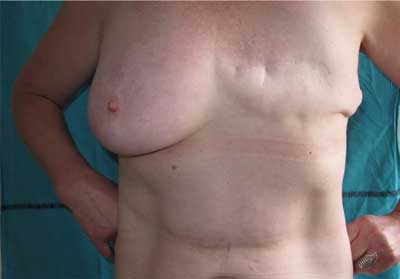
Ryc. 1. Stan po mastektomii lewostronnej – przed rekonstrukcją piersi wolnym płatem DIEP.
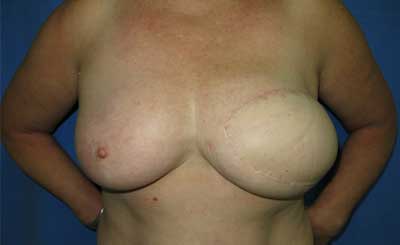
Ryc. 2. Sześć miesięcy po rekonstrukcji piersi lewej wolnym płatem DIEP.
Ze względu na rozległość zabiegu (ściana klatki piersiowej i powłoki brzuszne) i czas trwania procedury chirurgicznej do operacji rekonstrukcji piersi metodą wolnego płata stosuje się na ogół znieczulenie ogólne. Obarczone jest ono ryzykiem wystąpienia wielu powikłań pooperacyjnych, takich jak: nudności i wymioty, niewydolność oddechowa, zaburzenia fonacji spowodowane długotrwałą intubacją dotchawiczą i inne (3). Alternatywą jest zastosowanie złożonego znieczulenia podpajęczynówkowego w odcinku lędźwiowym i znieczulenia zewnątrzoponowego w odcinku piersiowym. Takie znieczulenie przewodowe w czasie wielogodzinnej operacji wymaga oczywiście zastosowania sedacji. Wybór tej metody stawia przed anestezjologiem nowe wyzwania, takie jak odpowiedni dobór środka znieczulenia miejscowego, kontrola ciśnienia tętniczego krwi, prowadzenie odpowiedniej płynoterapii, dostosowanie poziomu znieczulenia i sedacji do poszczególnych etapów zabiegu, a także przygotowanie psychiczne pacjentki na specyfikę odczuć w trakcie długotrwałej blokady centralnej (w okresie pooperacyjnym).
W literaturze opisywanych jest wiele przypadków znieczulenia zewnątrzoponowego w odcinku piersiowym do zabiegów onkologicznych w obrębie gruczołu piersiowego, dowodzących przewagi tej metody nad znieczuleniem ogólnym (3, 4). Niewiele jest natomiast opisów znieczulenia zewnątrzoponowego w odcinku piersiowym do operacji rekonstrukcji piersi wolnym płatem. W artykule przedstawiamy doświadczenia własne z zastosowania złożonego znieczulenia podpajęczynówkowego w odcinku lędźwiowym i zewnątrzoponowego ciągłego w odcinku piersiowym do operacji rekonstrukcji piersi wolnym płatem.
Cel pracy
Celem pracy jest udowodnienie, że zastosowanie złożonego znieczulenia podpajęczynówkowego w odcinku lędźwiowym i ciągłego zewnątrzoponowego w odcinku piersiowym ma szanse wyeliminować większość powikłań i trudności związanych z długotrwałym znieczuleniem ogólnym do operacji rekonstrukcyjnych.
Materiał i metody
W okresie od stycznia 2011 roku do kwietnia 2012 roku w Klinice Chirurgii Plastycznej Centrum Medycznego Kształcenia Podyplomowego przeprowadzono sześć zabiegów rekonstrukcji piersi metodą przeniesienia wolnego płata (DIEP/SIEA). Wiek pacjentek mieścił się w przedziale 35-49 lat, waga 56-79 kg, wskaźnik masy ciała 21,6-30 kg/m2 (ang. Body Mass Index – BMI). W jednym przypadku wskazaniem do zabiegu był zespół Polanda, w pozostałych pięciu stan po mastektomii z powodu raka piersi. Pacjentki zakwalifikowane były do znieczulenia z ryzykiem 2 według skali Amerykańskiego Towarzystwa Anestezjologicznego (American Society of Anesthesiologists – ASA) – negatywny wywiad w kierunku chorób układu krążenia i układu oddechowego.
W premedykacji zastosowano Midazolam (Midanium, Polfa Warszawa SA) doustnie w dawce 7,5 mg, na jedną godzinę przed rozpoczęciem zabiegu. W profilaktyce przeciwzakrzepowej pacjentki otrzymały enoksaparynę 40 mg podskórnie (Clexane, Sanofi-Aventis) na dwanaście godzin przed zabiegiem.
W sali operacyjnej prowadzono monitorowanie EKG, saturacji, ciśnienia tętniczego krwi metodą nieinwazyjną oraz diurezy. Uzyskano dostęp dożylny oraz rozpoczęto płynoterapię.
Używając standardowej igły Tuochy, metodą spadku oporu na powietrzu zidentyfikowano przestrzeń zewnątrzoponową na poziomie Th9/10 u dwóch pacjentek lub Th10/11 u czterech. Wprowadzono cewnik na głębokość 6-7 cm dogłowowo. Podano dawkę próbną 4 ml 0,5% Bupiwakainę z Adrenaliną (Marcaine – Adrenaline 0,5%, Astra Zeneca). Wykonanie ciągłego znieczulenia zewnątrzoponowego w odcinku piersiowym przebiegło we wszystkich przypadkach bez powikłań.
Następnie wykonano znieczulenie podpajęczynówkowe na poziomie L3/4 u czterech pacjentek lub L4/5 u dwóch pozostałych, podano od 3,4 do 4 ml Bupiwakainy (Marcaine 0,5% Heavy Spinal, Astra Zeneca) z dodatkiem Fentanylu 0,025 mg (Fentanyl, Polfa Warszawa SA). We wszystkich przypadkach uzyskano poziom blokady wystarczający do przeprowadzenia pierwszego etapu zabiegu, czyli wypreparowania płata skórno-podskórnego z powłok brzusznych.
Trzydzieści minut przed rozpoczęciem drugiego etapu operacji obejmującego ścianę klatki piersiowej (od 2 do 3,5 godziny od rozpoczęcia zabiegu) podawano bolus Ropiwakainy z Fentanylem do cewnika zewnątrzoponowego. Celem było uzyskanie blokady czuciowej do poziomu Th2. Aby to osiągnąć, podawano odpowiednio 10 ml 1% Ropiwakainy i 0,1 mg Fentanylu w pięciu przypadkach. Dwie pacjentki wymagały dodatkowej dawki leku, by uzyskać odpowiedni poziom blokady: w jednym przypadku było to dodatkowe 4 ml i po piętnastu minutach kolejne 6 ml 1% Ropiwakainy, a w drugim 4 ml 1% Ropiwakainy po 35 minutach od pierwszego bolusa. U szóstej pacjentki zdecydowano się podać bolus większej objętości Ropiwakainy w stężeniu 0,75% – łącznie zastosowano 19 ml 0,75% Ropiwakainy i 0,1 mg Fentanylu. Zakres znieczulenia we wszystkich przypadkach pozwolił na preparowanie ściany klatki piersiowej. U pięciu pacjentek po 90 minutach włączono wlew ciągły 1% Ropiwakainy (40 ml) z Fentanylem (0,4 mg). U jednej pacjentki, która otrzymała bolus Ropiwakainy o stężeniu 0,75%, zastosowano wlew 0,5% Ropiwakainy (20 ml) z Fentanylem (0,1 mg). Wlewy te kontynuowano do końca operacji. U jednej pacjentki po 3 godzinach wlewu zmieniono stężenie Ropiwakainy z 1% na 0,5% (pacjentka wymagała większych objętości wlewu do przestrzeni zewnątrzoponowej celem uzyskania skutecznej analgezji na poziomie Th3-Th2). Szybkość wlewu regulowano w zależności od aktualnego zapotrzebowania w granicach 3-7 ml/godzinę. Łącznie w trakcie zabiegu pacjentki otrzymały od 500 do 650 mg Ropiwakainy do przestrzeni zewnątrzoponowej. W żadnym przypadku nie przekroczono zalecanej dawki maksymalnej Ropiwakainy. Wszystkie pacjentki dobrze tolerowały podaną ilość leku znieczulenia miejscowego.
W drugim etapie operacji wycinano bliznę, odwarstwiano tkanki, preparowano naczynia piersiowe wewnętrzne lub ich perforatory w drugiej lub trzeciej przestrzeni międzyżebrowej. Wiązało się to z bardzo bolesnymi manipulacjami – usunięciem chrząstki trzeciego żebra. Dodatkowo preparowanie w tej okolicy wiązało się z dyskomfortem psychicznym i fizycznym pacjentek spowodowanym uciskaniem przez operatorów klatki piersiowej i okolicy szyi (żadna z pacjentek nie odczuwała bólu). Z tych powodów cztery z sześciu pacjentek wymagały pogłębienia sedacji poprzez podanie frakcjonowanych dawek Ketaminy (Ketanest, Pfizer) i/lub Propofolu (Propofol 1% MCT/LCT, Fresenius) oraz Fentanylu i.v. Było to łącznie 140-160 mg Ketaminy oraz 200 mg Propofolu (w dwóch przypadkach) i 0,2 mg Fentanylu (u 4 pacjentek).
W ostatnim etapie podwiązywano i przecinano naczynia szypuły płata, przenoszono go na klatkę piersiową, zespalano naczynia i modelowano tkanki, formując pierś.
Wszystkie pacjentki w trakcie zabiegu otrzymywały frakcjonowane dawki Midazolamu (Midanium, Polfa Warszawa SA) dożylnie (0,75-1,5 mg/godzinę, to jest odpowiednio dawki łączne od 10 do 16 mg).
Przez cały czas trwania zabiegu pacjentki pozostawały na oddechu spontanicznym z okresową suplementacją tlenu przez wąsy tlenowe.
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
24 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
59 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
119 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 28 zł
Piśmiennictwo
1. Cordeiro PG: Breast reconstruction after surgery for breast cancer. N Engl J Med 2008; 359: 1590-1601.
2. Rowland JH, Desmond KA, Meyerowitz BE et al.: Role of breast reconstructive surgery in physical and emotional outcomes among breast cancer survivors. J Natl Cancer Inst 2000; 92: 1422-1429.
3. Lynch EP, Welch KJ, Carabuena JM, Eberlein TJ: Thoracic epidural anesthesia improves outcome after breast surgery. Ann Surg 1995; 222(5): 663-669.
4. Belzarena SD: Comparative study between thoracic epidural block and general anesthesia for oncologic mastectomy. Rev Bras Anestesiol 2008; 58(6): 561-568.
5. Nociti JR, Serzedo PS, Zuccolotto EB, Gonzalez R: Thoracic epidural anesthesia with ropivacaine for plastic surgery. Rev Bras Anestesiol 2002; 52(2): 156-165.
6. McLeod G, Davies H, Munnoch N et al.: Postoperative pain relief using thoracic epidural analgesia: outstanding success and disappointing failures. Anaesthesia 2001; 56(1): 75-81.
7. McLeod GA, Cumming C: Thoracic epidural anaesthesia and analgesia. Contin Educ Anaesth Crit Care Pain 2004; 4(1): 16-19.
8. Manion SC, Brennan TJ: Thoracic Epidural Analgesia and Acute Pain Management. Anesthesiology 2011; 115(1): 181-188.
9. Steinestra R: The place of ropivacaine in anesthesia. Acta Anaesth Belg 2003; 54: 141-148.
10. Chen C, Nguyen MD, Bar-Meir E et al.: Effects of vasopressor administration on the outcomes of microsurgical breast reconstruction. Ann Plast Surg 2010; 65(1): 28-31.
11. Zhong T, Neinstein R, Massey C et al.: Intravenous fluid infusion rate in microsurgical breast reconstruction: important lessons learned from 354 free flaps. Plast Reconstr Surg 2011; 128(6): 1153-1160.
12. Srinivasa S, Tan ST: Postoperative fluid management in major elective plastic surgery. J Plast Reconstr Aesthet Surg 2010; 63: 992-995.
13. Holte K, Foss NB, Svensèn C et al.: Epidural anesthesia, hypotension, and changes in intravascular volume. Anesthesiology 2004; 100(2): 281-286.


