© Borgis - Nowa Pediatria 3/2014, s. 82-86
Karolina Raczkowska-Łabuda, Elżbieta Niemczyk, *Lidia Zawadzka-Głos
Pierwotna dyskineza rzęsek z perspektywy otolaryngologa dziecięcego
Primary ciliary dyskinesia from the paediatric laryngologist’s approach
Klinika Otolaryngologii Dziecięcej, Warszawski Uniwersytet Medyczny
Kierownik Kliniki: dr hab. n. med. Lidia Zawadzka-Głos
Summary
Primary ciliary dyskinesia (PCD), and in particular the Kartagener’s Syndrome, is rare disease of genetic origin, the most common autosomal recessive type of inheritance. Highly diversed manifestation of the disease depends in particular on the age of the patient. Symptoms are mostly related to the respiratory tract (nasal cavity, paranasal sinuses, Eustachian tube, middle ear, throat, trachea, bronchi and bronchioles), that results from impaired ciliary clearance mechanism. Kartagener’s Syndrome triad (chronic sinusitis, bronchiectasis and situs inversus totalis) origin of the cilia’s construction disorder. It was found that the mobility of these organelles determines the rotation of viscera during fetal development. Location of organs among children with defective cilia structure is random. Dextrocardia and situs inversus totalis occur among 50 percent of patients (probability of occurrence is equal to 0.5). Rapid diagnosis and appropriate management of the patient requires the cooperation of many specialists: pediatricians, allergists, pulmonologists, ENT or physiotherapists. No universal treatment algorithm for the PCD affected patients was developed yet. Many dissonant information regarding the PCD occur in the literature including not only the incidence but also recommended therapy. The treatment of chronic otitis with effusion is highly controversial. The article is based on a history of the disease of the 4.5-year-old boy with a Kartagener’s Syndrome. Case report includes the period up to the diagnosis, leading specialists and the OME treatment attitude in the Department of Pediatric Otolaryngology, Medical University of Warsaw.

WSTĘP
Pierwotna dyskineza rzęsek (PCD) to rzadki, uwarunkowany genetycznie zespół występujący z częstością 1:4000-1:40000 (1, 2). W praktyce lekarza występuje zdecydowanie rzadziej niż mukowiscydoza, co w pewnym stopniu tłumaczy późne rozpoznanie choroby. Oszacowano, że młody pacjent odwiedzi specjalistę około 50 razy, zanim zostanie postawiona prawidłowa diagnoza (3, 4). Szybkie rozpoznanie zespołu ma istotne znaczenie dla rokowania. Wcześnie podjęte właściwe leczenie z równoległym prowadzeniem fizjoterapii może znacząco zmniejszyć spadek rezerw układu oddechowego i powstrzymać rozwój rozstrzeni oskrzeli (5). Objęcie opieką laryngologiczną dzieci z upośledzonym w wyniku choroby słuchem bezpośrednio przekłada się na rozwój mowy i prawidłową adaptację psychospołeczną.
Łatwiej postawić poprawną diagnozę u tych pacjentów, którzy prezentują dekstrokardię i całkowite odwrócenie trzewi. W takim przypadku, w populacji dziecięcej, średni wiek rozpoznania choroby to 4,4 roku (5, 6). U około 25% pacjentów z situs inversus totalis lub heterotaksją występują również zaburzenia ruchu rzęsek (7). Stąd większość dostępnych w polskiej literaturze doniesień o zespole Kartagenera dotyczy dzieci.
OPIS PRZYPADKU
4,5-letni chłopiec, znajdujący się pod stałą opieką Poradni Pulmonologicznej i Laryngologicznej zgłosił się do Kliniki Otolaryngologii Dziecięcej Warszawskiego Uniwersytetu Medycznego z powodu chrapania, kilkusekundowych bezdechów i pogorszenia słuchu. W wywiadzie zgłoszono występowanie mokrego kaszlu od pierwszych godzin po narodzeniu, co było powodem wykonania zdjęcia rentgenowskiego klatki piersiowej już w trzeciej dobie życia (ryc. 1).
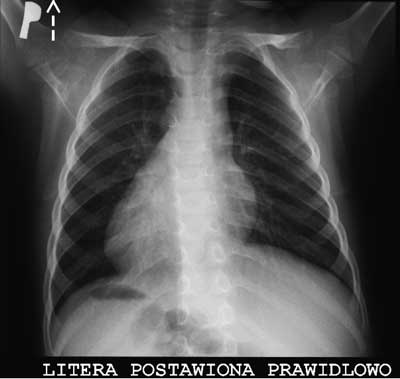
Ryc. 1. Zdjęcie rentgenowskie klatki piersiowej pacjenta z dekstrokardią i całkowitym odwróceniem trzewi.
W badaniu stwierdzono całkowite odwrócenie trzew nad- i podprzeponowe. Diagnostykę postnatalną uzupełniono o ultrasonografię jamy brzusznej, echokardiografię serca i elektrokardiogram metodą „lustrzanego odbicia” z ostatecznym wnioskiem: prawidłowa anatomia serca dziecka z całkowitym odwróceniem trzew. Wypisano do domu bez szczególnych zaleceń (ryc. 2).

Ryc. 2. Zapis Elektrokardiogramu metodą „lustrzanego odbicia” pacjenta z zespołem Kartagenera; zapis prawidłowy.
Po niecałych 4 miesiącach chłopiec był hospitalizowany na Oddziale Patologii Noworodka i Niemowlęcia ze względu na trwającą od 6 tygodni infekcję dróg oddechowych niepoddającą się leczeniu. Rozpoznano lewostronne zapalenie płuc, obturacyjne zapalenie oskrzeli oraz ostre zapalenie nosa i gardła. Po skutecznej dożylnej terapii cefuroksymem wypisano do domu ze skierowaniem do Poradni Alergologicznej. Efektem tej interwencji była ocena pobranych rzęsek w mikroskopie elektronowym (ryc. 3).

Ryc. 3. Przekrój poprzeczny przez rzęskę – brak obu ramion dyneinowych.
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
24 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
59 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
119 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 28 zł
Piśmiennictwo
1. Kuehni CE, Frischer T, Strippoli MP et al.: Factors influencing age at diagnosis of primary ciliary diskinesia in European children. Eur Respir J 2010; 36: 1248-1258. 2. Lucas JS, Walker WT, Kuehni CE et al.: Primary ciliary diskinesia. Courdier J-F, ed. Orphan lung diseases. Eur Resp Monogr 2011: 201-217. 3. Sommer JU, Schafer K, Omran H et al.: ENT manifestations in patients with primary ciliary diskinesia: prevalance and significance of otorhinolaryngologic comorbidities. Eur Arch Otorhinolaryng 2011; 268: 383-388. 4. Bajpai P, Singhai A, Bajpai I et al.: Kartagener’s syndrome: a case report. Int J Health Sci Res 2013; 3(12): 168-171. 5. Noone PG, Leigh MW, Sannuti A et al.: Primary ciliary diskinesia: diagnostic and phenotypic features. Am J Respir Crit Care Med 2004; 169: 459-467. 6. Barbato A, Frischer T, Kuehni CE et al.: Primary ciliary dyskinesia: a consensus statement on diagnostic and treatment approaches in children. Eur Respir J 2009; 34: 1264-1276. 7. Zhu L, Belmont JW, Ware SM: Genetics of human heterotaxis. Eur J Hum Genet 2006; 14: 17-25. 8. Bush A, Chodhari R, Collins N et al.: Primary ciliary dyskinesia: current state of the art. Arch Dis Child Dec 2007; 92(12): 1136-1140. 9. Lucas JS, Burgess A, Mitchison HM et al.: Diagnosis and management of primary ciliary dyskinesia. Arch Dis Child Apr 2014; 25. 10. O’Callaghan C, Chilvers M, Hogg C et al.: Diagnosing primary ciliary dyskinesia. Thorax 2007; 62: 656-657. 11. Coren ME, Meeks M, Morrison I et al.: Primary ciliary dyskinesia: age at diagnosis and symptom history. Acta Paediatr 2002; 91:667-669. 12. Van der Baan B: Ciliary function. Acta Oto-Rhino-Laryngologica Belg 2000; 54: 293-298. 13. Afzelius BA: A human syndrome caused by immotile cilia. Science 1976; 193:317-319. 14. Dębska M, Peradzyńska J, Chmielik M, Kulus M: Examination of the ultrastructure of the respiratory epithelium cilia in children with recurrent infection of the respiratory tract. New Med 2008; 3: 64-66. 15. Stannard WA, Chilvers MA, Rutman AR et al.: Diagnostic testing of patients suspected of primary ciliary dyskinesia. Am J Respir Crit Care Med 2010; 181:307-314. 16. Majithia A, Fong J, Hariri M et al.: Hearing outcomes in children with primary ciliary dyskinesia – a longitudinal study. Int J Pediatr Otorhinolaryngol 2005; 69: 1061-1064. 17. Bush A, Cole P, Hariri M et al.: Primary ciliary dyskinesia: diagnosis and standards of care. Eur Respir J 1998; 12: 982-988. 18. Hadfield PJ, Rowe-Jones JM, Bush A et.al.: Treatment of otitis media with effusion in children with primary ciliary dyskinesia. Clin Otolaryngol Allied Sci 1997; 22: 302-306. 19. Campbell RG, Birman CS, Morgan L: Management of otitis media with effusion in children with primary ciliary dyskinesia: a literature review. Int J Pediatr Otorhinolaryngol 2009; 73: 1630-1638. 20. el-Sayed Y, al-Sarhani A, al-Essa AR: Otological manifestations of primary ciliary dyskinesia. Clin Otolaryngol Allied Sci 1997; 22: 266-270. 21. Wolter NE, Dell SD, James AL et al.: Middle ear ventilation in children with primary ciliary dyskinesia. Int J Pediatr Otorhinolaryngol 2012; 76: 1565-1568.



