© Borgis - Postępy Nauk Medycznych 5/2015, s. 329-335
*Michał Studniarek1, Marek Durlik2, Jerzy Siekiera3, Katarzyna Gwoździewicz1, Katarzyna Skrobisz1, Joanna Pieńkowska4, Tomasz Gorycki5, Stanisław Hać6
Wskazania, przeciwwskazania i ryzyko związane z zabiegiem nieodwracalnej elektroporacji (IRE) u chorych z gruczolakorakiem trzustki – opis trzech przypadków i przegląd piśmiennictwa
Indications, contraindications and a risk related to irreversible electroporation (IRE) of pancreatic cancer – report of three cases and review of the literature
1Zakład Radiologii, Gdański Uniwersytet Medyczny
Kierownik Zakładu: prof. dr hab. med. Michał Studniarek
2Klinika Chirurgii Gastroenterologicznej i Transplantologii, Centralny Szpital Kliniczny Misterstwa Spraw Wewnętrznych i Administracji, Warszawa
Kierownik Kliniki: dr hab. med. Marek Durlik, prof. PAN
3Oddział Kliniczny Urologii Onkologicznej, Centrum Onkologii, Bydgoszcz
Kierownik Oddziału: dr med. Jerzy Siekiera
4II Zakład Radiologii, Gdański Uniwersytet Medyczny
Kierownik Zakładu: dr hab. med. Edyta Szurowska, prof. nadzw.
5Zakład Diagnostyki Obrazowej i Radiologii Interwencyjnej, Centrum Onkologii, Bydgoszcz
Kierownik Zakładu: dr med. Jadwiga Szabo-Moskal
6Klinika Chirurgii Ogólnej i Transplantacyjnej, Gdański Uniwersytet Medyczny
Kierownik Kliniki: prof. dr hab. med. Zbigniew Śledziński
Streszczenie
Celem pracy jest przeanalizowanie wskazań, przeciwwskazań i powikłań nieodwracalnej elektroporacji miejscowo zaawansowanego raka trzustki.
Przedstawiono trzy przypadki wykonania IRE w różnych sytuacjach klinicznych, kiedy zabieg zastosowano dla osiągnięcia indywidualnie określonego efektu.
W pierwszym przypadku wykonano śródoperacyjnie IRE raka trzustki T4 z przerzutem do wątroby (stadium IV), osiągając natychmiastowe i trwałe ustąpienie bólu oraz znaczącą redukcję wielkości guza utrzymującą się ponad 6 miesięcy. Przerzut do wątroby skutecznie zniszczono MWA.
W drugim przypadku zastosowano IRE w schyłkowym okresie choroby, po wyczerpaniu wszelkich możliwości leczenia onkologicznego, przy pełnym rozsiewie do węzłów chłonnych, jamy otrzewnej i wątroby, w celu zmniejszenia dolegliwości bólowych, trudnych do opanowania mimo zewnątrzoponowej blokady na poziomie piersiowym kręgosłupa. Rozległa cytoredukcja (bez powikłań miejscowych) nie doprowadziła do zmniejszenia bólu, ale chora przeżyła kolejne 4 miesiące.
W trzecim przypadku IRE wykonano u chorego w stadium III choroby, w trakcie chemioterapii gemcytabiną, uzyskując zmniejszenie masy guza i zmianę charakteru bólu. W trakcie leczenia zaobserwowano spadek stężenia Ca19-9 z 11 000 do 150 U/ml.
Stwierdzono, że sugerowane wskazania ograniczające zastosowanie IRE wyłącznie do stadium III raka trzustki nie są odpowiednie.
Summary
The purpose of the paper is the analysis of indications, contraindications and complications of irreversible electroporation (IRE) of locally advanced pancreatic cancer.
Report of three cases is presented where IRE was performed in three different types of indications.
In the first case IRE was applied during laparotomy in stage IV pancreatic cancer (T4N0M1). Immediate resolution of severe abdominal pain was observed. Significant tumor volume reduction is present after 6 months observation. Simultaneously liver metastasis was successfully ablated using MWA 2.45 GHz.
In the second case IRE was performed in locally advanced PCa stage IV (liver, lymph nodes and peritoneal metastases) due to reduct severe abdominal pain, uncontrolled even with the use of extradural anesthesia with catheter place at the level of Th8. Huge cytoreduction was received with no local complications, but without reduction of pain. Patients has survived 4 months more.
In the third case IRE was performer in stage III of PCa, just after the fourth cycle of gemcytabine treatment. At the begining serum level of Ca19-9 was 11 000 U/ml, after three cycles of chemotherapy 1700 U/ml, and after IRE the Ca19-9 concentration was 150 U/ml.
Indications for IRE proposed in the literature and limited to stage III of localle advanced PCa should be changed.

Wstęp
Rak trzustki jest nowotworem o fatalnym rokowaniu, z odsetkiem pięcioletnich przeżyć poniżej 5% (3,5-9%). Według Krajowego Rejestru Nowotworów w 2011 roku zanotowano 4448 zgonów (M = K) na raka trzustki, w tym ok. 90% u osób po 60. roku życia (1). Częstość zgonów wśród mężczyzn wynosi obecnie ok. 80/mln rocznie, a wśród kobiet ok. 50/mln. Podobną śmiertelność odnotowały pozostałe kraje Unii Europejskiej. W statystykach z lat 2010 i 2011 nowych zachorowań rejestruje się o 1/4 mniej niż liczba zgonów, co dowodzi całkowitej nieskuteczności współczesnej medycyny w leczeniu raka trzustki. Najczęściej przebieg choroby jest skryty, a rozpoznanie następuje w jej zaawansowanym stadium i zaledwie u 15-20% chorych możliwa jest resekcja guza (2). U pozostałych 80-85% naciekanie dużych naczyń i obecność odległych przerzutów oraz oporność na możliwe do zastosowania szeroko rozumiane leczenie onkologiczne pozwalają na przeżycie zaledwie kilku miesięcy. Sung-Sik i wsp. (3) przeanalizowali przeżycia chorych z rakiem trzustki w ich jednostce i stwierdzili 5-letnie przeżycie u 1,3% chorych (11 z 789 leczonych w latach 1985-1999, w tym 123 operowanych z intencją wyleczenia – dawniej R0). Pięcioletnie przeżycie u radykalnie zoperowanych chorych uzyskano u 12% pacjentów. W licznych publikacjach wyniki nie odbiegają znacząco od wyżej przytoczonych. Przebieg raka trzustki w późnym okresie jest bardzo szybki. Nie ma odpowiednich warunków do testowania nowych schematów leczenia i nowych chemioterapeutyków. Niektórzy autorzy donoszą o skuteczności nowych ChT (4), ale inni natychmiast reagują tonująco wobec tych doniesień (5). Podejmowano liczne próby lokalnej cytoredukcji dla uzyskania kontroli nad wzrostem guza. Testowano RFA, krioablację, MWA, LITT i HIFU. Doniesienia o skuteczności i częstości powikłań związanych z zastosowaną techniką są różnorodne i niejednoznaczne, od entuzjastycznych do bardzo krytycznych. Głównymi przyczynami słabych ocen są – od braku możliwości wykonania radykalnej ablacji nowotworu trzustki przez powikłania związane z termicznym uszkodzeniem naczyń i struktur przewodowych w polu trzustkowym, ostre krwotoczne i martwicze zapalenie trzustki, aż do wysokiej śmiertelności (6). Od 2005 roku pojawiają się doniesienia o nowej metodzie ablacji nowotworów, która nie jest związana z koagulacją termiczną. Jest to nieodwracalna elektroporacja (ang. nonthermal irreversible electroporation – NT IRE), wykorzystująca efekt trwałego wzrostu przepuszczalności błon komórkowych po zastosowaniu impulsów elektrycznych o wysokim gradiencie potencjału (prąd stały 1500 V/cm). Komórki tracą równowagę homeostatyczną i giną w wyniku mechanizmu zbliżonego do apoptozy (7). Nie dochodzi do uszkodzenia łącznotkankowego podścieliska, struktur tubularnych, naczyń i nerwów.
W kilku szpitalach w Polsce wykonano pierwsze zabiegi IRE zaawansowanych raków trzustki. W Szpitalu MSWiA w Warszawie oraz UCK w Gdańsku przeprowadzono zabiegi u 10 chorych z nowotworem trzustki w stadium III lub IV, jako metodę leczenia uzupełniającego w przebiegu standardowej terapii. Nie modyfikowano leczenia standardowego, ponieważ nie jest znana skuteczność nowej metody, nie wiadomo również, czy w jakimś sensie przewyższa leczenie chemiczne. Wszystkie zabiegi przedstawiane w niniejszej pracy wykonano po uzyskaniu zgody lokalnych Komisji Bioetycznych ds. Badań Naukowych.
Celem niniejszego opracowania jest analiza przebiegu ablacji za pomocą IRE raka trzustki u trzech wybranych chorych w krańcowo różnych okolicznościach klinicznych i przegląd piśmiennictwa dotyczącego potencjalnych i praktycznych skutków użycia prądu stałego o wysokim napięciu i natężeniu. Nieliczne doniesienia naukowe definiują optymalne, zdaniem autorów, wskazania do tej eksperymentalnej metody leczenia oraz opisują wczesne i bardziej odległe wyniki leczenia.
Przypadek 1
Chory lat 66 z guzem trzonu trzustki w stadium IV, z naciekiem pnia trzewnego i początkowego odcinka tętnicy wątrobowej oraz niedrożnością żyły śledzionowej i MPD. Zmiana ogniskowa o średnicy 4,5 cm naciekająca otoczenie z silnymi bólami typowymi dla raka trzustki. Zweryfikowana biopsją gruboigłową jako gruczolakorak przewodowy. W badaniu MRI uwidoczniono również 5 mm przerzut do segmentu IVb wątroby (ryc. 1a, b). W trakcie laparotomii potwierdzono brak możliwości resekcji guza i nieobecność innych zmian przerzutowych. Wykonano IRE zestawem sześciu elektrod wprowadzonych pod kontrolą śródoperacyjnej usg przy użyciu 6-igłowego stabilizatora, zakończoną cholecystektomią i MWA ogniska w wątrobie. Uzyskano praktycznie pełną ablację obu ognisk, z obecnością 7 mm resztkowej masy w miejscu nacieku obwodowej części MPD. Bezpośrednio po zabiegu ustąpiły dolegliwości bólowe. Chory rozpoczął ChT gemcytabiną. Po 6 miesiącach od zabiegu nie stwierdzono wznowy miejscowej ani rozsiewu odległego (ryc. 2a, b).
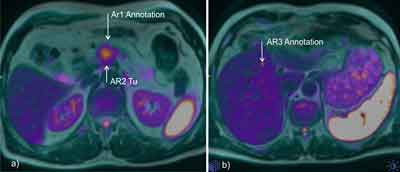
Ryc. 1. Przypadek 1. Fuzja obrazów MR w sekwencjach DWI i T2. a) Guz trzustki w stadium T4; b) przerzut do segmentu IV wątroby – stadium IV raka trzustki.
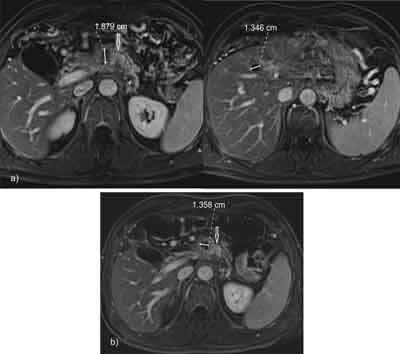
Ryc. 2. Przypadek 1. a) 3 miesiące po IRE. Obrazy MR 4 minuty po dożylnym podaniu środka kontrastującego w sekwencji T1 FS po subtrakcji: lewy – niewielka awaskularna poablacyjna strefa w trzustce (strzałka – poszerzony główny przewód trzustkowy), prawy – awaskularna strefa po ablacji mikrofalowej przerzutu do wątroby; b) 6 miesięcy po IRE (strzałka – poszerzony główny przewód trzustkowy). Bez cech wznowy.
Przypadek 2
Chora lat 35 ze wznową gruczolakoraka trzonu trzustki w stadium IV, po obwodowej resekcji trzustki i guza T3N1M0 (stadium IIb) 12 miesięcy wcześniej. Po operacji przeprowadzono typową ChT, a po 7 miesiącach od operacji wykonano również RT w dawce radykalnej – praktycznie bez efektu. W momencie IRE stwierdzono rozległą wznowę miejscową o średnicy 4 cm, niedrożność żyły wrotnej, liczne przerzuty w wątrobie, jamie otrzewnej i węzłach chłonnych (ryc. 3a, b). Zabieg wykonano z powodu silnych dolegliwości bólowych w celu ich opanowania. Rozległa cytoredukcja wykonana została pod kontrolą przezskórnej usg, z wielokrotnym repozycjonowaniem użytego zestawu elektrod. Uzyskano obszar ablacji mierzący ponad 5 cm średnicy, który objął całą masę odrastającego guza w miejscu operacji (ryc. 4a, b). Nie uzyskano ustąpienia bólu. Chora zmarła 4 miesiące później.
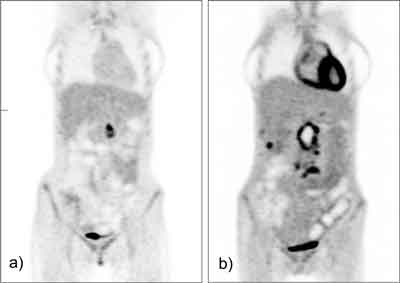
Ryc. 3. Przypadek 2. Obrazy 18F-FDG PET. a) 5 miesięcy po resekcji raka trzustki T3N1M0 i po pięciu cyklach chemioterapii standardowej – miejscowa wznowa T4N0M0; b) 6 miesięcy później po radykalnej radioterapii – progresja miejscowej wznowy z rozsiewem do węzłów chłonnych, jamy otrzewnej i wątroby T4N2M1 (stadium IV).
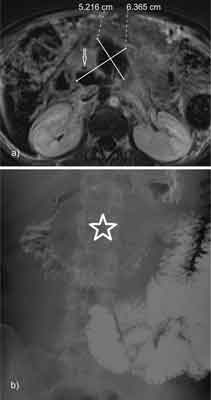
Ryc. 4. Przypadek 2. 30 dni po wielosesyjnej ablacji IRE z intencją opanowania ciężkiego bólu. a) Obrazy MR 4 minuty po dożylnym podaniu środka kontrastującego w sekwencji T1 FS po subtrakcji; rozległa awaskularna strefa po ablacji – średnicy 7 cm (strzałka – proteza w PŻW); b) pasaż przewodu pokarmowego po podejrzeniu podniedrożności w miejscu wznowy – prawidłowy obraz górnego odcinka przewodu pokarmowego (położenie wznowy – gwiazdka).
Przypadek 3
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
24 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
59 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
119 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 28 zł
Piśmiennictwo
1. Didkowska J, Wojciechowska U, Zatoński W: Cancer in Poland in 2011, KRN 2013.
2. Sener S, Fremgen A, Menck H, Winchester D: Pancreatic cancer: a report of treatment and survival trends for 100313 patients diagnosed from 1985-1995, using the National Cancer Database. ACS 1999; 189(1): 1-7.
3. Sung-Sik H, Jin-Young J, Sun-Whe K et al.: Analysis of long-term survivors after surgical resection for pancreatic cancer. Pancreas 2006; 32(3): 271-275.
4. Von Hoff D, Ervin T, Arena F et al.: Increased survival in pancreatic cancer with nab-Paclitaxel pluc Gemcytabine. NEJM 2013; 369(18): 1691-1703.
5. Saltz L, Bach P: Albumin bound Paclitaxel plus Gemcytabine in pancreatic cancer. Correspondence and authors reply. NEJM 2014; 370(5): 478-480.
6. Ikuta S, Kurimoto A, Iida H et al.: Optimal combination of radiofrequency ablation with chemotherapy for locally advanced pancreatic cancer. WJCO 2012; 3(1): 12-14.
7. Miller L, Leor J, Rubinsky B: Cancer cells ablation with irreversible electroporation. Technology in Cancer Research and Treatment 2005; 4: 1-6.
8. Martin R, McFarland K, Ellis S, Velanovich V: Irreversible electroporatin in locally advanced pancreatic cancer: Potential improved overall survival. Ann Surg Oncol 2013; 20(3): S443-449.
9. Martin R: Irreversible electroporation of locally advanced pancreatic head carcinoma. J Gastrointest Surg 2013; 17(10): 1850-1856.
10. Martin R, Philips P, Ellis S et al.: Irreversible electroporation of unresectable soft tissue tumors with vascular invasion: effective paliation. BMC Cancer 2014; 14(540): 1-9.
11. Moir J, White S, French J et al.: Systematic review of irreversible electroporation in the treatment of advanced pancreatic cancer. EJSO 2014; 40: 1598-1604.
12. Mir L, Orlowski S, Belehradek J, Paoletti C: Electrochemotherapy potentiation of antitumour effect of bleomycin by local electric pulses. Eur J Cancer 1991; 27(1): 68-72.
13. Sersa G, Miklavcic D, Cemazar M et al.: Electrochemotherapy in treatment of tumours. Eur J Surg Oncol 2008; 34(2): 232-240.
14. Arena C, Sano M, Rossmeisl J et al.: High-frequency irreversible electroporation (H-FIRE) for non-thermal ablation without muscle contraction. BioMedical Engineering OnLine 2011; 10: 102.




