© Borgis - Postępy Nauk Medycznych 8/2015, s. 611-614
Adam Tarkowski, Andrzej Głowniak, Anna Jaroszyńska, *Andrzej Wysokiński
Etiologia i patogeneza migotania przedsionków
Atrial fibrillation – etiology and pathogenesis
Chair and Department of Cardiology, Medical University, Lublin
Head of Department: prof. Andrzej Wysokiński, MD, PhD
Streszczenie
Migotanie i trzepotanie przedsionków są wciąż istotnym problemem klinicznym, społecznym i ekonomicznym w dzisiejszym systemie opieki zdrowotnej. Wiedza o ich etiologii i patogenezie pozostaje wciąż niepełna. Może to w pewien sposób tłumaczyć brak pełnej skuteczności obecnie stosowanych metod zapobiegania napadom tych arytmii, jak również wciąż niezadowalającą skuteczność leczenia. Poszukiwania czynników etiologicznych oraz prace nad mechanizmami prowadzącymi do epizodów migotania i trzepotania przedsionków pozwoliły zidentyfikować pewne stany kliniczne mogące sprzyjać pojawianiu się napadów arytmii, jak również prowadzić do przejścia ich w postać przewlekłą. Stres oksydacyjny, powiększenie i/lub rozciągnięcie przedsionków, przeładowanie kardiomiocytów jonami wapnia, mikro RNA, czynniki zapalne oraz aktywacja miofibroblastów wydają się być zaangażowane w procesy prowadzące do remodelingu przedsionków. Jedynie pełne poznanie związków zachodzących pomiędzy poszczególnymi mechanizmami może doprowadzić do stworzenia nowego celu prewencji i terapii migotania i trzepotania przedsionków oraz umożliwić skuteczniejsze kontrolowanie omawianych arytmii, a w konsekwencji znacząco poprawić jakość życia i sytuację zdrowotna pacjentów, których problem ten dotyczy. W niniejszej pracy przedstawiono najnowsze dane z zakresu etiologii i patofizjologii migotania i trzepotania przedsionków, jak również omówiono wzajemne zależności poszczególnych patomechanizmów.
Summary
Etiology and pathomechanisms of atrial fibrillation and atrial flutter are complicated and the knowledge about them still remains incomplete. This may be the reason why currently applied methods of prevention as well as treatment remain unsatisfied. A number of clinical situations were identified that may conduce to occurrence of atrial fibrillation and atrial flutter and also lead to chronic forms of arrhythmia. Oxidative stress, enlargement/extension of atrium, cardiomyocytes overloaded by calcium ions, microRNA, inflammative factors and miofibroblasts’ activation seem to be most engaged in process leading to atrial remodelling. Complete recognition of relationships between individual mechanisms may possibly enable to form new goals for prevention and therapy of atrial fibrillation and atrial flutter which may lead to better health and better quality of life in patients affected with the discussed heart arrhythmia. The paper presents the revision of current knowledge concerning etiology and pathophysiology of the above arrhythmia as well as explains relationships and interactions among particular mechanisms.

INTRODUCTION
Atrial fibrillation (AF) and atrial flutter (AFL) are the most common arrhythmias in clinical practice. These arrhythmias are the aim of the basic research and clinical studies for more than 100 years. Nevertheless, the mechanisms of AF/AFL initiations are still unknown and this may be the reason why prevention and treatment of these arrhythmias remain suboptimal.
Definitions
Atrial fibrillation is the most common supraventricular arrhythmia characterized by fast (350-700/min), electrically uncoordinated atrial activity which causes the loss of hemodynamic effective contraction of the atria. It is associated with irregular ventricular rate (fig. 1).
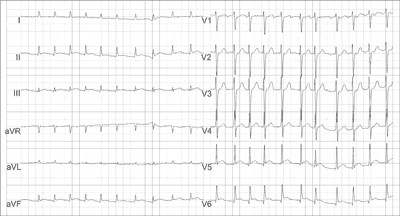
Fig. 1. Atrial fibrillation (AF).
Atrial flutter is defined as regular, fast rhythm with an atrial rate of 240-350 per minute which arises in the re-entry mechanism (fig. 2).
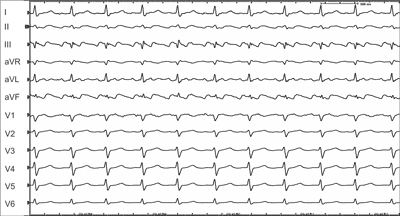
Fig. 2. Typical atrial flutter (AFL).
OCCURANCE
Atrial fibrillation poses one of the most common arrhythmia in clinical practice and often coexists with AFL (1-5). More than 6 million people in Europe suffer from AF. The incidence of this arrhythmia doubled in last five decades as a result of population ageing (6).
The incidence of AF/AFL increases with increasing age of patient – from < 0.5% at the age of 40-50 to 5-15% at the age of 80. It appears more common in women than the in men. The risk of AF in the people over 40 is about 25%. The incidence of AF is better known in caucasian race (6).
Predictive factors of AF/AFL are shown in table 1.
Table 1. Causes of AF/AFL.
| Cardiac factors | Noncardiac factors |
– Hypertension
– Valvular heart disease
(especially mitral valve
disease)
– Coronary heart disease
– Cardiomiopathies
– Congenital heart diseases
– Myocarditis and pericarditis
– History of cardiac surgery
– Brady-tachy syndrome
– Preexcitation
– Systemic diseases affecting
heart (ex. amyloidosis)
– Primary and metastatic heart
tumours | – Hyperthyreosis
– Obstructive sleep apnoea
– Acute infections
– General anaesthesia
– Pulmonary diseases
– Pheochromocytoma
– Alcohol, caffein, carbon
monoxide, drugs
(ex. β-mimetics)
– Diabetes
– Obesity
|
According the Polish Society of Cardiology (PTK) and European Society of Cardiology (ESC) (7), atrial fibrillation and atrial flutter can be divided in five types:
1. AF/AFL recognized for the first time – in the group of patients with the first episode of AF/AFL in life regardless of arrhythmia duration.
2. Paroxysmal AF/AFL – usually arrhythmia resolves by itself within 48 hour. It may last up to 7 days.
3. Persistent AF/AFL – usually arrhythmia lasts more than 7 days or requires pharmacological or electrical cardioversion (DCC).
4. Long-lasting persistent AF/AFL – arrhythmia lasting ≥ 1 year at the time of decision to return to sinus rhythm.
5. Permanent AF/AFL – arrhythmia accepted by patient and physician.
Atrial fibrillation and atrial flutter occurs as important clinical and population problem. It is responsible for increased risk of death, stroke, thromboembolic complications, development of heart failure, tachyarrhythmic cardiomyopathy, hospitalization and impairs quality of life. All patients from AF/AFL group need to be asses according to CHA2DS2-VASC score (8), in aspects of most common risk factor for stroke/TIA incidence in clinical practice, such as:
– Congestive heart failure,
– Hypertension,
– Age ≥ 75 years (2 pts),
– Diabetes,
– Stroke (2 pts)
– Vascular disease,
– Age 65-74 years,
– Sex category (female).
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
29 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
69 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
129 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 78 zł
Piśmiennictwo
1. Roithinger FX, Lesh MD: What is the Relationship of Atrial Flutter and Fibrillation? Pacing Clin Electrophysiol 1999; 22: 643-654.
2. Waldo AI, Cooper TB: Spontaneous onset of type I atrial flutter in patients. J Am Coll Cardiol 1996; 28: 707-712.
3. Waldo AL, Feld GK: Inter-Relationships of Atrial Fibrillation and Atrial Flutter: Mechanisms and Clinical Implications. J Am Coll Cardiol 2008; 51: 779-786.
4. Ortiz J, Niwano S, Abe H et al.: Mapping the conversion of atrial flutter to atrial fibrillation and atrial fibrillation to atrial flutter. Insights into mechanisms. Circ Res 1994; 74: 882-894.
5. Calo L, Lamberti F, Loricchio ML et al.: Atrial flutter and atrial fibrillation: which relationship? New insights into the electrophysiological mechanisms and catheter ablation treatment. Italian heart journal: official journal of the Italian Federation of Cardiology 2005; 6: 368-373.
6. Zipes DP, Jalife J: Cardiac Electrophysiology: From cell to bedside. Fifth edition. Saunders Elsevier, Philadelphia 2009.
7. European Heart Rhythm Association, European Association for Cardio-Thoracic Surgery, Camm AJ et al.: Guidelines for the management of atrial fibrillation: the Task Force for the Management of Atrial Fibrillation of the European Society of Cardiology (ESC). Eur Heart J 2010; 31: 2369-2429.
8. Wytyczne ESC dotyczące postępowania w migotaniu przedsionko?w na 2012 rok. Kardiol Pol 2012; 70: 197-234.
9. Yesilot Barlas N, Putaala J, Waje-Andreassen U et al.: Etiology of first-ever ischaemic stroke in European young adults: the 15 cities young stroke study. Eur J Neurol 2013; 20: 1431-1439.
10. Kirchhof P, Auricchio A, Bax J et al.: Outcome parameters for trials in atrial fibrillation: recommendations from a consensus conference organized by the German Atrial Fibrillation Competence NETwork and the European Heart Rhythm Association. Europace 2007; 9: 1006-1023.
11. Jalife J, Kaur K: Atrial remodeling, fibrosis, and atrial fibrillation. Trends Cardiovasc Med 2014; 31: S1050-1738(14)00253-9. doi: 10.1016/j.tcm. 2014.12.015. [Epub ahead of print].
12. Bonda T, Sobkowicz B, Winnicka M: Remodeling mięsnia sercowego w przebiegu tachyarytmii nadkomorowych. Kardiol Pol 2008; 66, 10 (supl. 3): 332-340.
13. Wijffels MC, Kirchhof CJ, Dorland R, Allessie MA: Atrial fibrillation begets atrial fibrillation. A study in awake chronically instrumented goats. Circulation 1995; 92: 1954-1968.
14. Ausma J, Litjens N, Lenders MH et al.: Time course of atrial fibrillation-induced cellular structural remodeling in atria of the goat. J Mol Cell Cardiol 2001; 33: 2083-2094.
15. Allessie M, Ausma J, Schotten U: Electrical, contractile and structural remodeling during atrial fibrillation. Cardiovasc Res 2002; 54: 230-246.
16. Neuberger HR, Schotten U, Blaauw Y et al.: Chronic atrial dilation, electrical remodeling, and atrial fibrillation in the goat. J Am Coll Cardiol 2006; 47: 644-653.
17. Iwasaki YK, Nishida K, Kato T, Nattel S: Atrial Fibrillation Pathophysiology Implications for Management. Circulation 2011; 124: 2264-2274.
18. Dobrev D, Nattel S: New insights into the molecular basis of atrial fibrillation: mechanistic and therapeutic implications. Cardiovasc Res 2011; 89: 689-691.
19. Wang L, Myles RC, De Jesus NM et al.: Optical mapping of sarcoplasmic reticulum Ca2+ in the intact heart: ryanodine receptor refractoriness during alternans and fibrillation. Circ Res 2014; 114: 1410-1421.
20. Martins RP, Kaur K, Hwang E et al.: Dominant frequency increase rate predicts transition from paroxysmal to long-term persistent atrial fibrillation. Circulation 2014; 129: 1472-1482.
21. Greiser M, Williams GS, Voigt N et al.: Tachycardia-induced silencing of subcellular Ca2+ signaling in atrial myocytes. J Clin Invest 2014; 124: 4759-4772.
22. Christ T, Engel A, Berk E et al.: Arrhythmias, elicited by catecholamines and seroto- nin, vanish in human chronic atrial fibrillation. Proc Natl Acad Sci U S A 2014; 111: 11193-11198.
23. Suarez G: Heart failure and galectin 3. Ann Transl Med 2014; 2: 86.
24. Ambros V: MicroRNA pathways in flies and worms: growth, death, fat, stress, and timing. Cell 2003; 113: 673-676.
25. Marian AJ: Recent developments in cardiovascular genetics and genomics. Circ Res 2014; 115: e11-17.
26. Dong S, Hao B, Hu F et al.: MicroRNA-21 promotes cardiac fibrosis and development of heart failure with preserved left ventricular ejection fraction by up-regulating BCL-2. Int J Clin Exp Pathol 2014; 7: 565-574.
27. LuY Z, Wang N, Pan Z et al.: MicroRNA-328 contributes to adverse electrical remodeling in atrial fibrillation. Circulation 2010; 122: 2378-2387.


