© Borgis - Nowa Pediatria 1/2016, s. 20-25
Izabela Janiec1, Beata Kucińska2, *Bożena Werner2
Drożny otwór owalny i ubytek przegrody międzyprzedsionkowej typu wtórnego – znaczenie i postępowanie u dzieci
Patent foramen ovale and secundum atrial septal defect – clinical implication and management in children
1Oddział Kliniczny Kardiologii i Pediatrii, Samodzielny Publiczny Dziecięcy Szpital Kliniczny, Warszawa
Kierownik Oddziału: prof. dr hab. n. med. Bożena Werner
2Klinika Kardiologii Wieku Dziecięcego i Pediatrii Ogólnej, Warszawski Uniwersytet Medyczny
Kierownik Kliniki: prof. dr hab. n. med. Bożena Werner
Summary
Foramen ovale is a very important part of fetal circulation. In postnatal life the closure occurs usually during the first 3 months. If is still present after the age of 3 months, the diagnosis of persistent foramen ovale (PFO) is established. Persistent foramen ovale is present in 25-30% of general population. It causes transient shunt between atrias due to insufficiency of foramen ovale valve. Children with uncomplicated PFO do not require any treatment nor pediatric cardiologist supervision.
Secundum atrial septal defect (ASD II) is one of the most common congenital heart defects. It is a communication between the atrias. Hemodynamically significant ASD leads to right atrial and right ventricular enlargement, dilatation of the pulmonary trunk and the increase of pulmonary to systemic flow ratio. In typical clinical course of isolated defects symptoms begin in adulthood and include fatigue, right ventricular failure, arrhythmia, and risk of pulmonary hypertension. Children usually are asymptomatic and even the defect with significant shunt may be diagnosed late. ASD II with hemodynamically significant shunt does not require urgent closure. Small defects are used to close spontaneously, bigger ones are rather prone to enlarge. The treatment of choice is percutaneous procedure. Surgical treatment can be indicated in infants and in patients with defects too big in size or with localization not suitable for interventional treatment.

Wstęp
Drożny otwór owalny jest pozostałością z życia płodowego. Komunikacja na poziomie przedsionków wynika z niedomykalności zastawki otworu owalnego. Przeciek krwi jest zazwyczaj śladowy, bez istotności hemodynamicznej. Występuje bardzo powszechnie, szacuje się, że nawet u około 1/3 dorosłej populacji. Nie jest wadą serca i nie wymaga leczenia. Współistnienie innych patologii z drożnym otworem owalnym, jak na przykład tendencja do nadkrzepliwości czy choroba kesonowa, sporadycznie mogą być jednak przyczyną powikłań i wskazaniem do rozważenia zamknięcia.
Ubytek przegrody międzyprzedsionkowej typu otworu wtórnego (ang. secundum atrial septal defect – ASD II) to jedna z najczęstszych wrodzonych wad serca. Jest to niesinicza wada serca należąca do grupy tak zwanych wad przeciekowych, do których zaliczane są także między innymi ubytek przegrody międzykomorowej i przetrwały przewód tętniczy. Polega na braku ciągłości przegrody międzyprzedsionkowej i bezpośredniej komunikacji pomiędzy lewym i prawym przedsionkiem, co powoduje lewo-prawy przepływ krwi zgodnie z różnicą ciśnień i zwiększony przepływ w krążeniu płucnym. Przebieg kliniczny u dzieci jest zazwyczaj łagodny, a rokowanie dobre. W pierwszych dwóch dekadach życia rzadko występują objawy. Większość ubytków przegrody międzyprzedsionkowej typu II leczy się metodą kardiologii interwencyjnej, rzadko wymagana jest operacja kardiochirurgiczna. W małych ubytkach istnieje możliwość samoistnego zamknięcia się lub zmniejszenia.
Drożny otwór owalny
Przegroda międzyprzedsionkowa składa się z dwóch części: grubszej górnej przegrody wtórnej (łac. septum secundum), tworzącej rąbek otworu owalnego, i dolnej przegrody pierwotnej (łac. septum primum), której wiotka górna część stanowi zastawkę otworu owalnego, dachówkowato nachodząc na górną część przegrody (ryc. 1).
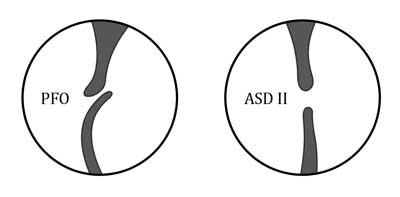
Ryc. 1. Schemat przegrody międzyprzedsionkowej z drożnym otworem owalnym (PFO) i ubytkiem międzyprzedsionkowym (ASD)
W życiu płodowym 90-95% krwi omija wysokooporowe krążenie płucne – ok. 1/3 przepływa z prawego do lewego przedsionka przez otwór owalny, pozostałe 2/3 przez przewód tętniczy. Po porodzie w ciągu kilku godzin dochodzi do wzrostu ciśnienia w lewym przedsionku ponad ciśnienie w prawym przedsionku, co powoduje dociśnięcie zastawki otworu owalnego do przegrody międzyprzedsionkowej i jej czynnościowe zamknięcie. Czynnikami, które mogą spowodować prawo-lewy przeciek krwi przez otwór owalny, są stany powodujące wzrost ciśnienia w prawym przedsionku i otwierające zastawkę otworu owalnego, takie jak: próba Valsalvy, zatrzymanie oddechu, kichanie, kaszel, wysokie ciśnienie w krążeniu płucnym wynikające z innych wad serca, nadciśnienia płucnego lub przyczyn pulmonologicznych (np. zespół zaburzeń oddychania). Zamknięcie anatomiczne zastawki otworu owalnego następuje do 2. roku życia, a pozostałością jest widziany od prawego przedsionka dół owalny (łac. fossa ovalis). Niemniej jednak u około 25-30% populacji dorosłych zachowana jest cały czas śladowa drożność przetrwałego otworu owalnego (ang. persistent foramen ovale, patent foramen ovale – PFO). Termin PFO używany jest po 3. miesiącu życia, wcześniej mówi się o otworze owalnym (łac. foramen ovale – FO).
Izolowany drożny otwór owalny nie jest związany z istotnym hemodynamicznie przeciekiem i nie powoduje przebudowy serca ani objawów klinicznych oraz nie wymaga leczenia i opieki kardiologicznej dzieci.
Lewo-prawy przeciek przez przetrwały otwór owalny może być większy niż śladowy u pacjentów z patologiami powodującymi rozciągnięcie przegrody międzyprzedsionkowej, np. przy powiększeniu lewego przedsionka obserwowanego w istotnym hemodynamicznie drożnym przewodzie tętniczym lub ubytku przegrody międzykomorowej, przy stenozie mitralnej lub aortalnej czy koarktacji aorty. Po korekcji tych wad i normalizacji zaburzeń hemodynamicznych zastawka otworu owalnego może się zamknąć, a przeciek zaniknąć.
W sytuacjach wyżej wymienionych, w których dochodzi do zwiększenia ciśnienia w prawym przedsionku, istnieje możliwość odwrócenia kierunku przepływu krwi z lewo-prawego na prawo-lewy. Wówczas obecny w krążeniu żylnym systemowym materiał zatorowy przez PFO może przedostać się do systemowego obwodowego układu tętniczego i stać się przyczyną zatoru skrzyżowanego i udaru kryptogennego, migrenowych bólów głowy oraz powikłań choroby kesonowej u nurków. Optymalne postępowanie w takich przypadkach nie jest w pełni ustalone. Decyzja o zamknięciu przetrwałego drożnego otworu owalnego u pacjentów z powikłaniami jest podejmowana indywidualnie.
Ubytki przegrody międzyprzedsionkowej
Ubytek przegrody międzyprzedsionkowej to wrodzona wada serca polegająca na braku ciągłości tkanki przegrody, co powoduje bezpośrednią komunikację pomiędzy prawym i lewym przedsionkiem. W zależności od umiejscowienia ubytku w przegrodzie międzyprzedsionkowej wyróżniamy kilka typów wady (ryc. 2). Najczęściej występującym (75%) typem ubytku przegrody międzyprzedsionkowej jest ubytek typu otworu wtórnego ASD II (łac. ostium secundum) zlokalizowany zwykle pośrodkowo w okolicy otworu owalnego. Najczęściej ubytek jest pojedynczy, ale może być mnogi. Ponadto może współwystępować tętniak całej przegrody międzyprzedsionkowej lub tylko dołu owalnego.
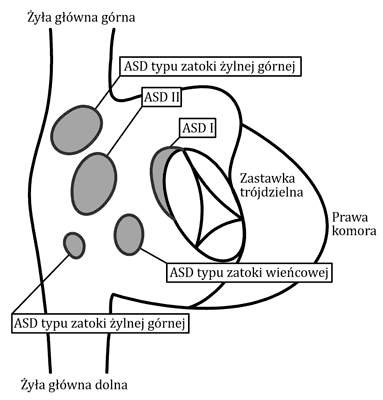
Ryc. 2. Typy ubytków przegrody międzyprzedsionkowej (ASD) – widok od strony prawego przedsionka
Znacznie rzadziej (15-20%) występuje ASD I – ubytek przegrody międzyprzedsionkowej typu I (łac. ostium primum), zlokalizowany w jej dolnej części. ASD I współistniejące z anomalią zastawki mitralnej jest nazywane częściowym ubytkiem przedsionkowo-komorowym (dawniej częściowy kanał przedsionkowo-komorowy). ASD I współistniejące z ubytkiem przegrody międzykomorowej i wspólną zastawką przedsionkowo-komorową to całkowity ubytek przegrody przedsionkowo-komorowej (dawniej zwany całkowitym kanałem). Najczęściej występuje u dzieci z trisomią 21 chromosomu.
Ubytki zlokalizowane w okolicy ujścia żył systemowych, tzw. ubytki typu zatoki żylnej (łac. sinus venosus), stanowią około 5-10% wszystkich połączeń międzyprzedsionkowych. Wiążą się zazwyczaj z częściowym nieprawidłowym spływem żył płucnych (ang. partial anomalus pulmonary venous drenage – PAPVD). Wada ta polega na ujściu prawych żył płucnych do prawego przedsionka lub do żyły głównej (częściej górnej, rzadziej dolnej) zamiast do lewego przedsionka.
Najrzadszym (< 1%) typem komunikacji międzyprzedsionkowej jest ubytek typu zatoki wieńcowej (łac. sinus coronarius), w którym brakuje stropu zatoki wieńcowej, dlatego inną stosowaną nazwą jest niezadaszona zatoka wieńcowa (ang. unroofed coronary sinus). W ubytku tym nie ma przerwania ciągłości przegrody międzyprzedsionkowej, a komunikacja pomiędzy lewym i prawym przedsionkiem odbywa się przez zatokę wieńcową. Wadzie tej zazwyczaj towarzyszy przetrwała lewa żyła główna górna (1).
Ubytek przegrody międzyprzedsionkowej typu otworu wtórnego – asd II
Ubytek przegrody międzyprzedsionkowej typu otworu wtórnego to jedna z najczęstszych wad serca. Stanowi ok. 5-10% wrodzonych wad serca jako wada izolowana, a jako składowa występuje aż u 30% dzieci ze złożonymi wadami serca. Częściej występuje u dziewczynek i dzieci o szczupłej budowie ciała.
Ubytek przegrody międzyprzedsionkowej typu II może występować w różnych zespołach genetycznych – w trisomii 21 chromosomu (zespół Downa), trisomii 18 chromosomu (zespół Edwardsa), trisomii 13 chromosomu (zespół Pataua), zespole Holt-Orama, zespole Noonan. Zidentyfikowano kilka genów związanych z ASD II: GATA4, TBX5, NKX2.5 (ASD II związane z blokiem przedsionkowo-komorowym) oraz ACT1, MYH6 i MYH7. Wada może występować rodzinnie, ale najczęściej ma charakter sporadyczny (2).
Zaburzenia hemodynamiczne
Ubytek przegrody międzyprzedsionkowej ASD II to niesinicza wada serca należąca do grupy tak zwanych przeciekowych wad serca.
Patofizjologia wady zależy głównie od wielkości przecieku przez przegrodę na poziomie przedsionków.
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
24 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
59 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
119 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 28 zł
Piśmiennictwo
1. Warnes CA, Wiliams RG, Bashore TM et al.: ACC/AHA 2008 Guidelines for the Management of Adults with Congenital Heart Disease: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (writing committee to develop guidelines on the management of adults with congenital heart disease). Circulation 2008; 118: e714-833. 2. Kuijpers JM, Mulder BJM, Bouma BJ: Secundum atrial septal defect in adults: a practical review and recent developments. Neth Heart J 2015; 23: 205-211. 3. Skiendzielewski J: Metody klinicznej oceny zaawansowania niewydolności serca u niemowląt z ubytkiem przegrody międzykomorowej. Nowa Pediatr 2013; 4: 135-142. 4. Martin SS, Shapiro EP, Mukherjee M: Atrial septal defects – clinical manifestations, echo assessment, and intervention. Clin Med Insights Cardiol 2015; 8 (suppl. 1): 93-98. 5. Fiszer R, Szkutnik M, Chodór B, Białkowski J: Spontaneous closure of a large atrial septal defect in an infant. Postępy Kardiol Interwencyjnej 2014; 10: 264-266. 6. Galea N, Grech V: Spontaneous closure of a large secundum atrial septal defect. Images Paediatr Cardiol 2002; 4: 21-29. 7. Park MK: Left-to-right shunt lesions. [In:] Park MK (ed.): Park’s Pediatric Cardiology for Practitioners. 6th Edition. Mosby Elsevier, United State of America 2008: 155-160. 8. Ooi YK, Kelleman M, Ehrlich A et al.: Transcatheter Versus Surgical Closure of Atrial Septal Defects in Children: A Value Comparison. JACC Cardiovasc Interv 2016; 9: 79-86. 9. Chen TH, Hsiao YC, Cheng CC et al.: In-Hospital and 4-Year Clinical Outcomes Following Transcatheter Versus Surgical Closure for Secundum Atrial Septal Defect in Adults: A National Cohort Propensity Score Analysis. Medicine (Baltimore) 2015; 94: e1524. 10. Kucinska B, Werner B, Wróblewska- -Kałużewska M: Assessment of right atrial and right ventricular size in children after percutaneous closure of secundum atrial septal defect with Amplatzer septal occluder. Arch Med Sci 2010; 6(4): 567-572. 11. Humenberger M, Rosenhek R, Gabriel H et al.: Benefit of atrial septal defect closure in adults: impact of age. Eur Heart J 2011; 32: 553-560. 12. Kucińska B: Ubytek przegrody międzyprzedsionkowej. [W:] Werner B (red.): Wady serca u dzieci dla pediatrów i lekarzy rodzinnych. Medical Tribune Polska, Warszawa 2015: 59-70.


