© Borgis - Medycyna Rodzinna 4/2016, s. 217-222
Jarosław Paprocki, Monika Gackowska, Marta Pawłowska, Alina Woźniak
Aktualne zastosowanie hiperbarii tlenowej
The current use of hyperbaric oxygen treatment
Katedra Biologii Medycznej, Uniwersytet Mikołaja Kopernika – Collegium Medicum w Bydgoszczy
Summary
The effect of the use of hyperbaric oxygen (HBO) on the human body. The course of treatment is described in detail with specified medical oxygen cycles. Also summarizes the indications, contraindications and possible complications of the use of this procedure in Practice of Medicine. The article also contains a list of centers in Poland dealing with hyperbaric medicine That has signed a contract with the National Health Fund.

Rys historyczny hiperbarii tlenowej
Hiperbaria tlenowa (ang. hyperbaric oxygen – HBO) jest to metoda leczenia urazów i chorób w komorze hiperbarycznej. Wykorzystuje ona ciśnienie wyższe od atmosferycznego. W trakcie zabiegu chorzy oddychają czystym, 100% tlenem. Uważa się, że ciśnienie wewnątrz komory powinno przewyższać 1,4 ATA. Wykorzystywane podczas zabiegów leczniczych w dostępnych obecnie komorach ciśnienie wynosi zazwyczaj 2,5 ATA (1, 2), dzięki temu można wielokrotnie zwiększyć ilość tlenu dostarczonego do komórek organizmu.
Początki wykorzystania tlenu hiperbarycznego w terapii chorych sięgają XVII wieku, kiedy to brytyjski lekarz i fizjolog C. Henshaw zaprojektował pierwszą komorę hiperbaryczną (3). Za ojca współczesnej hiperbarii tlenowej uważany jest holenderski chirurg I. Boerema. Przeprowadził on doświadczenie, w którym udowodnił, że do życia wystarczy tlen rozpuszczony fizycznie w surowicy krwi. Eksperyment ten polegał na kilkugodzinnym sprężeniu w komorze hiperbarycznej młodych świń, których krew pozbawiono hemoglobiny (4). W Polsce pionierami badań nad wpływem wysokiego ciśnienia na organizmy żywe byli J. Świątecki i F. Sulikowski, którzy w 1899 roku opisali zmniejszenie liczby erytrocytów u zwierząt doświadczalnych poddanych działaniu hiperbarii. W 1935 roku A. Oszacki otworzył pierwszy w Polsce oddział gazolecznictwa w Państwowym Szpitalu św. Łazarza w Krakowie. Dysponował on namiotami tlenowymi (leczono w nich mieszaninami gazowymi) oraz komorą hiperbaryczną, umożliwiającą leczenie pod ciśnieniem 2 ATA (5).
Mechanizm działania HBO
Tlen w warunkach hiperbarycznych jest dostarczany do komórek organizmu nie tylko przez utlenowanie hemoglobiny, ale i w postaci rozpuszczonej w osoczu krwi (6). Wykazano, że w jednym litrze surowicy krwi znajdują się 3 ml rozpuszczonego fizycznie tlenu. Wiadomym jest, że oddychając 100% tlenem w warunkach normobarii, wysycenie surowicy krwi tlenem wzrasta do 20 ml/l. Pełne zapotrzebowanie organizmu będącego w spoczynku na tlen można zrealizować, oddychając 100% tlenem w warunkach hiperbarii tlenowej, co prowadzi do wzrostu stężenia rozpuszczonego w surowicy tlenu do 50 ml/l (1, 2, 4, 6).
Przebieg zabiegu HBO
Typowy zabieg tlenoterapii w komorze hiperbarycznej składa się z trzech 20-minutowych cykli oddychania tlenem hiperbarycznym, rozdzielonych 5-minutowymi przerwami oddychania powietrzem (ryc. 1). Łączny czas oddychania tlenem hiperbarycznym wynosi 60 min na ekspozycję. Zabieg obejmuje również dwa dziesięciominutowe okresy kompresji oraz dekompresji, podczas których chorzy oddychają powietrzem. Okresy te znajdują się odpowiednio na początku i na końcu zabiegu.
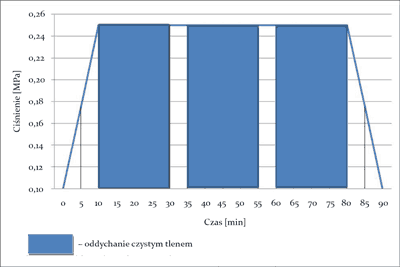
Ryc. 1. Schemat przebiegu leczniczego w komorze hiperbarycznej
Komory hiperbaryczne – rodzaje i zastosowanie
W terapii hiperbarycznej zastosowanie mają komory jedno- lub wielomiejscowe oraz worki Gamowa (7).
Komory jednomiejscowe (ang. monoplane) występują w różnych kształtach. Wyróżniamy komory cylindryczne (chory przebywa w pozycji horyzontalnej) oraz kuliste (pacjent leczony jest w pozycji siedzącej). Wykorzystanie komór typu monoplace związane jest głównie z leczeniem oparzeń twarzy oraz szyi. Chorym nie zakłada się maski na twarz (której zastosowanie jest konieczne w komorach wielomiejscowych) (1, 2, 7). Zabiegi w komorze jednomiejscowej mogą być stosowane tylko u osób stabilnych krążeniowo i oddechowo.
Komory wielomiejscowe (multiplace) są wykorzystywane do leczenia w tym samym czasie dwóch lub większej liczby chorych (ryc. 2). Tlen wdychany jest poprzez specjalną maskę, która szczelnie przywiera do twarzy. Wnętrze komory wypełnia powietrze pod zwiększonym ciśnieniem (1, 2, 7).

Ryc. 2. Komora hiperbaryczna typu multiplace, Mazowieckie Centrum Terapii Hiperbarycznej i Leczenia Ran (fot. J. Paprocki)
Worek Gamowa jest to nadmuchiwany worek służący między innymi do leczenia choroby wysokościowej, poprzez utrzymanie chorego w warunkach podwyższonego ciśnienia. Worki te wykorzystuje się głównie w punktach medycznych położonych na dużej wysokości nad poziomem morza. Wykorzystywane są również w leczeniu uzdrowiskowym oraz komercyjnym (7).
Wskazania oraz przeciwwskazania do leczenia w komorze hiperbarycznej
Lista wskazań oraz przeciwwskazań do stosowania HBO została ustalona w roku 2013 przez European Committee of Hyperbaric Medicine (ECHM) (tab. 1).
Tab. 1. Wskazania do leczenia hiperbarycznego refundowane przez NFZ (8)
| Jednostki chorobowe o przebiegu ostrym | – choroba dekompresyjna,
– zatory gazowe,
– zatrucie tlenkiem węgla,
– martwicze zakażenie tkanek miękkich (beztlenowe i mieszane),
– ostre niedokrwienie tkanek miękkich,
– uraz mięśniowo-szkieletowy,
– uraz wielonarządowy – zespoły kompartmentalne i następstwa urazów zmiażdżeniowych,
– oparzenia termiczne (II stopień > 10% u dzieci i III stopień > 20% u dorosłych),
– nagła głuchota idiopatyczna,
– głuchota po urazie akustycznym |
| Schorzenia przewlekłe | – popromienne uszkodzenie tkanek i narządów,
– zespół stopy cukrzycowej,
– zakażenie, martwica kikuta po amputacji,
– zapalenie skóry i tkanki podskórnej,
– rozlane, złośliwe zapalenie ucha zewnętrznego,
– owrzodzenia odleżynowe,
– zapalenie i martwica kości,
– przeszczepy skóry zagrożone martwicą,
– rekonstrukcja tkanek zagrożona martwicą,
– zakażenie rany pourazowej,
– zapalenie mostka, śródpiersia pooperacyjne, niestabilność mostka, ropnie |
Wskazaniem do HBO są m.in.: choroba dekompresyjna, zatorowość powietrzna lub inna gazowa, zatrucie tlenkiem węgla, zator naczyń siatkówki, zgorzel gazowa, martwicze zakażenia tkanek miękkich, urazy wielonarządowe oraz oparzenia termiczne. W stanach ciężkich warunkiem skutecznego leczenia jest odpowiednio szybkie podjęcie terapii tlenem hiperbarycznym. Wymagany jest bezzwłoczny transport chorego do specjalistycznych ośrodków, najlepiej w czasie 3-5 godzin od wystąpienia pierwszych objawów (7).
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
24 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
59 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
119 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 28 zł
Piśmiennictwo
1. Jain KK: Textbook of hyperbaric medicine. Wyd. 4. Hogrefe & Huber Publishers, Göttingen 2004. 2. Mathieu D: Handbook on hyperbaric medicine. Springer, Dordecht 2006. 3. Narożny W, Siebert J: Możliwości i ograniczenia stosowania hiperbarii tlenowej w medycynie. Forum Med Rodz 2007; 1(4): 368-375. 4. Boerema I, Meyne N, Brummelkamp W et al.: Life without blood: a study of the influence of high atmospheric pressure and hypothermia on dilution of the blood. J Cardiovasc Surg 1960; 1: 133-146. 5. Streszczenie IX konferencji Polskiego Towarzystwa Medycyny i Techniki Hiperbarycznej. Sopot 1-2 grudnia 2007. PHR 2007; 4(24): 57-74. 6. Konturek S: Fizjologia człowieka – podręcznik dla studentów medycyny. Wyd. 1. Elsevier Urban & Partner, Wrocław 2007. 7. Sieroń A, Cieślar G, Kawecki M: Zarys medycyny hiperbarycznej. α-Medica Press, Bielsko-Biała 2006. 8. Zarządzenie Prezesa Narodowego Funduszu Zdrowia Nr 88/2013/DSOZ z dnia 18 grudnia 2013 r. w sprawie określenia warunków zawierania i realizacji umów w rodzaju świadczenia zdrowotne kontraktowane odrębnie. 9. Sheffield P, Heimbach R: The physican and chamber safety. Hyperbaric and Undersea Medicine. Vol. 1. Medical SEMINARS, San Antonio 1981. 10. Boussuges A, Blanc P, Molenat F: Prognosis in iatrogenic gas embolism. Minerva Med 1995; 86: 453-457. 11. Abramovich A, Shupak A, Ramon Y et al.: Hyperbaric oxygen for carbon monoxide poisoning. Harefuah 1997; 132: 21-24. 12. Guzman J: Carbon monoxide poisoning. Crit Care Clin 2012; 28: 537-548. 13. Norkool D, Kirkpatrick J: Treatment of acute carbon monoxide poisoning with hyperbaric oxygen. A review of 115 cases. Ann Emerg Med 1985; 14: 1168-1171. 14. Korhonen K: Hyperbaric oxygen therapy in acute necrotizing infections with a special reference to the effects on tissue gas tensions. Ann Chir Gynaecol 2000; 214: 7-36. 15. Wilkinson D, Doolette D: Hyperbaric oxygen treatment and survival from necrotizing soft tissue infection. Arch Surg 2004; 139: 1339-1345. 16. Grzybowski J: Biologia rany oparzeniowej. Wyd. 1. α-Medica Press, Bielsko-Biała 2001. 17. Constant J, Suh D, Hussain M et al.: Wound healing angiogenesis: the metabolic basis of repair. Plenum Press, New York 1996: 151-159. 18. Winter G, Perrins D: Effect of hyperbaric oxygen treatment on epidermal regeneration. Tokyo Igaku Shoin Ltd., Tokyo 1970. 19. Radović V, Barić D, Petricević A et al.: War injuries of the crural artieries. Br J Surg 1995; 82: 777-783. 20. Jacey M, Tappan D, Kifzler K: Hematologic responses to severe decompression stress. Aerospace Mede 1974; 45: 417-421. 21. Cianci P, Lueders H, Lee H et al.: Adjunctive hyperbaric oxygen reduced the need for surgery in 40-80% burns. J Hyperb Med 1988; 3: 97-171. 22. Maxwell G, Meites H, Silvertein P: Cost effectiveness of hyperbaric oxygen therapy in burn care. Winter Symposium on Baromedicine 1991. 23. Jadczak M, Rapiejko P, Kantor I et al.: Ocena wyników leczenia nagłej głuchoty idiopatycznej z zastosowaniem terapii tlenem hierbarycznym. Otolaryngol Pol 2007; 61: 887-891. 24. Narożny W: Hiperbaria tlenowa w patologii ucha wewnętrznego – fakty i mity. Otolar Pol 2006; 5: 153-161. 25. Fagan P, McKenzie B, Edmonds C: Sinus barotrauma in divers. Ann Otol Rhinol Laryng 1976; 85: 61-64. 26. Capes J, Tomaszewski C: Prophylaxis against middle ear barotrauma in US hyperbaric oxygen therapy center. Am J Emerg Med 1996; 14: 645-648. 27. Grzegorz B: Druga twarz tlenu. Wydawictwo Naukowe PWN, Warszawa 1995. 28. Takahashi H, Kobayashi S: New indications for hyperbaric oxygen therapy and its complication. Adv Otorhinolaryngol 1998; 54: 1-13. 29. Asadamongkol B, Zhang J: The development of hyperbaric oxygen therapy for skin rejuvenation and treatment of photoaging. med. Gas Res 2014; 4: 1-7. 30. John B, Chamilos G, Kontoyiannis D: Hyperbaric oxygen as an adjunctive treatment for zygomycosis. Clin Microbiol Infect 2005; 11: 515-517. 31. Bennett M, Jepson N, Lehm J: Hyperbaric oxygen therapy for acute coronary syndrome. Cochrane Database Syst Rev 2015; 7(23): CD004818. 32. Ingvar H, Lessen N: Treatment of focal cerebral ischemia with hyperbaric oxygen. Acta Neurol Scand 1965; 41: 92-95.


