*Elżbieta Wawrzyniak-Dzierżek1, Agnieszka Pomykała-Słupianek1, Grażyna Wróbel1, Kornelia Gajek1, Jowita Frączkiewicz1, Małgorzata Salamonowicz1, Katarzyna Bąbol-Pokora2, Marek Ussowicz1
Trudności diagnostyczne i lecznicze w małopłytkowości opornej na leczenie – opis przypadku
Diagnostic and therapeutic difficulties in a refractory thrombocytopenia – a case report
1Klinika Transplantacji Szpiku, Onkologii i Hematologii Dziecięcej, Uniwersytet Medyczny im. Piastów Śląskich we Wrocławiu
Kierownik Kliniki: prof dr hab. n. med. Alicja Chybicka
2Klinika Pediatrii Onkologii i Hematologii, Uniwersytet Medyczny w Łodzi
Kierownik Kliniki: prof. dr hab. n. med. Wojciech Młynarski
Summary
The most common cause of thrombocytopenia in children is the immune thrombocytopenia, diagnosed in case of typical clinical manifestation and after exclusion of other background. In the case of refractory immune thrombocytopenia, the diagnostic approach should be expanded due to possible other etiology. In the new-born male, thrombocytopenia was discovered immediately after birth. The pregnancy was uncomplicated, and the family did not reveal significant morbidities. During the work-up, the most common causes of thrombocytopenia in neonatal age were excluded, including infectious background, fetal hypoxia, alloimmune thrombocytopenia, and myeloproliferative diseases. The patient was treated according to the recommendations for the management of immune thrombocytopenia, but did not achieve normalization of the platelet number. The genetic testing identified a mutation in the WAS gene (new pathogenic variant NM_000377.2: c.274-1G > A – splice acceptor variant), which allowed to establish the Wiskott-Aldrich syndrome diagnosis. The described case reminds the need for in-depth diagnostics in patients with therapy resistant immune thrombocytopenia.

Wstęp
Według definicji o małopłytkowości mówimy, gdy liczba płytek krwi spada poniżej 100 x 109/l. Najczęstszą postacią u dzieci jest małopłytkowość immunologiczna (ang. idiopathic thrombocytopenic purpura – ITP) wynikająca z obecności auto- lub alloprzeciwciał przeciwpłytkowych. Zgodnie z kryteriami ITP stanowi izolowany problem, bez współistnienia innych odchyleń w morfologii krwi (1). Diagnostyka małopłytkowości immunologicznej w okresie noworodkowym jest diagnostyką przez wykluczanie jednostek chorobowych mogących stanowić inne prawdopodobne przyczyny wyszczególnione w tabeli 1.
Tab. 1. Przyczyny małopłytkowości w okresie noworodkowym (na podstawie (2))
| Przyczyna | Częstość występowania (%) |
| Sepsa | 47 |
| Niedotlenienie płodu | 25 |
| Martwicze zapalenie jelit | 4,1 |
| Anomalie chromosomalne | 3,9 |
| Choroba hemolityczna noworodka | 2,4 |
| Infekcja cytomegalowirusowa | 2,4 |
| Choroby rozrostowe szpiku | 1,6 |
| Noworodkowa małopłytkowość alloimmunologiczna | 1 |
| Inne | 1,5 |
Postępowanie w przypadku małopłytkowości immunologicznej u dzieci zależy od stanu pacjenta, charakteru skazy i może polegać na przyjęciu postawy obserwacyjnej lub aktywnym leczeniu. Większość przypadków ITP ulega samoistnemu wyleczeniu, a zastosowanie terapii ma znaczenie w skróceniu okresu małopłytkowości i zmniejszeniu ryzyka wystąpienia przewlekłej małopłytkowości (3, 4) (ryc. 1).
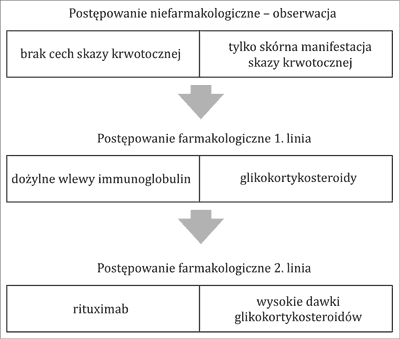
Ryc. 1. Postępowanie w małopłytkowości immunologicznej u dzieci (na podstawie (1))
W niewielkim odsetku pacjentów z małopłytkowością obserwuje się złą odpowiedź na leczenie. W razie braku remisji, nawrotów choroby lub oporności na podstawową terapię za pomocą glikokortykosteroidów lub dożylnych wlewów immunoglobulin wskazane jest zastosowanie kolejnych linii leczenia. Metody terapeutyczne w opornej małopłytkowości zależą w dużym stopniu od rozwiązań systemowych, doświadczeń lekarza i czynników leżących po stronie rodziny (5). Szeroko rekomendowaną i akceptowaną nowoczesną opcją leczniczą jest zastosowanie eltrombopagu, który jest lekiem o wielokierunkowym działaniu, wysokiej skuteczności i korzystnym profilu bezpieczeństwa w leczeniu przewlekłej małopłytkowości (6, 7).
W przypadku małopłytkowości immunologicznej opornej na leczenie, po przeprowadzeniu rozszerzonej diagnostyki możliwa jest zmiana rozpoznania. Istotnym elementem algorytmu diagnostycznego jest również wiek pacjenta i przy małopłytkowości u noworodka nieodpowiadającej na standardowe leczenie należy rozważyć w diagnostyce różnicowej również przyczyny wrodzone (8). Lee z Singapuru opublikował wyniki, z których wynika, że nawet u 10% dzieci, u których pierwotnie rozpoznano izolowaną małopłytkowość, ostatecznie odnaleziono inną przyczynę obniżonej liczby płytek (9).
Opis przypadku
Przedstawiamy przypadek noworodka płci męskiej z ciąży drugiej, porodu drugiego, urodzonego przez cięcie cesarskie. U rodziców nie stwierdzono istotnych schorzeń, a wywiad rodzinny nie wykazał obciążeń. Okres ciąży był niepowikłany, matka nie przyjmowała w tym okresie żadnych leków. Dziecko po urodzeniu było w dobrym stanie ogólnym i otrzymało 10 punktów w skali Apgar, a w badaniu fizykalnym nie wykazano odchyleń. W rutynowych badaniach laboratoryjnych bezpośrednio po urodzeniu stwierdzono małopłytkowość 30 x 109/l.
Podczas diagnostyki przeprowadzonej na oddziale noworodkowym wykluczono infekcję wewnątrzmaciczną – wyniki testów w kierunku kiły, wrodzonego zespołu TORCH, wirusowego zapalenia wątroby oraz HIV były ujemne. W toku diagnostyki stwierdzono niezgodność antygenową pomiędzy dzieckiem a matką (w zakresie antygenów płytkowych HPA-3 i HPA-15), jednak nie wykryto przeciwciał przeciwpłytkowych. W związku z podejrzeniem immunologicznego tła małopłytkowości już na oddziale neonatologicznym czterokrotnie podano dożylny wlew immunoglobulin, a później glikokortykosteroidy (początkowo dożylnie metyloprednizolon, następnie doustnie prednizon). Ze względu na utrzymującą się małopłytkowość pacjent w wieku 3 miesięcy trafił pod opiekę kliniki hematologii.
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
24 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
59 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
119 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 28 zł
Piśmiennictwo
1. Neunert C, Lim W, Crowther M et al.: Review article The American Society of Hematology 2011 evidence-based practice guideline for immune thrombocytopenia. Blood 2018; 117(16): 4190-4208.
2. Resch E, Hinkas O, Urlesberger B et al.: Neonatal thrombocytopenia – causes and outcomes following platelet transfusions. Eur J Pediatr 2018; 177(7): 1045-1052.
3. Heitink-Pollè KMJ, Uiterwaal CSPM, Porcelijn L et al.: Intravenous immunoglobulin vs observation in childhood immune thrombocytopenia: a randomized controlled trial. Blood [Internet] 2018; 132(9): 883-891.
4. Bennett CM, Neunert C, Grace RF et al.: Predictors of remission in children with newly diagnosed immune thrombocytopenia: Data from the Intercontinental Cooperative ITP Study Group Registry II participants. Pediatr Blood Cancer [Internet] 2018; 65(1): e26736.
5. Grace RF, Despotovic JM, Bennett CM et al.: Physician decision making in selection of second-line treatments in immune thrombocytopenia in children. Am J Hematol [Internet] 2018; 93(7): 882-888.
6. Kim TO, Despotovic J, Lambert MP: Eltrombopag for use in children with immune thrombocytopenia. Blood Adv [Internet] 2018; 2(4): 454-461.
7. Guo J-C, Zheng Y, Chen H-T et al.: Efficacy and safety of thrombopoietin receptor agonists in children with chronic immune thrombocytopenia: a meta-analysis. Oncotarget [Internet] 2018; 9(6): 7112-7125.
8. Sharma R, Botero JP, Jobe SM: Congenital Disorders of Platelet Function and Number. Pediatr Clin North Am 2018; 65: 561-578.
9. Lee AC: Isolated thrombocytopenia in childhood: what if it is not immune thrombocytopenia? Singapore Med J 2018; 59(7): 390-393.
10. Roberts I, Stanworth S, Murray NA: Thrombocytopenia in the Neonate. Blood Rev 2008; 22(4): 173-186.
11. Carr R, Kelly M, Williamson LM: Neonatal Thrombocytopenia and Platelet Transfusion – A UK Perspective. Neonatology 2015; 107(1): 1-7.
12. Tadashi A, Masafumi Y, Florecita P et al.: Detection of a novel splice-site mutation that results in skipping exon 3 of the WASP gene in a patient with Wiskott-Aldrich syndrome. Biochimica et Biophysica Acta 1996; 1317; 158-160.
13. Massaad MJ, Ramesh N, Geha RS: Wiskott-Aldrich syndrome: a comprehensive review. Ann N Y Acad Sci 2013; 1285: 26-43.
14. Medina SS, Siqueira LH, Colella MP et al.: Intermittent low platelet counts hampering diagnosis of X-linked thrombocytopenia in children: report of two unrelated cases and a novel mutation in the gene coding for the Wiskott-Aldrich syndrome protein. BMC Pediatr [Internet] 2017; 17(1): 151.
15. Kaneko R, Yamamoto S, Okamoto N et al.: Wiskott-Aldrich syndrome that was initially diagnosed as immune thrombocytopenic purpura secondary to a cytomegalovirus infection. SAGE Open Med Case Reports [Internet] 2018; 6: 2050313X17753788.
16. Oved JH, Lee CSY, Bussel JB: Treatment of Children with Persistent and Chronic Idiopathic Thrombocytopenic Purpura: 4 Infusions of Rituximab and Three 4-Day Cycles of Dexamethasone. J Pediatr [Internet] 2017; 191: 225-231.
17. Yoshihara H, Arai F, Hosokawa K et al.: Thrombopoietin/MPL Signaling Regulates Hematopoietic Stem Cell Quiescence and Interaction with the Osteoblastic Niche. Cell Stem Cell [Internet] 2007; 1(6): 685-697.
18. Tanaka T, Inamoto Y, Yamashita T et al.: Eltrombopag for Treatment of Thrombocytopenia after Allogeneic Hematopoietic Cell Transplantation. Biol Blood Marrow Transplant [Internet] 2016; 22(5): 919-924.

