*Halina Ekiert1, Agnieszka Sondej1, Marta Klimek-Szczykutowicz1, Radosław J. Ekiert2, Agnieszka Szopa1
Nowe surowce roślinne w Farmakopei Europejskiej. Cz. 2. Rozwar wielkokwiatowy (Platycodon grandiflorus) – źródło nowego surowca saponinowego
The new plant raw materials in the European Pharmacopoeia. Part 2. Balloon flower (Platycodon grandiflorus) – new saponin raw material
1Katedra i Zakład Botaniki Farmaceutycznej, Wydział Farmaceutyczny, Uniwersytet Jagielloński – Collegium Medicum, Kraków
Kierownik Katedry i Zakładu: prof. dr hab. n. farm. Halina Ekiert
2KZZ Herbapol SA w Krakowie
Streszczenie
W jednym z najnowszych suplementów do Farmakopei Europejskiej (Supl. 9.4) figuruje kilka nowych roślinnych surowców leczniczych, nieznanych i niewykorzystywanych do tej pory w oficjalnym lecznictwie w Europie Środkowej. W pierwszej części zaplanowanej serii artykułów przedstawiono walory lecznicze gatunków z rodzaju Bupleurum (Przewiercień), które są źródłem nowego surowca saponinowego. Część druga poświęcona jest charakterystyce botanicznej, ekologicznej i chemicznej Platycodon grandiflorus – Rozwaru wielkokwiatowego. Gatunek ten dostarcza również nowego surowca saponinowego (Platycodi radix). Znaczna część artykułu poświęcona jest przeglądowi różnych zastosowań terapeutycznych surowca, potwierdzonych badaniami naukowymi. W artykule podkreślono, że surowiec ten od dawna ma utrwaloną pozycję w tradycyjnej medycynie chińskiej. Ponadto zwrócono uwagę na fakt, że od ok. 20 lat ma on monografię World Health Organization (WHO). Zasygnalizowano także rolę rozwaru w produkcji żywności i kosmetyków. Zadaniem artykułu jest przybliżenie podstawowych informacji o tym gatunku w środowisku farmaceutyczno-lekarskim.
Summary
In the one of the last supplements to the European Pharmacopoeia (Supl. 9.4) figures several herbal medicinal raw materials, so far unknown and not used in official Central European phytotherapy. In the first part of planed article series, the therapeutic values of species from Bupleurum genus, which are a new saponin providing raw materials, were presented. The second part is devoted to the botanical, ecological and chemical characteristics of Platycodon grandiflorus (balloon flower). This species also provides the new saponin raw material – Platycodi radix. The major part of the article is concerned to the review of different therapeutic applications of that raw material confirmed by the scientific researches. In the article the well established use in the traditional chinese medicine was emphasized. Moreover, the attention was paid also on the fact, that for about 20 years, plant has had the World Health Organization (WHO) monograph. In addition, the importance of the plant in the food and cosmetic industry was pointed. The aim of the article is familiarization with the basic knowledge about this species in the pharmaceutical and medical environment.

Wstęp
W wyniku powszechnej globalizacji obserwuje się w ostatnim 10-leciu wyraźny wzrost oferty fitoterapeutycznej w Europie. Do oficjalnego lecznictwa europejskiego wprowadzane są liczne gatunki roślin od dawna znane i wykorzystywane w celach leczniczych na innych kontynentach. Szczególnie duża liczba nowych gatunków pochodzi z Azji Południowo-Wschodniej oraz z Ameryki Południowej.
W Suplemencie 9.4 do Farmakopei Europejskiej (1) można znaleźć monografie 6 nowych surowców pochodzenia wschodnio-azjatyckiego, które od dawna znane są i wykorzystywane w tradycyjnej chińskiej medycynie (TCM). Nowością są także dwie monografie surowców południowo-amerykańskich (guarana i mate) oraz jedna monografia surowca azjatyckiego (herbata). Surowce te od dawna są powszechnie znane, ale dopiero teraz awansowały na listę surowców farmakopealnych w krajach Unii Europejskiej.
W części pierwszej zaplanowanej serii artykułów przedstawiono charakterystykę botaniczno-ekologiczno-chemiczno-farmakologiczną gatunków roślin dostarczających nowego surowca saponinowego – Bupleurum sp. (Przewiercień) (2).
Celem drugiej części jest przybliżenie podstawowej wiedzy na temat Platycodon grandiflorus (Jacq.) A.DC. – rozwaru wielkokwiatowego, gatunku dostarczającego kolejnego nowego surowca saponinowego – Platycodi radix. Najbardziej istotną częścią artykułu jest przegląd możliwych zastosowań terapeutycznych surowca, udowodnionych badaniami farmakologicznymi.
Platycodon grandiflorus (rozwar wielkokwiatowy) – status w tradycyjnym i oficjalnym lecznictwie
Platycodi radix w tradycyjnej medycynie chińskiej stosowany jest jako surowiec wykrztuśny, łagodzący ból gardła i ucisk w klatce piersiowej oraz w terapii ropni płucnych. Surowiec używany jest także w leczeniu czerwonki oraz stanów zapalnych skóry. W Japonii i w Korei wykorzystuje się go również do leczenia przewlekłego nieżytu nosa, przewlekłego zapalenia migdałków podniebiennych, astmy, gruźlicy, cukrzycy oraz innych chorób o podłożu zapalnym. Zwiększenie efektu terapeutycznego można osiągnąć poprzez łączenie surowca z korzeniem i kłączem lukrecji, kłączem pineli trójlistkowej lub korzeniem krzyżownicy (3).
Monografia Platycodi radix figuruje w Farmakopei Chińskiej, a od 1999 roku surowiec ma również monografię WHO (4). Surowcem farmaceutycznym według Suplementu 9.4 Farmakopei Europejskiej jest wysuszony, cały lub połamany, obrany lub nieobrany, korzeń Platycodon grandiflorus (Jacq.) A.DC. z usuniętymi korzonkami, zebrany wiosną lub jesienią (1). P. grandiflorus powinien zawierać minimum 0,3% sumy saponin w przeliczeniu na platykodynę D (1) (ryc. 1).
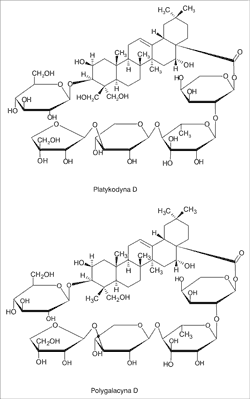
Ryc. 1. Struktura chemiczna platykodyny D i polygalacyny D
Rodzaj Platycodon – informacje ogólne
Rodzaj Platycodon należy do rodziny Campanulaceae (Dzwonkowate) i obejmuje tylko jeden gatunek – P. grandiflorus. Gatunek ten występuje naturalnie we wschodniej części Azji, w Chinach, Korei, Japonii, Mongolii, a także w południowo-zachodnich rejonach Syberii.
Jako gatunek sprowadzony, P. grandiflorus występuje także w USA, m.in. w stanach: Nowy Jork, Pensylwania i Północna Karolina (5). Ze względu na walory ozdobne zarówno w Europie, jak i w Polsce rozwar spotykany jest głównie w przydomowych ogródkach. Odmiany karłowate hodowane są również w doniczkach.
Roślina uprawiana jest w krajach azjatyckich, szczególnie w Chinach (3). W Korei poza zastosowaniami medycznymi surowiec często wykorzystuje się jako produkt spożywczy (6).
Platycodon grandiflorus
Taksonomia
P. grandiflorus jest gatunkiem znanym pod licznymi łacińskimi nazwami synonimowymi: P. autumnalis Decne., P. chinensis Lindl. & Paxton, P. glaucus (Thunb.) Nakai, P. sinensis Lem., P. mariesii (Lynch) Wittm., Campanula grandiflora Jacq. oraz C. glauca Thunb. (7, 8).
P. grandiflorus znany jest jako: platykodon, chinese bellflower, balloon flower (ang.), jie geng (chiń.), doraji (kor.) (9, 10). Od nazwy „platykodon” biorą nazwę główne związki aktywne surowca – saponiny określane jako platykodyny.
Charakterystyka botaniczno-ekologiczna
Gatunek ten jest byliną osiągającą wysokość 20-120 cm. Łodyga rośliny jest prosta (rzadko się rozgałęzia), najczęściej bez włosków, gładka. Liście mają wymiary 2-7 x 0,5-3,5 cm, kształt jajowaty, lancetowaty lub eliptyczny, u podstawy szeroko klinowaty lub zaokrąglony. Wierzchołki liści są ostre lub zaostrzone. Brzeg blaszki liściowej jest szeroko ząbkowany. Kwiaty są fioletowoniebieskie, rzadziej białe bądź różowe, duże i zwykle pojedyncze, niekiedy podwójne. Płatki korony przyjmują kształt trójkątny. Owocem jest torebka pękająca od góry. Roślina kwitnie od lipca do września, owocuje od sierpnia do października. Gatunek ten ma dużą zdolność adaptacyjną (3, 7).
P. grandiflorus rośnie na nasłonecznionych lub półcienistych łąkach, polanach oraz na skalistych miejscach wśród innych roślin, zarośli i krzewów (7).
Charakterystyka fitochemiczna
P. grandiflorus jest źródłem wielu grup związków chemicznych. Na przestrzeni lat z surowca (Platycodi radix) wyizolowano ponad 100 związków chemicznych, głównie saponiny triterpenowe – platykodyny i polygalacyny, flawonoidy, kwasy fenolowe, poliacetyleny, polisacharydy i sterole (tab. 1).
Tab. 1. Główne grupy związków chemicznych występujące w Platycodon grandiflorus
| Grupa związków – przykłady | Piśmiennictwo |
Saponiny triterpenowe:
platykodyna A, B, C, D, J, K, L; polygalacyna D i D2, dezapioplatykodyna D; platykozydy A-F, G1, G2, G3, H-L, M-1, M-2, M-3, O; platykodygenina, kwas polygalowy | (11-17) |
Flawonoidy:
– wyizolowane z nasion i kwiatów – platykonina (2R, 3R), taksyfolina, platykozyd, 7-O-glukozyd kwercetyny, 7-O-rutynozyd kwercetyny, 7-O-glukozyd luteoliny
– wyizolowane z części nadziemnych – 7-O-glukozyd apigeniny, apigenina i luteolina | (18-20) |
Związki fenolowe:
– wyizolowane z ekstraktu etero-naftowego z korzeni – estry kwasów palmitynowego oraz oleinowego z alkoholem koniferylowym
– wyizolowane z części nadziemnych – kwas kawowy, 3,4-dimetoksycynamonowy, ferulowy, izoferulowy, m-, o- i p-kumarynowy, p-hydroksybenzoesowy, 2,3-dihydroksybenzoesowy, 3,5-dihydroksybenzoesowy, 2-hydroksy-4-metoksybenzoesowy, homowanilinowy i chlorogenowy | (20, 21) |
| Poliacetyleny: lobetiol, lobetiolina | (22, 23) |
Polisacharydy:
inulina, skrobia, polisacharydy zbudowane z glukozy, mannozy, arabinozy, galaktozy, ksylozy i ramnozy | (24, 25) |
| Sterole: spinasterol, α-spinasterylo-3-O-β-D-glukozyd, stigmast-7-en-3-on | (26) |
| Inne związki: betulina, grandozyd, kwasy tłuszczowe, aminokwasy | (24, 25) |
Najważniejszymi, aktywnymi biologicznie składnikami są zawarte w korzeniach P. grandiflorus saponiny triterpenowe – głównie związki pentacykliczne typu oleananu, w tym platykodyna D i polygalacyna D (ryc. 1). Do tej pory z P. grandiflorus udało się wyizolować około 70 saponin triterpenowych (3, 4). Związki te są najczęściej glikozylowane przy C-3 i C-28, a część cukrową stanowi D-glukoza, L-arabinoza, L-ramnoza oraz D-ksyloza. W zależności od budowy aglikonu wyróżnia się platykodynę A, B, C, D i E. Sapogeninami są głównie kwas poligalowy i platykodigenina (tab. 1).
Platycodi radix – działanie farmakologiczne
Działanie na drogi oddechowe
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
24 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
59 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
119 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 28 zł
Piśmiennictwo
1. European Pharmacopoeia. 9th ed., Suplement 9.4. Council of Europe, Strasbourg 2017.
2. Ekiert H, Sondej A, Klimek-Szczykutowicz M i wsp. Nowe surowce roślinne w Farmakopei Europejskiej. Cz. I. Gatunki rodzaju Bupleurum (przewiercień) – źródło nowego surowca saponinowego. Post Fitoter 2018; 4:248-256.
3. Zhang L, Wang Y, Yang D i wsp. Platycodon grandiflorus – An ethnopharmacological, phytochemical and pharmacological review. J Ethnopharmacol 2015; 164:147-61.
4. Radix Platycodi. [W:] WHO Monographs on Selected Medicinal Plants. World Health Organization, Geneva 1999; 213-20.
5. United States Department of Agriculture. https://plants.usda.gov/core/profile?symbol=PLGR7#.
6. Nyakudya E, Jeong JH, Lee NK i wsp. Platycosides from the roots of Platycodon grandiflorum and their health benefits. Prev Nutr Food Sci 2014; 19:59-68.
7. Deyuan H, Song G, Lammers TG i wsp. Cucurbitaceae through Valerianaceae, with Annonaceae and Berberidaceae. Flora of China 2011; 19:529.
8. The Plant List. Platycodon grandiflorus. http://www.theplantlist.org/tpl1.1/record/kew-354641.
9. http://www.tropicos.org. http://www.tropicos.org/Name/5502935.
10. U.S. National Plant Germplasm System. https://npgsweb.ars-grin.gov/gringlobal/taxonomydetail.aspx?id=28819.
11. Kim YS, Kim JS, Choi SU i wsp. Isolation of a new saponin and cytotoxic effect of saponins from the root of Platycodon grandiflorum on human tumor cell lines. Planta Med 2005; 71:566-8.
12. Konishi T, Tada A, Shoji J i wsp. The structures of platycodin A and C, monoacetylated saponins of the roots of Platycodon grandiflorum A.DC. Chem Pharm Bull 1978; 26:668-70.
13. Fu WW, Shimizu N, Dou DQ i wsp. Five new triterpenoid saponins from the roots of Platycodon grandiflorum. Chem Pharm Bull 2006; 54:557-60.
14. Fu WW, Shimizu N, Takeda T i wsp. New A-ring lactone triterpenoid saponins from the roots of Platycodon grandiflorum. Chem Pharm Bull 2006; 54:1285-7.
15. He Z, Qiao C, Han Q i wsp. New triterpenoid saponins from the roots of Platycodon grandiflorum. Tetrahedron 2005; 61:2211-5.
16. Fu WW, Fu JN, Zhang WM i wsp. Platycoside O, a new tri-terpenoid saponin from the roots of Platycodon grandiflorum. Molecules 2011; 16:4371-8.
17. Ryu CS, Kim CH, Lee SY i wsp. Evaluation of the total oxidant scavenging capacity of saponins isolated from Platycodon grandiflorum. Food Chem 2012; 132:333-7.
18. Toshio G, Tadao K, Hirotoshi T. Stucture of platycodin A diacylated anthocyanin isolated from the Chinese Platycodon grandiflorum. Tetrahedron Lett 1983; 24:2181-4.
19. Inada A, Murata H, Somekawa M. Phytochemical studies of seeds of medicinal plants. II. A new dihydroflavonol glycoside and a new 3-methyl-1-butanol glycoside from seeds of Platycodon grandiflorum A.DC. Chem Pharm Bull 1992; 3081-3.
20. Mazol I, Glensk M, Cisowski W. Polyphenolic compounds from Platycodon grandiflorum A.DC. Acta Pol Pharm 2004; 61:203-8.
21. Lee JY, Yoon JW, Kim CT i wsp. Antioxidant activity of phenylpropanoid esters isolated and identified from Platycodon grandiflorum A.DC. Phytochem 2004; 65:3033-9.
22. Ahn JC, Hwang B, Tada H i wsp. Polyacetylenes in hairy roots of Platycodon grandiflorum. Phytochem 1996; 42:69-72.
23. Tada H, Shimomura K, Ishimaru K. Polyacetylenes in Platycodon grandiflorum hairy root and campanulaceous plants. J Plant Physiol 1995; 145:7-10.
24. Zhao SC, Fu L, Liu ML i wsp. Determination on the nutrition component of Platycodon grandiflorum etc tree kinds of plants. Food Science 1994; 4:47-9.
25. Ding CJ, Wei YC, An ZY i wsp. Analysis on essentials oils of Platycodon grandiflorum. Acta Baiqiuen Med Univers 1996; 22:471-7.
26. Jiangsu Medical College: A Dictionary of Chinese Medicine Shanghai: Shanghai Science and Technology Press 1977.
27. Shin CY, Lee WJ, Lee EB i wsp. Platycodin D and D3 increase airway mucin release in vivo and in vitro in rats and hamsters. Planta Med 2002; 68:221-5.
28. Choi JH, Hwang YP, Lee HS i wsp. Inhibitory effect of Platycodi radix on ovalbumin-induced airway inflammation in a murine model of asthma. Food Chem Toxicol 2009; 47:1272-9.
29. Sun RR, Zhang MY, Chen Q. Platycodin capsules inflammatory cough asthma research. Pharmacol Clin Chin Mater Med 2010; 26:27-9.
30. Han SB, Park SH, Lee KH i wsp. Polysaccharide isolated from the radix of Platycodon grandiflorum selectively activates B cells and macrophages but not T cells. Int Immuno-pharmacol 2001; 1:1969-78.
31. Choi CY, Kim JY, Kim YS i wsp. Augmentation of ma-crophage functions by an aqueous extract isolated from Platycodon grandiflorum. Cancer Lett 2001; 166:17-25.
32. Choi CY, Kim JY, Kim YS i wsp. Aqueous extract isolated from Platycodon grandiflorum elicists the release of nitric oxide and tumor necrosis factor-α from murine macorphages. Int J Immunopharmacol 2001; 6:1141-51.
33. Xie Y, Pan H, Sun H i wsp. A promising balanced Th1and Th2 directing immunological adjuvant, saponins from the root of Platycodon grandiflorum. Vaccine 2008; 26:3937-45.
34. Ahn KS, Noh EJ, Zhoa HL i wsp. Inhibition of inducible nitric oxide synthase and cyclooxygenase II by Platycodon grandiflorum saponins via supperssion of nuclear factor-κB activation in RAW264.7 cells. Life Sci 2005; 76:2315-28.
35. Lee JH, Choi YH, Kang HS i wsp. An aqueous extract of Platycodi radix inhibits LPS-induced NF-κB nuclear translocation in human cultured airway epithelial cells. Int J Mol Med 2004; 13:843-7.
36. Kim YS, Kim JS, Choi SU i wsp. Isolation of a new saponin and cytotoxic effect of saponins from the root of Platycodon grandiflorum on human tumor cell lines. Planta Med 2005; 71:566-8.
37. Kim MO, Moon DO, Choi YH i wsp. Platycodin D induces apoptosis and decreases telomerase activity in human leukemia cells. Cancer Lett 2008; 261:98-107.
38. Li W, Qi Y, Wang Z i wsp. Study on anti-tumor activity of saponins from Platycodi radix in vitro. Pharmacol Clin Chin Mater Med 2009; 2:37-9.
39. Lee KJ, Kim JY, Choi JH i wsp. Inhibition of tumor invasion and metastasis by aqueous extract of the radix of Platycodon grandiflorum. Food Chem Toxicol 2006; 44:1890-6.
40. Zheng J, He J, Ji B i wsp. Antihyperglycemic effects of Platycodon grandiflorum (Jacq.) A.DC. extract on streptozotocin-induced diabetic mice. Plant Foods Hum Nutr 2007; 62:7-11.
41. Kim YJ, Choi JY, Ryu R i wsp. Platycodon grandiflorus root extract attenuates body fat mass, hepatic steatosis and insulin resistance through the interplay between the liver and adipose tissue. Nutrients 2016; 8:532.
42. Kim KS, Seo EK, Lee YC i wsp. Effect of dietary Platycodon grandiflorum on the improvement of insulin resistance in obese zucker rats. J Nutr Biochem 2000; 11:420-4.
43. Xu BJ, Zheng YN, Han LK. Studies on the adipose metabolizability of Platycodon grandiflorum. Dalian University 2000; 77-9.
44. Khanal T, Choi JH, Hwang YP i wsp. Saponins isolated from the root of Platycodon grandiflorum protect against acute ethanol-induced hepatotoxicity in mice. Food Chem Toxicol 2009; 47:530-5.
45. Khanal T, Choi JH, Hwang YP i wsp. Protective effects of saponins from the root of Platycodon grandiflorum against fatty liverin chronic ethanol feeding via the activation of AMP-dependent protein kinase. Food Chem Toxicol 2009; 47:2749-54.
46. Lee KJ, You HJ, Park SJ i wsp. Hepatoprotective effects of Platycodon grandiflorum on acetaminophen-induced liver damage in mice. Cancer Lett 2001; 174:73-81.
47. Lee KJ, Kim JY, Jung KS i wsp. Suppressive effects of Platycodon grandiflorum on the progress of carbon tetrachloride-induced hepatic fibrosis. Arch Pharmacol Res 2004; 27:1238-44.
48. Lee KJ, Choi JH, Kim HG i wsp. Protective effect of saponins derived from the roots of Platycodon grandiflorum against carbon tetrachloride induced hepatotoxicity in mice. Food Chem Toxicol 2008; 46:1778-85.
49. Wu J, Yang G, Zhu W i wsp. Anti-atherosclerotic activity of platycodin D derived from roots of Platycodon grandiflorum in human endothelial cells. Biol Pharm Bull 2012; 35:1216-21.
50. Yu R, Shin WO, Kim S i wsp. Protective effect of platycodin D in the acute gastric ulcer induced by ibuprofen in rats. J Vet Clin 2013; 30:5-11.
51. Kim, J, Jeon SG, Kim KA i wsp. Platycodon grandiflorus root extract improves learning and memory by enhancing synaptogenesis in mice hippocampus. Nutrients 2017; 9:794.
52. Choi SS, Han EJ, Lee TH i wsp. Antinociceptive mechanisms of platycodin D administered intracerebroventriculary in the mouse. Planta Med 2002; 68:794-8.
53. Choi JH, Jin SW, Han EH i wsp. Platycodon grandiflorum root-derived saponins attenuate atopic dermatitis-like skin lesions via suppression of NF-κB and STAT1 and activation of Nrf2/ARE-mediated heme oxygenase-1. Phytomed 2014; 21:1053-61.
54. Jeong HM, Han EH, Jin YH i wsp. Saponins from the roots of Platycodon grandiflorum stimulate osteoblast differentiation via p38MAPK-and ERK-dependent RUNX2 activation. Food Chem Toxicol 2010; 48:3362-8.
55. European Food Safety Authority. http://www.efsa.europa.eu/.
56. Cosmetic Ingredients Database https://ec.europa.

