© Borgis - Postępy Fitoterapii 1/2006, s. 47-60
*Katarzyna Karłowicz-Bodalska1, Elżbieta Rudkowska2, Małgorzata Han-Marek3
Leki naturalne o działaniu ochraniającym ściany naczyń krwionośnych
Hasco-Lek S.A. we Wrocławiu

Jednym z często rozpoznawanych schorzeń układu krążenia jest chroniczna niewydolność żylna (chronic venous insufficiency – CVI). Według danych statystycznych schorzenie to występuje u 10-15% dorosłych mężczyzn i 20-25% kobiet (1). Do typowych objawów CVI należy zastój w układzie żylnym na obwodzie, wybroczyny krwawe i obrzęki, zwłaszcza kończyn dolnych i in. (niewydolność żylna jest powodem ok. 2/3 owrzodzeń kończyn dolnych). Podstawą tego stanu jest zmniejszenie aktywności profibrynolitycznej oraz nadmierny wzrost agregacji krwinek płytkowych (2-4). Leczenie CVI u wielu pacjentów nie ogranicza się wyłącznie do terapii zachowawczej lecz wymaga hospitalizacji połączonej nie rzadko z zabiegiem chirurgicznym.
Spośród substancji naturalnych, pomocnych w leczeniu CVI, na uwagę zasługują rozpowszechnione w świecie roślinnym związki flawonoidowe, pochodne benzo-γ-pironu, o szerokim spektrum działania biologicznego. Substancje te odgrywają ważną rolę w biochemii i fizjologii roślin, działając m.in. jako antyoksydanty, inhibitory wielu systemów enzymatycznych, prekursory barwników, a także jako substancje osłaniające przed nadmiernym nasłonecznieniem. Flawonoidy wywierają również wpływ na aktywność szeregu układów enzymatycznych u ssaków, co wskazuje na ich znaczący udział w reakcjach biochemicznych oraz działaniu farmakologicznym. Od dawna znane są ich właściwości antyoksydacyjne, zdolność wygaszania wolnych rodników, chelatowania niektórych kationów, pobudzania procesów fosforylacji białek komórkowych i wiele innych (5).
Do znanych i udokumentowanych właściwości farmakologicznych tej grupy związków należy m.in. działanie wzmacniające ściany naczyń krwionośnych. Opisano 31 flawonoidów unieczynniających hialuronidazę, enzym depolimeryzujący kwas hialuronowy do oligosacharydów. Kwas ten jest mukopolisacharydem utworzonym z połączenia N-acetyloglukozaminy z kwasem D-glukuronowym. Jest składnikiem wielu tkanek ciała, płynu stawowego, wszystkich tkanek łącznych, ciałka szklistego oka, zastawek serca i in. Jego obecność w tkance łącznej warunkuje spoistość naczyń kapilarnych i przeciwdziała przesiękom surowicy krwi do jam ciała, zapobiegając tym samym obrzękom i stanom zapalnym.
Poza działaniem deaktywującym hialuronidazę związki flawonoidowe wykazują działanie antyagregacyjne, co w kontekście leczenia CVI ma niewątpliwie duże znaczenie. Znane są również właściwości oksydacyjno-redukcyjne tych związków, m. in. zapobiegające utlenianiu wit. C.
Główny przedstawiciel bioflawonoidów – rutozyd (rutyna) (ryc. 1) jest otrzymywany na skalę przemysłową z ziela gryki Fagopyrum esculentum Moench. lub pąków kwiatowych perełkowca japońskiego Sophora japonica L. Rutozyd jest 3-ramnoglukozydem kwercetyny, występującym w wielu surowcach roślinnych. Wykazuje zdolność uszczelniania i wzmacniania ścian naczyń kapilarnych, czego wynikiem jest zmniejszenie ich kruchości i przepuszczalności, a tym samym ustąpienie typowych objawów CVI. W lecznictwie jest stosowany od dawna per se lub w postaci wielu preparatów złożonych w terapii przewlekłej niewydolności żylnej, w obrzękach kończyn dolnych, wybroczynach krwawych i żylakach podudzi. Ze względu jednak na słabą rozpuszczalność w wodzie, w leczeniu schorzeń żylnych preferuje się lepiej rozpuszczalne pochodne rutozydu, np. propanosulfoniany lub hydroksyalkilopochodne, z których na szczególną uwagę zasługuje O-β-hydroksyetylo-rutozyd (trokserutyna) o udokumentowanym działaniu farmakologicznym i klinicznym (6).
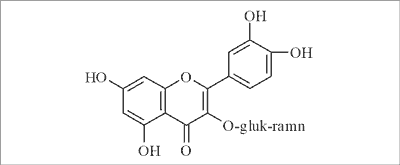
Ryc. 1. Rutyna.
Trokserutyna
Charakterystyka chemiczna i biologiczna
Trokserutyna (3´4´-7-tri-/β-etylo-/-rutozyd) – półsyntetyczna pochodna rutyny – (ATC: C 05 CA; CAS: 7085-55-4) znalazła szerokie zastosowanie w terapii CVI.
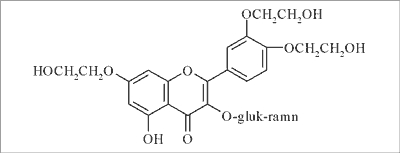
Ryc. 2. Trokserutyna.
Handlowy preparat jest mieszaniną mono-, di, tri- i tetrahydroksyetylowych pochodnych rutyny z przewagą tri-O-β-hydroksyetylorutozydu.
Trokserutyna działa przeciwzakrzepowo, zwiększa napięcie ścian naczyń żylnych oraz reguluje ich przepuszczalność. W dużych dawkach poprawia warunki reologiczne krwi poprzez ułatwienie deformacji krwinek czerwonych oraz poprzez antyagregacyjny wpływ na płytki i krwinki czerwone (w badaniach klinicznych stwierdzono statystycznie znamienne zmniejszenie agregacji krwinek płytkowych po dożylnym podaniu trokserutyny). Jest stosowana w leczeniu zaburzeń krążenia żylnego i limfatycznego, zwłaszcza kończyn dolnych, w stanach zapalnych żył, zespole pozakrzepowym, żylakach kończyn dolnych i odbytu (2, 3, 7, 8). Jej właściwość zmniejszania przepuszczalności naczyń włosowatych wykorzystano w leczeniu retinopatii cukrzycowej i in. naczyniowych uszkodzeń siatkówki, a także w zakrzepach i wylewach podspojówkowych 9-11).
Mechanizm działania, metabolizm i eliminacja
Mechanizm działania trokserutyny wiąże się z jej głównymi właściwościami: hamowaniem tworzenia się skrzepliny w kapilarach żylnych (wenulach) (działanie przeciwzakrzepowe), hamowaniem mechanizmu płytkowego (efekt antyagregacyjny) oraz z działaniem ochronnym na komórki śródbłonka naczyń ( venoprotectivum) (12).
Z przewodu pokarmowego trokserutyna wchłania się łatwo, osiągając największe stężenie w osoczu po upływie 2-3 h. Jest metabolizowana do pochodnych glukuronowych oraz produktu częściowej degradacji – trihydroksyetylokwercetyny. We krwi występuje również w postaci niezmienionej. W organizmie utrzymuje się długo. Jest wydalana głównie (65%) z kałem.
Właściwości farmakologiczne i badania kliniczne trokserutyny
Farmakologia trokserutyny została szeroko opisana w licznych pracach eksperymentalnych, publikowanych już z początkiem lat siedemdziesiątych minionego stulecia. Skuteczność tego preparatu badano przede wszystkim w terapii CVI.
Badanie działania przeciwzakrzepowego trokserutyny przeprowadzone w ostatnich latach ubiegłego wieku (1996) na zwierzętach (szczury) wykazało, że trokserutyna w dawkach 10 mg/kg znacząco hamowała tworzenie się skrzepu w kapilarach żylnych (wenulach), natomiast do wywołania takiego samego efektu w arteriolach należało zastosować wyższe dawki (50 mg/kg). Po podaniu zwierzętom pojedynczej dawki trokserutyny (100 mg/kg) hamowanie skrzepu w wenulach trwało 6-7,5 h, a w arteriolach 4,5-6 h. W stężeniu 100 mg/ml odnotowano nie tylko hamowanie zlepności lecz także rozpraszanie płytek krwi. Przeprowadzone badania potwierdzają, że aktywność przeciwzakrzepowa trokserutyny przebiega poprzez hamowanie agregacji erytrocytów, korzystny wpływ na właściwości fibrynolityczne krwi oraz działanie ochronne na komórki śródbłonka (2, 12).
W eksperymentach na szczurach różnego wieku wykazano, że trokserutyna znacznie podwyższała oporność ścian naczyń włosowatych skóry (13).
Badano także in vivo wpływ trokserutyny na efekt hamowania obrzęków przez indometacynę. Zwierzęta (szczury) przed sprowokowaniem stanu zapalnego (obrzęk łapy) otrzymywały dziennie dootrzewnowo 100 mg/kg trokserutyny przez 6 dni, a następnie indometacynę w dawkach 1, 2 lub 4 mg/kg mc., na 1 h przed indukcją stanu zapalnego. Stwierdzono, że premedykacja trokserutyną spowodowała znaczące podwyższenie stopnia zahamowania obrzęku przez indometacynę (6).
Wiele prac poświęcono klinicznym badaniom działania przeciwobrzękowego (zmniejszenie obrzęku kończyn dolnych) trokserutyny u pacjentów z CVI (3, 4, 7).
Diebschlag i wsp. (7) podawali p.o.60 pacjentkom z rozpoznanym CVI trokserutynę w dawkach 500 lub 100 mg w roztworze vs placebo w randomizowanej podwójnie ślepej próbie przez 12 tygodni. Obie dawki leku wykazywały lepsze wyniki niż placebo. Zaobserwowano zmniejszenie obrzęku w zależności od dawki i okresu trwania kuracji, jak również ogólną poprawę stanu pacjentek. Wynik leczenia utrzymywał się przez ok. 4 tyg. od zakończenia podawania leku. Autorzy stwierdzili wyraźną zależność między działaniem a stosowaną dawką trokserutyny u pacjentów z CVI (7).
Praca Casley´a (14) przedstawia krótki przegląd stosowania benzopyronów w leczeniu obrzęków typu lymphoedema (wywołanych niedrożnością naczyń chłonnych) oraz innych wysokobiałkowych obrzęków. Widoczna redukcja tych stanów pod wpływem omawianych leków jest wynikiem podwyższenia liczby makrofagów, ich normalnej proteolizy, a tym samym eliminacji nadmiaru białka z ustroju. Autor podkreśla przy tym zalety stosowanych leków – ich bardzo niską toksyczność, brak efektów ubocznych oraz możliwość stosowania leków zarówno wewnętrznie, jak i miejscowo. W pracy przedstawiono korzystne wyniki leczenia klinicznego tych schorzeń w Australii, Indiach i Chinach.
Rehn i wsp. (6) przeprowadzili badania skuteczności terapeutycznej w CVI różnych galenowych form i roztworu wodnego O-β-hydroksyetylorutozydów w porównaniu z placebo. Głównym kryterium było zmniejszenie objętości kończyn dolnych po 12 tyg. kuracji. Stwierdzono, że wszystkie formy leku wykazują aktywność i są biologicznie równoważne.
Kilka pozycji piśmiennictwa podkreśla korzystny wpływ trokserutyny w zaburzeniach krążenia siatkówkowego (9-11), które charakteryzuje spowolniony przepływ krwi, stwarzając dogodne warunki dla zlepiania się erytrocytów i utworzenia skrzepu. U 64 pacjentów ze stwierdzonym zamknięciem żyły siatkówkowej (retinal vein occlusion – RVO) stwierdzono istotny wzrost poziomu fibrynogenu oraz znaczące podwyższenie agregacji krwinek czerwonych. Uzyskane wyniki sugerują, że (podkreślana przez wielu autorów w tym schorzeniu) nadmierna lepkość krwi może odgrywać ważną rolę w patogenezie RVO (11).
Również Glacet-Bernard i wsp. (11) uważają, że czynniki reologiczne krwi odgrywają istotną rolę w patogenezie oraz prognozowaniu RVO. W badaniach wpływu trokserutyny, substancji o znanych właściwościach hemoreologicznych, na przebieg tego schorzenia autorzy stwierdzili, że chorzy otrzymujący trokserutynę wykazywali (w porównaniu z placebo) znaczne polepszenie ostrości widzenia, zmniejszenie niedokrwienia oraz obrzęku siatkówki i obniżenie agregacji erytrocytów.
Dobre wyniki uzyskiwano w skojarzonym leczeniu objawów CVI trokserutyną z innymi substancjami, np. z wyciągiem z nasion kasztanowca (HCE) (6) lub z kumaryną (8). Działanie przeciwzapalne preparatu Venalot-Depot (15 mg kumaryny + 90 mg trokserutyny) badano na 560 pacjentkach poddanych epizjotomii (nacięcie krocza przy porodzie). Stwierdzono większą skuteczność tego preparatu od działania poszczególnych składników. Skojarzone leczenie trokserutyną z wyciągiem HCE prowadzono na 137 pacjentkach (po menopauzie) z CVI II st., podzielonych na 3 grupy, otrzymujących kolejno: 1000 mg trokserutyny, 600 mg HCE i 1000 mg HCE dziennie przez 4 tyg., a następnie we wszystkich grupach po 500 mg trokserutyny dziennie przez 12 tygodni. Głównym kryterium poprawy było zmniejszenie objętości kończyn dolnych. Obie substancje wykazywały pozytywne działanie, nieco lepsze w odniesieniu do trokserutyny. Stwierdzono przy tym, że podtrzymująca dawka trokserutyny (500 mg/dz.) zachowuje przez 12 tygodni efekt uzyskany w ciągu 4-tygodniowego leczenia.
Zaobserwowano także, że leczenie pacjentów z CVI za pomocą ucisku (pończocha elastyczna) jest bardziej korzystne w połączeniu z trokserutyną. Odnotowano większą redukcję obrzęku w porównaniu z placebo (3).
Farmakodynamika trokserutyny
U pacjentów z CVI farmakodynamikę trokserutyny badano z zastosowaniem podwójnie ślepej próby. Celem tych badań, po pojedynczej dawce doustnej, była ocena równowagi hemokoagulacyjnej i fibrynolitycznej oraz zmian reologicznych krwi. Uzyskane dane umożliwiają poszerzenie charakterystyki farmakologicznej trokserutyny, ze szczególnym uwzględnieniem aktywności profibrynolitycznej i hemoreologicznej.
Badania określające wychwyt i lokalizację trokserutyny w ścianach naczyń żylnych u pacjentów otrzymujących ten związek przed zabiegiem chirurgicznym na żyle odpiszczelowej wykazały, że trokserutyna była znacząco akumulowana, zarówno w wewnętrznych, jak i zewnętrznych częściach ścian naczyń żylnych. Podczas gdy przenikanie trokserutyny przez wewnętrzną ścianę przebiegało na drodze dyfuzji wprost przez światło naczynia, pobieranie tej substancji przez zewnętrzną ścianę żyły zachodziło przez naczynka odżywcze naczyń ( vasa vasorum) (15, 16).
Toksyczność trokserutyny
Dotychczasowe badania nie wykazały właściwości toksycznych trokserutyny. Cerlek (17) na podstawie przeprowadzonych badań wykazał, że preparat Venalot, stosowany w terapii miejscowych obrzęków pochodzenia urazowego, żylnego lub limfatycznego (zastój limfy), może być podawany w dawkach leczniczych, lub wyższych od zwykle stosowanych, nawet w przypadku jednoczesnego uszkodzenia miąższu wątroby.
Podobne badania przeprowadzili Preuss-Ueberschar i wsp. Autorzy badali na zwierzętach (szczury) wpływ preparatu Venalot na teratogenność oraz rozwój płodu w okresie pre- i postnatalnym. Analiza histopatologiczna prowadzona na przestrzeni 3 generacji wykluczyła występowanie jakichkolwiek zmian patologicznych.
Działania niepożądane
Niekiedy mogą wystąpić napadowe zaczerwienienia twarzy i nudności, które jednak ustępują, jeśli lek jest przyjmowany w trakcie posiłku.
Wskazania do stosowania oraz dawki (19)
Trokserutyna jest stosowana przede wszystkim w leczeniu zaburzeń obwodowego krążenia żylnego i limfatycznego (zwłaszcza w obrębie kończyn dolnych), w zespole pozakrzepowym, zapaleniach żył, żylakach kończyn dolnych i odbytu, obrzękach i krwiakach pourazowych.
Stosowana jest również w retinopatii cukrzycowej i innych naczyniowych uszkodzeniach siatkówki, nadmiernej przepuszczalności naczyń włosowatych, krwawieniach do siatkówki i ciała szklistego, zakrzepach i wylewach podspojówkowych.
Do użytku wewnętrznego lek jest produkowany w tabletkach, kapsułkach, drażetkach, w postaci granulatu lub proszku (torebki 1 g). Zewnętrznie – w postaci 2% żelu, 5 i 10% kropli do oczu oraz czopków.
Dawka dzienna p.o.początkowo 1,8-4 g, dawka podtrzymująca 300-900 mg na dobę w 3 porcjach. Krople do oczu: 1-2 krople 3 x dz.; czopki – 2 x dz. czopek, żel lub maść – wcierać miejscowo 2 x dz.
Preparaty proste:
CILKANOL kapsułki (Lečiva);
DRISI-VEN tabletki powl. (Sertürner);
PHERARUTIN drażetki (Kanoldt);
PAROVEN (Zyma);
POSORUTIN tabl. krople do oczu (Ursapharm);
RUTINOVEN żel 2% (R i C);
RUTOVEN tabl. powlekane; żel 2% (Herbapol, Poznań);
TROXERUTIN kapsułki (Pliva Kraków);
TROXERUTIN kaps. twarde (Synteza);
TROXERUTIN-RATIOPHARM kaps. (Ratiopharm);
TROXEVASIN kapsułki; żel 2% (Pharmachim [Medica] BG);
TROXEVEN tabl. powlekane (Kreussler);
VENOLAN kaps. (Polfa Grodzisk Maz., PL);
VENOTREX kaps. (Pliva, Kraków);
Preparaty złożone:
SAPOVEN T żel – trokserutyna, wyciąg z kasztanowca (Hasco-Lek S.A., Wrocław);
SAPOVEN T kaps. – trokserutyna, wyciąg z kasztanowca (Hasco-Lek S.A., Wrocław);
VENESCIN żel – trokserutyna, wyciąg z kasztanowca (Herbapol, Wrocław);
ALLIORUT tabl. powl. – czosnek, trokserutyna, wyciąg suchy z głogu (Herbapol, Poznań);
ALLIOGEL żel – czosnek, trokserutyna, alantoina (Herbapol, Poznań).
Hippocastani semen – nasienie kasztanowca (syn. Semen Hippocastani, Semen Castaneae equinae)
Najszersze zastosowanie w medycynie w leczeniu CVI znalazły wyciągi z nasion kasztanowca ( Aesculus hippocastanum L.), drzewa powszechnie występującego oraz hodowanego w parkach i ogrodach w licznych krajach świata (m.in. ze względu na dużą odporność na warunki środowiska). Surowcami stosowanymi w lecznictwie są, poza nasionami, kwiaty, liście oraz kora młodych gałęzi. Doniesienia piśmiennictwa, datowane od 18 wieku, wymieniają głównie nasiona jako lek o szerokim spektrum działania biologicznego (1). Już z końcem 19 w. Artault de Vevey (1886) opisał właściwości przeciwhemoroidalne kasztanowca. W schorzeniu tym autor zastosował z pozytywnym efektem nalewkę z nasion kasztanowca, której działanie farmakologiczne warunkuje mieszanina saponozydów zwana escyną. Substancja ta jest izolowana z nasion kasztanowca dla celów przemysłowych.
Drugą grupę substancji czynnych nasion, a także liści i kwiatów kasztanowca, stanowią glikozydy flawonolowe – mono-, di- i triozydy pochodne kwercetyny i kemferolu oraz garbniki skondensowane, leukoantocyjany i procyjanidyny. Kumaryny, głównie eskulina (6-glukozyd eskuletyny), wykazująca zbliżone do escyny i rutyny właściwości ochronne na ściany naczyń kapilarnych, występują najobficiej w korze kasztanowca.
Hippocastani semen jest wymieniany w farmakopeach: DAB 1997, Belg. IV, Port. 35, Mar. 29, PF X (1988), Ph.Eur. (2003), w aktualnych wydaniach monografi: ESCOP, PDR for Herbal Medicines i in.
Surowiec stanowią wysuszone nasiona, zawierające nie mniej niż 3% glikozydów triterpenowych, wyrażonych jako bezwodna escyna, obliczonych w odniesieniu do suchego surowca (DAB, PF X). Surowiec ten stosuje się najczęściej w postaci wyciągu płynnego lub suchego ( Extr. Hippocastani ex semine fluidum aut siccum), standaryzowanego na glikozydy triterpenowe w przeliczeniu na escynę (zwykle 20%).
Skład chemiczny
Charakterystyczne składniki surowca, nazwane ogólnie escyną (3-10%) są mieszaniną diacylowych glikozydów triterpenowych, których aglikony są strukturalnie pokrewnymi pochodnymi protoescygeniny, zacylowanymi kwasem octowym na C-22 i kwasem angelikowym lub tyglinowym na C-21 (ryc. 3). Część cukrowa składa się z kwasu glukuronowego, podstawionego dwiema resztami cukrowymi (glukozy, galaktozy lub ksylozy) (20, 21).
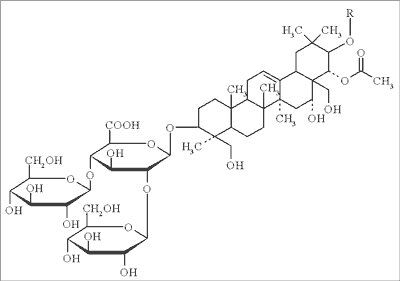
Ryc. 3. Escyna.
Yoshikawa i wsp. (22) wyizolowali z nasion kasztanowca oraz określili strukturę pięciu oligoglikozydów triterpenowych, pochodnych 22-acetyloprotoescygeniny, a w latach 1998-1999 siedmiu nowych acylowanych oligoglikozydów triterpenowych pochodnych polihydroksyoleananu, wyjaśnili strukturę tych związków oraz opracowali metodę (HPLC) ich ilościowego oznaczania (23, 24).
Obecne w surowcu flawonoidy są mono, di- i triozydami kwercetyny i kemferolu, zawierającymi w części cukrowej glukozę, ramnozę, ksylozę i arabinozę (21). W naowocni i łupinie nasiennej występują garbniki skondensowane, leukoantocyjany, (+)-katechina, (-)-katechina, w niedojrzałych nasionach – dimer procyjanidyny oraz procyjanidyno-epikatechina. Stwierdzono również obecność trimerów, a nawet tetramerów katechiny i epikatechiny (garbniki kasztanowca – eskulitaniny A-G) (25, 26).
Kumaryny w nasionach nie występują
Stanowią one składnik czynny kory i kwiatów kasztanowca (21). Wyczerpujący przegląd badań chemicznych, farmakologicznych i klinicznych surowców otrzymywanych z kasztanowca opracowali (20).
W licznych badaniach farmakologicznych i klinicznych stwierdzono, że wyciąg z nasion kasztanowca (HCE /horse chestnut extract/) i wyizolowana z niego escyna stanowią substancje o dużym znaczeniu w farmakologicznym leczeniu przewlekłej niewydolności żylnej (CVI), zwłaszcza w zakrzepowym zapaleniu żył i owrzodzeniach żylakowatych.
Działanie farmakologiczne wyciągu z nasion kasztanowca (HCE)
HCE i wydzielona z niego escyna [ATC: C 05 CX; CAS 6805- 41- O] należą do leków roślinnych dobrze zbadanych farmakologicznie i klinicznie. Stwierdzono, że obie substancje działają tonizująco na naczynia ( venoprotectivum), głównie poprzez uszczelnienie i wzmocnienie ścian włośniczek, z jednoczesnym działaniem przeciwwysiękowym ( antiexudativum) i przeciwobrzękowym ( antioedematicum). Właściwości te są uwarunkowane długotrwałym i skutecznym działaniem escyny, która w badaniach na zwierzętach okazała się 600 razy bardziej aktywna od rutyny (27).
Według Blekic´a (28) HCE spełnia wszelkie kryteria skuteczności terapeutycznej w niewydolności naczyń, ponieważ wykazuje, poza działaniem przeciwobrzękowym i ochronnym na naczynia, właściwości diuretyczne.
Guillaume i Padioleau (29) opracowali profil farmakologiczny HCE w celu dostarczenia naukowych podstaw do wyjaśnienia skuteczności tego wyciągu w terapii CVI. Badania prowadzono z HCE zawierającym 70% escyny. Autorzy zaobserwowali, że działanie wzmacniające układ żylny i pobudzające tworzenie się chłonki zależy od dawki stosowanego wyciągu. HCE w dawkach 5 x 10-5 – 5 x 10-4 g/ml powoduje skurcz wyizolowanej żyły odpiszczelowej psa, trwający ponad 5 h; zwiększa także stopień odpowiedzi skurczowej na adrenalinę. Wzrost ciśnienia żylnego od 18,4 do 33,4% zaobserwowano po podaniu 25-50 mg HCE (odpowiednio). Podawany psom in situ, HCE polepsza funkcje żyły udowej i antagonizuje jej rozszerzenie wywołane zaciskiem podczas wlewu udowo-szyjnego ze stałym przepływem. Podawany dożylnie HCE w dawce 2,5 i 5,0 mg/kg podwyższa znacząco ciśnienie i przepływ w żyle udowej psa, łącznie z piersiowym przepływem limfatycznym, nie powodując zmian w parametrach tętniczych.
HCE w zależności od dawki (50-400 mg/kg p.o.) zmniejsza skórną przepuszczalność włośniczek indukowaną u szczurów działaniem histaminy lub serotoniny (śródskórna iniekcja) oraz u królików (wywołaną działaniem chloroformu jako środka drażniącego). Wyciąg ten podany p.o.świnkom morskim, pozostawionym na diecie szkorbutogennej, podwyższa odporność naczyń włosowatych skóry.
HCE wykazuje również własności antyoksydacyjne i antywolnorodnikowe in vitro i in vivo. W zależności od dawki hamuje enzymatyczne i nieenzymatyczne utlenianie lipidów. In vivo przeciwdziała szkodliwemu działaniu rodników tlenowych w różnych eksperymentalnych modelach stresu tlenowego, (np. wywołanie obrzęku u myszy działaniem oksydazy glukozowej lub wywołanie cukrzycy u szczurów działaniem alloksanu (29).
Na podstawie oceny wielu randomizowanych, kontrolowanych placebo badań klinicznych, z zastosowaniem podwójnie ślepej próby, można wnioskować, że HCE jest bezpiecznym i skutecznym środkiem w objawowym leczeniu chronicznej niewydolności układu żylnego (6, 30-36).
Właściwości farmakokinetyczne
Kuntz i wsp. (37) nie stwierdzili znaczących różnic w biodostępności HCE przyjmowanego p.o.zarówno z form leku szybko uwalniających substancję czynną, jak i z preparatów o przedłużonym działaniu, podczas gdy Schräder i wsp. (38) i Dittgen M i wsp. (39) oznaczyli wyższą biodostępność z form szybko uwalniających lek. Maksymalne stężenie w osoczu odnotowano między 1,9 a 3,3 h, w zależności od typu preparatu. Końcowe okresy półtrwania w osoczu oznaczono jako 17,8 -21,2 h (40) i 18,5-24,0 h (39). Wiązanie się z białkiem osocza określono na 84% (41).
Toksyczność
Wartości LD50 dla HCE, oznaczane na różnych zwierzętach doświadczalnych, wynosiły (mg/kg masy ciała): myszy 990; szczury 2150; świnki morskie 1120, króliki 1530. Oznaczenia tego nie przeprowadzono dla psów, ponieważ dawki większe niż 130 mg/kg powodowały wymioty i zwracanie substancji krótko po podaniu. Podawana szczurom i.v.dawka ok. 30 mg/kg (7-krotna dzienna terapeutyczna dawka podawana ludziom p.o.) nie powodowała objawów zatrucia (41).
Nie stwierdzono również objawów toksycznych ani degeneracji narządów po 34-tyg. stosowaniu HCE p.o.psom w dawkach 20, 40 i 80 mg/kg mc. dziennie i szczurom w dawkach 100, 200 i 400 mg/kg mc. dziennie. Najwyższa dawka podawana psom odpowiadała 8-krotnej, a najwyższa dawka podawana szczurom – 40 krotnej dziennej dawce terapeutycznej stosowanej dla ludzi.
Teratogenność
Nie stwierdzono objawów teratogenności (w porównaniu ze zwierzętami kontrolnymi) przy podawaniu p.o.szczurom i królikom HCE w dawce 100 mg/kg mc. dziennie oraz szczurom przy 300 mg/kg mc. dziennie (ostatnia wartość odpowiada ok. 30-krotnej rekomendowanej dawce terapeutycznej u ludzi (41).
Preparaty proste zawierające wyciąg z kasztanowca jako substancję czynną:
AESCUVEN Forte tabl. – (Cesra);
ESCEVEN tabl. powl. – (Herbapol, Poznań);
VENOPLANT tabl. o przedłuż. uwalnianiu (Dr. Willmar Schwabe);
VENASTAT kaps (retard) – (Boeringer-Ingelheim);
VENITAN krem – (Lek S.A.);
VENOTONIN kaps. (Phytopharm Klęka)
Preparaty złożone:
EMORECT żel – dodatkowo nalewka z arniki (EMO);
ESCALAR maść – dodatkowo wyciąg gęsty z arniki i nagietka (Hasco-Lek S.A.);
SAPOVEN T żel – dodatkowo trokserutyna (Hasco-Lek S.A.);
SAPOVEN AT czopki – dodatkowo trokserutyna (Hasco-Lek S.A.);
SAPOVEN T kapsułki – dodatkowo trokserutyna (Hasco-Lek S.A.);
MAŚĆ KASZTANOWA – dodatkowo wyciąg z krwawnika, olejek lawendowy i tymiankowy (Alpine Herbs);
FITOVEN pasta – dodatkowo wyciągi: z kwiatostanu głogu, ziela gryki, nawłoci, kwiatostanu lipy (Herbapol, Pruszków);
VENESCIN draż. – dodatkowo eskulina i rutyna (Herbapol, Wrocław);
VENESCIN żel – dodatkowo trokserutyna (Herbapol, Wrocław);
HEMOROL czopki – wyciągi: z kory kasztanowca, koszyczków rumianku, pokrzyku wilczej jagody, janowca, krwawnika, kłącza pięciornika + benzokaina (Herbapol, Wrocław).
Escyna. Charakterystyka chemiczna
Escyna, główna substancja działająca wyciągu z nasion kasztanowca wykazała klinicznie udowodnioną skuteczność w leczeniu CVI, żylaków odbytu i obrzęków pooperacyjnych.
Substancja ta występuje w postaci mieszaniny, w której wyróżnia się dwie formy (α lub β) o odmiennej temperaturze topnienia, skręcalności właściwej, rozpuszczalności w wodzie oraz o różnym indeksie hemolitycznym. β-Escyna jest aktywnym składnikiem mieszaniny i jest obecna w większości dostępnych produktów farmaceutycznych. α-Escyna tworzy się w wyniku migracji kwasowej grup hydroksylowych w pozycjach C-21, C-22 i C-28 podczas ogrzewania wodnego roztworu β-escyny do temp. 100°C (1).
Chemizm saponozydów, podobnie jak mechanizm działania substancji czynnych kasztanowca, stanowi dotąd temat nieustannych badań.
Badania farmakologiczne escyny
Prowadzone od dawna liczne badania farmakologiczne escyny potwierdziły działanie przeciwobrzękowe i przeciwzapalne tej substancji. W badaniach na zwierzętach wykazano, że escyna zmniejsza obrzęk łapy szczura wywołany działaniem albumin jaja kurzego, formaliny i dekstranu, przy czym najsilniejszy efekt przeciwzapalny zaobserwowano po dożylnym podaniu preparatu na 16 h przed wprowadzeniem środka wywołującego obrzęk (27). Podobne wyniki uzyskano po podaniu zwierzętom doświadczalnym escyny w dawce jednorazowej (0,3-0,5 mg/kg) na 16 h przed zastosowaniem środka prowokującego obrzęk (dekstran, karagenina). Obniżenie stopnia tego obrzęku wynosiło ok. 30% w porównaniu z grupą kontrolną. Stwierdzono również obniżenie wywołanej eksperymentalnie przepuszczalności kapilar w granicach 12-26% po podaniu zwierzętom dożylnie escyny w dawce 0,5-2,0 mg/kg mc. Działanie powyższe zostało potwierdzone w badaniach klinicznych u ludzi (42). Zaobserwowano przy tym, że im wyższa zawartość (%) substancji aktywnej tym wyższa skuteczność terapeutyczna stosowanego leku (20).
Matsuda i wsp. (43, 44) w badaniach na modelach zwierzęcych wykazali zróżnicowane działanie przeciwzapalne i przeciwwysiękowe poszczególnych escyn, wydzielonych z nasion kasztanowca. Produkty degradacji alkalicznej badanych związków – deacyloescyny – okazały się w stosowanych testach nieaktywne. Autorzy wnioskują, że w układzie struktura chemiczna – aktywność biologiczna escyn, obecność reszt acylowych w cząsteczce związku ma istotne znaczenie.
Profil farmakologiczny β-escyny badano szczególnie intensywnie w ostatnich latach. Celem prowadzonych badań było ustalenie mechanizmu działania wyjaśniającego stosowanie tej substancji w leczeniu objawów CVI. Większość badań prowadzono z wyciągiem gęstym z nasion kasztanowca (HCE – horse chestnut extract), zawierającym ok. 70% escyny. Potwierdzono skuteczność terapeutyczną tej substancji w badaniach in vitro oraz in vivo na różnych modelach zwierzęcych w zakresie działania przeciwobrzękowego, przeciwzapalnego oraz wzmacniającego naczynia krwionośne. Działanie to jest powiązane z właściwością polepszania, za pomocą molekularnego mechanizmu, odpowiedzi escyny na jony Ca2+ i podwyższania tym samym napięcia żylnego zarówno w warunkach in vivo jak i in vitro (1).
Biodostępność escyny z ekstraktu z nasion kasztanowca, w porównaniu z biodostępnością escyny z roztworu, wynosi 100% (41). Podobnie, jak w badaniach na zwierzętach, u ludzi również zaobserwowano występowanie bariery krew-mózg dla escyny (45).
Farmakokinetyka escyny
Schrodter i wsp. (46) badali porównawczo farmakokinetykę i względną biodostępność β-escyny pochodzącej z wyciągu HCE oraz z preparatu zawierającego escynę. Badania te prowadzono po osiągnięciu stanu stacjonarnego leku w osoczu w randomizowanej, podwójnie ślepej próbie. Stężenie escyny w surowicy oznaczano z zastosowaniem testu radioimmunologicznego. Autorzy stwierdzili dużą rozbieżność uzyskanych wyników, co tłumaczą wysoką specyficznością metody i niejednorodnością badanej substancji.
W badaniach farmakokinetycznych ustalono, że escyna podana w roztworze p.o.zostaje szybko zresorbowana z przewodu pokarmowego. Jest wydalana głównie przez wątrobę i nerki, częściowo w formie zmetabolizowanej (46).
Przeciwwskazania i interakcje
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
29 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
69 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
129 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 78 zł
Piśmiennictwo
1. Sirtori C.R.: Aescin: Pharmacology, pharmacokinetics and therapeutic profile. Pharmacol. Res. 2001, 44, 183. 2. Boisseau M.R. et al.: Fibrinolysis and hemorheology in chronic venous insufficiency, a double blind study of troxerutin efficiency. J. Cardiovasc. Surg. 1995, 36, 369. 3. Unkauf M., Rehn D. et al: Investigation of the efficacy of oxerutins compated to placebo in patients with chronic venous insufficiency treated with compression stockings. Arzneim.-Forsch. 1996, 46, 478. 4. Blazso G., Gabor M.: Influenze of O-(β-hydroksyethyl)-rutin on the edema-inhibiting effect of indometacin. Acta Pharm. Hung. 1994, 64, 123. 5. Middleton E. J., Kandaswami C.: The impact of plant flavonoids on mammalian biology: implications for immunity, inflammation and cancer. The Flavonoids: Advances in research since 1986 (Red. J.B. Harborne) Chapman and Hall, London 1993. 6. Rehn D., Unkauf M. et al: Comparative clinical efficacy and tolerability of oxerutins and horse-chestnut extract in patients with chronic venous insufficiency. Arzneim.-Forsch. 1996, 46, 483. 7. Diebschlag W. et al: Clinical comparison of two doses of O-(β-hydroksyethyl)-rutosides in patients with chronic venous insufficiency. J. Pharm. Med. 1994, 4, 7. 8. Petho A.: Die Wirksamkeit von Benzopyronen bei der posttraumatischen Entzundung. Arzneim.-Forsch. 1981, 31, 1303. 9. Lureau M.A., Glacet-Bernard A., Coscas G.: Occlusion de la veine centrale de la retine bilaterale et anticoagulant circulant. J. Fr. Ophtalmol. 1995, 18, 468. 10. Glacet-Bernard A., Coscas G. et al: A randomized, double-masced study of the treatment of retinal vein occlusion with troxerutin. Am. J. Ophtalmol. 1994, 118, 421. 11. Glacet-Bernard A., Coscas G. et al: Erythrocyte aggregation and retinal vein occlusion. Preliminary data for a randomized study on the efficacy of anti-erythrocyte aggregation (troxerutin) in retinal vein occlusion. Bull Soc. Ophtalmol. Fr. 1989, 89, 1393. 12. Krupiński K., Giedrojć J., Bielawiec M.: Effect of troxerutin on laser-induced thrombus formation in rat mesenteric vessels, coagulation parameters and platelet function. Pol. J. Pharmacol. 1996, 48, 335. 13. Gabor M.: Capillary resistance raising action of venoruton. Acta Pharm. Hung. 1983, 53, 115. 14. Casley-Smith J.R.: Modern treatment of lymphoedema II. The benzo-pyrones. Austral. J. Dermatol. 1992, 33, 69. 15. Patwardhan A., Carlsson K.: The affinity of troxerutin for the venous wall measured by laser scanning microscopy. J. Cardiovasc. Surg. (Torino) 1995, 36, 381. 16. Carlsson K., Patwardhan A: Transport and localisation of troxerutin in the venous wall. J. Mal. Vasc. 1996, 21 (Suppl.C), 270. 17. Cerlek S.: Effect of a benzopyrone compound on liver function. Arzneim.-Forsch. 1977, 27, 611. 18. Preuss-Ueberschar C., Ueberschar S.: Reproduction toxicologic studies on rats following oral administration of benzopyrone preparations. Arzneim.-Forsch. 1984, 34, 1305. 19. Podlewski J.K., Chwalibogowska-Podlewska A.: Leki współczesnej terapii. Fundacja Buchnera, Warszawa 1999. 20. Bombardelli E. et al.: Aesculus hippocastanum L. (review); Fitoterapia 1996, 67, 483. 21. Hänsel R., Keller K: Hager´s Handbuch der Pharm Praxis, T. 4 Springer Verlag, Berlin-Heidelberg-N York 1992. 22. Yoshikawa M., Murakami T. et al.: Bioactive saponins and glycosides. III. Horse chestnut (I): The structures, inhibitory effects on ethanol absorption and hypoglemic activity of escins Ia, Ib, IIa, IIb and IIIa from the seeds of Aesculus hippocastanum L. Chem. Pharm. Bull 1996, 44, 1454. 23. Yoshikawa M., Murakami T. et al.: Bioactive saponins and glycosides. Horse chestnut. Part 2. Structures of escins IIIb, IV, V and isoescins Ia, Ib and V, acylated polyhydroksyoleanane triterpene oligoglycosides from the seeds of horse chestnut trees ( Aesculus hippocastanum L., Hippocastanaceae). Chem. Pharm. Bull 1998, 11, 1764. 24. Yoshikawa M., Murakami T. et al.: Bioactive saponins and glycosides. Horse chestnut. Part 3. Quantitative analysis of escins Ia, Ib, IIa and IIb by means of HPLC. J. Pharm. Soc. Jap. 1999, 119, 81. 25. Morimoto S., Nonaka G.I., Nishioka I: Tannins and related compounds. LIX. Aesculitannins, novel proanthocyanidins with double-bonded structures from Aesculus hippocastanum L. Chem. Pharm. Bull. 1987, 38, 499. 26. Santos-Buelga C., Kołodziej H., Treutter D.: Procyanidin trimers possesing a doubly linked structure from Aesculus hippocastanum. Phytochem. 1995, 38, 499. 27. Lorenz D., Marek M.L.: Das therapeutisch wirksame Prinzip der Rosskastanie ( Aesculus hippocastanum). Arzneim.-Forsch. 1960, 10, 263. 28. Blekic J.: Horse chestnut seeds ( Aesculus hippocastanum L.) in the treatment of phlebopathological disorders: Farmaceutski Glasnik 1996, 52, 145. 29. Guillaume M., Padioleau F.: Veinotonic effect, vascular protection, antiinflammatory and free radical scavenging properties of horse chestnut extract. Arzneim.-Forsch. 1994, 44, 25. 30. Pittler M.H., Ernst E.: Horse-chestnut seed extract for chronic venous insufficiency. A criteria-based systematic review. Arch. Dermatol. 1988, 134, 1356. 31. Steiner M.: Untersuchung zur odemvermindernden und odemprotektiven Wirkung von Rosskastaniemsamenextrakt. Phlebol. Proktol 1990, 19, 239. 32. Steiner M., Hillemanns H.G.: Venostasin retard in the management of venous problems during pregnancy. Phlebology 1990, 5, 41. 33. Diehm C., Trampisch H.J. et al: Comparison of leg compression stocking and oral horse-chestnut seeds extract therapy in patients with chronic venous insufficiency. Lancet 1996, 347, 297. 34. Vayssairat M., Debure C. et al: Horse-chestnut seed extract for chronic venous insufficiency (letters). Lancet 1996, 347, 1182. 35. Bisler H. et al.: Wirkung von Rosskastaniensamenextrakt auf die transkapillare Filtration bei chronischer venöser Insuffizienz. Dtsch. Med. Wchschr. 1986, 111, 1321. 36. Calabrese C., Preston P.: Report of the results of a double-blind, randomized, single-dose trial of a topical 2% escin gel versus placebo in the acute treatment of experimentally-induced hematoma in volunteers. Planta Med. 1993, 59, 394. 37. Kunz K., Lorkowski G. et al.: Bioavailability of escin after administration of two oral formulations containing aesculus extract. Arzneim.-Forsch. 1998, 48, 822. 38. Schrader E., Schwankl W. et al: Vergleichende Untersuchung zur Bioverfügbarkeit von β-Aescin nach oraler Einmalverabreichung zweier Rosskastaniensamenextrakt enthaltender, galenisch unterschiedlicher Darreichungsformen. Pharmazie 1995, 50, 623. 39. Dittgen M., Zimmermann H. et al: Untersuchung der Bioverfügbarkeit von β-Aescin nach oraler Verabreichung verschiedener Darreichungsformen. Pharmazie 1996, 51, 608. 40. Oschman R., Biber A. et al.: Pharmakokinetik von β-Aescin nach Gabe verschiedener Aesculus -Extract enthaltenden Formulierungen. Pharmazie 1996, 51, 577. 41. Hitzenberger G.: Die terapeutische Wirksamkeit des Rosskastaniensamen-Extraktes. Wiener Med. Wschr. 1989, 17, 385. 42. Henschler D., Hempel K. et al: Zur Pharmakokinetik von Aescin. Arzneim.-Forsch. 1971, 21, 1682. 43. Matsuda M., Li Y. et al: Effects of escins Ia, Ib, Iia, Iib from horse-chestnut the seeds of Aesculus hippocastanum L. on acute inflammation in animals. Biol. Pharm. Bull. 1997, 20, 1092. 44. Matsuda M., Li Y. et al: Antiinflammatory effect of escin Ia, Ib, IIa and IIb from horse chestnut, the seeds of Aesculus hippocastanum L. Bioorg. Med. Chem. Lett. 1997, 7, 1611. 45. Ascher P.W, Paltauf F: Klinische Untersuchungen über die Pharmakodynamik von tritiummarkierten Aescin. Aerztl. Forsch. 1970, 24, 294. 46. Schrodter A., Loew D. et al.: Validity of pharmakokinetic data for β-escin from horse chestnut seed extracts determined by radioimmunological methods. Arzneim.-Forsch. 1998, 48, 905. 47. Willuhn G.: Arnica montana L. – Porträt einer Arzneipflanze. Pharm. Ztg. 1991, 136, 2453. 48. Hall I.H., Lee K.H. et al: Antitumor agents XXX: Evaluation of α-methylene-γ-lactone-containing agents for inhibition of tumor growth, respiration and nucleic acid synthesis. J. Pharm. Sci. 1978, 67, 1235. 49. Hall I.H., Lee K.H. et al: Antiinflammatory activity of sesquiterpene lactones and related compounds. J. Pharm. Sci. 1979, 68, 537. 50. Hall I.H., Starnes C.O. et al: Mode of action of sesquiterpene lactones as anti- inflammatory agents. J. Pharm. Sci. 1980, 69, 537. 51. Lyss G., Schmidt T.J. et al: Helenalin, an anti-inflammatory sesquiterpene lactone from Arnica, selectively inhibits transcription factor NF-kB. Biol. Chem. 1997, 378, 951. 52. ESCOP. Monographs, Second Ed. 2003. 53. Passreiter C.M., Willuhn G., Roder E.: Tussilagine and isotussilagine: two pyrrolizidine alkaloids in the genus Arnica. Planta Med. 1992, 58, 556. 54. Passreiter C.M.: Co-occurrence of 2-pyrrolidineacetic acid with the pyrrolizidines tussilaginic acid and isotussilaginic acid and their 1-epimers in Arnica species and Tussilago farfara. Phytochem. 1992, 32, 4135. 55. Akihisa T., Yasukawa K. et al.: Triterpene alcohols from the flowers of Compositae and their antiinflammatory effects. Phytochem. 1996, 43, 1255. 56. Zitterl-Eglseer K., Sosa S. et al: Anti-oedematous activities of the main triterpendiol esters of marigold ( Calendula officinalis L.). J. Ethnopharmacol 1997, 57, 139. 57. Vidal-Ollivier E., Elias R. et al: Flavonol glycosides from Calendula officinalis flowers. Planta Med. 1989, 55, 73. 58. Varljen J., Liptak A., Wagner H.: Structural analysis of a rhamnoarabinogalactan and arabinogalactans with immuno-stimulating activity from Calendula officinalis. Phytochemistry 1989, 28, 2379. 59. Dumenil G., Chemli R. et al: Etude des proprietes antibacteriennes des fleurs de Souci Calendula officinalis L. et des teintures meres homeopathiques de C. officinalis L. et C. arvensis L. Ann Pharm. Fr. 1980, 38, 493. 60. Kalvatchev Z., Walder R., Garzaro D: Anti-HIV activity of extracts from Calendula officinalis flowers. Biomed. Pharmacother. 1997, 51, 176. 61. Samochowiec E., Urbańska L. et al: Assessment of the action of Calendula officinalis and Echinacea angustifolia extracts on Trichomonas vaginalis in vitro. Wiad. Parazytol. 1979, 25,77. 62. Gracza L.: Oxygen-containing terpene derivatives from Calendula officinalis. Planta Med, 1987, 53, 227. 63. Bezakova L., Masterova I. et al: Inhibitory activity of isorhamnetin glycosides from Calendula officinalis L. on the activity of lipoxygenase. Pharmazie 1996, 51, 126. 64. Popovic M., Kaurinovic B., et al: Combined effects of plant extracts and xenobiotics on liposomal lipid peroxidation. Part 2. Marigold extract-CCl4/fullerenol. Oxid Commun. 2000, 23, 178. 65. Popovic M., Kaurinovic B. et al.: V. Combined effects of plant extracts and xenobiotics on liposomal lipid peroxidation. Part 1. Marigold extract-ciprofloxacin-pyralene. Oxid Commun 1999, 22, 487. 66. Patrick K.F.M., Kumar S. et al.: Induction of vascularisation by an aqueous extract of the flowers of Calendula officinalis, the European marigold. Phytomed. 1996, 3, 11. 67. Klouchek-Popova E., Popov A. et al: Influenze of the physiological regeneration and epitelization using fractions isolated from Calendula officinalis. Acta Physiol. Pharmacol. Bulg. 1982, 8, 63. 68. Oana L., Mates N. et al: Studies concerning the wound healing action of some medicinal herb extracts. Bulet. Univ. de Stiinte Agricole, Ser. Zootech. Med. Veterin. 1995, 49, 461. 69. Peri de Carvalho P.S., Tagliavini D.G., Tagliavini R.L.: Cutaneous cicatrization after topical application of calendula cream and comfrey, propolis and honey association in infected wounds of kin. Clinical and histological study in rats. Rev. Cienc. Biomed. (Sao Paulo) 1991, 12, 39. 70. Delaveau P., Lalloulette P., Tessier A.M.: Drogues vegetales stimulant l´activite phagocytaire du systeme reticulo-endothelial. Planta Med 1980, 40, 49. 71. Shipochliev T., Dimitrov A., Aleksandrova E.: Study on the inflammatory effect of a group of plant extracts. Vet.-Med. Nauk. (Sofia) 1981, 18, 87. 72. Della Loggia R. et al.: The role of triterpenoids in the topical anti-inflammatory activity of Calendula officinalis flowers. Planta Med. 1994, 60, 516. 73. Della Loggia R., Becker H. et al: Topical anti-inflammatory activity of Calendula officinalis extracts. Planta Med. 1990, 56, 658. 74. Lievre M., Marichy J. et al: Controlled study of three ointments for the local management of 2nd and 3rd degree burns. Clin. Trials and Meta-Anal. 1992, 28, 9. 75. Baranov A.P.: Calendula – Wie ist die Wirksamkeit bei Verbrennungen und Verbrühungen? . Dtsch. Apoth. Ztg. 1999, 139, 2135.



