© Borgis - Postępy Fitoterapii 3-4/2005, s. 80-86
Sebastian Turek
Ziele dziurawca zwyczajnego – składniki czynne i potencjalne zastosowania lecznicze
St. John´s wort – active compounds and potential medical application
Katedra i Zakład Farmakognozji Akademii Medycznej we Wrocławiu
Kierownik Katedry i Zakładu: prof. dr hab. Wojciech Cisowski
Summary
St. John´s wort is Hypericum perforatum L., Hypericaceae, a herbaceous perennial plant native to western United States, Europe and Asia, and its various preparations are widely used for the treatment of some disorders. The article presents the appearance of the plant and the stock, the chemical composition with regard to biological active compounds and indication. The flavonoids (rutin, quercetin, and isoquercetin), hypericin and hyperforin are the main active substances of St. John´s wort. They support regeneration of human body cells, provide disinfection, and act as antiviral and anti-inflammation tools. Hyperforin has also been shown to have antimicrobial activity against Gram-positive bacteria. The antitumor properties of St. John´s wort are attributed to hypericin, which is a powerful photosensitizer. Once taken up by tumor cells, hypericin reacts in the presence of oxygen and activates multiple apoptosis pathways that results in malignant cell death. But the most common indication of St. John"s wort is the treatment of mild-to-moderately severe depressive disorders.

Dziurawiec zwyczajny ( Hypericum perforatum, Hypericaceae – dziurawcowate) jest rośliną leczniczą znaną od starożytności i szeroko stosowaną dzięki swoim właściwościom biologicznym. Nazwa „hypericum” składa się z dwóch członów pochodzących z języka greckiego. „hyper” oznacza „ponad, przez”, a „eikon” – zjawa, duch. Wynika to z wierzeń, że roślina miała zdolność ochrony przed złymi mocami. Słowo „ perforatum ” pochodzi z łaciny i oznacza „podziurawiony” ze względu na charakterystyczną budowę liścia (1). Inni autorzy wywodzą nazwę z greckiego słowa hypericon – hypo = pod + ereike = wrzos – co miałoby wskazywać na miejsca występowania rośliny (2).
W polskiej medycynie ludowej roślina nazywana była zielem świętego Jana, ponieważ okres jej kwitnienia przypada na drugą połowę czerwca. Sok z dziurawca zwany był niegdyś przez znachorów „fuga daemonum” i używany do wypędzania złych duchów, a także do przepowiadania chorób. Sądzono, że ziele dziurawca zostało „przez diabła we wściekłości pokłute” (3). Inne nazwy ludowe związane są ze zwyczajami i ziołolecznictwem. Nazywano więc roślinę – arlika, durawy, dziurawnik, dziurkawiec, krew Chrystusa, krew Matki Bożej, krewka, krzyżowe ziele, michałkowe ziele, przestrzelon, wrzosowiec, zanowyt czy żółtokwioutka (2). Podobnie nazwy dziurawca w innych językach nawiązują do ludowych wierzeń: St. John`s wort (ang.), Herbe ŕ mille trous (fr.), Johanniskraut (niem.).
Walory lecznicze dziurawca zwyczajnego zostały opisane przez uczonych starożytnych: Hippokratesa (460-377 p.n.e.), Theofrastusa (372-287 p.n.e.), Dioskoridesa (pierwszy wiek n.e.), Galena (130-200 n.e.) i Pliniusza w Księdze XXIV jego „Historianum mundi” (1). Paracelsus (1493-1541) twierdził, że nie ma drugiego, równie skutecznego ziela w leczeniu „szaleńczych fantazji” (3). Od wieków więc zalecano ziele dziurawca jako środek skuteczny w schorzeniach dróg oddechowych, moczowych, w zaburzeniach trawienia, w leczeniu hemoroidów, urazów, oparzeń, ran i różnego pochodzenia wrzodów (1). Od czasów Paracelsusa stosowano także ziele dziurawca w schorzeniach neurologicznych i psychicznych, jak neuralgia, niepokój, a także depresja.
Dziurawiec zwyczajny jest rośliną ruderalną powszechnie występującą w Europie, Azji (za wyjątkiem dalekiej północy), Ameryce Północnej, Australii oraz w północnej części Afryki na suchych, słonecznych łąkach, polach i w widnych lasach. W Polsce jest pospolity na całym obszarze. Cała rodzina Hypericaceae liczy około 400 gatunków szeroko rozpowszechnionych na świecie. Roślina kwitnie od czerwca do sierpnia. Zbioru dokonuje się dwa razy w roku. Ścina się kwitnące wierzchołki, po czym suszy się je na powietrzu, w cieniu, w cienkich warstwach lub w suszarniach w temperaturze nie wyższej niż 35°C, aby uniknąć rozkładu istotnych dla działania biologicznego związków.
Większość preparatów z dziurawca zwyczajnego dostępnych na rynku polskim i europejskim to ekstrakty wodno-etanolowe lub suche ekstrakty w postaci tabletek lub kapsułek. Badania fitochemiczne ziela dziurawca rozpoczęły się w 1830 roku i zostały przeprowadzone przez Büchnera, który wyodrębnił olejek z dziurawca, a składnik nadający mu czerwoną barwę nazwał „hypericum red” (1). Około sto lat później – w 1911 roku – Cerny dokonał izolacji tego składnika i nadał mu nazwę hyperycyna. Ten sam uczony wydobył z olejku dwa inne związki podobne do hyperycyny, ale nie potrafił określić ich rzeczywistej struktury (1). Ostatecznie budowa hyperycyny została ustalona w 1953 roku przez Brockmanna dzięki rozwojowi technik analitycznych (4). Także w tym roku Brockmann i wsp. dokonali syntezy hyperycyny z trimetyloeteru bromoemodyny. Wcześniej hyperycynę otrzymywano również przez rozkład oksypenicilliopsiny produkowanej przez grzyb Penicilliopsis clavariaeformis. Całkowitą syntezę związku przeprowadzili Brockmann i Kluge w 1955 roku (4). Badania fitochemiczne z pierwszej połowy ubiegłego wieku koncentrowały się głównie na identyfikacji składników olejku i ze względu na trudności techniczne były w dużej mierze obarczone błędami.
W 1971 roku grupa rosyjskich badaczy stwierdziła, że za działanie przeciwbakteryjne dziurawca, które zostało odkryte w latach 40. XX wieku, odpowiadają związki o szkielecie floroglucyny (5). Od tego czasu trwały badania nad określeniem ich struktury. W 1975 Bystrov pierwszy opisał izolację hyperforyny i określił jej chemiczne właściwości, nie znając jeszcze jej wzoru chemicznego (6). Absolutną konfigurację hyperforyny ustalono w roku 1983 na podstawie analizy rentgenowskiej jej estru z kwasem p-bromobenzoesowym (6). W latach dziewięćdziesiątych, kiedy odkryto przeciwdepresyjne właściwości hyperforyny, badania rozszerzono na dużą grupę związków bardziej polarnych od hyperforyny, które prawdopodobnie są produktami jej utlenienia (6, 7).
W zielu dziurawca wyróżnić można liczne związki należące do kilku grup.
Naftodiantrony – hyperycyna, pseudohyperycyna, cyklopseudohyperycyna, protohyperycyna i protopseudohyperycyna
Związki te są charakterystyczne dla rodzaju Hypericum. Hyperycyna i pseudohyperycyna (ryc. 1) zostały znalezione w 27 z 36 gatunków dziurawca i odpowiedzialne są za czerwoną barwę soku z dziurawca (8). Większość gatunków zawiera oba związki. Niektóre, jak Hypericum hirsutum i Hypericum empetrifolium zawierają tylko hyperycynę, podczas gdy Hypericum formosissimum tylko pseudohyperycynę. Często w badaniach oznacza się łącznie hyperycynę i pseudohyperycynę i określa się je jako całkowita hyperycyna, zaś protohyperycynę i protopseudohyperycynę jako protopigmenty.
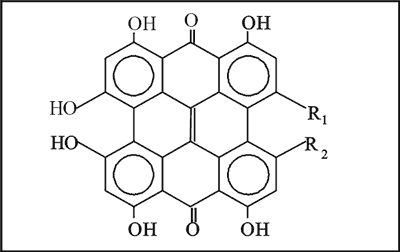
Ryc. 1. Budowa chemiczna hyperycyny i pseudohyperycyny.
R1=CH3; R2=CH3 Hyperycyna
R1=CH3; R2=CH2OH Pseudohyperycyna
Kwitnący dziurawiec zwyczajny zawiera około 30% hyperycyn w postaci protoform, przy czym największa zawartość jest w pąkach (48%), kwiatach (30%), mniejsza w liściach (17%). Stosunkowo mniejsza zawartość protopigmentów w liściach odpowiada ich największej ekspozycji słonecznej. Transformacja protoform we właściwe pigmenty (ryc. 2) jest procesem uzależnionym od długości fali świetlnej, intensywności promieniowania i zawartości azotu w powietrzu (9,10). Tempo przekształcenia jest największe w okresie kwitnienia rośliny, kiedy jest najwięcej światła. Jest ono jednak jeszcze większe podczas suszenia surowca na świetle oraz podczas ekstrakcji. W stanie naturalnym szybkość przekształceń protopigmentów w pigmenty jest mniejsza prawdopodobnie ze względu na obecność związków fenolowych działających jako naturalne fotoprotektory. Uważa się również, że wysokie stężenie hyperycyn w gruczołach także zmniejsza tempo postępującej transformacji (11).
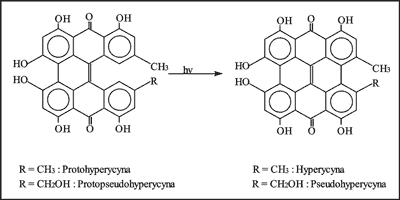
Ryc. 2. Przekształcenie protohyperycyny i protopsedohyperycyny w hyperycynę i pseudohyperycynę.
Zawartość całkowitej hyperycyny jest uzależniona od okresu zbioru, siedliska rośliny, sposobu suszenia i przechowywania ziela oraz innych czynników (10). Najmniejszą zawartość hyperycyny stwierdzono w gatunku Hypericum empetrifolium (0,009%), a największą w gatunku Hypericum boissieri (0,512%). Dla gatunku Hypericum perforatum ilość to waha się w granicach 0,05-0,15% (8).
Pochodne floroglucynowe – hyperforyna, adhyperforyna, furohyperforyna
Pochodne floroglucyny – hyperforyna, adhyperforyna i furohyperforyna (ryc. 3), stanowią dużą grupę związków o istotnym znaczeniu dla działania biologicznego dziurawca zwyczajnego. Odkrycie w 1975 roku hyperforyny zapoczątkowało badania na szeroką skalę nad jej działaniem biologicznym (6). W roku 1992 dokonano izolacji i identyfikacji adhyperforyny (6).
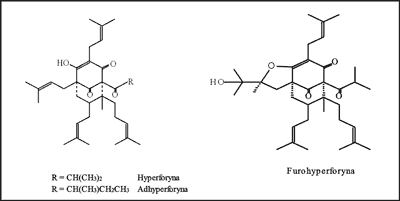
Ryc. 3. Budowa chemiczna hyperforyny, adhyperforyny i furohyperforyny.
Kwiaty zawierają około 2% hyperforyny i 0,2% adhyperforyny, przy czym zawartość ta się zwiększa w miarę przekwitania rośliny. Owoce dziurawca zwyczajnego mają już 5% hyperforyny i 2% adhyperforyny (51). Uważa się, że adhyperforyna i furohyperforyna stanowią naturalne układy i nie są produktami utleniania hyperforyny (12, 13). Oprócz tych trzech głównych pochodnych floroglucyny, stwierdzono obecność licznych polarnych związków, których ilość waha się między 0,05-0,3%. Te właśnie bardziej polarne związki są obecnie intensywnie badane, lecz nie wykazano, aby miały jakąkolwiek aktywność przeciwdepresyjną (14-19).
Bazując na szkielecie hyperforyny i adhyperforyny, dokonuje się również syntez nowych związków, które służą następnie do badań nad zależnością budowy od działania przeciwdepresyjnego. Część zsyntetyzowanych związków wykazuje pewną aktywność przeciwdepresyjną oraz działanie bakteriobójcze (20, 21). Dotychczas wyodrębniono następujące pochodne: 33-dezoksy-33-hydroperoksyfurohyperforynę, ortoforynę, oksepaforynę, 8,1-hemiacetal 8-hydroksyhyperforynę, pirano (7, 28) hyperforynę oraz hydroperoksykadyforynę, będącą połączeniem szkieletu kadyforyny z hyperforyną. Związki te powstają prawdopodobnie w procesie utleniania hyperforyny, która jest substancją bardzo niestabilną i utlenia się pod wpływem światła i podwyższonej temperatury (11, 22). Dlatego też stabilność ekstraktów z dziurawca zwyczajnego zwiększa się znacznie, jeśli przechowuje się je w opakowaniach ograniczających dostęp światła, co potwierdziły badania własne autora (23).
Flawonoidy
Flawonoidy (24-27) – łączna zawartość flawonoidów wynosi od 2 do 5% (70). Wyodrębniono następujące grupy związków:
– flawonole: kemferol, kwercetyna (0,3%),
– flawony: luteolina, eter 5,3"-dimetylowy luteoliny,
– glikozydy, głównie kwercetyny: hiperozyd (0,5-2,0%), rutyna (0,3-1,6%), kwercytryna (0,3%), izokwercytryna (0,3%), jak również glikozydy luteoliny, zwłaszcza 5-glukozyd i 3"-glukozyd luteoliny,
– biflawonoidy: amentoflawon (0,26%).
Proantocyjanidyny
Proantocyjanidyny (1, 25) – stanowią około 12% suchej masy surowca, włączając nasiona. Są to głównie katechiny i epikatechiny w postaci dimerów, trimerów, tetramerów oraz polimerów.
Kwasy fenolowe
Kwasy fenolowe (25) – zidentyfikowano m.in. kwas kawowy, chlorogenowy, p-kumarowy, ferulowy, izoferulowy, p-hydroksybenzoesowy, wanilinowy.
Olejki eteryczne
Olejki eteryczne (25, 28) – zawartość wynosi 0,05-1,0%, z czego mniej niż 30% stanowi 2-metylooktan. Występują także n-nonan, n-undekan, 2-metylodekan, a- i b-pinen, a-terpineol, geraniol, b-kariofylen (ok.14%), humulen i ślady monoterpenów (mircen, limonen).
Ksantony
Ksantony (29) – związki te występują dość rzadko w świecie roślin, ale są dosyć charakterystyczne dla rodziny Hypericaceae.
Inne składniki
Inne składniki (1, 25) – kwasy (izowalerianowy, nikotynowy, laurynowy, mirystynowy, palmitynowy, stearynowy), karotenoidy (luteina, violaxantyna, cis-trolina, trolichromon), cholina, witamina C, nikotynamid, pektyny, b-sitosterol, węglowodory nasycone (C16-C30) i alkohole (C24-C28).
Obecnie najbardziej powszechnym zastosowaniem ziela dziurawca jest wspomaganie leczenia umiarkowanych stanów depresyjnych. Początkowo działanie przeciwdepresyjne ekstraktu z dziurawca zwyczajnego wiązano z obecnością naftodiantronów, a w szczególności hyperycyny. Wykazano bowiem, że hyperycyna ma zdolność hamowania monoaminooksydazy A (MAO) – enzymu zaangażowanego w metabolizm amin katecholowych w mózgu, m.in. serotoniny (5-HT) i noradrenaliny (NA), co w konsekwencji nasila przekaźnictwo neuronalne zaburzone w przebiegu depresji (1). Podobny MAO-antagonizm stwierdzono dla części flawonoidów występujących w dziurawcu. W obu jednak przypadkach stężenia hamujące aktywność MAO były w ekstraktach zbyt małe, aby miało to istotne znaczenie kliniczne (25). W dalszych badaniach skupiono się na określeniu aktywności farmakologicznej różnych ekstraktów z dziurawca, przy czym badano ekstrakty etanolowe zawierające głównie pochodne naftodiantronowe, ekstrakty metanolowe zawierające większość aktywnych składników ziela dziurawca oraz ekstrakty n-heptanowe, w których dominowały składniki lipofilowe, jak hyperforyna (13). W badaniach wykazano, że związki zawarte w ekstrakcie etanolowym mają słabe działanie zmniejszające aktywność MAO. Hamują również aktywność b-hydroksylazy dopaminy, wykazują antagonizm w stosunku do receptora NMDA i hamują efekt działania GABA i kwasu a-amino-3-hydroksy-5-metylo-4-izopropionowego, prawdopodobnie poprzez wpływ na kanały jonowe (25).
Ekstrakt metanolowy, a w szczególności ekstrakt n-heptanowy, hamowały wychwyt serotoniny, noradrenaliny i dopaminy z przestrzeni synaptycznej, ale w sposób nieselektywny, przy czym ekstrakt heptanowy miał blisko dziesięciokrotnie silniejsze działanie w porównaniu do ekstraktu metanolowego, co korelowało z zawartością hyperforyny w obu ekstraktach (13). Ostatnie badania nad prawdopodobną przyczyną takiego działania ekstraktów z dziurawca zwyczajnego wykazały, że jest ona konsekwencją uwalniania amin katecholowych z cytoplazmatycznych zbiorników w neuronach, co zwiększa ich stężenie w cytoplazmie i w efekcie ujemnego sprzężenia zwrotnego, hamuje wychwyt z przestrzeni synaptycznej. Jest to więc mechanizm bardziej zbliżony do działania rezerpiny niż klasycznych leków przeciwdepresyjnych (30).
W następnym etapie szeroko zakrojonych badań nad skutecznością przeciwdepresyjną ziela dziurawca skoncentrowano się głównie na określeniu aktywności farmakologicznej poszczególnych związków, których identyfikacji dokonano uprzednio za pomocą technik analitycznych. W badaniach wykazano, że hyperycyna hamuje głównie aktywność b-hydroksylazy dopaminy, nieznacznie zmniejsza aktywność MAO, słabo wiąże się z receptorem 5-HT1. Natomiast jej wpływ na receptory adenozynowe (A1 i A2), adrenergiczne (a1, a2, b1), angiotensynowe (AT1), bradykininowe (b2), dopaminowe (D1), tachykininowE (NK1), opioidowe oraz wazopresynowe (V1), pozostaje bardzo mały lub żaden. Wykazuje natomiast umiarkowane działanie antagonistyczne w stosunku do receptorów CCKA, D2, endotelinowego ETA, NMDA i ośrodkowego H1, które jednak nie są prawdopodobnie zaangażowane w rozwój i przebieg depresji (1, 25).
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
24 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
59 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
119 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 28 zł
Piśmiennictwo
1. Bombardelli E., Marazzoni P.: Hypericum perforatum. Fitoterapia, 1995, 46, 43. 2. Moraczewski I. i wsp.: Flora ojczysta. Rośliny pospolite, chronione, ciekawe.... Stigma S.C., 2000. 3. Nutt D.: Management of patients with depression associated with anxiety symptoms. J. Clin. Psychiat. 1997, 58, 11. 4. Budavari S. et al: The Merck Index. Twelfth edition. Merck & Co. Inc., Whitehous Station, NY 1996. 5. Chatterjee S.S. et al.: Antidepressant activity of Hypericum perforatum and hyperforin: the neglected possibility. Pharmacopsychiatry 1998, 31, 7. 6. Erdelmeier C.A.J.: Hyperforin, possibly the major non-nitrogenosus secondary metabolite of Hypericum perforatum. Pharmacopsychiatry 1998, 31, 2. 7. Verotta L. et al.: Hyperforin analogues from St. John´s wort ( Hypericum perforatum). J. Nat. Prod. 2000, 63, 412. 8. Kitanov G.: Hypericin and pseudohypericin in some Hypericum species. Biochem. Syst. Ecol. 2001, 29, 171. 9. Briskin D., et al.: Influence of nitrogen on the production of hypericins by St. John´s wort. Plant Physiol. Biochem. 2000, 38, 413. 10.Southwell I.A. et al.: Seasonal variation in hypericin content of Hypericum perforatum L.. Phytochemistry 2001, 56, 437. 11.Poutaraud A., et al.: Effect of light on hypericin contents in fresh flowering tops parts and in an extract of St. John"s wort ( Hypericum perforatum). Planta Med. 2001, 67, 254. 12. Verotta L., et al.: Furohyperforin, a prenylated phlorogulcinol from St. John´s wort ( Hypericum perforatum). J. Nat. Prod. 1999, 62, 770. 13.Jensen A.G., et al.: Adhyperforin as a contributor to the effect of Hypericum perforatum L. in biochemical models of antidepressant activity, Life Sci. 2001, 68, 1593. 14.Fukuyama Y., et al.: Subellinone, a polyisoprenylated phloroglucinol derivative from Garcinia subelliptica. Phytochemistry 1993, 33, 483. 15.Trifunović S., et al.: Oxydation products of Hypericum perforatum. Phytochemistry 1998, 49, 1305. 16.Maisenbacher P., Kovar K.A.: Adhyperforin: A homologue of hyperforin from Hypericum perforatum. Planta Med. 1992, 58, 291. 17.Orth H., et al.: Orthoforin : The main degradation product of hyperforin from Hypericum perforatum. Pharmazie 1999, 54, 76. 18.Rűcker G., et al.: A C50- hydroperoxide from Hypericum perforatum. Arch. Pharm. (Weinheim) 1995, 328, 725. 19.Shan M.D., et al.: Three new hyperforin analogues from Hypericum perforatum. J. Nat. Prod. 2001, 64, 127. 20.Verotta L., et al.: Synthesis and biological evaluation of hyperforin analogues. J. Nat. Prod. 2002, 65, 433.21. Vugdelija S., et al.: A new heterocyclization product of adhyperforin from Hypericum perforatum (St. John"s wort). Molecules 2000, 5, 158. 22.Meisenbacher P., Kovar K.A.: Analysis and stability of Hyperici oleum. Planta Med. 1992, 58, 351. 23.Turek S.: Badania chromatograficzne ziela i preparatów z dziurawca zwyczajnego - Hypericum perforatum L.. Praca niepublikowana. 24.Muszyński J.: Farmakognozja. Zarys nauki o surowcach leczniczych. PZWL, Warszawa 1971. 25.Bilia A.R., et al.: St. John´s wort and depression. Efficacy, safety and tolerability-an update. Life Sci. 2002, 70, 3077. 26.Tekelova D., et al.: Quantitive changes of dianthrones, hyperforin and flavonoids content in the flower ontogenesis of Hypericum perforatum. Planta Med. 2000, 66, 778. 27.Dias A., et al.: Unusual flavonoids produced by callus of Hypericum perforatum. Phytochemistry 1998, 48, 7, 1165. 28.Borkowski B.: Zarys farmakognozji. Surowce o budowie tkankowej. PZWL, Warszawa 1952. 29.Kohlműnzer S.: Farmakognozja. PZWL, Warszawa 1998. 30.Roz N., et al.: Inhibition of vasicular uptake of monoamines by hyperforin. Life Sci. 2002, 71, 2227. 31.Vandenbogaerde A., et al.: Evidence that total extract of Hypericum perforatum affects exploratory behavior and exerts anxiolytic effects in rats. Pharmacol. Biochem. 2000, 65, 4, 627. 32.Kaehler S.T., et al.: Hyperforin enhances the extracellular concentrations of catecholamines, serotonin and glutamate in the rat locus coeruleus. Neurosci. Lett. 1999, 262, 199. 33.Langosch J.M., et al.: St. John´s wort ( Hypericum perforatum) modulates evoked potentials in guinea pig hippocampal slices via AMPA and GABA receptors. Eur. Neuropsychopharm. 2002, 12, 209. 34.Butterweck V., et al.: In vitro receptor screening of pure constituents of St. John´s wort reveals novel interaction with a number of GPCRs. Psychopharmacology 2002, 162, 193. 35.Barnes J., et al.: Herbal Medicines. A guide for healthcare professionals. Pharmaceutical Press, London 444. 36.Calapai G., et al.: Interleukin involvement in antidepressant action of Hypericum perforatum. Pharmacopsychiatry 2001, 34, 8. 37.Agostinis P., et al.: Hypericin in cancer treatment: more light on the way. Int. J. Biochem. Cell B 2002, 34, 221. 38.Chaloupka R. et al.: The effect of hypericin and hypocrellin-A on lipid membranes and membrane potential of 3T3 fibroblasts. Biochem. Bioph. Acta 1999, 1418, 39. 39.Kamuhabwa A.: Skin photosensitization with topical hypericin in hairless mice. J. Photoch. Photobio. 1999, 53, 110. 40.Koren H., et al.: Hypericin in phototerapy. J. Photoch. Photobio. B 1996, 36, 113. 41.Hlava B., et al: Rośliny kosmetyczne. PWRiL, Warszawa 1984. 42.Lavagna S., et al.: Efficacy of Hypericum and Calendula oils in the ephitelial reconstruction of surgical wounds in childbirth with caesarean section. Farmaco 2001, 56, 451. 43.Kang B.Y., et al.: Inhibition of interleukin-12 production in lipopolysaccharide-activated mouse macrophages by hypericin, an active component of Hypericum perforatum. Planta Med. 2001, 67, 364. 44.Hostanska K., et al.: Aqueous ethanolic extract of St. John"s wort ( Hypericum perforatum) induce growth inhibition and apoptosis in human malignant cells in vitro. Pharmazie 2002, 57, 323. 45.Albert D., et al.: Hyperforin is a dual inhibitor of cyclooxygenase-1 and 5-lipoxygenase. Biochem. Pharmacol. 2002, 64, 1767. 46.Samochowiec L.: Kompendium ziołolecznictwa. Wyd. Med. Urban&Partner, Wrocław 2002. 47.Gibbons S., et al.: The genus Hypericum - a voluable resource of anti- Staphylococcal leads. Fitoterapia 2002, 73, 300. 48.Carai M.A., et al.: Potential use of medicinal plants in the treatment of alcoholism. Fitoterapia 2000, 71, 38. 49.Ernst E.: Herbal medicinal products during pregnancy: are they safe? BJOG: Int. J. Gynaecol. Obstet. 2002, 109, 227. 50.Di Carlo G., et al.: St. John´s wort: Prozac from the plant Kingdom, Trends in Pharmaceutical Sciences 2001, 22, 6, 292. 51.Bombardelli E., et al.: IDN 5491 (Hyperforin trimethoxybenzoate). A new antidepressive drug. Eur. Neuropsychopharm. 2002, 12, 3, 240. 52.Ożarowski A.: Farmakodynamika surowców roślinnych. Wydawnictwo Przemysłu Lekkiego i Spożywczego, Warszawa 1960.



