Szanta zaliczana jest do roślin naziemnopączkowych (hemikryptofitów). Pędy tych roślin obumierają na zimę, natomiast pączki przezimowują, chronione przed przemarznięciem przez warstwę ściółki, obumarłych i żywych liści oraz glebę. Roślina ta dorasta do 80 cm wysokości. Łodygi rozgałęziają się w górnej części, są czterokanciaste i owłosione. Liście mają kształt okrągławy w dolnej części łodygi lub sercowaty w górnej części. Liście wyrastają ułożone względem siebie naprzeciwlegle, ich brzegi są nierówno ząbkowane i na dolnej powierzchni pokryte kutnerem. Kwiaty drobne, dwuwargowe i zrostłopatkowe, wyrastające w nibyokółkach w kątach liści. Kielich ma długość do 0,8 cm i złożony jest z 10 ząbków. Korona również jest pokryta kutnerem, ma biały kolor i długość do 0,6 cm. Warga górna ma długość do 3 mm, jest wąska i w szczytowej części krótko dwułatkowa. Warga dolna z kolei jest trzyłatkowa, a jej łatka środkowa ma kształt eliptyczny. Łatka środkowa jest w szczytowej części wycięta. Łatki boczne wyraźnie mniejsze i wydłużone. Kwitnie od czerwca do sierpnia. Owoce rośliny to rozłupina złożona z 4 rozłupek (7-9). Liście mają charakterystyczny smak i zapach piżma, który zanika podczas suszenia (10-12).
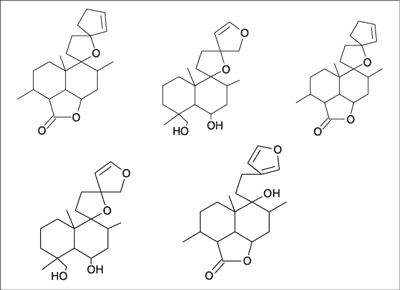
Głównym składnikiem ziela szanty jest mieszanina związków terpenowych (marubina – 0,3-1%, premarubina – 0,1%), alkoholi diterpenowych (marubenol, premarubenol, peregrinol, wulgarol) (13-15), steroli i triterpenów (kwas ursolowy 0,1%), pochodne fenolokwasów z grupy fenylopropanoidów (16-18), flawonoidów (apigenina, luteolina, kwercetyna) i ich glikozydy (19), tanin i garbników (7%), alkaloidów typu pirolidyny (betonicyna 0,3%, truicyna, cholina), olejków eterycznych (0,05%) i innych związków, takich jak kwasy organiczne, sole mineralne, saponiny (16, 20-22), hormony (gibereliny), witaminy (grup A, E, K), chromoforowe składniki purpury wzrokowej (retinina), alkoholowy składnik chlorofilów (fitol), kwasy żywiczne (np. kwas abietynowy), alkaloidy (koniina) oraz czynniki słodzące (stewiozyd). Biogeneza związków terpenowych wywodzi się od geranylogeraniolu, który powstaje w reakcji przedłużenia łańcucha prenylowego z udziałem pirofosforanu fernazylu (FPP) oraz pirofosforanu izopentynylu (IPP). Reakcję katalizuje transferaza prenylowa. Substancje z tej grupy są nielotne z parą wodną i stanowią składniki żywic i tzw. balsamów, które są bardzo złożonymi mieszaninami związków terpenowych, pochodnych fenylopropanu i wielu innych (23-26).
Niecykliczne składniki pirofosforanu geranylu (GGPP) mogą ulegać cyklizacji, przechodząc w izomeryczny pirofosforan geraniolu, który cyklizuje do dicyklicznego pirofosforanu labdanylu, a ten z kolei w wyniku dalszych przemian może tworzyć furanolabdany i ich pochodne (ryc. 1).
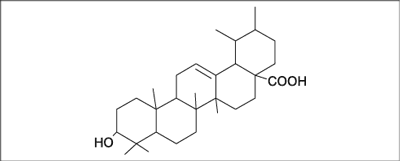
Dużą grupę związków zawartych w szancie stanowią sterole, m.in. β-sitosterol, kwas ursolowy (triterpen) (0,1%) (ryc. 2). Wykazują one właściwości cytotoksyczne, przeciwzapalne i zmniejszające stężenie cholesterolu we krwi (27-30).
1. Schaffner W. Rośliny lecznicze – chemizm, działanie, zastosowanie. Multico, Warszawa 1996.
2. Paluch A. Świat roślin w tradycyjnych praktykach leczniczych wsi polskiej. Acta Univ Wrat 1988; 263, 752.
3. Hedge IC. A global survey of biogeography of the Labiatae. Advances in Labiatae Science. Royal Bot Gard, Kew 1992; 7:17.
4. Mirek Z, Piękoś-Mirkowa H, Zając A i wsp. Flowering plants and pteridophytes of Poland. Pol Acad Sci, Kraków 2002; (1):442.
5. Zarzycki K, Szeląg Z. Czerwona lista roślin naczyniowych w Polsce. PAN, Kraków 2006; 9-20.
6. Zając M, Zając A, Tokarska-Guzik B. Extinct and endangered archaeophytes and the dynamics of their diversity in Poland. Biodiv Res Conserv 2009; 13:17-24.
7. Pawłowska S. Marrubium L. Szanta. Flora Polski 11. PWN, Kraków 1967; 97.
8. Cullen J, Tutin TG, Heywood VH i wsp. Red. Marrubium L. Flora Eur 3. Univ Press, Oxford 1972; 137-8.
9. Rutkowski L. Klucz do oznaczania roślin naczyniowych Polski niżowej. PWN, Warszawa 2006; 814.
10. Matuszkiewicz W. Przewodnik do oznaczania zbiorowisk roślinnych Polski. PWN, Warszawa 2008; 537.
11. Podlech D. Rośliny lecznicze. Muza, Warszawa 1997; 178.
12. Kącki Z, Czarnecka M. Marrubium vulgare (Lamiaceae) na Dolnym Śląsku – gatunek, który wymaga szczegółowych badań. Acta Bot Sil Suppl 2011; (1):165-7.
13. Rumińska A, Ożarowski A (red.). Leksykon roślin leczniczych. PWRiL, Warszawa 1990; 481.
14. Newal CA, Anderson LA, Philipson JD. Herbal Medicine: A guide for healthcare professionals. Pharm Press, London 1996; 165.
15. Bruneton J. Pharmacognosy, phytochemistry, medicinal plants. Lavoisier Londres, Paris 1999; 650.
16. Roth L, Dauderer M, Kormann K. Giftpflanzen Pflanzengifte. Nikol, Hamburg 1994.
17. Martin-Nizard F, Sahpaz S, Furman C i wsp. Natural phenylopropanoids protect endothelial cells against oxidized LDL-induced cytotoxity. Planta Med 2003; 69(3):207-11.
18. Martin-Nizard F, Sahpaz S, Kandoussi A i wsp. Natural phenylopropanoids inhibit lipoprotein-induced endothelin-1 secretion by endothelialcells. J Pharm Pharmacol 2004; 56(12):1607-11.
19. Kowalewski Z, Matławska J. Flavonoid compounds in the herb of Marrubium vulgare L. Herba Pol 1978; 24:183.
20. Ożarowski A. Wątroba – zapobieganie chorobom i leczenie sposobami naturalnymi. Portal Farm-Med, Warszawa 2006; 45.
21. Wawrzyniak E. Leczenie ziołami – kompendium fitoterapii. IWZZ, Warszawa 1992; 464.
22. Borkowski B (red.). Rośliny lecznicze w fitoterapii. Inst Rośl Przetw Ziel, Poznań 1994; 396.
23. Kączkowski J. Biochemia roślin, T 1, PWN, Warszawa 1982; 349.
24. Kączkowski J. Biochemia roślin. T 2, PWN, Warszawa 1985; 114.
25. Siemion JZ. Biostereochemia. PWN, Warszawa 1985; 311.
26. Kopcewicz J, Lewak S (red.). Fizjologia roślin. PWN, Warszawa 2005; 365.
27. Wolski T, Baj T, Matosiuk D i wsp. Szanta zwyczajna (Marrubium vulgare L.) – roślina lecznicza i miododajna. Ann Univ MCS 2007; 62(2):80-93.
28. Kohlmünzer S. Farmakognozja. PZWL, Warszawa 2000; 309-41.
29. Strzelecka H, Kowalski J. Encyklopedia zielarstwa i ziołolecznictwa. PWN, Warszawa 2000; 645.
30. Różański H. Medycyna dawna i współczesna. http://http://rozanski.li/?s=szanta.
31. Nagy M, Svajdlenka E. Comparison of essential oils from Marrubium vulagre L. and M. peregrinum L. J Essent Oil Res 1998; 10:585-7.
32. Bal Y, Kaban S, Kirimer N i wsp. Composition of essential oil of Marrubium parviflorum Fisch. et Mey ssp. oligodon (Boiss.) Seybold. J Essent Oil Res 1999; 11:300-2.
33. Lazari DM, Skaltsa HD, Constantinidis T. Essential oils of Marrubium velutinum Sm. and Marrubium peregrinum L., growing wild in Greece. Flav Fragr J 1999; 14:290-2.
34. Baher NZ, Mirza M, Shahmir F. Essential oil of Marrubium cuneatum Russell and its secretory elements. Flav Fragr J 2004; 19(3): 233-5.
35. Khanavi M, Ghasemian L, Motlagh EH i wsp. Chemical composition of essential oils of Marrubium parviflorum Fish. and C.A. Mey and Marrubium vulgare L. from Iran. Flav Fragr J 2005; 20(3):324-6.
36. Sahpaz S, Garbacki N, Tits M i wsp. Isolation and pharmacological activity of phenylpropanoid esters from Marrubium vulgare. J Ethnopharmacol 2002; 79(3):389-92.
37. Roman RR, Alarcon-Aguilar F, Lara-Lemus A i wsp. Hypoglycemic effect of plants used in Mexico as antidiabetics. Arch Med Res 1992; 23(1):59-64.
38. de Souza MM, De Jesus RAP, Cechinel-Filho V i wsp. Analgesic profile of hydroalcoholic extract obtained from Marrubium vulgare. Phytomed 1998; 5(2):103-7.
39. Schlemper V, Ribas A, Nicolau M i wsp. Antispasmodic effect of hydroalcoolic extract of Marrubium vulgare. Phytomed 1998; 5(2):211-6.
40. El Bardai S, Lyoussi B, Wibo M, Morel N. Comparative study of the antihypertensive activity of Marrubium vulgare and of the dihydropyrine calcium antagonist amlodipine in spontaneously hypertensive rat. Clin Exp Hypertens 2004; 26(6):465-74.
41. Meyre-Silva C, Cechinel-Filho V. A review of the chemical and pharmacological aspects of the genus Marrubium. Curr Pharm Des 2010; 16(3):3503-18.
42. Kahlouche-Riachi F, Mansour-Djalab H, Serakta-Delmi M i wsp. Evaluation of antibacterial activity of some wild plant of Algeria. Int J Med Arom Plant 2012; 2(2):275-80.
43. Nolte O, Haag H, Zimmerman A i wsp. Staphylococcus aureus positive for Panton-Valentine Leukocidin genes but susceptible to methicillin in patients with furuncles. Eur J Clin Microbiol Infect Dis 2005; 24(7):477-9.
44. Miklasevics E, Haeggman S, Balode A i wsp. Report on the first PVL-Positive community acquired MRSA strain in Latvia. Euro Surv 2004; 9(11):29-30.
45. Havaei SA, Ohadian S, Pourmand MR i wsp. Prevalence of genes encoding bi-component leukocidins among clinical isolates of methicillin resistant Staphylococcus aureus. Iran J Publ Health 2010; 39(1):8-14.
46. Boubaker K, Diebold P, Blanc DS. Panton – Valentine Leukocidin and staphylococcal skin infections in school children. Emerg Infect Dis 2004; 10(1):121-4.
47. Rim JY, Bacon AE. Prevalence of community – acquired methicillin-resistant Staphylococcus aureus colonization in a random sample of healthy individuals. Infect Control Hosp Epidemiol 2007; 28(9):1044-6.
48. Bokaeian M, Saboori E, Saeidi A i wsp. Phytochemical analysis, antibacterial activity of Marrubium vulgare L. against Staphylococcus aureus in vitro. Zahedan J Res Med Sci 2004; 16(10):60-4.
49. Wagner H, Bladt S. Plant Drug Analysis, Springer Verlag, Berlin 2001; 92.
50. Schlemper V, Ribas A, Nicolau M i wsp. Antispasmodic effects of hydroalcoholic extract of Marrubium vulgare on isolated tissues. Phytomed 1996; 3(2):211-6.
51. Ożarowski A, Jaroniewski W. Rośliny lecznicze i ich zastosowanie. IWZZ, Warszawa 1987; 365.
52. Matławska I (red.). Farmakognozja. AM, Poznań 2005; 214.
53. El Bardai S, Wibo M, Hamaide MC i wsp. Characterisation of marrubenol, a diterpene extracted from Marrubium vulgare, as an L-type calcium channel blocker. Br J Pharmacol 2003; 140(7):1211-6.
54. Sahpaz S, Garbacki N, Tits M i wsp. Isolation and pharmacological activity of phenylpropanoid esters from Marrubium vulgare. J Ethnopharmacol 2002; 79(3):389-92.
55. Vander Jagt TJ, Ghattas R, Vander Jagt DJ i wsp. Comparison of the total antioxidant content of 30 widely used medicinal plants of New Mexico. Life Sci 2002;70(9):1035-40.
56. Roman RR, Alarcon-Aguilar F, Lara-Lemus A i wsp. Hypoglycemic effect of plants used in Mexico as antidiabetics. Arch Med Res 1992; 23(1):59-64.
57. Herrera-Arellano A, Aguilar Santamaria L, Garcia-Hernandez B i wsp. Clinical trial of Cecropia obtusifolia and Marrubium vulgare leaf extracts on blood glucose and serum lipids in type 2 diabetics. J Phytomed 2004; 11(7-8):561-6.
58. De Souza MM, De Jesus RA, Cachinel-Filho V i wsp. Analgesic profile of hydroalkoholic extract obtained from Marrubium vulgare. Phytomed 1998; 5:103.
59. De Jesus RA, Cechinel-Filho V, Oliveira AE i wsp. Analysis of antinociceptive properties of marrubin isolated from Marrubium vulgare. Phytomed 2000; 7:111-5.
60. Meyre-Silva C, Yunes RA, Schlemper V i wsp. Analgesic potential of marrubin derivatives, a bioactive diterpene present in Marrubium vulgare (Lamiaceae). Farmaco 2005; 60(4):321-6.