© Borgis - Nowa Pediatria 1/2005, s. 30-38
Anna Popiel
Odma opłucnowa i krwioplucie u chorych na mukowiscydozę
Pneumothorax and haemoptysis in patients with cystic fibrosis
z Kliniki Pneumonologii, Alergologii Dziecięcej i Immunologii Klinicznej Akademii Medycznej w Poznaniu
Kierownik Kliniki: prof. dr hab. med. Jerzy Alkiewicz
Streszczenie
Cystic fibrosis is the most common inherited genetic disease among Caucasians. Expression of the protein encoded by cystic fibrosis gene in many organs is responsible for various clinical manifestation. Severity of lung pathology influences morbidity and mortality the most. Pulmonary complications can happened at every age. Epidemiology, pathogenesis, clinical symptoms, diagnosis and management of pneumothorax and haemoptysis in cystic fibrosis patients are discussed.

WSTĘP
Mukowiscydoza (CF-cystic fibrosis) jest najczęstszą genetycznie uwarunkowaną, śmiertelną chorobą rasy kaukaskiej zależną od mutacji pojedynczego genu. Gen mukowiscydozy zlokalizowany na ramieniu długim chromosomu 7 koduje białko zw. CFTcR (Cystic Fibrosis Trnamembrane conductance Regulator). Jest ono umieszczone w błonie szczytowej komórek i reguluje między innymi transport jonów – przede wszystkim chlorkowego i sodowego – przez błony komórkowe. Następstwem mutacji genu jest brak białka CFTcR i/lub jego funkcji w komórce. Ekspresja białka CFTcR w wielu narządach odpowiedzialna jest za różnorodną manifestację objawów klinicznych choroby. U większości chorych obserwuje się przede wszystkim zaburzenia ze strony układu oddechowego i pokarmowego. To właśnie stopień ciężkości przewlekłej choroby oskrzelowo-płucnej decyduje najczęściej o długości i jakości życia chorych na mukowiscydozę. Następstwem dysfunkcji białka CFTcR w nabłonku oddechowym jest nieprawidłowy skład środowiska wewnątrz dróg oddechowych zarówno w odniesieniu do stężenia jonów jak i zawartości wody i pozostałych składników śluzu oraz niedoboru naturalnych mechanizmów obronnych. Nadmierna lepkość śluzu oraz upośledzony klirens śluzowo-rzęskowy prowadzą do obturacji dróg oddechowych oraz sprzyjają rozwojowi przewlekłych infekcji bakteryjnych i przewlekłego zapalenia. Typowymi dla CF patogenami odpowiedzialnymi za rozwój zmian infekcyjno-zapalnych są Haemophilus influenzae, Staphylococcus aureus, Pseudomonas aeruginosa oraz Burkholderia cepacia. Szczególnie charakterystyczne dla mukowiscydozy jest zakażenie Pseudomonas aeruginosa. Dochodzi do niego często już we wczesnym dzieciństwie, jest złym rokowniczo momentem choroby, u większości chorych obserwuje się z czasem pojawienie się śluzowego typu bakterii oraz ich stałą obecność w wydzielinie z dróg oddechowych i praktycznie niemożliwą do uzyskania, mimo intensywnej terapii, eradykację zakażenia. Następstwem przewlekłej choroby oskrzelowo-płucnej jest rozwój rozstrzeni i innych nieodwracalnych zmian strukturalnych w układzie oddechowym, które doprowadzają ostatecznie do niewydolności oddechowej (1).
POWIKŁANIA W PRZEBIEGU PRZEWLEKŁEJ CHOROBY OSKRZELOWO-PŁUCNEJ
Powikłania związane z układem oddechowym mogą wystąpić u chorych na mukowiscydozę w każdym wieku. U młodszych dzieci zalicza się do nich:
– zapalenie oskrzelików, któremu towarzyszyć może ostra niewydolność oddechowa,
– niedodmę płatową (szczególnie w obrębie płata środkowego płuca prawego),
– gronkowcowe zapalenie płuc,
– oraz refluks żołądkowo-przełykowy.
U starszych dzieci, młodzieży i dorosłych przebieg przewlekłej choroby oskrzelowo-płucnej komplikować mogą:
– niedodma – segmentowa bądź płatowa,
– odma opłucnowa,
– krwioplucie,
– alergiczna oskrzelowo-płucna aspergilloza,
– serce płucne,
– ropniak opłucnej,
– i niewydolność oddechowa (2).
Właśnie odma opłucnowa i krwioplucie u chorych na mukowiscydozę będą przedmiotem rozważań w niniejszym artykule.
ODMA OPŁUCNOWA
Epidemiologia
Według doniesień literaturowych częstotliwość występowania incydentów samoistnej odmy opłucnowej w ciągu całego życia pacjentów chorych na CF oceniana jest na 2,8 do 18,9%. Średnia z danych opublikowanych w latach siedemdziesiątych i osiemdziesiątych to 6,4%, chociaż u chorych powyżej 10 roku życia wartość ta wynosi już 11%. Oczywiście, zachorowalność wzrasta razem z wiekiem chorych ze względu na progresję choroby oskrzelowo-płucnej dokonującą się z upływem czasu. Większość epizodów odmy opłucnowej występuje u chorych z umiarkowaną lub ciężką postacią choroby, przy czym parametry spirometryczne obserwowane u tych chorych w okresie poprzedzającym wystąpienie odmy to FEV1 (natężona objętość wydechowa pierwszosekundowa) poniżej 50% wartości należnej, nierzadko około 30% (3, 4). Według danych amerykańskiego rejestru chorych na CF u ok. 1% pacjentów rocznie występuje odma opłucnowa, 5 do 8% chorych doświadcza przynajmniej raz w ciągu życia tego powikłania, dla dzieci liczby te wynoszą 2-10%, a dla chorych dorosłych (powyżej 18 roku życia) 16 do 20% (5, 6). Ryzyko wystąpienia odmy opłucnowej jest takie samo dla kobiet jak i mężczyzn, nie obserwuje się również częstszego występowania odmy po jednej ze stron ciała. Wysoka jest natomiast częstotliwość występowania odmy opłucnowej po przeciwnej stronie po pierwszym epizodzie – 46%, a także bardzo wysoka jest częstość nawrotów, które definiowane są jako ponowne wystąpienie odmy opłucnowej po tej samej stronie w czasie powyżej 7 dni od ustąpienia poprzedniego epizodu (3).
Patogeneza
Najczęściej przyczynę powstawania odmy opłucnowej u chorych na CF tłumaczy się pękaniem podopłucnowo zlokalizowanych pęcherzy rozedmowych powstających w przebiegu choroby oskrzelowo-płucnej. Znajduje to potwierdzenie w stwierdzanej u 84% pacjentów poddawanych pleurodezie poprzez abrazję opłucnej obecności pęcherzy rozedmowych (5, 6). Jednakże u większości chorych opłucna płucna, poza cechami zapalenia, wydaje się być strukturalnie prawidłowa i nie różni się od opłucnej stwierdzanej u chorych z samoistną odmą opłucnową niecierpiących na CF. Tworzenie torbieli w płucach jest cechą charakterystyczną mukowiscydozy, w jednym z badań stwierdzano je u wszystkich chorych, u których wystąpiła odma opłucnowa, ale tylko u 60% chorych, u których powikłanie to nie wystąpiło. Powstawanie odmy jednakże nie koreluje z procentem objętości płuc objętym powstawaniem torbieli. Innym wytłumaczeniem powstawania odmy opłucnowej u chorych na CF może być mechanizm, w którym na skutek pułapki powietrza w pęcherzykach płucnych powstającej poprzez zatykanie śluzem drobnych oskrzeli i ich stan zapalny dochodzi do przedostawania się powietrza do śródmiąższu, a stamtąd do wnęk i śródpiersia. Wzrost ciśnienia powietrza w śródpiersiu miałby doprowadzać do przerwania śródpiersiowej opłucnej ściennej. Jest to mechanizm proponowany dla pierwotnej samoistnej odmy opłucnowej (3).
Sugeruje się, iż zwiększone ciśnienie w drogach oddechowych, zarówno w czasie mechanicznej wentylacji, a nawet w postaci nieinwazyjnych metod wspomagania oddychania, jak i w czasie zabiegów fizjoterapeutycznych ze zwiększonym, dodatnim ciśnieniem wydechowym może zwiększać ryzyko odmy. Jednakże doniesiono jak dotąd tylko o jednym przypadku powstania odmy opłucnowej u dziecka w cztery godziny po rehabilitacji oddechowej z użyciem dodatniego ciśnienia wydechowego, a mechaniczne wspomaganie oddychania musi opierać się na precyzyjnie i indywidualnie w stosunku do każdego pacjenta dobranych parametrach oddychania (7, 8). Podobnie jak u innych chorych istnieje także możliwość powstania odmy opłucnowej jatrogennej jako powikłania w czasie zakładania wkłucia centralnego.
Rozpoznawanie
Do typowych objawów klinicznych odmy opłucnowej należą: nagły ból w klatce piersiowej (dotyczący zazwyczaj jednej połowy ciała) względnie ból barku i/ /lub szyi oraz duszność lub przyspieszony oddech. Często objawom tym towarzyszyć może niewielkie krwioplucie. Obserwuje się także przyspieszoną czynność serca, bladość powłok skórnych względnie sinicę. U znacznej części chorych na mukowiscydozę odma opłucnowa może mieć przebieg bezoobjawowy i wykrywana jest przypadkowo w czasie rutynowego zdjęcia radiologicznego klatki piersiowej. W badaniu przedmiotowym stwierdzany jest odgłos opukowy bębenkowy, osłabienie względnie zniesienie szmeru pęcherzykowego i drżenia piersiowego nad płucem po stronie odmy oraz zmniejszona ruchomość klatki piersiowej. Odmie opłucnowej z nadciśnieniem towarzyszy przesunięcie śródpiersia objawiające się w badaniu przedmiotowym zmianą położenia uderzenia koniuszkowego i przesunięciem położenia tchawicy, towarzyszyć jej mogą także odma podskórna i objawy niewydolności krążenia. Najważniejszym badaniem dodatkowym służącym postawieniu diagnozy jest zdjęcie tylno-przednie klatki piersiowej, względnie boczne, lub w przypadku trudności diagnostycznych zdjęcia w fazie wdechu i wydechu (powietrze uwidacznia się w jamie opłucnowej w czasie zapadania się płuc w wydechu) lub w pozycji leżącej na boku (powietrze unosi się do góry i rąbek powietrza widoczny jest w prawej jamie opłucnowej w pozycji leżącej na lewym boku w przypadku odmy opłucnowej prawostronnej) (3, 5). Rzadko zachodzi konieczność wykonywania tomografii komputerowej klatki piersiowej, wskazane jest to w sytuacjach wymagających dokładnego określenia wielkości i lokalizacji odmy przed planowanym leczeniem inwazyjnym.
Leczenie
Każdy chory na mukowiscydozę z nowo zdiagnozowaną odmą opłucnową wymaga obserwacji szpitalnej. Jeśli w przypadku odmy bezobjawowej, małej (<20% objętości połowy klatki piersiowej lub zgodnie z aktualnymi zaleceniami British Thoracic Society wtedy, gdy na zdjęciu tylno-przednim klatki piersiowej grubość warstwy powietrza między brzegiem płuca a ścianą klatki piersiowej mierzy poniżej 2 cm) przy stabilnym stanie pacjenta, po 24 godzinach obserwacji, rtg klatki piersiowej nie wykazuje powiększania się odmy, względnie jej zmniejszanie się, chory może być zwolniony do domu do dalszej obserwacji w warunkach ambulatoryjnych (3, 5, 6, 9, 10, 11). Schemat postępowania w przypadku takiej odmy przedstawiono na rycinie 1.
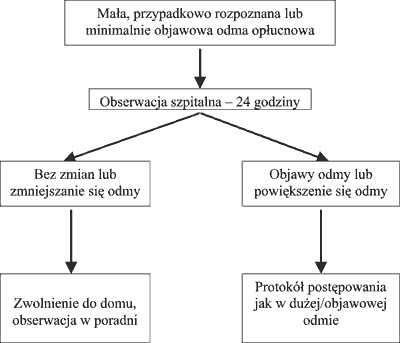
Ryc. 1. Postępowanie w odmie opłucnowej małej, przypadkowo rozpoznanej, bezobjawowej lub minimalnie objawowej u chorych na mukowiscydozę.
Odma opłucnowa objawowa, duża (>20% objętości połowy klatki piersiowej lub gdy na zdjęciu tylno- -przednim klatki piersiowej grubość warstwy powietrza między brzegiem płuca a ścianą klatki piersiowej wynosi 2 cm lub więcej) wymaga założenia drenu do jamy opłucnej. Dren musi mieć odpowiednio dużą średnicę. Miejsce założenia drenu zależy od lokalizacji odmy. Ze względu na wysokie prawdopodobieństwo, iż pacjent będzie wymagał w przyszłości zabiegu torakochirurgicznego należy unikać preferowanych przez torakochirurgów miejsc dostępu do klatki piersiowej. Najbardziej optymalnym miejscem jest zazwyczaj piąta lub szósta przestrzeń międzyżebrowa w linii pachowej środkowej, konieczne jest umieszczenie drenu o odpowiedniej długości i skierowanie go ku szczytowi płuca.
W przypadku dużych odm początkowo nie jest konieczne stosowanie ssania, jako że płuca mają tendencję do samorozoprężania się po ewakuacji wolnego powietrza z jamy opłucnej. Zastosowane do drenażu ssącego ujemne ciśnienie nie powinno przekraczać minus 20 cm słupa wody. Zbyt gwałtowne rozprężanie się zapadniętego płuca powoduje dyskomfort chorego i grozi powstaniem obrzęku płuc. Po założeniu drenażu jamy opłucnej konieczna jest kontrola radiologiczna. W przypadku utrzymywania się odmy opłucnowej można rozważyć założenie dodatkowego drenu do jamy opłucnej. Jeśli odma opłucnowa zmniejsza się można obserwować chorego przez 24-48 godzin, ale jeśli po tym okresie wyczekiwania odma opłucnowa jest ciągle obecna konieczny jest zabieg chirurgiczny. Brak objawów klinicznych, ustąpienie odmy, całkowite rozprężenia się płuca i brak przecieku powietrza do jamy opłucnej jest wskazaniem do usunięcia drenu. Większość lekarzy skłania się do wcześniejszego zamknięcia drenu na 12 godzin i obserwacji chorego przed ostatecznym usunięciem drenu. Jeśli mimo ustąpienia objawów klinicznych i rozprężenia płuca utrzymuje się przeciek powietrza, konieczna jest kontynuacja obserwacji chorego. Jeśli po pięciu dniach nadal utrzymuje się przeciek powietrza należy odstawić drenaż ssący i zastosować drenaż wodny. Po przeprowadzeniu ponownej oceny klinicznej i radiologicznej, w razie ponownego gromadzenia się powietrza w jamie opłucnej konieczny jest zabieg chirurgiczny. Pozostawianie drenu w jamie opłucnej na czas dłuższy niż 7 dni u pacjentów z CF związane jest z 50% śmiertelnością, konieczne jest więc w takich sytuacjach podjęcie decyzji o bardziej inwazyjnym leczeniu, podobnie jak w przypadku nawrotu odmy (3, 5, 6, 10-13). Protokół postępowania w przypadku odmy dużej, objawowej przedstawiono na rycinie 2.
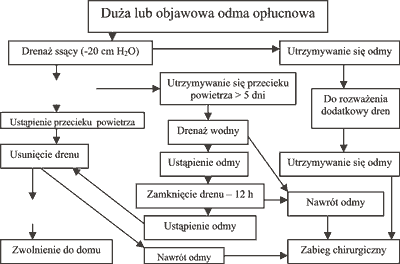
Ryc. 2. Postępowanie w odmie opłucnowej dużej, objawowej u chorych na mukowiscydozę.
Podawanie do jamy opłucnej czynników drażniących w celu wywołania zapalenia opłucnej, osiągnięcia zrostu między opłucną płucną a opłucną ścienną i zapobieżenie w ten sposób ponownemu gromadzeniu się powietrza w jamie opłucnej nosi nazwę pleurodezy chemicznej. Warunkiem powodzenia takiego postępowania jest wcześniejsze rozprężenie się płuca przed podaniem czynnika drażniącego tak, by opłucna płucna sąsiadowała bezpośrednio z opłucną ścienną, bez warstwy powietrza między nimi. Czynnik sklerotyzujący musi osiągnąć maksymalną dostępną powierzchnię mesotelium, bowiem to właśnie komórki mesotelialne są pierwotnym inicjatorem biologicznej kaskady prowadzącej do pleurodezy. Proces ten rozpoczyna się uruchomieniem kaskady krzepnięcia w opłucnej, następnie pojawia się sieć z włókien fibryny, w końcu dochodzi do proliferacji fibroblastów. Od 1935 roku kiedy to zastosowano talk doopłucnowo w celu uzyskania zrostów między opłucną płucną a ścienną, zaproponowano ponad 30 różnych czynników w celu uzyskania pleurodezy. Należą do nich między innymi wspomniany talk, tetracyklina, doxycyklina, minocyklina, bleomycyna, kwinakryna, Corynebacterium parvum, azotan srebra, 50% glukoza (3, 5, 9, 10, 11, 13-16). Zabiegi pleurodezy chemicznej są zazwyczaj bardzo bolesne, dlatego wymagają odpowiedniego postępowania przeciwbólowego tak miejscowego jak i ogólnego. Zaletą pleurodezy chemicznej jest zmniejszenie nawrotowości odmy opłucnowej u chorych z CF w porównaniu z postępowaniem zachowawczym czy zastosowaniem tylko drenażu przy jednoczesnym uniknięciu zabiegu chirurgicznego oraz koniecznego najczęściej wówczas znieczulenia ogólnego. Wadą tego leczenia jest brak możliwości bezpośredniej obserwacji dystrybucji środka drażniącego w jamie opłucnej oraz nieprzewidywalne chemiczne następstwa pleurodezy przede wszystkim pod postacią zrostów płuca z opłucną ścienną. Jest to szczególnie niebezpieczne w przypadku opłucnej przeponowej, ponieważ może uniemożliwiać prawidłowe kurczenie się przepony. Jeszcze do niedawna zastosowanie u chorych na CF pleurodezy chemicznej w przeszłości stanowiło bezwzględne przeciwwskazanie do transplantacji płuc w większości ośrodków zajmujących się transplantacją, ze względu na trudności w oddzieleniu płuc z powodu rozległych zrostów, a także możliwość obfitego krwawienia w czasie zabiegu. Aktualnie w większości ośrodków fakt ten nie stanowi już przeciwwskazania, bądź przeciwwskazanie względne. Panuje też opinia, iż ponieważ zdecydowana mniejszość (<20%) pacjentów z CF zakwalifikowanych do przeszczepu ostatecznie poddawanych jest temu zabiegowi, w razie konieczności podejmowania wcześniej decyzji odnośnie pleurodezy chemicznej chorzy powinni otrzymywać optymalne dla nich w danym momencie leczenie, nawet jeśli oznaczałoby to odstąpienie w przyszłości od transplantacji płuc. Dlatego uważa się, że chemiczna pleurodeza powinna być zarezerwowana dla tych chorych, których stan kliniczny jest na tyle ciężki, iż ryzyko zabiegu operacyjnego byłoby większe niż potencjalne korzyści z niego wynikające. Spośród stosowanych doopłucnowo czynników drażniących najskuteczniejsze w leczeniu odmy opłucnowej są kwinakryna i talk (3, 6, 9, 12, 14).
Postępowanie chirurgiczne w odmie opłucnowej u chorych na CF obejmuje otwartą torakotomię z ograniczoną chirurgiczną pleurodezą lub częściową pleurektomią, chirurgiczne zabezpieczenie pęcherzy rozedmowych poprzez założenie staplerów i zaszycie oraz wycięcie i rzadko usunięcie płata płuca z dużą liczbą pęcherzy rozedmowych (3, 4, 5, 10, 11, 13). Coraz częściej stosowane są też z powodzeniem zabiegi torakoskopii, w czasie których dokonuje się laserowej abrazji opłucnej, założenia staplerów na pęcherze rozedmowe, a przede wszystkim podania na ograniczonej przestrzeni pod kontrolą wzroku czynnika drażniącego, głównie talku (5, 6, 9, 17, 18, 19).
Nakłucie opłucnej i ewakuacja powietrza u chorych na CF z odmą opłucnową jest ograniczone tylko do sytuacji urgensowych, ratujących życie. Zastawki Heim- licha, nie zawsze wystarczające do całkowitej ewakuacji powietrza z jamy opłucnej, zapobiegające natomiast powstaniu odmy z nadciśnieniem, mają również ograniczone zastosowanie, najczęściej u pacjentów w czasie transportu względnie u tych, którzy mają być wkrótce poddani transplantacji płuc (5, 20).
Ze względu na wysoką nawrotowość odmy opłucnowej u chorych na CF leczonych zachowawczo względnie wyłącznie drenażem opłucnej sugerowane jest wczesne postępowanie inwazyjne z uprzywilejowaniem interwencji chirurgicznej, choć brak jest w tym zakresie wieloośrodkowych badań dotyczących oceny skuteczności różnych metod leczenia, których wyniki służyć by mogły wyborowi leczenia optymalnego. Niektórzy sugerują nawet konieczność interwencji po stronie zdrowej już po pierwszym epizodzie odmy opłucnowej ze względu na częste występowanie odmy po stronie przeciwnej w przebiegu choroby. Wyniki skuteczności różnych metod leczenia odmy opłucnowej u chorych z CF zostały zebrane przez Patricka Flume´a. Oparte są one na retrospektywnej analizie historii chorób, a nie na wynikach kontrolowanych prób klinicznych (tab. 1) (3).
Tabela 1. Wyniki różnych metod leczenia odmy opłucnowej u chorych na mukowiscydozę wg P. A. Flume´a.
| Sposób leczenia | Liczba pacjentów | Niepowodzenie | Wyleczenie | Nawrót |
| Obserwacja | 131 | 46 (35,1%) | 85 (64,9%) | 43 (50,7%) |
| Nakłucie | 31 | 17 (54,8%) | 14 (45,2%) | 11 (78,6%) |
| Drenaż | 221 | 83 (37,6%) | 138 (62,4%) | 75 (54,3%) |
| Pleurodeza chemiczna: Kwinakryna | 33 | 9 (27,3%) | 24 (72,7%) | 2 (8,3%) |
| Azotan srebra | 10 | 3 (30,0%) | 7 (70,0%) | 3 (42,9%) |
| Tetracyklina | 16 | 3 (18,8%) | 13 (81,3%) | 8 (61,5%) |
| Talk | 15 | 0 (0%) | 15 (100,0%) | 0 (0%) |
| Częściowa pleurektomia/abrazja | 118 | 4 (3,4%) | 114 (96,9%) | 9 (7,9%) |
Niepowodzenie – pacjenci, którzy wymagali dodatkowej interwencji.
Nawrót – pojawienie się odmy po tej samej stronie w czasie powyżej 7 dni od momentu ustąpienia poprzedniej odmy.
Powikłania
Najczęstszymi powikłaniami odmy opłucnowej u chorych na CF są niewydolność oddechowa, wstrząs, krwotok oraz ropniak opłucnej. Na podkreślenie zasługuje konieczność kontynuacji zabiegów rehabilitacyjnych, bowiem nie wpływają one na wynik leczenia odmy, są natomiast niezbędne dla leczenia mukowiscydozy (5).
Rokowanie
Odma opłucnowa jest niestety złym rokowniczo objawem w mukowiscydozie. Średnia długość życia po epizodzie odmy wynosi 30 miesięcy, choć są też doniesienia o pacjentach, którzy po epizodzie odmy żyją ponad 17 lat (3). Szczególnie niekorzystne jest rokowanie w przypadku odmy opłucnowej z nadciśnieniem, która występuje u około 40% chorych (6).
Zapobieganie
Zapobieganie wystąpieniu odmy opłucnowej u chorych z CF polega na unikaniu sytuacji i manewrów, które mogą doprowadzać do dużych wahań ciśnienia śródopłucnowego.
Dotyczy to dźwigania ciężarów, intensywnych ćwiczeń izometrycznych, nurkowania (z wyłączeniem basenów i płytkich zbiorników wodnych) oraz stosowania zabiegów fizjoterapeutycznych z wysokim dodatnim ciśnieniem wydechowym. Nie powinno się również podróżować samolotem ani helikopterem oraz wykonywać badań spirometrycznych przynajmniej przez dwa tygodnie po ustąpieniu odmy opłucnowej (5, 18).
Wszyscy chorzy na CF i ich opiekunowie muszą być poinformowani o wysokiej częstości nawrotów odmy opłucnowej, również po stronie przeciwnej niż w pierwszym epizodzie i konieczności szukania natychmiastowej pomocy lekarskiej w razie wystąpienia jakichkolwiek objawów sugerujących to powikłanie.
KRWIOPLUCIE
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
29 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
69 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
129 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 78 zł
Piśmiennictwo
1. Chmiel J.F., Davis P.B.: State of the Art.: Why do the lungs of patients with cystic fibrosis become infected and why can´t they clear the infection?. Resp. Res., 2003, 4, 8. 2.Marshall S.G., et al.: Hodson M. E.: Respiratory system. [W:] Cystic Fibrosis, Hodson M. E. , Geddes D.M., Arnold, London 2000, 203-242. 3.Flume P.A.: Pneumothorax in Cystic Fibrosis. Chest, 2003, 123, 217. 4.Seddon D.J., Hodson M.E.: Surgical management of pneumothorax in cystic fibrosis. Thorax, 1988, 43, 739. 5.Schidlow D.V., et al.: Cystic Fibrosis Foundation Consensus Conference Report on Pulmonary Complications of Cystic Fibrosis. Pediatr. Pulmonol., 1993, 15, 187. 6.Noppen M., et al.: Successful Management of Recurrent Pneumothorax in Cystic Fibrosis by Localized Apical Thoracoscopic Talc Poudrage. Chest, 1994, 106, 262. 7.Zach M., Oberwaldner B.: Effect of positive expiratory pressure breathing in patients with cystic fibrosis [letter]. Thorax, 1992, 47, 66. 8.Haworth C.S., et al.: Pneumothorax in adults with cystic fibrosis dependent on nasal intermittent positive pressure ventilation (NIPPV): a management dilemma. Thorax, 2000, 55, 620 9. Henry M., et al.: BTS guidelines for the management of spontaneous pneumothorax. Thorax, 2003, 58 (Suppl. II), ii39. 10.Aebersold A., Schaad U.B.: Pneumothorax bei zystischer Fibrose. Schweiz. Med. Wochenschr., 1991, 121, 174. 11.Schuster S.R., et al.: Management of Pneumothorax in Cystic Fibrosis. J. Pediatr. Surg., 1983, 18, 492. 12.Noyes B.E., Orenstein D.M.: Treatment of Pneumothorax in Cystic Fibrosis in the Era of Lung Transplantation. Chest, 1992, 101, 1187. 13.Spector M.L., Stern R.C.: Pneumothorax in cystic fibrosis: a 26-year experience. Ann. Thorac. Surg., 1989, 47, 204. 14.Rodriguez-Panadero F., Antony V.B.: Pleurodesis: state of art. Eur. Respir. J., 1997, 10, 1648. 15.Yancu Y., et al.: Peumothorax in cystic fibrosis: intrapleural instillation of Atabrine. Harefuah, 1991, 120, 264. 16. Kattwinkel J., et al.: Intrapleural Instillation of Quinacrine for Recurrent Pneumothorax. Use in a patient With Cystic Fibrosis. JAMA, 1973, 226, 557. 17.Daniel T.M., et al.: Thoracoscopy and Talc Poudrage for Pneumothoraces and Effusions. Ann. Thorac. Surg., 1990, 50, 186. 18.Tribble C.G., et al.: Talc Poudrage in the Treatment of Sontaneous Pneumothoraces in Patients with Cystic Fibrosis. Ann. Sur., 1986, 204, 677. 19.Ozcan C., et al.: Thoracoscopic treatmnet of spontaneous pneumothorax in children. J. Pediatr. Surg., 2003, 38, 1459. 20.Edenborough F.P., et al.: Use of a Heimlich flutter valve for pneumothorax in cystic fibrosis. Thorax, 1994, 49, 1178. 21.Barben J., et al.: Bronchial Artery Embolization for Hemoptysis in Young Patients with Cystic Fibrosis. Radiology, 2002, 224, 124. 22.Brinson G. M., et al.: Bronchial Artery Embolization for the Treatment of Hemoptysis in Patients with Cystic Fibrosis. Am. J. Respir. Crit. Care Med., 1998, 157, 1951. 23.Pinet C., et al.: Management of an Intrabronchial Rupture of Right Main Pulmonary Artery. A Case Report., Chest, 2002, 121, 988. 24.Antonelli M., et al.: Bronchial Artery Embolization for the Management of Nonmassive Hemoptysis in Cystic Fibrosis. Chest 2002, 121, 796. 25.Thomas S.R.: The pulmonary physician in critical care. Illustrative case 1: Cystic fibrosis. Thorax, 2003, 58, 357. 26.Sood N., et al.: Outcomes of Intensive Care Unit Care in Adults with Cystic Fibrosis. Am. J. Respir. Crit. Care Med., 2001, 163, 335. 27.Savage R.: Prone position as a life-saving measure for acute pulmonary haemorrhage in a young adult with cystic fibrosis. Anaesth. Intensive Care, 2002, 30, 223. 28.Savage S.: Prone, head down for pulmonary haemorrhage. Correspondence. Br. J. Anaesth., 2002, 89, 185. 29.Pogorzelski A., i wsp.: Krwawienie z dolnych dróg oddechowych u dzieci. Klinika Pediatryczna, 1996, 4, 43. 30.Graff G.R.: Treatment of recurrent severe hemoptysis in cystic fibrosis with tranexamic acid. Respiration, 2001, 68, 91. 31.Wong L.T., et al.: Treatment of recurrent hemoptysis in a child with cystic fibrosis by repeated bronchial artery embolizations and long-term tranexamic acid. Pediatr. Pulmonol., 1996, 22, 275. 32.Salerno S., et al.: Lateral thoracic artery embolization in cystic fibrosis. Acta Radiol., 2002, 43, 167. 33.Cipolli M., et al.: Bronchial artery embolization in the management of hemoptysis in cystic fibrosis. Pediatr. Pulmonol., 1995, 19, 344. 34.Thalhammer A., et al.: Bronchialarterienembolisation bei rezidivierenden oder akuten pulmonalen Blutungen von Patienten mit zystischer Fibrose. Rofo. Fortschr. Geb. Rontgenstr. Neuen Bildgeb. Verfahr., 2002, 174, 588. 35.Cohen A.M.: Haemoptysis - role of angiography and embolisation. Pediatr. Pulmonol. - Suppl., 1992, 8, 85. 36.Kaukuntla H.K., et al.: Extrapleural bronchial artery ligation for life-threatening hemoptysis in cystic fibrosis- a case report. Angiology, 2000, 51, 787.


