© Borgis - Nowa Pediatria 4/2004, s. 151-155
Jan Józefczuk1, Andrzej Radzikowski2, Piotr Albrecht2, Marcin Kuczyński1, Elżbieta Koprowska1
Zapalenia płuc u małych dzieci leczone cefuroksymem
Small children´s pneumonia treated with cefuroksym
1 z Oddziału Dziecięcego Szpitala Powiatowego w Nowej Dębie
Ordynator Oddziału: dr n. med. Jan Józefczuk
2 z I Katedry Pediatrii Akademii Medycznej w Warszawie
Kierownik Katedry: prof. dr hab. med. Andrzej Radzikowski
Streszczenie
Community acquired pneumonia (CAP) is still significant diagnostic problem in infants and small children. In this age group clinical differentiation between bacterial (pneumococcal and haemophilus) and viral CAP enable a proper choice of treatment. The betalactam antibiotic should be the initial first and basic empirical treatment for community acquired pneumonia in small children. It does not change the course of viral and bacterial atypical pneumonia but eradicating bacterial pathogens in case of bacterial typical pneumonia protects against purulent complications. Cefuroxime (parenteral sodium salt and oral axetil derivative) is a good choice in CAP in small children for its antibacterial activity (Str. pneumoniae including intermediate sensitivity and Haemophilus influenzae including beta lactamase positive strains) and also for small number of adverse effects. In this paper 2 year retrospective analysis is presented which demonstrates clinical success (improvement and cure) in 107/118 (90%) infants and small children and absence of serious adverse effects.

Wg definicji WHO, szczególnie aktualnej w krajach rozwijających się gdzie niedostępne jest powszechnie badanie radiologiczne, zapaleniem płuc nazywamy chorobę gorączkową przebiegającą z produktywnym kaszlem, dusznością tj. przyspieszeniem oddechu (w/s do norm wiekowych) i wciąganiem międzyżebrzy w przypadkach gdy nie można ustalić innych przyczyn tych objawów. Wg kryteriów europejskich i stosowanych w Ameryce Północnej zapalenie płuc to zakażenie dolnych dróg oddechowych, któremu towarzyszą: kaszel, duszność, gorączka i charakterystyczne zmiany obrazu radiologicznego płuc (1, 2, 3, 4).
Rozróżniamy dwie podstawowe kategorie zapalenia płuc (ZP): pozaszpitalne (PZP) i wewnątrzszpitalne tzw. nosokomialne (NZP). Częstość występowania PZP wynosi 2 do 15 na 1000 osób na rok. Najwyższa częstość występuje u dzieci małych (do 4. roku życia) i u osób starszych powyżej 65 rż. (5, 6). Natomiast nawet względna częstość NZP jest bardzo trudna do oceny. Przyjmuje się, że jest to druga najczęstsza postać zakażeń wewnątrzszpitalnych, a jednocześnie bardzo częsta przyczyna śmiertelności hospitalizowanych w szpitalu szczególnie u osób starszych (7). Przed wprowadzeniem amoksycyliny – pierwszego doustnego antybiotyku o wysokiej biodostępności – PZP leczono z zasady w szpitalu antybiotykami podawanymi parenteralnie. Wprowadzenie amoksycyliny, a następnie cefalosporyn doustnych o dobrej biodostępności i dużej aktywności przeciw pneumokokom (cefakloru, cefuroksymu aksetylu i cefprozylu) otworzyło nowe perspektywy dla ambulatoryjnego i domowego leczenia pzp. (8, 9). Ogromny postęp stanowiło wprowadzenie tzw. leczenia sekwencyjnego (kontynuowanego) tj. rozpoczętego w szpitalu parenteralnie a kontynuowanego w domu doustną formą tego samego leku lub jego odpowiednikiem (10, 11). Cefuroksym ze względu, że występuje i jest stosowany zarówno w postaci parenteralnej jak i zestryfikowanej doustnej szczególnie nadaje się do tej roli (11, 12).
Minęło dziesięć lat od wprowadzenia terapii kontynuowanej PZP w polskich szpitalach. Ten sposób leczenia wdrażaliśmy w warunkach niedostatku miejsc w naszych oddziałach, co powodowało konieczność przyspieszenia wypisu chorych do domu. Mimo że w niektórych regionach ustała przyczyna powodująca wprowadzenie tej metody czyli brak miejsc, to jednak skrócenie czasu hospitalizacji zmniejsza ryzyko zakażeń wewnątrzszpitalnych, a w szczególności biegunek rotawirusowych, a także zmniejsza stres wynikający z pobytu dziecka w szpitalu. Stąd pełna akceptacja rodziców. Do tego należy dodać niewątpliwe – pozytywne – efekty farmakoekonomiczne. Wszystko to uzasadnia dalsze stosowanie tej metody.
OBJAWY I ROZPOZNANIE
Głównymi objawami wczesnodziecięcego (do 4. roku życia) zp. są: kaszel (początkowo suchy, a następnie wilgotny), gorączka (często powyżej 39°C), przyspieszony oddech w/s norm wiekowych, stękanie oddechowe, wydłużenie fazy wydechowej, poruszanie skrzydełkami nosa, odwrócony typ oddychania (przerwa po wydechu) i niejednokrotnie „brzuch pneumoniczny”.
W badaniu osłuchowym, nad polami płucnymi, stwierdza się obecność dźwięcznych rzężeń drobnobańkowych. W badaniu opukowym zazwyczaj nie występują istotne zmiany patologiczne. W badaniu radiologicznym występuje znaczny polimorfizm zmian, od pojedynczych plamistych zagęszczeń, aż do zmian wieloogniskowych, niejednokrotnie zlewających się.
Badanie krwi często wykazuje znacznie podwyższoną: leukocytozę z przesunięciem obrazu w prawo, podwyższone OB, CRP.
Badanie mikrobiologiczne wydzieliny z tylnej ściany gardła i nagłośni pobieranej podczas laryngoskopii wnosi wiele istotnych informacji rozstrzygających o rodzaju stosowanej antybiotykoterapii (kontynuacja wdrożonej empirycznie lub zmiana). Badanie plwociny nie jest możliwe u dzieci poniżej 6. roku życia.
LECZENIE
Trudności w szybkim ustaleniu etiologii PZP, a w szczególności odróżnienia zakażenia wirusowego od bakteryjnego, a jeszcze trudniej wirusowego od mniej prawdopodobnego w tym wieku zakażenia bakteriami atypowymi u dzieci do 2 rż., powodują konieczność stosowania antybiotyku wdrażanego empirycznie, szczególnie w pierwszych dniach. We wstępnej antybiotykoterapii musimy uwzględniać nie tylko zakażenia Streptococcus pneumoniae, ale również, Haemophilus influenzae, Moraxella catarrhalis, a także kopatogenezę gronkowcową lub „hemofilusową”. Stąd wybór cefuroksymu jako leku zapewniającego eradykację ww. bakterii. Jest to zgodne z aktualnymi polskimi zaleceniami dotyczącymi leczenia PZP (13, 14).
Farmakokinetyka tego preparatu podanego dożylnie [soli sodowej przy dawkowaniu co 8 g (q8h) i po podaniu doustnym formy zestryfikowanej co 12 g (q12h)] pozwala na uzyskanie terapeutycznego poziomu we krwi i innych płynach ustrojowych przy dawkowaniu co 8g (q8h), co przestawiono na rycinie 1 (15). Natomiast wg najnowszych badań nad etiologią PZP nie musi być brana pod uwagę w tej grupie wiekowej etiologii „atypowej” jako mniej prawdopodobnej (16, 17, 18, 19, 20, 21, 22). Ze względu na to, że w referowanym materiale nie stwierdzaliśmy przypadków wskazujących na zachłyśnięcie, dokonując doboru leczenia empirycznego nie braliśmy pod uwagę kopatogenezy beztlenowcowej. Stąd wybór cefalosporyny a nie aminopenicyliny z inhibitorem betalaktamaz np. amoksycyliny z kwasem klawulonowym.
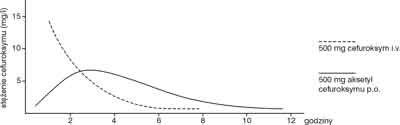
Ryc. 1. Stężenie cefuroksymu w surowicy uzyskiwane w następstwie podania dożylnego i doustnego (8).
MATERIAŁ I METODA
Analizą retrospektywną objęto 118 małych dzieci (70 chłopców, 48 dziewczynek) z zapaleniami płuc leczonych w latach 2000 i 2001. Średnia wieku – 18 miesięcy. Rozpoznanie ustalono na podstawie starannie zebranego wywiadu, dokładnego badania fizykalnego i badań dodatkowych.
W pierwszej fazie leczenia szpitalnego podawano cefuroksym dożylnie 100 mg/kg mc./24 h w trzech co 8 godzin dawkach.
W drugiej fazie (tzw. domowej) podawano aksetyl cefuroksymu 15-25 mg/kg mc./24 h w dwóch dawkach doustnie.
Kliniczny efekt leczenia oceniano według skróconej, czterostopniowej skali:
1. Wyleczenie – całkowite ustąpienie objawów.
2. Poprawa – wyraźne zmniejszenie objawów (bez konieczności zmiany antybiotyku).
3. Niepowodzenie – brak poprawy i konieczność zmiany antybiotyku.
4. Nawrót – ponowne wystąpienie objawów w ciągu czterech tygodni od zakończenia antybiotykoterapii.
WYNIKI
W obrazie klinicznym chorych dzieci dominował kaszel i podwyższona ciepłota ciała (tab. 1). Badania laboratoryjne i radiologiczne zebrano w tabelach 2-5.
Tabela. 1. Zestawienie objawów klinicznych.
| Objawy kliniczne | Liczba dzieci |
| Kaszel | 106 |
| Gorączka (>39°C) | 97 |
| Poruszanie skrzydełkami nosa | 71 |
| Stękanie oddechowe | 54 |
| Tachypnoe | 63 |
| Wydłużenie fazy wydechowej | 69 |
| Odwrócenie typu oddychania | 29 |
Tabela. 2. Wyniki OB.
| OB po godzinie | >30 | >60 | >100 |
| Liczba dzieci | 28 | 71 | 19 |
Tabela. 3. Stopień podwyższenia leukocytozy.
| Leukocytoza | >12 G/l | >20 G/l | >30 G/l |
| Liczba dzieci | 52 | 64 | 2 |
Tabela. 4. Nasilenie zmian radiologicznych.
| RTG klatki piersiowej | Stopień zmian |
| minimalny | średni | znaczny |
| Liczba dzieci | 36 | 59 | 23 |
Tabela. 5. Wyniki posiewów bakteriologicznych.
| Liczba dzieci |
| Streptococus pneumoniae | 51 |
| Moraxella catarrhalis | 19 |
| Haemofilus influenzae | 17 |
| Enterobacteriacae | 11 |
| Mieszana flora bakteryjna | 20 |
Zapalenie płuc w analizowanej grupie przebiegało z wyraźnie podwyższonym OB, wysoką leukocytozą i średnim stopniem zmian radiologicznych. W posiewach pobranych z nosogardła występuje wyraźna przewaga bakterii Streptococus pneumoniae.
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
29 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
69 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
129 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 78 zł
Piśmiennictwo
1. Campbell H.: Acute respiratory infection: a global challenge. Arch Dis Child 1995, 73:281-3. 2. The WHO Young Infants Study Group. Serious infections in young infants in developing countries: rationale for multicenter study. Pediatr Infect Dis J 1999, 18(10 suppl) S4-7. 3. Pneumonia. Diagnosis and treatment in hospital. Based on a round table meeting of UK specialist s Synergy Medical Education Synergy Hause 1993 Richmond UK. 4. Shidlow D.V. Callahan C.V.: Zapalenie płuc. Ped in Reviev wyd. pol., 1997, 1:4-7. 5. Chazan R.: Zakażenia układu oddechowego. Postępowanie diagnostyczno-terapeutyczne. Alfa-medica press, 1998. 6. Pogorzelski A.: Zapalenia płuc u dzieci. Klinika pediatryczna, 2002, 2, 253-256. 7. Mandell L.: Managing patients with nosocomial pneumonia Synergy Medical Education Synergy House 2000. Richmond UK. 8. Barlett S.J.G.: Impact of new oral antibiotics on the tratment of infectious diseases. Infectious Diseases in Clinical Practice 1995, 4 (Suppl.) 50-57. 9. Legnani D.: Role of oral antibiotics in the tratment of community-acquired lower respiratory tract infections. Diagn. Microbiol, Infect Dis 1997, 27:41-47. 10. Vogel F.: Transitional parenteral-to-oral therapy in community-acquired pneumonia. Hospital Practice Symposium Suppl 1996, 6:21-26. 11. Shalt I. et al.: Cefuroxime efficacy in pneumonia: sequential short course iv/oral suspension therapy. Israel J Med. Sci 1994, 30:684-89. 12. Scott L.J.: Ormrod D. and all: Cefuroxime axetil: an updated review of its use in the management of bacterial infections. Drags, 2001, 61, 1455-1500. 13. Hryniewicz W. i wsp.: Zakażenia układu oddechowego etiologia, rozpoznawanie i leczenie. Rekomendacje. 97 Fundacja Mikrobiologia Polska 1997. 14. Chazan R.: Zakażenia układu oddechowego. Postępowanie diagnostyczno-terapeutyczne w zakażeniach dróg oddechowych a-media press 1998. 15. Wiese R. et al.: The pharmacokinetics of orally absorbed cefuroksime compared with amoxycillin/clavulanic acid. J. Antimicrob Chemother, 1984, 13, 603-610. 16. Nelson J.D.: Community-acquired pneumonia in children: guidelines for treatment. Pediatr Infect Dis j 2000,19:251-3. 17. Ruuskanen O., Mertsola J.: Childhood community - acquired pneumonia. Semin Respir Infect 1999,14:163-172. 18. Izaacs D.: Problems in determining the etiology of community-acquired childhood pneumonia. Ped.Inf.Dis. J 1989, 8:143-49. 19. Korppi M.: Aetiology of community-acquired pneumonia in children treated in hospital. Eur J Ped 1993, 152:24-30. 20. Hriskanen-Kosma T.: Aetiology of childhood pneumonia: serologic results of prospective population-based study. Ped Infect Dis J 1998, 17:986-991. 21. Wubbel L.: Etiology and traatment of community-acquiredpneumonia in ambulatory children. Ped. Inf Dis J 1998, 18:98-104. 22. JuvenT. et al.: Etiology of community acquired pneumonia in 254 bhospitalised children pediatr. Infect Dis. J 2000, 19:293-8. 23. McCracken G.H.: Etiology and treatment of pneumonia. Pediatr Infect Dis J 2000, 19:273-7. 24. Radzikowski A., Albrecht P.: Leczenie objawowe zakażeń dróg oddechowych - podstawy patofizjologiczne i strategia postępowania Ped Pol 1998, 73: 1-8. 25. Trzciński K., Hryniewicz W. i Grupa Robocza Projektu Alexander: Wrażliwość na chemioterapeutyki szczepów bakteryjnych izolowanych z typowych zakażeń dolnych dróg oddechowych w Polsce w 1996. Med. Sc Monitor 1997, 3:714-22. 26. Marchant C.D. et al.: Measuring the comparative efficasy of antidacterial agents for acute otitis media: the pollyanna phenomenon. J Pediatr 1992, 120:72-7. 27. Dagan R. et al.: Bacteriologic and clinical efficacy of amoxicillin - clavulate vs.azitromycinin acute otitis media. Pediatr Infect Dis J 2000, 19:95-102. 28. Emeryk A.: Mykoplazma pneumoniae i Chlamydia pneumoniae w zakażeniach dróg oddechowych i chorobach obturacyjnych płuc. Wyd Medycyna Praktyczna 200. 29. Grossman D.F.: Zapalenia płuc wywołane prze bakterie atypowe. Medycyna Po Dyplomie. Wydanie Specjalne, sierpień 1999, 7-16. 30. Barlett J.G. et al.: File TM Community-Acquired Pneumonia in Adults: Guidelines for Management Clinical Infectious Disease 1998, 26:811-38. 31. Mandell L.A. Niederman M.: Antimicrobial treatment of community acquired pneumonia in adults:A conference report. Canadian J Infect Dis 1993, 4:25-28. 32. Garau J.: Basing Empiric Treatment Choices for respiratory Tract Infection. Journal of Chemotherapy 1999, 11:5-21. 33. Garau J.: Clinical failures: the tip of iceberg ? Respiratory Medicine 2001, 95 (supplement) S5-S11. 34. Heffelfinder J.D. et al.: Management of community acquired pneumonia in era of pneumococcal resistance. Arch Intern Med. 2000, 160:1399-408. 35. Mc Farland L.V. et al.: Pediatric clostridium difficile.: A Phantom menace or Clinical reality. J Ped Gastroent and Nutrition 2000, 31:220-231.

