© Borgis - Medycyna Rodzinna 1/2010, s. 14-19
*Marzena Zboch1, Bernadetta Gwizdak-Siwkowska1, Jarosław Serafin1, Krzysztof Śmigórski1, Paweł Tyfel1, Jerzy Leszek2
Niedobór witaminy B12 jako czynnik rozwoju procesu otępiennego
Deficit of vitamin B12 as a factor affecting development of the dementive process
1Ośrodek Badawczo-Naukowo-Dydaktyczny Chorób Otępiennych Akademii Medycznej we Wrocławiu
Kierownik Ośrodka: lekarz, specjalista chorób układu nerwowego Marzena Zboch
2Akademia Medyczna we Wrocławiu, Katedra i Klinika Psychiatrii
Kierownik Katedry i Kliniki: prof. dr hab. Andrzej Kiejna
Summary
Introduction:There are numerous reports available which show that vitamin B12 may be a factor of conversion of mild cognitive impairment into Alzheimer's Disease, of progression of Vascular Dementia and Alzheimer's Disease through a similar pathomechanism of brain blood vessels damage. The role of cyanocobalamine deficit in progression of potentially reversible dementia with prevalence of subcortical characteristics is commonly recognized. The untreated disease leads to irreversible dementia though.
Methods: The article presents a review of literature on vitamin B12 characteristics and its pathophysiology considered as a factor conducive to dementive process progression.
Results: B12 vitamin, its methabolic cycle altogether with causes and consequences of its disorders are described. Attention is paid to somatic, neurological, psychiatric manifestations of vitamin B12 deficit and diagnostic techniques enabling its identification. Discussion on the possibilities of the therapy of vitamin B12 deficit is also included.
Conclusions: B12 deficiency is an underestimated problem in clinical practice, while in fact it may be a significant cause of neurologic and psychiatric disorders, especially in geriatric populations. Emphasis put on the role of B12 deficiency and its consequences should make general practitioners more sensitive to a need of early detection of this hypovitaminosis and systematic supplementation.

Wstęp
W związku ze starzeniem się społeczeństwa obserwuje się wzrost ilości osób chorujących na choroby otępienne. Ocenia się, że obecnie około 24 miliony osób cierpi na jedną z form zaburzeń dementywnych, co roku zaś diagnozowanych jest ok. 4,6 miliona nowych przypadków. Szacuje się, że liczba osób dotkniętych chorobą otępienną będzie podwajać się co 20 lat, sięgając około 81 milionów w 2040 roku (1). Im wcześniejsze jest rozpoznanie objawów zaburzeń z kręgu demencji, tym większe możliwości efektywnego spowolnienia ich rozwoju. Z tego względu bardzo istotne jest obserwowanie czynników ryzyka tych chorób. Jednym z nich, pozostającym na marginesie zainteresowań klinicystów, jest obniżenie poziomu witaminy B12 (cyjanokobalaminy) w osoczu krwi. Związek pomiędzy niedoborem witaminy B12 w organizmie a deficytami funkcji poznawczych u osób starszych jest zjawiskiem dobrze udokumentowanym (2, 3). Pomimo zaleceń diagnozowania poziomu tej substancji w osoczu krwi (4, 5, 6), w codziennej praktyce są rzadko stosowane. Artykuł stanowi przegląd informacji na temat patofizjologii witaminy B12, omówienie zaburzeń internistycznych, neurologicznych, psychiatrycznych oraz zmian w funkcjonowaniu poznawczym spowodowanych niedoborem tej substancji.
Budowa i funkcje witaminy B12
Witamina B12 występuje w czystej postaci w postaci kryształków przypominających czerwone igiełki. Znajduje się naturalnie w wątrobie, mięsie, drożdżach, białku jaja kurzego i w różnych jarzynach. Posiada ugrupowania nukleotydowe, kobalaminowe oraz grupę cyjanową z atomem kobaltu (ta ostatnia bywa zastępowana przez inne ugrupowania – np. OH, CNS, NO2) (7).
Taka struktura determinuje jej bardzo ważne funkcje w przemianach biochemicznych: w cyklu aktywnego metylu jest kofaktorem metylotransferazy homocysteinowej, która katalizuje przemianę homocysteiny w metioninę; ponadto bierze udział w przekształceniu metylomalonylokoenzymu A w sukcynylokoenzym A i w konwersji rybonukleotydów w dezoksyrybonukleotydy.
Niedobór cyjanokobalaminy prowadzi do zaburzenia ww. mechanizmów biochemicznych i skutkuje nagromadzeniem homocysteiny, kwasu metylomalonowego oraz upośledzeniem syntezy DNA. Wysoki poziom homocysteiny uważany jest za niezależny czynnik ryzyka rozwoju miażdżycy, ale również otępienia naczyniopochodnego i choroby Alzheimera. Natomiast zmniejszenie syntezy DNA prowadzi do spowolnienia podziałów komórkowych – najlepiej zauważalnych w przypadku komórek układu krwiotwórczego. Ten ostatni patomechanizm skutkuje niedokrwistością, ale może spowodować również małopłytkowość i leukopenię.
Proces wchłaniania witaminy B12 dzieli się na kilka etapów. Pierwszy zaczyna się już w jamie ustnej w obecności śliny – tutaj witamina B12 łączy się z białkiem R i przechodzi do żołądka celem połączenia się z czynnikiem wewnętrznym Castle'a; taki kompleks wchłania się w jelicie cienkim. Stąd drogą krążenia wrotnego dostaje się do wątroby – gdzie zostaje zmagazynowany. Zapasy tej witaminy wynoszą kilka miligramów i przeważnie wystarczają na 1-2 lata (8).
Prawdziwe rozpowszechnienie niedoboru cyjanokobalaminy nie jest znane, istnieją jednak doniesienia o wzroście ryzyka niedoboru z wiekiem. Dotyka on ok. 5% osób w wieku 65-74 lat, zwiększa się do ponad 10% osób w wieku 75 lat i starszych (9), wg innych źródeł występuje u 15% osób powyżej 65. roku życia.
Niedobór foliatów jest powszechny u starszych osób, aczkolwiek tylko u 10% z niskim poziomem witaminy B12 odnotowano niski poziom foliatów. Przy diagnostyce niedoboru witaminy B12 istotne jest oznaczanie stężenia kwasu foliowego w surowicy, gdyż bierze on udział w tych samych procesach metabolicznych.
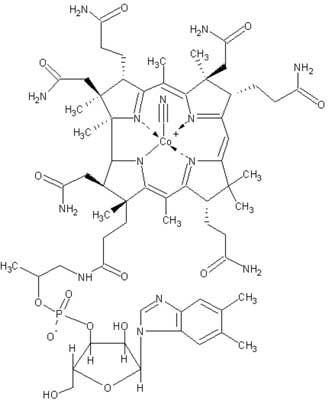
Ryc. 1. Struktura witaminy B12 (7).
Objawy kliniczne niedoboru witaminy B12 można umownie podzielić na tzw. internistyczne (dotyczące morfologii i przewodu pokarmowego) oraz dotyczące układu nerwowego (neurologiczne i psychiatryczne). Na pierwszy plan wysuwają się symptomy wynikające z zaburzenia funkcji układu krwiotwórczego. Należą do nich takie objawy niedokrwistości jak:
? stopniowo postępujące osłabienie,
? nietolerancja wysiłku,
? narastająca duszność,
? w skrajnych przypadkach – niewydolność krążenia.
W badaniu fizykalnym stwierdza się blado-szarawo-żółtawą cerę oraz szmery czynnościowe serca. W obrazie krwi obwodowej stwierdza się najczęściej makrocytozę erytrocytów i retikulopenię, może pojawić się małopłytkowość i leukopenia. Mielogram wykazuje obecność odnowy megaloblastycznej.
Tabela 1. Przyczyny niedoboru witaminy B12.
| Przyczyny niedoboru witaminy B12 (10) |
? obecność przeciwciał przeciwko komórkom okładzinowym żołądka i czynnikowi wewnętrznemu;
? niedobór czynnika wewnętrznego uwarunkowany genetycznie (dziedziczenie autosomalne recesywne);
? uszkodzenie błony śluzowej żołądka związane z infekcją Helicobacter pylori lub resekcją;
? niedostateczna podaż - u wegetarian, dzieci matek - wegetarianek, u alkoholików;
? schorzenia jelita cienkiego - zapalenie jelita, resekcja jelita, w zespołach genetycznych (mutacja na chromosomie 10p12.1), uchyłkowatość jelita;
? współzawodnictwo o kobalaminę - obecność pasożytów (bruzdogłowiec szeroki);
? achlorhydria - w przebiegu zanikowego nieżytu śluzówki żołądka, niedoczynność trzustki;
? zespół Zollingera-Ellisona;
? stosowanie lekarstw - np. kolchicyny, neomycyny, zydowudyny, kwasu paraaminosalicylowego, cholestyraminy, H2- blokerów (cimetidyny, famotidyny, ranitydyny), biguanidów, fenytoiny, fenobarbitalu, prymidonu, inhibitorów pompy protonowej - omeprazolu, pantoprazolu;
? nieprawidłowy transport białek - niedobór transkobalaminy II (dziedziczenie autosomalne recesywne - gen TCN2 - mutacja w obrębie chromosomu - 22q11.2);
? zaburzenia wewnątrzkomórkowego metabolizmu kobalaminy - metylomalonowa aciduria, homocystynuria u niemowląt;
? ekspozycja na NO;
? w przebiegu AIDS - prawdopodobnie proces złożony (niedostateczna podaż, przewlekła biegunka). |
W badaniach biochemicznych zazwyczaj odnotowuje się następujące odchylenia od normy (11):
? obniżony poziom witaminy B12,
? podwyższony poziom homocysteiny i kwasu metylomalonowego,
? nieznaczna hiperbilirubinemia i hipersyderemia,
? wysoka wartość LDH.

Ryc. 2. Cykl aktywnego metylu; (Objaśnienia: B-6 – pirydoksyna – witamina B-6; B-12 – cyjanokobalamina – witamina B-12; BH2 – dihydrobiopteryna; BH3 – trihydrobiopteryna; BH4 – tetrahydrobiopteryna; CBS – synteza beta-cystationinowa; NOS – śródbłonkowa synteza NO; 5MTHF – metylotetrahydrofolian; THF – tetrahydrofolian).
Niedobór cyjanokobalaminy z reguły diagnozuje się, gdy jej poziom w surowicy jest niższy od 150 pmol/l (1, 8). Jednak objawy niedoboru mogą pojawić się przy poziomie w osoczu witaminy B12 <200 pmol i wyższym. Bardziej wiarygodnym markerem jest podwyższony poziom homocysteiny (powyżej 20 pmol/l) (11, 9) lub kwasu metylomalonowego w surowicy (prawidłowe wartości zawarte są w przedziale 70-350 nM/l) (11, 12).
Ze strony przewodu pokarmowego pojawiają się objawy niedoborowe, zazwyczaj mało charakterystyczne, takie jak (11):
? nudności,
? biegunki lub zaparcia,
? cechy stanu zapalnego błony śluzowej jamy ustnej z utratą smaku.
Obraz „bawolego” języka, spowodowany zanikiem błony śluzowej, może wstępnie naprowadzić na właściwą diagnozę.
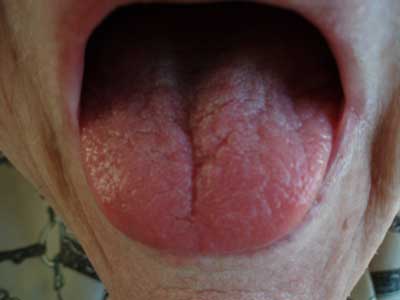
Ryc. 3. „Bawoli” język.
W powyższej sytuacji postępowanie lekarskie powinno obejmować dodatkowo: założenie sondy Key'a (pomiar BAO, MAO), wykonanie gastroskopii z pobraniem wycinka śluzówki, określenie obecności przeciwciał przeciw komórkom okładzinowym i czynnikowi wewnętrznemu.
W typowych przypadkach należy oczekiwać niskich wartości wydzielania żołądkowego (histaminooporna achlorhydria), cech zaniku błony śluzowej żołądka oraz ww. przeciwciał w chorobie Addisona-Biermera.
Zaburzenia neurologiczne w przebiegu niedoboru witaminy B12
Wpływ niedoboru kobalaminy na rozwój patologii układu nerwowego nie jest dokładnie poznany. Zaburzenia neurologiczne przypisuje się niewydolności mutazy metylomalonylo-CoA, enzymu zależnego od kobalaminy, który ma zasadniczy wpływ na zachowanie włókien mielinowych. Istotne znaczenie odgrywa redukcja s-adenozynometioniny (w skrócie SAM) i wzrost kwasu metylomalonowego (w skrócie MMA) (10, 12).
Niedobór SAM skutkuje nieprawidłową metylacją fosfolipidów, a w efekcie tego defekt mieliny w centralnym układzie nerwowym i może powodować encefalopatię i myelopatię. W dodatku, SAM wpływa na syntezę serotoniny, norepinefryny i dopaminy. To sugeruje, że deficyt witaminy B12 obok strukturalnych konsekwencji, wywiera czynnościowy wpływ na syntezę neurotransmiterów, co może być istotne dla pojawiania się zmian stanu psychicznego (10).
Podwyższony poziom MMA powoduje zmiany w strukturze złożonych kwasów tłuszczowych i następnie zaburzenia mielinizacji, prawdopodobnie prowadzące do nieprawidłowej transmisji nerwowej (10).
Ostatnie badania przedstawiają odmienny model: witamina B12 ma wpływ na koncentrację poziomu cytokin i czynnika wzrostu w obrębie mózgu, rdzenia i płynu mózgowo-rdzeniowego (10, 12, 13). Zwierzęce modele ujawniają, że niedobór foliatów i wysoki poziom homocysteiny niekorzystnie wpływa na odnowę DNA w neuronach hipokampa i czyni je podatnymi na toksyczność β amyloidu. Wzrost poziomu homocysteiny czy niedobór B12 koreluje z zanikiem mózgu w badaniu autopsyjnym oraz poprzez udział w mechanizmie uszkadzania naczyń krwionośnych jest czynnikiem ryzyka rozwoju choroby Alzheimera (AD – Alzheimer's disease) (14).
Objawy neurologiczne mogą się rozwinąć bez objawów anemii (20-30% przypadków) (9). Choroba rozwija się powoli, początkowo mogą pojawić się parestezje w obrębie rąk i stóp, niepewność chodu oraz objaw Lhermitte'a, następnie (w miarę utrzymywania się stanu niedoboru) rozwijają się inne objawy.
Przy występowaniu objawów neurologicznych w przebiegu niedoboru witaminy B12 wykonuje się neuroobrazowanie oraz elektrodiagnostykę układu nerwowego.
Badanie obrazowe (10):
? badanie MRI rdzenia kręgowego (z sekwencją T2 i FLAIR) – może wykazywać hiperintensywność sygnału w obrębie sznurów tylnych rdzenia w odcinku piersiowym lub u pacjentów ze schorzeniem przewlekłym zanik rdzenia,
? badanie MRI mózgowia – może pokazywać w sekwencjach T2 i FLAIR hiperintensywność sygnału w istocie białej i wokół komory czwartej.
Elektrodiagnostyka (10):
? somatosensoryczne potencjały wywołane (Somatosensory Evoked Potentials – SSEP) – mogą wykazywać wydłużenie latencji L3-P27,
? wzrokowe potencjały wywołane (Visual Evoked Potential – VEP) – wykazuje wydłużenie P100 (nawet bez zaburzeń wzroku, a normalizacja może wystąpić po wyrównaniu niedoboru),
? elektromiografia (Electromiography EMG – obniżenie prędkości przewodzenia oraz amplitudy neuronów czuciowych i ruchowych,
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
29 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
69 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
129 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 78 zł
Piśmiennictwo
1. Balk MD et al.: Vitamin B6, B12, and Folic Acid Supplementation and Cognitive Function. A Systematic Review of Randomized Trials. Arch Intern Med 2007; 167: 21-30. 2. Ravaglia G et al.: Homocysteine and folate as risk factors for dementia and Alzheimer disease. Am J Clin Nutr 2005; 82: 636-643. 3. Selhub J et al.: B vitamins, homocysteine, and neurocognitive function in the elderly. Am J Clin Nutr 2000; 71: 614S-620. 4. Moojiaart SP et al.: Homocysteine, vitamin B12, and folic acid and the risk of cognitive decline in old age: the Leiden 85-Plus Study. Am J Clin Nutr 2005; 82: 866-871. 5. Knopman DS, DeKosky ST, Cummings JL: Practice parameter: diagnosis of dementia (an evidence-based review). Report of the Quality Standards Subcommittee of the American Academy of Neurology. Neurology 2001; 56: 1143-1153. 6. Feldman HH et al.: Diagnosis and treatment of dementia. CMAJ 2008; 178: 7: 825-836. 7. Kraczkowska S, Suchocka Z, Pachecka J: Podwyższone stężenie homocysteiny we krwi jako wskaźnik zagrożenia zdrowia. Biul Wydz Farm AMW, Warszawa, 2005. 8. Hames D, Hooper NM: Krótkie wykłady BIOCHEMIA. Wyd. Naukowe PWN, Warszawa, 2007. 9. Clarke R et al.: Vitamin B12 and folate deficiency in later life. Age and Ageing 2004; 3334-3341. 10. Niranjan N, Florian P: Vitamin B12 – associated neurological diseases. www.E-medicine.com, 2008. 11. Dmoszyńska A, Robak T (red.): Podstawy hematologii. Wydawnictwo Czelej, Lublin, 2008. 12. Szczudlik A, Liberski P, Barcikowska M: Otępienie. Wydawnictwo UJ, Kraków, 2004: 422-424. 13. Kwieciński H, Kamińska AM: Neurologia Merritta. Urban and Partner Wrocław, 2004: 902-904. 14. Luchsinger J. et al.: Relation of higher folate intake to lower risk of Alzheimer disease in the elderly. Arch Neurol 2007; 64: 86: 86-92. 15. Masal R et al.: Cobalamine-Responsive Psychosis as the Sole Manifestation of Vitamin B12 Deficiency. JMAJ, 2001; 3: 701-703. 16. Reynolds EH: Folic acid, ageing, depression, and dementia. BMJ, 2002; 324: 1512-1515. 17. Brenda WJ et al.: Vitamin B12 Deficiency and depression in Physically Disabled Older Women: Epidemiologic Evidence From the Women's Health and Aging Study. Am J Psychiatry, 2000; 157: 715-721. 18. Tiemeyer H et al.: Vitamin B12, Folate, and Homocysteinein in Depression: The Rotterdam study. Am J Psychiatry, 2002; 159: 2099-2101. 19. Durand C et al.: Psychiatric Manifestations of Vit. B12 Deficiency: a Case Report. Encephale, 2003; 29 (6): 560-565. 20. Lerner V, Kanevsky M: Dementia with delirium caused by vitamin B12 deficiency. The International Journal of Psychiatry in Medicine, 2002; 2: 215-220. 21. Goggans FC: A case of Mania secondary to vitamin B12 deficiency. Am J Psychiatry, 1984; 141: 300-301. 22. Gomez-Bernal GJ, Bernal-Perez M: Vitamin B12 deficiency Manifested as Mania: A Case Report. J Clin Psychiatry, 2007; 9 (3): 238. 23. Ositek B, Szczupień E, Pniewski J: Trudności diagnostyczne w przebiegu podostrej paraplegii u kobiet z chorobą Adissona – Biermera. Neurologia i Neurochirurgia Polska 2004; 38 (5): 431-436. 24. Köseoglu E, Karaman Y: Relations between homocysteine, folate and vitamin B12 in vascular dementia and in Alzheimer disease. Clin Biochem 2007; 40 (12): 859-863. 25. Clarke R et al.: Low vitamin B12 status and risk of cognitive decline in older adults. Am J Clin Nutr 2007; 86 (5): 1384-1391. 26. Domýngueza RO et al.: Homocysteine, vitamin B12 and folate in Alzheimer's and vascular dementias: The paradoxical effect of the superimposed type II diabetes mellitus condition. Clinica Chimica Acta 2005; 359: 163-170. 27. Tsolaki M et al.: Relation between serum vitamin B12 levels and the progression of Alzheimer's disease, European Journal of Neurology 2005; 87: 37-300. 28. Wang HX et al.: Vitamine B12 and folate in relation to the developmentof Alzhaimner's disease. Neurology 2001; 56: 1188-1194. 29. Elias MF et al.: Homocysteine, Folate, and Vitamins B6 and B12 Blood Levels in Relation to Cognitive Performance: The Maine-Syracuse Study. Psychosomatic Medicine 2006; 68: 647-554. 30. Sułek K, Budziszewska K: Leczenie niedokrwistości. Wydawnictwo α- Medica Press, Bielsko-Biała 2002. 31. Malouf R: Vitamine B12 for cognition. Areosa Sastre 2003. 32. Eussen SJ et al.: Effect of oral vitamin B12 with or without folic acid on cognitive function in older people with mild vitamin B12 deficiency; a randomized, placebo-controlled trail,. Am J Clin Nutr 2006; 84 (2): 361-370.



