© Borgis - Medycyna Rodzinna 2/2013, s. 68-72
*Agnieszka Tołwińska1, Piotr Laudański2
Przewlekłe bóle brzucha u kobiet: przyczyny gastrologiczne czy ginekologiczne? Rola lekarza pierwszego kontaktu
Chronic pelvic pain in women: gastrological or gynecological causes? The role of primary care physician
1Niepubliczny Zakład Opieki Zdrowotnej EDMED w Białymstoku
Kierownik Zakładu: dr n. med. Edyta Eljasiewicz
2Klinika Perinatologii i Położnictwa, Uniwersytet Medyczny w Białymstoku
Kierownik Kliniki: prof. dr hab. n. med. Tadeusz Laudański
Summary
Chronic abdominal pain is a leading cause that brings women to see a primary care physician. In Great Britain 3.8% of female patients aged between 15-73 years suffer from pelvic pain. In comparison 3.7% suffer from asthma and 2% from migraine headaches (1). Diseases of the gastrointestinal tract are the cause of about 38% of pain symptoms in the pelvic area and gynecologic disorders about 20% (1, 2). Among the gynecologic medical conditions, endometriosis plays a significant role. Gastrointestinal disorders causing chronic pelvic pain most commonly include irritable bowel syndrome (IBS), inflammatory bowel disease – Crohn’s disease, ulcerative colitis and colorectal cancer. Clinical image of these diseases is very similar which causes a great risk of misdiagnosis. It requires interdisciplinary approach. The role of the primary care physician is to take a detailed medical history and conduct patient examination, as well as, accurately interpret additional test results and imaging test results. The next step in the diagnosis requires consultation with specialists i.e. gynecologists and gastrologists.

Wstęp
Przewlekłe bóle brzucha stanowią wiodącą przyczynę zgłaszania się kobiet do lekarza pierwszego kontaktu. W Wielkiej Brytanii wśród pacjentek w wieku 15-73 lata na przewlekłe bóle miednicy cierpi 3,8% kobiet. Dla porównania 3,7% choruje na astmę, a 2% zgłasza migrenowe bóle głowy (1).
Choroby przewodu pokarmowego stanowią przyczynę ok. 38% dolegliwości bólowych miednicy mniejszej, a dolegliwości ginekologicznych ok. 20% (1, 2). W pracy skupiono się na endometriozie, która wśród przyczyn ginekologicznych zajmuje dominujące miejsce oraz na patologiach przewodu pokarmowego, takich jak zespół jelita nadwrażliwego, nieswoiste zapalenia jelit i nowotwory jelita grubego. Obraz kliniczny powyższych schorzeń często bywa podobny i sprawia klinicystom trudności w prawidłowej diagnozie.
Endometrioza
Endometrioza jest estrogenozależną, zapalną chorobą, definiowaną jako obecność tkanek podobnych do endometrium poza jamą macicy, głównie w otrzewnej miednicy mniejszej i jajnikach (3). Może pojawić się również w miejscach odległych, poza miednicą mniejszą, np. w żołądku, płucach, mózgu, trzustce, śledzionie, wątrobie, nerkach, przeponie czy oku (4). Stwierdza się ją u kobiet w wieku od 12 do 80 lat, przy czym średni wiek diagnozy to 28 lat (5). Według różnych źródeł dotkniętych jest nią powyżej 10% kobiet w wieku reprodukcyjnym, 70-80% kobiet i nastolatek z przewlekłymi bólami miednicy oraz ok. 50% kobiet z niepłodnością (6, 7). Endometriozę ma 1/3 kobiet poddanych laparoskopii z różnych przyczyn oraz 5% kobiet poddanych laparoskopii, które nie mają przewlekłego zespołu bólowego miednicy mniejszej lub niepłodności (8).
Czynnikami zmniejszającymi ryzyko endometriozy są liczne porody, długie okresy laktacji, późny wiek pierwszej miesiączki. Z drugiej strony, krótkie cykle menstruacyjne, długie krwawienia miesięczne zwiększają ryzyko endometriozy. Rzadziej występuje u kobiet rasy czarnej i Azjatek niż u kobiet rasy kaukaskiej.
Jest kilka dość dobrze znanych teorii patogenezy endometriozy. Najbardziej popularną jest teoria menstruacji wstecznej, która zakłada, iż w trakcie menstruacji komórki endometrium poprzez jajowody transportowane są do jamy miednicy, gdzie dochodzi do implantacji na strukturach miednicy mniejszej. Menstruacja wsteczna występuje u ok. 90% kobiet, jednakże zaledwie u 10% rozwija się endometrioza. Może to świadczyć o pewnych zaburzeniach na poziomie molekularnym u wybranej grupy kobiet, w obrębie endometrium eutopowego (9) oraz szeregu dysfunkcji miejscowej i uogólnionej reakcji immunologicznej w zakresie wydzielania różnego typu substancji biologicznie aktywnych, takich jak hemokiny czy metaloproteinazy macierzy pozakomórkowej (10, 11). Kolejna teoria to rozprzestrzenianie się komórek endometrium drogą naczyń krwionośnych i chłonnych. Tłumaczy to lokalizację endometriozy poza jamą miednicy, na przykład w płucach i oku. Jeszcze inna teoria, tzw. metaplazji komórek otrzewnej, opisuje różnicowanie pod wpływem określonych czynników komórek mezotelium otrzewnej w komórki endometrialne.
Najczęstsza lokalizacja endometriozy to jajnik, zatoka Duglasa, więzadło szerokie macicy, więzadło maciczno-krzyżowe, macica, jajowody, jelito kręte, wyrostek robaczkowy i więzadło okrężne (12) (ryc. 1). Rzadziej zajęte są pochwa, szyjka macicy, przegroda maciczno-pochwowa, odbytnica, jelito czcze, kanały pachwinowe, pęcherz moczowy, moczowody i pępek (13). Sporadycznie endometrioza może wystąpić w gruczole piersiowym, trzustce, wątrobie, śledzionie, przeponie i centralnym układzie nerwowym (4).
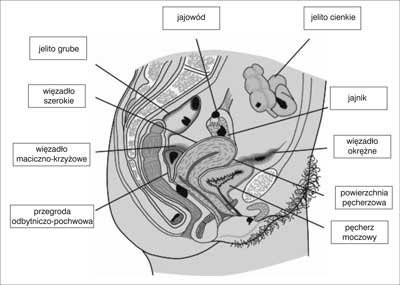
Ryc. 1. Lokalizacja endometriozy.
Amerykańskie Towarzystwo Medycyny Rozrodu klasyfikuje endometriozę ze względu na rozległość, głębokość naciekania i obecność zrostów (ryc. 2). Dzielimy ją na endometriozę minimalną (stage I – minimal) (ryc. 3), w której widoczne są izolowane implanty bez obecnych zrostów, endometriozę łagodną (stage II – mild), gdzie powierzchowne implanty naciekają otrzewną do średnicy 5 cm, bez widocznych zrostów, oraz umiarkowaną (stage III – moderate) z licznymi implantami powierzchownymi i głęboko naciekającymi, z obecnymi zrostami okołojajowodowymi i okołojajnikowymi. Ostatni stopień w klasyfikacji endometriozy to choroba zaawansowana (stage IV – severe), z licznymi powierzchownymi i głęboko naciekającymi implantami dotyczącymi również jajników. Obecne są też liczne zrosty.
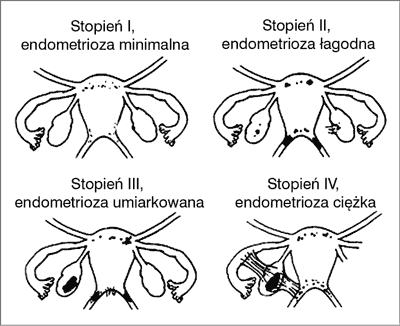
Ryc. 2. Klasyfikacja endometriozy.
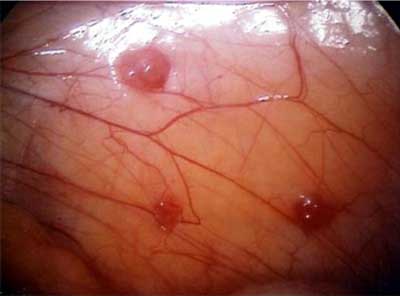
Ryc. 3. Endometrioza minimalna.
Endometrioza jest ściśle związana z zespołem objawów bólowych, takich jak bolesne krwawienia menstruacyjne (dysmenorrhea), bolesne stosunki płciowe (dyspareunia), przewlekłe bóle miednicy, bóle krzyża, bolesne oddawanie moczu i stolca (dysuria i dyshezja), zaparcia, krwawienia z odbytu, biegunka, krwiomocz, przewlekłe zmęczenie oraz niepłodność.
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
24 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
59 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
119 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 28 zł
Piśmiennictwo
1. Samraj GPN, Kuritzki LR, Whit Curry JR: Chronic Pelvic Pain in Women. Evaluation and Management in Primary Care. Comprehensive Therapy 2005; 31(1): 28-39. 2. Zontervan KT, Yudkin PL, Vessey MP et al.: Prevalence and incidence in primary care of chronic pelvic pain in women: evidence from a national general practice database. BJOG 1999; 106: 1149-1155. 3. Giudice LC, Kao LC: Endometriosis. Lancet 2004; 364: 1789-1799. 4. Redwine DB: Diaphragmatic endometriosis: diagnosis, surgical management and long-term results of treatment. Fertil Steril 2002; 77: 288. 5. Rawson JM: Prevalence of endometriosis in asymptomatic women. J Reprod Med 1991; 36: 513-515. 6. Eskenazi B, Warner ML: Epidemiology of endometriosis. Obstet Gynecol Clin North Am 1997; 24: 235-258. 7. Giudice LC: Endometriosis. The New England Journal of Medicine 2010; 24: 2389-2398. 8. Howard FM: Endometriosis end mechanisms of pelvic pain. J Minim Invasive Gynecol 2009; 16: 540-550. 9. Laudański P, Szamatowicz J, Kowalczuk O et al.: Expression of selected tumor suppressor and oncogenes in endometriumof women with endometriosis. Hum Reprod 2009; 24(8): 1880-1890. 10. Szamatowicz J, Laudański P, Tomaszewska I et al.: Hemokine growth-regulated-alpha: a possible role in the pathogenesis of endometriosis. Gynecol Endocrinol 2002; 16(2): 137-141. 11. Laudański P, Szamatowicz J, Ramel P: Matrix metalloproteinase-13 and membrane type-1 matrix metalloproteinase in peritoneal fluid of women with endometriosis. Gynecol Endocrinol 2005; 21(2): 106-110. 12. Jenkins S, Olive DL, Haney AF: Endometriosis: pathogenetic implications of the anatomic distribution. Obstet Gynecol 1986; 67: 335-338. 13. Victory R, Diamond MP, Johns DA: Villar’s nodule: a case report and systematic literature review of endometriosis externa of the umbilicus. J Minim Invasive Gynecol 2007; 14: 23-32. 14. Weed JC, Ray JE: Endometriosis of the bowel. Obstet Gynecol 1987; 69: 727-730. 15. Fauconnier A, Chapron C, Dubuisson JB et al.: Relation between pain symptoms and the anatomic location of deep infiltrating endometriosis. Fertil Steril 2002; 78: 719-726. 16. Tokushiege N, Markham R, Russel P et al.: High density of small nerve fibres in the functional layer of the endometrium in women with endometriosis. Hum Reprod 2006 a; 21: 782-787. 17. Barkley KJ, Rapkin AJ, Papka RE: The pains of endometriosis. Sciens 2005; 308: 1587-1589. 18. Al-Jefout M, Dezarnaulds G, Cooper M et al.: Diagnosis of endometriosis by detection of nerve fibres in en endometrium biopsy; a double blind study. Hum Reprod 2009; 24(12): 3019-3024. 19. Longstreth GF, Thompson WG, Chey WD et al.: Functional bowel disorders. Gastroenterology 2006; 130: 1480-1491. 20. Mulak A, Waszczuk E: Zespół jelita nadwrażliwego. [W:] Paradowski L (red.): Zaburzenia czynnościowe przewodu pokarmowego. Wydawnictwo Cornetis, Wrocław 2007; 111-124. 21. Grant Thompson W: Zespół jelita nadpobudliwego. [W:] Bianchi Porro G (red.): Gastroenterologia i Hepatologia. Wydawnictwo Czelej, wyd. I, Lublin 2003; 365-372. 22. Banerjee S, Farrel R, Lembo T: Gastroenterological causes of pelvic pain. Word J Urol 2001; 19: 166-172. 23. Drossman DA, Whitehead WE, Camilleri M: Irritable bowel syndrome: a technical review for practise guideline development. Gastroenterology 1997; 112: 2120-2137. 24. Moore J, Barlow D, Jewell D et al.: Do gastrointestinal symptoms vary with the menstrual cycle? Br J Obstet Gynaecol 1998; 105: 1322-1325. 25. Lea R, Bancroft K, Whorwell PJ: Irritable bowel syndrome, chronic pelvic inflammatory disease and endometriosis: a comparison of symptomatology. Eur J Gastroenterol Hepatol 2004; 16(12): 1269-1272. 26. Ferrero S, Abbamonte LH, Remorgida V et al.: Irritable bowel syndrome and endometriosis. Eur J Gastroenterol Hepatol 2005; 17: 687. 27. Bartnik W: Choroby jelita grubego. [W:] Szczeklik A (red.): Choroby wewnętrzne. Medycyna Praktyczna, Kraków 2005; 811-838. 28. Boulton R, Chawla MH, Poole S et al.: Ileal Endometriosis Masquerading Crohn’s Ileitis. Journal of Clinical Gastroenterology 1997; 25(1): 338-342. 29. Harty RF, Kaude JV: Invasive Endometriosis of the Terminal Ileum. A Cause of Small Bowel Obstruction of Obscure Origin. South Med J 1983; 766(2): 253-255. 30. Yantiss RK, Clement PB, Young RH: Endometriosis of the Intestinal Tract. The Am J Surg Pathol 2001; 25(4): 445-454. 31. Lopez PA, Martin L, Vicente M et al.: Ileal endometriosis and Crohn’s disease. A difficult differential diagnosis. Cirugia Espanola 2007; 82(2): 122-124. 32. Orholm M, Munkholm P, Langholz E et al.: Familiar occurrence of inflammatory bowel disease. N Engl J Med 1991; 324: 84-88. 33. Greenstein AJ, Sachar DB, Gibas A et al.: Outcome of toxic dilatation in ulcerative and Crohn’s colitis. J Clin Gastroenterol 1985; 7: 137-144. 34. Ledley GS, Shenk IM, Heit HA: Sigmoid colon perforation due to endometriosis not associated with pregnancy. Am J Gastroenterol 1988; 83: 1424-1426. 35. Langlois NE, Park KG, Keenan RA: Mucosal changes in the large bowel with endometriosis: a possible cause of misdiagnosis of colitis. Hum Pathol 1994; 25(10): 1030-1034. 36. Siegel R, Ward E, Brawley O et al.: Cancer statistics 2011: The impact of eliminating socioeconomic and racial disparties on premature cancer deaths. CA Cancer J Clin 2011; 61: 212-236. 37. Speights VO, Johnson MW, Stoltenberg PH et al.: Colorectal cancer: current trends in initial clinical manifestations. South Med J 1991; 84: 575-578. 38. Hartman D, Schilling D, Roth SU et al.: Endometriosis of the transverse colon – a rare localization. Deutsche Medizinische Wochenschrift 2002; 127(44): 2317-2320. 39. Yang Q, Wang H, Cho HY et al.: Carcinoma of mullerian origin presenting as colorectal cancer: clinicopathologic study of 13 cases. Ann Diag Pathol 2011; 15(1): 12-18.



