© Borgis - Nowa Stomatologia 3/2013, s. 120-124
*Agnieszka Mielczarek1, Joanna Michalik2, Marek Kujawa3
Wpływ wybranych preparatów fluorowych na mikrostrukturę szkliwa z wczesnymi zmianami próchnicowymi
The effect of selected fluoride products on microstructure of early caries lesions
1Katedra Stomatologii Zachowawczej, Warszawski Uniwersytet Medyczny
Kierownik Katedry: prof. dr hab. n. med. Elżbieta Jodkowska
2Zakład Informatyki Medycznej i Telemedycyny, Warszawski Uniwersytet Medyczny
Kierownik Zakładu: prof. dr hab. n. med. Robert Rudowski
3Katedra Histologii i Embriologii, Warszawski Uniwersytet Medyczny
Kierownik Zakładu: prof. dr hab. n. med. Jacek Malejczyk
Summary
Aim: The evaluation of the effect of selected fluoride formulations on microstructure of early caries lesions.
Material and methods: 120 polished human enamel specimens, embedded in cylindrical acrylic blocks served as a study material. The specimens were randomly assigned to 4 equinumerous groups, according to baseline microhardness of the enamel surface. The enamel samples were subjected to the preliminary demineralization, simulating the initial carious lesion. Upon demineralization one half of each specimen was covered with a protective varnish. Specimens were subjected to the 3 week cycle of pH changes, according to the protocol as follows: AC group – toothpaste containing nanohydroxyapatite (nano-HAP) and 1450 ppm F b.i.d., D group – Duraphat varnish once a week and toothpaste containing 1450 ppm b.i.d., F group – toothpaste containing 1450 ppm b.i.d., K(-) group – distilled water application. Samples were sectioned longitudinally and obtained surfaces were prepared for SEM examination.
Results: The analysis of SEM images revealed that toothpaste containing nano-HAP and fluoride was the most effective to reduce demineralization lesions within the subsurface enamel region, while Duraphat application was especially effective on the enamel surface.
Conclusions: The results proved that all the therapeutic protocols assessed succeeded to inhibit caries progression as well as to increase enamel mineralization. The effectiveness of particular remineralization procedures differed between various areas of carious lesions.

Wstęp
Wstępne stadium choroby próchnicowej – próchnica początkowa, ma charakter odwracalny. Etap ten charakteryzuje się powolnym tempem rozwoju. Przez kilka lat wczesna zmiana próchnicowa może rozwijać się w obrębie szkliwa i nie przekracza granicy szkliwno-zębinowej. Ognisko demineralizacji wykryte w tej fazie rozwoju ma charakter odwracalny – istnieje możliwość naprawy mikrouszkodzeń. Zmiana próchnicowa musi być jednak odpowiednio monitorowana i leczona metodami nieinwazyjnymi. Istotą nieinwazyjnego leczenia próchnicy jest zahamowanie tempa procesów demineralizacyjnych i inicjowanie procesów naprawy struktury szkliwa bez konieczności preparowania tkanek. Dotychczas główną zasadą wspomnianej terapii była eliminacja płytki nazębnej i aplikacja preparatów fluorowych (1). Postępowanie takie miało na celu inicjowanie zjawiska remineralizacji – hamowanie postępu procesu próchnicowego i odbudowę struktury szkliwa (2).
Obecność jonu fluorkowego w środowisku jamy ustnej blokuje lub spowalnia tempo demineralizacji oraz inicjuje remineralizację. Stężenie fluoru w stosowanym preparacie warunkuje przebieg jego reakcji ze szkliwem. Przy niskim stężeniu fluoru (poniżej 1%) wbudowuje się on w struktury szkliwa, tworząc fluorohydroksyapatyt lub fluoroapatyt. Wysokiemu stężeniu jonów fluorkowych towarzyszy natomiast tworzenie ziarnistości w postaci mikrokryształów fluorku wapnia z wbudowanymi fosforanami. Depozyty te precypitują na powierzchni szkliwa, biofilmu, zagłębień retencyjnych czy ubytków próchnicowych. Tworząc warstwę ochronną i stabilny rezerwuar fluoru ziarnistości fluorku wapnia, mogą stanowić jednocześnie barierę wymiany jonowej z podpowierzchniowymi strefami szkliwa (3, 4).
Warunkiem właściwie rozumianej remineralizacji wczesnych zmian próchnicowych jest optymalna rekrystalizacja zarówno warstwy powierzchownej, jak i strefy centralnej. Trwają więc poszukiwania skutecznych formuł terapeutycznych, które wykorzystają pełen potencjał remineralizacyjny twardych tkanek zęba. Na rynku pojawiają się preparaty o różnej zawartości fluoru i biodostępnych związków mineralnych, przeznaczonych do naprawy wczesnych, próchnicowych uszkodzeń szkliwa (5-7). Zasadne wydaje się więc prowadzenie badań w celu opracowania skutecznych modeli nieinwazyjnego leczenia wczesnych zmian próchnicowych.
Cel pracy
Celem prezentowanej pracy jest ocena wpływu wybranych preparatów fluorowych na mikrostrukturę szkliwa z próchnicą początkową.
Materiał i metody
Jako materiał badawczy wykorzystano ludzkie zęby trzonowe i przedtrzonowe. Wycięto z nich fragmenty prawidłowego szkliwa w kształcie walca o przekroju 6 mm. Próbki zatopiono w bloczkach akrylowych (Villacryl Hard Rapid, Zhermack, Włochy), płukano w myjce ultradźwiękowej, szlifowano oraz polerowano ostatecznie pastą polerską z tlenkiem glinu o wielkości ziarna 3 μm (Linde 3, AB Gamma Alumina). Na podstawie uśrednionej z 5 pomiarów wykonanych w punktach referencyjnych średniej powierzchniowej mikrotwardości szkliwa (SMH) próbki randomizowano do 4 grup. Zestawienie materiału badawczego przygotowanego do dalszych badań zaprezentowano w tabeli 1.
Tabela 1. Zestawienie materiału badawczego.
| Nazwa grupy | Symbol grupy | Cecha grupy | Rodzaj preparatu | Czas aplikacji |
Grupa 1
30 próbek | AC | 1% Nano-HAP
1450 ppm F- | Pasta Apa Care,
Cumdente,
Niemcy | 2 min,
2 × dz., 15 dni |
Grupa 2
30 próbek | D | 1450 ppm F-
22 600 ppm F- | Pasta Blend-a-med,
P & G, USA
Duraphat,
Colgate, USA | 2 min,
2 × dz., 15 dni
1 × tydz., 3 dni |
Grupa 3
30 próbek | K(+) | 1450 ppm F- | Pasta Blend-a-med,
P & G, USA | 2 min,
2 × dz., 15 dni |
Grupa 4
30 próbek | K(-) | 0 ppm F- | Woda destylowana,
DEMI-POL, Polska | 2 min,
2 × dz., 15 dni |
W próbkach inicjowano wczesne sztuczne zmiany próchnicowe wg procedury opisanej przez White’a (8). Połowę powierzchni każdej próbki izolowano lakierem kwasoodpornym, a następnie zastosowano trwający 3 tygodnie cykl naprzemiennych zmian pH opracowany przez Featherstone’a i opisany we wcześniejszej publikacji (9, 10). W trakcie cyklu demineralizacji i remineralizacji próbek aplikowano testowane preparaty wg protokołu: w grupie AC – 2 razy dziennie pastę do zębów z nanohydroksyapatytem (nano-HAP) i 1450 ppm fluoru, w grupie D – 1 raz w tygodniu lakier Duraphat i 2 razy dziennie pastę do zębów 1450 ppm, w grupie K(+) – 2 razy dziennie pastę do zębów 1450 ppm, w grupie K(-) wodę destylowaną. Schematyczny diagram stosowanych procedur badawczych przedstawiono na rycinie 1.
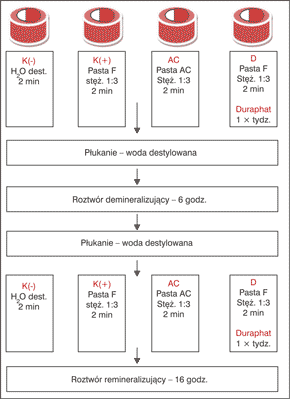
Ryc. 1. Dobowy model zastosowanych w badaniu cyklicznych zmian pH.
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
29 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
69 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
129 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 78 zł
Piśmiennictwo
1. Pawlaczyk-Kamieńska T: Nowe propozycje leczenia próchnicy zębów mlecznych – na podstawie piśmiennictwa. Czas Stomatol 2010; 63(10): 638-644. 2. Piesiak-Pańczyszyn D, Kaczmarek U, Woźniak J: Wpływ wytrawiania powierzchni wczesnej zmiany próchnicowej na proces jej leczenia z użyciem różnych preparatów remineralizacyjnych – badania in vitro. Czas Stomatol 2005; 9: 620-627. 3. Kaczmarek U: Mechanizmy kariostatyczne fluoru. Czas Stomatol 2005; 6: 404-413. 4. Featherstone JD: Prevention and reversal of dental caries: role of low level fluoride. Community Dent Oral Epidemiol 1999; 27: 31-40. 5. Lu KL, Zhang JX, Meng XC, Li XY: Remineralization effect of the nano-HAP toothpaste on artificial caries. Key Eng Mater 2007; 167-270, 330-332. 6. Todd MA, Staley RN, Kanellis MJ et al.: Effect of fluoride varnish on demineralization adjacent to orthodontic brackets. Am J Orthod Dentofacial Ortop 1999; 116: 159-167. 7. Reynolds EC: Remineralization of enamel subsurface lesions by casein phosphopeptide – stabilized calcium phosphate solutions. J Dent Res 1997; 76: 1587-1595. 8. White DJ: Use of synthetic polymer gels for artificial carious lesion preparation. Caries Res 1987; 21: 228-242. 9. Featherstone JDB, O’Reilly MM, Shariati M, Brugler S: Enhancement of remineralization in vitro and in vivo. Factors relating to demineralization and remineralization of the teeth. Leach SA, IRL Press Ltd, Oxford 1986; 23-34. 10. Mielczarek A, Michalik J: Wpływ pasty z nanohydroksyapatytem na mikrotwardość powierzchni szkliwa z próchnicą początkową – badania in vitro. Nowa Stomatologia 2013; 2: 73-77. 11. Trairatworakur C, Kladkaew S, Songsiripradabboon S: Active management of incipient Caries and choice of materials. J Dent Res 2008; 87(3): 228-232. 12. Poggio C, Lombardini M, Vigorelli P, Matteo C: Analysis of dentin/enamel remineralization by CPP-ACP Paste: AFM and SEM study. Scanning 2013; 9999: 1-9. 13. Kotsanos N, Darling AL, Levers BG, Tyler JE: Simulation of natural enamel caries in vitro with methylcellulose acid gels: effect of addition of calcium and phosphate ions. J Biol Buccale 1989; 17(3): 159-165. 14. Ten Cate JM, Duijsters PP: Alternating demineralization and remineralization of artificial enamel lesions. Caries Res 1982; 16: 201-210. 15. Larsen MJ, Fejerskov O: Chemical and structural challenges in remineralization of dental enamel lesions. Scand J Dent Res 1989; 97: 285-296. 16. Hicks MJ, Silverstone LM: Acid-etching of caries-like lesions of enamel: a polarized light microscopic study. Caries Res 1984; 18(4): 315-326. 17. Al-Khateeb S, Exterkate R, Angmar-Mansson B, Ten Cate B: Effect of acid-etching on remineralization of enamel white spot lesions. Acta Odontol Scand 2000; 58(1): 31-36.

