Tomasz Ozorowski, Ewa Fischbach, Paweł Gruszczyński, Maria Nowacka, Mirosława Wilk, Paweł Grzesiowski1
(przy współpracy Krajowej Grupy Roboczej ds. zakażeń szpitalnych przy Krajowym Specjaliście w dziedzinie mikrobiologii klinicznej)
Zintergowany system szpitalnej polityki antybiotykowej – doświadczenia Wielkopolskiego Centrum Chorób Płuc i Gruźlicy w Poznaniu
Integrated system of hospital antibiotic policy – experiences of the Centre for Pneumonology and Tuberculosis in Poznań
z Wielkopolskiego Centrum Chorób Płuc i Gruźlicy w Poznaniu
1 z Centralnego Laboratorium Surowic i Szczepionek w Warszawie

Wprowadzenie
Wprowadzanie na rynek farmaceutyczny nowych leków przeciwbakteryjnych, ich szerokie stosowanie, często nadmierne, prowadzą do niekontrolowanego wzrostu oporności bakterii oraz kosztów leczenia.
Polska jest jednym z nielicznych krajów, w których w dziedzinie terapii zakażeń i gospodarowania zasobami leków przeciwbakteryjnych istnieje pełna dowolność. Jest to spowodowane pomijaniem w przeszłości aspektów ekonomicznych w działalności zakładów opieki medycznej, a także braku przygotowania merytorycznego środowiska lekarskiego do szybko powiększającego się rynku leków oraz dynamicznych zmian w mikrobiologii. W chwili obecnej do najpoważniejszych zagrożeń epidemiologicznych w środowisku szpitalnym zaliczane są metycylinooporne gronkowce (MRSA), penicylinooporne pneumokoki (PNSP), wankomycynooporne enterokoki (VRE) oraz wielooporne pałeczki Gram-ujemne. Jednym z niezbędnych elementów walki z narastającą opornością bakterii jest ograniczenie i racjonalizacja użycia antybiotyków w środowisku szpitalnym.
Cel pracy
Celem obecnej pracy było opracowanie kompleksowego systemu szpitalnej polityki antybiotykowej i eksperymentalne wdrożenie w Wielkopolskim Centrum Chorób Płuc i Gruźlicy (WCChPiG) w Poznaniu.
Materiał i metoda
Wielkopolskie Centrum Chorób Płuc i Gruźlicy jest 250-łóżkowym szpitalem specjalistycznym przyjmującym rocznie około 7000 pacjentów. Szpital posiada 8-łóżkowy oddział intensywnej opieki medycznej, torakochirurgii, onkologii, leczenia gruźlicy, 3 oddziały pulmonologiczne i oddział wewnętrzny.
W 1998 roku został powołany zespół ds. antybiotykoterapii, którego zadaniem było opracowanie i przedstawienie Komitetowi Terapeutycznemu założeń szpitalnej polityki antybiotykowej. W skład zespołu weszły 3 osoby: lekarz ds. kontroli zakażeń szpitalnych ze specjalizacją w zakresie chorób wewnętrznych, kierownik apteki szpitalnej i mikrobiolog kliniczny.
Projekt szpitalnej polityki antybiotykowej składał się z następujących elementów:
1. Określenie zakresu odpowiedzialności i zadań zespołu ds. antybiotykoterapii.
2. Analiza retrospektywna zużycia antybiotyków na podstawie danych z apteki szpitalnej (umożliwiła ocenę zużycia antybiotyków wg kosztów, dni leczenia, i rozbicia tych danych na poszczególne oddziały).
3. Analiza wrażliwości drobnoustrojów na leki przeciwzakaźne na podstawie danych z laboratorium szpitalnego, Konsultanta Wojewódzkiego w Dziedzinie Mikrobiologii oraz Alexander Project Group i Polish Alexander Project Collaborative Group.
4. Kampania edukacyjna dla środowiska lekarskiego.
5. Receptariusz szpitalny i rekomendacje do leczenia najczęściej występujących zakażeń.
6. Formularz zlecania antybiotyków.
7. Strategia zapobiegania narastania oporności drobnoustrojów na antybiotyki.
8. Zasady kontroli działań marketingowych firm farmaceutycznych na terenie szpitala.
9. Nadzór nad przepływem informacji o przedszpitalnej antybiotykoterapii.
10. Współpraca z lekarzami rodzinnymi i kasą chorych w zakresie kreowania regionalnej polityki antybiotykowej.
Wyniki i omówienie
W 1997 roku wydatki na antybiotyki stanowiły 30-35% budżetu apteki przeznaczonego na zakup leków. Stosowano 45 różnych preparatów leków przeciwzakaźnych, przy czym antybiotyki podawane pozajelitowo stanowiły 60% całkowitej ilości stosowanych leków przeciwbakteryjnych. Zużycie według grup antybiotyków i poszczególnych preparatów przedstawiano w tabeli 1 oraz na rycinie 1. Zestawienie zużycia wszystkich antybiotyków umożliwiło zlokalizowanie tych, które są najczęściej zlecane i których racjonalizacja stosowania będzie istotna dla polityki antybiotykowej, a tym samym dla budżetu szpitala. Mimo stosowania w WCChPiG 45 różnych preparatów przeciwbakteryjnych, koszt 8 z nich stanowił 70% środków finansowych wydawanych na tę grupę leków (ryc. 2).
Tabela 1. Antybiotyki stosowane w WCChPiG w 1997 r. – wg częstości stosowania i procent kosztów całkowitych wydanych na zakup antybiotyków.
| Antybiotyk | % kosztów | Antybiotyk | % kosztów |
| 1. Amoksycylina/klawulonian | 15 | 24. Flukonazol | NI |
| 2. Doksycyklina | 2 | 25. Ciprofloksacyna | 2 |
| 3. Pefloksacyna | 2 | 26. Karbenicylina | 2 |
| 4. Trimetoprim/sulfametoksazol | NI | 27. Ceftazydym | 2 |
| 5. Penicylina | 10 | 28. Cefaleksyna | NI |
| 6. Cefuroksym | 7 | 29. Norfloksacyna | NI |
| 7. Gentamycyna | NI | 30. Natamycyna | NI |
| 8. Ceftriakson | 10 | 31. Klarytromycyna | NI |
| 9. Netylmycyna | 12 | 32. Ampicylina | NI |
| 10. Roksytromycyna | 2 | 33. Piperacylina/tazobaktam | 2 |
| 11. Ketokonazol | NI | 34. Cefradyna | NI |
| 12. Klindamycyna | 10 | 35. Tobramycyna | NI |
| 13. Ofloksacyna | 1 | 36. Linkomycyna | NI |
| 14. Nystatyna | NI | 37. Cefoperazon | NI |
| 15. Piperacylina | 6 | 38. Cefaklor | NI |
| 16. Cefotaksym | 4 | 39. Spiramycyna | NI |
| 17. Cefazolina | 2 | 40. Wankomycyna | NI |
| 18. Kolistyna | 1 | 41. Amoksycylina | NI |
| 19. Cykloseryna | NI | 42. Imipenem | NI |
| 20. Erytromycyna | NI | 43. Cefadroksyl | NI |
| 21. Amikacyna | NI | 44. Teikoplanina | NI |
| 22. Ceftibuten | NI | 45. Amfoterycyna B | NI |
| 23. Ampicylina/sulbaktam | 2 | NI - nieistotne | |
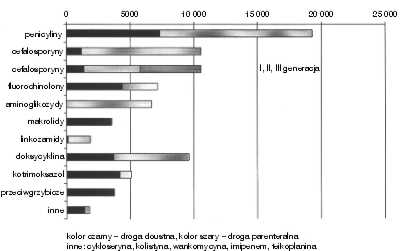
Ryc. 1. Zużycie antybiotyków w WCChPiG w 1997 r., w przeliczeniu na osobodni leczenia.
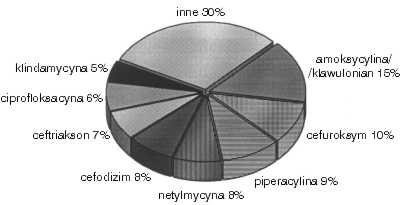
Ryc. 2. Antybiotyki konsumujące 70% środków finansowych przeznaczonych na zakup tej grupy leków.
Na podstawie przeprowadzonych analiz i zaproponowanej administracyjnej metody kontroli zużycia, antybiotyki zostały podzielone na trzy kategorie dostępu:
1. Kategoria I: antybiotyki ogólnie dostępne.
2. Kategoria II: antybiotyki kontrolowane, tj. zamawiane dla określonego pacjenta przez konkretnego lekarza na podstawie wypełnionego odpowiedniego formularza (ryc. 3). Dla tych antybiotyków pierwsze zlecenie jest realizowane na okres do 3 dni w leczeniu empirycznym i do 5 dni w leczeniu celowanym (opis poniżej).
FORMULARZ ZAMAWIANIA ANTYBIOTYKU
Pacjent ............................................................. Nr historii choroby .............................. Wiek ..................
Waga .................... Oddział .............................. Alergie ..............................................
I. Leczenie empiryczne (zamówienie I na okres do 72 godz.)
1. Zakażenie: podejrzenie [ ] potwierdzone [ ] Rodzaj zakażenia.............................................
2. Zlecone posiewy: nie zlecono [ ] plwocina [ ] popłuczyny [ ] mocz
[ ] rana [ ] krew [ ] inne.................................. |
| Data | Godzina | Antybiotyk | Dawka
jednorazowa | Droga podania | Częstość
podawania na dobę | Liczba dni leczenia | Podpis |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
II. Leczenie celowane (zamówienie I na okres do 5 dni)
Rodzaj zakażenia .......................... Patogen ............................................... Istotna wrażliwość ................................................ |
| Data | Godzina | Antybiotyk | Dawka
jednorazowa | Droga podania | Częstość
podawania na dobę | Liczba dni leczenia | Podpis |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
III. Profilaktyka antybiotykowa (preparat, liczba dawek)
................................................................................................................................................................................................................................
IV. Antybiotyki podawane przed zleceniem
................................................................................................................................................................................................................................
V. Uwagi:
Lekarz......................................
Potwierdzenie.......................... |
Ryc. 3. Formularz zamawiania antybiotyku w WCChPiG.
3. Kategoria III: antybiotyki zastrzeżone: do realizacji zamówienia wymagana jest zgoda wyznaczonego członka Komitetu Terapeutycznego lub innego konsultanta, w ostatecznej sytuacji ordynatora oddziału. Pozostałe elementy jak dla kategorii II.
Listę antybiotyków z podziałem na kategorie dostępu podano w tabeli 2.
Tabela 2. Lista antybiotyków stosowanych w WCChPiG i kategoria dostępu, po wdrożeniu polityki antybiotykowej.
| Antybiotyk | Kategoria |
| Cefalosporyny |
| 1. Cefazolina | I |
| 2. Cefadroksyl | I |
| 3. Cefuroksym | II |
| 4. Ceftriakson | III |
| 5. Ceftazydym | III |
| 6. Cefepim | III |
| Penicyliny |
| 1. Penicylina benzylowa | I |
| 2. Penicylina fenoksylowa | I |
| 3. Amoksycylina | I |
| 4. Ampicylina | I |
| 5. Amoksycylina/klawulonian | II |
| 6. Piperacylina | II |
| 7. Piperacylina/tazobactam | III |
| 8. Kloksacylina | I |
| Fluorochinolony |
| 1. Ciprofloksacyna | p/o: II
i/v: III |
| 2. Norfloksacyna | II |
| Makrolidy |
| 1. Erytromycyna | I |
| 2. Klarytromycyna | p/o II
i/v III |
| Aminoglikozydy |
| 1. Gentamycyna | I |
| 2. Amikacyna | III |
| 3. Tobramycyna | II |
| Leki przeciwgrzybicze |
| 1. Flukonazol | II |
| 2. Ketokonazol | I |
| 3. Itrakonazol | III |
| 4. Amfoterycyna | III |
| Inne |
| 1. Wankomycyna | III |
| 2. Teikoplanina | III |
| 3. Imipenem | III |
| 4. Klindamycyna | p/o II
i/v III |
| 6. Doksycyklina | I |
| 7. Trimetoprim/sulfametoksazol | I |
| 8. Acyklowir | II |
Najistotniejsze zmiany wprowadzone wraz z wdrożeniem szpitalnej polityki antybiotykowej:
1. Penicyliny:
a) stosowania amoksycyliny w terapii empirycznej zakażeń dróg oddechowych: w 1997 tylko 5 pacjentów było leczonych tym preparatem. W nowym receptariuszu amoksycylina jest antybiotykiem I rzutu w zaostrzeniu przewlekłej obturacyjnej choroby płuc i łagodnych zapaleniach płuc,
b) wycofanie karbenicyliny: penicylina stosowana w leczeniu zakażeń
Pseudomonas aeruginosa. Ze względu na szerokie stosowanie w przeszłości jest rzadko skuteczna w leczeniu zakażeń powodowanych przez ten drobnoustrój,
c) amoksycylina/kw. klawulanowy: lek zajmował pierwszą pozycję w częstości stosowania i konsumpcji środków finansowych przeznaczanych na antybiotyki; niezmiernie istotne było więc określenie jasnych wskazań do stosowania tego antybiotyku i monitorowanie jego zużycia.
2. Cefalosporyny:
a) I generacja: zredukowano liczbę antybiotyków z tej grupy do cefazoliny i cefadroksylu; cefazolina jest zarezerwowana do profilaktyki okołooperacyjnej; przydatność drugiej cefalosporyny I generacji jest dyskusyjna, ze względu na niewielkie różnice między preparatami tej grupy o wyborze może decydować cena zakupu i łatwość podania,
b) II generacja: w receptariuszu umieszczono cefuroksym ze względu na szersze spektrum działania niż cefaklor, obecność formy dożylnej i doustnej, dobrą penetrację do układu oddechowego; dotychczasowa wysoka pozycja cefuroksymu w ogólnej konsumpcji antybiotyków stwarza konieczność ścisłej kontroli jego zużycia,
c) III generacja: zawarto dwa leki z tej grupy – ceftazydym lub cefoperazon, jako cefalosporyny aktywne wobec
Pseudomonas aeruginosa oraz ceftriakson lub cefotaksym, stosowane w pozostałych wskazaniach. Wybór ceftazydymu jest podyktowany tym, że cefoperazon odznacza się mniejszą aktywnością w stosunku do
P. aeruginosa i jest mniej stabilny w stosunku do betalaktamaz produkowanych przez pałeczki Gram-ujemne, aniżeli inne preparaty tej grupy (11). Cefotaksym i ceftriakson zostały uznane za leki równoważne; wybór ceftriaksonu był podyktowany większym przyzwyczajeniem środowiska lekarskiego do tego antybiotyku. Zużycie obu tych cefalosporyn jest ściśle monitorowane. Wydaje się, że należy rozważyć zasadność umieszczania w receptariuszu szpitalnym leków z tej grupy podawanych doustnie,
d) IV generacja: wprowadzenie do receptariusza cefepimu może być alternatywą dla leczenia imipenemem; przydatność tego preparatu jest oceniana przez laboratorium mikrobiologiczne, również jest monitorowana efektywność kliniczna leczonych pacjentów.
3. Fluorchinolony:
a) nie jest uzasadnione umieszczenie więcej niż dwóch przedstawicieli tej grupy w receptariuszu,
b) ciprofloksacyna wyczerpuje wskazania do stosowania fluorochinolonów; można rozważyć wprowadzenie norfloksacyny do leczenia zakażeń układu moczowego,
c) wycofano z receptariusza pefloksacynę ze względu na niższą aktywność w stosunku do Enterobacteriaceae i P. aeruginosa oraz wyższe MIC dla H. Influenzae (11).
d) ofloksacyna: ze względu na leczenie gruźlicy lek umieszczono w receptariuszu; jednakże warto zaznaczyć, że ciprofloksacyna jest uważana za preparat o podobnej skuteczności w terapii Mycobacterium tuberculosis (12, 13).
4. Makrolidy:
a) w 1997 roku w WCChPiG 80% środków wydanych na makrolidy było związane ze stosowaniem roksytromycyny,
b) nie odnotowano różnic, które miałyby decydujące znaczenie o zastosowaniu jednego z 3 makrolidów: erytromycyny, roksytromycyny, rowamycyny. Wyższa jest aktywność klarytromycyny i azytromycyny w stosunku do
H. influenzae oraz istotna dla szpitala pulmonologicznego aktywność klarytromycyny wobec prątków niegruźliczych (11),
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
29 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
69 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
129 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 78 zł
Piśmiennictwo
1. Record K.E., Dickens G.R.: Implementation of a criteria-based antimicrobial formulary system. Am. J. Health-Syst. Pharm., 1995, vol. 52, Mar 15, suppl. 2:S34-S38. 2. Reimann H.A.: The misuse of antibiotics. Med. Clin. North Am., 1961, 45:849-54. 3. Marr J.J. et al.: Guidelines for improving the use of antimicrobial agents in hospitals: a statement by the Infectious Disease Society of America, 1987, 157:869-76. 4. Bryan Ch.S.: The role of the infectious diseases physician in setting guidelines for antimicrobial use. Bull N.Y. Acad. Med., 1987, vol. 63, no 6:627-636. 5. Working Party Report „Hospital antibiotic control measures in the UK”. J. Antimicrob Chemother, 1994, 34:21-42. 6. Polk R.E.: The role of the infectious diseases physician in monitoring antimicrobial use; a pharmacy perspective. Bull N.Y. Acad. Med., 1987, vol. 63, no 6:612-624. 7. Craven D.E. et al.: Preventing nosocomial pneumonia: state of the art and perspectives for the 1990s. Am. J. Med., 1991, 91:44S. 8. Bartlett J.G.: Management of respiratory tract infections. Williams and Wilkins, 1997. 9. Haley R.W.: The nationwide nosocomial infection rate: A new need for vital statistics. Am. J. Epidemiol., 1985, 121:159. 10. Crowe H.M., Quintiliani R.: Antibiotic formulary selection. Med. Clin. North Am., 1995, vol. 79, no 3:463-476. 11. Kucers A. et al.: The use of antibiotics. Butterworth and Heinemann, 1997, 324. 12. Heifets L.B.: Drug susceptibility in the chemotherapy of mycobacterial infections. 13. Boca raton, FL, CRC Press, 1991, 13. 14. Garcia-Rodriguez J.A., Gomez Garcia A.C.: In-vitro activities of quinolones against mycobacteria. J. Antimicrob Chemother, 1993, 32:797-808. 15. Prins J.M. et al.: Once-daily gentamicin versus once-daily netilmicin in patients with serious infections-a randomized clinical trial. J. Antimicrob Chemother, 1994, 33:823. 16. Kahlmeter G., Dahlager J.I.: Aminoglycoside toxicity – a review of clinical studies published between 1975 and 1982. J. Antimicrob Chemother, 1984, 13 suppl. A:9. 17. Rifenburg R.P. et al.: Benchmark analysis of strategies hospitals use to control antimicrobial expenditures. Am. J. Health-Syst. Pharm., 1996, vol. 53, Sep 1:2054-2062. 18. Holzmann M.S.: Antimicrobial formulary management: a consultant perspective. Pharmacotherapy, 1991, 11 (1 Pt 2):14S-18S. 19. Dunagan W.C., Medoff G.: Formulary control of antimicrobial usage. Diagn. Microbiol. Infect. Dis., 1993, 16:265-274. 20. Freeman C.D. et al.: Once-daily dosing of aminoglycosides; review and recommendations for clinical practice. J. Antimicrob Chemother, 1997, 39:677-686. 21. Goldmann D.A. et al.: Strategies to prevent and control the emergence and spread of antimicrobial – resistant microorganisms in hospitals. JAMA 1996, vol. 275, no 3:234-24+0.
Pozostałe artykuły z numeru 9/1999:



