© Borgis - Postępy Nauk Medycznych 4/2010, s. 306-311
*Karol Szadejko1, Michał Schinwelski1, Piotr Robowski1, Jarosław Sławek1,2
Parkinsonizm naczyniowy: patogeneza, diagnostyka i leczenie
Vascular parkinsonism: pathogenesis, diagnostics and treatment
1Oddział Neurologii, Szpital Specjalistyczny św. Wojciecha w Gdańsku
Kierownik Oddziału: dr hab. n. med. Jarosław Sławek
2Zakład Pielęgniarstwa Neurologiczno-Psychiatrycznego, Gdański Uniwersytet Medyczny
Kierownik Zakładu: dr hab. n. med. Jarosław Sławek
Streszczenie
Parkinsonizm naczyniowy (vascular parkinsonism: VaP) na przestrzeni niemal 80 lat od pierwszych opisów pozostaje do dziś jednym z bardziej kontrowersyjnych zagadnień w neurologii. Od pionierskiej pracy Critchley"a z 1920 r. wprowadzającej pojęcie „Arteriosclerotic parkinsonism” terminologia tej niejednorodnej klinicznie jednostki chorobowej wielokrotnie ewoluowała aż do 1980 r., kiedy to ostatecznie zaakceptowano określenie VaP. Dotąd nie stworzono jednak jednoznacznych kryteriów rozpoznania, co mimo wskazywanych cech charakterystycznych tego schorzenia oraz rosnących możliwości diagnostycznych, przyczynia się niewątpliwie do dość wysokiego odsetka błędnie stawianej diagnozy. Również na polu leczenia, podobnie jak w wielu innych schorzeniach będących konsekwencją patologii naczyń nadal największą uwagę przywiązuje się do profilaktyki z uwagi na niewielkie możliwości leczenia objawowego.
W pracy podjęto próbę podsumowania obecnego stanu wiedzy dotyczącej VaP. Szczególną uwagę poświęcono różnicowaniu VaP z idiopatyczną chorobą Parkinsona, a także roli zmian naczyniowych w idiopatycznej chorobie Parkinsona.
Summary
Vascular parkinsonism (VaP for nearly 80 years, has remained one of the most controversial entities in neurology. Since its first discription by Critchley in 1920, introducing the term 'artheriosclerotic parkinsonism', nomenclature of this clinically heterogeneous disorder had been evolving till 1980, when the term VaP was finally accepted. However, despite recognizable specific features of this disorder and increasing diagnostic possibilities, there are no widely accepted and strict diagnostic criteria of VaP. It contributes undoubtedly to a high rate of misdiagnosis. In terms of management, similarly to other disorders secondary to vascular pathology, the greatest emphasis is still put on prophylaxis, as symptomatic treatment options are limited. This paper summarizes current knowledge about VaP. Differentiation between VaP and idiopathic Parkinson's disease and the possible role of vascular factors in idiopathic Parkinson's Disease are particularly emphasized.

Wprowadzenie
Częstość występowania parkinsonizmu naczyniowego szacuje się na około 3-5% (13) wszystkich przypadków parkinsonizmu. Obok parkinsonizmu polekowego jest to jedna z najczęstszych form tzw. parkinsonizmu wtórnego.
Pierwsze badania dotyczące tego zagadnienia sięgają początku XX wieku, kiedy temat ten podjęli Lhermitte i Cornil w 1921 r. i wprowadzili pojęcie parkinsonizmu lakunarnego. Za najsilniejszego propagatora naczyniowej etiologii dla części przypadków parkinsonizmu i pioniera w zakresie badań nad VaP uważany jest jednak obecnie Critchley, który w 1929 r. opublikował pracę zatytułowaną „Arteriosclerotic parkinsonism” (APS) (1), sumującą ówczesny stan wiedzy na temat tego kontrowersyjnego zagadnienia. W tym czasie odróżniano już chorobę Parkinsona (idiopathic Parkinson`s disease: IPD) od parkinsonizmu jako pojęcia szerszego, mieszczącego w sobie przypadki parkinsonizmu poinfekcyjnego, toksycznego oraz w przebiegu innych chorób neurozwyrodnieniowych. W swej pracy Critchley wskazywał różnice w obrazie klinicznym IPD i VaP. Jako typowe dla VaA wskazywał takie objawy jak: sztywność, hipomimię, dominujące zaburzenia chodu, zazwyczaj symetryczny charakter objawów, brak drżenia spoczynkowego, cechy zespołu rzekomoopuszkowego, objawy piramidowe, otępienie i nietrzymanie moczu. Te obserwacje do dziś dnia są aktualne. Critchley przyczyny parkinsonizmu upatrywał w makroskopowych zmianach niedokrwiennych i krwotocznych w obrębie zwojów podstawy i śródmózgowia. Mogło się wydawać, że taka patogeneza może mieć również znaczenie w IPD. Dopiero w latach 60-tych i 70-tych XX wieku udowodniono brak związku pomiędzy miażdżycą naczyń mózgowych a IPD (34-36). W kolejnych latach, uzupełniając wiedzę potwierdzano kliniczne spotrzeżenia Critchley`a, wprowadzono jednak w miejsce APS pojęcia parkinsonizmu dolnej połowy ciała (lower body parkinsonism: LBP) oraz w 1980 r. termin parkinsonizm naczyniowy (VaP). Inne spotykane często w literaturze określenia to „vascular pseudo-parkinsonism”, który zaproponował zresztą sam Critchley w 1981 r. (37) czy „cerebrovascular gait disorder” (15). Pod koniec XX wieku wraz z wprowadzeniem technik neuroobrazowych, zwłaszcza rezonansu magnetycznego, następnie neuroobrazowania czynnościowego, nastąpił znaczący postęp w diagnostyce VaP. W ostatnich latach problem spotyka się z rosnącym zainteresowaniem badaczy, co znajduje wyraz w rosnącej ilości artykułów traktujących o VaP. Nie ma to jednak niestety przełożenia na stworzenie jasnych kryteriów diagnostycznych ani skutecznego leczenia.
Opis przypadku
69-letni mężczyzna, emerytowany muzyk wojskowy, obciążony nadciśnieniem tętniczym, hiperlipidemią, paleniem papierosów, dną moczanową, hiperhomocysteinemią, przerostem prostaty oraz kamicą nerkową od sześciu lat skarżył się na postępujące zaburzenia pod postacią spowolnienia ruchowego, spowolnienia chodu i chodu na poszerzonej podstawie, „szurania” nogami oraz zaburzeń równowagi. W badaniu neurologicznym oprócz opisanych wyżej zaburzeń stwierdzono ataksję w kończynach dolnych, brak odruchów ze ścięgien Achillesa obustronnie i objaw Babińskiego po stronie prawej. W zakresie kończyn górnych nie obserwowano hipokinezji ani sztywności. W kończynach dolnych obecna była niewielka sztywność, nie stwierdzano niedowładu. W badaniu neuropsychologicznym natomiast rozpoznano łagodne zaburzenia poznawcze. Badanie tomografii rezonansu magnetycznego (MRI) głowy wykazało nasilone zmiany naczyniopochodne w obu półkulach mózgu i moście, które w istocie białej dają obraz rozlanych obszarów o podwyższonym sygnale w obrazach PD i T2 zależnych, a ponadto rozsianych drobnych jam poudarowych w jądrach podstawy oraz poszerzonych przestrzeni okołonaczyniowych ( status lacunaris) (ryc. 1 a, b). W badaniu dopplerowskim tętnic szyjnych stwierdzono drobne blaszki miażdżycowe i poszerzenie kompleksu intima-media w tętnicy szyjnej wspólnej prawej, natomiast w badaniu echokardiograficznym wysunięto podejrzenie przetrwałego otworu owalnego. W badaniu dna oka rozpoznano angiopatię nadciśnieniową drugiego stopnia. Dodatkowo stwierdzono podwyższony poziom homocysteiny w surowicy (22 umol/l). Obserwowano umiarkowaną poprawę kliniczną po zwiększeniu dawki lewodopy (z 300 mg do 750 mg na dobę, którą zwiększono w czasie hospitalizacji): w III części UPDRS III: 9 pkt (przed zwiększeniem dawki) do – 5 pkt (po 4 miesiącach). Sam chory zauważył jedynie niewielką poprawę stanu ruchowego. Rozpoznano parkinsonizm dolnej połowy ciała o podłożu naczyniowym.
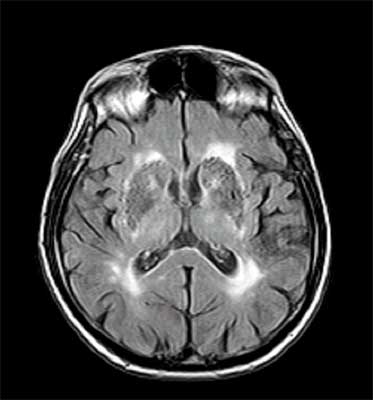
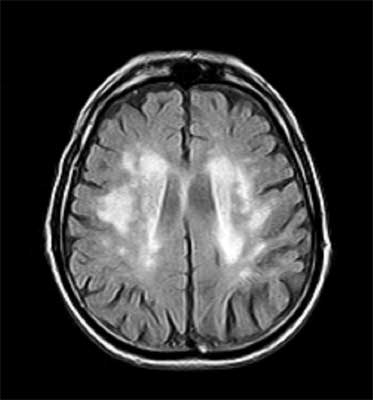
Ryc. 1 a, b. Wybrane obrazy MRI 69-letniego mężczyzny z VaP wykazujące cechy nasilonego uszkodzenia naczyniopochodnego istoty białej obu półkul mózgu oraz jąder podkorowych.
Definicja
Do rozpoznania VaP konieczne są objawy parkinsonizmu (obecność spowolnienia ruchowego i dodatkowo jednego spośród objawów: sztywności, drżenia spoczynkowego, zaburzeń postawy) u pacjenta po udarze mózgu, bez neuropatologicznego podłoża IPD. Ta klasyczna definicja odpowiadająca najłatwiejszemu do rozpoznania „pakinsonizmowi poudarowemu” jest niewystarczająca, obejmuje niewielką część przypadków. Nie zostały dotąd sformułowane oficjalne kryteria rozpoznania VaP.
Epidemiologia
Pomimo wątpliwości sprzed lat, czy choroby naczyń mózgowych mogą dawać objawy parkinsonizmu, obecnie nie ma wątpliwości, że jest to możliwe. Wraz ze starzeniem się społeczeństw w krajach wysoko rozwiniętych częstość VaP podobne jak częstość udarów mózgu i ich następstw będzie narastała. Obecnie uważa się, że stanowi on około 3-5% ogółu przypadków parkinsonizmu (13). Większość autorów zaznacza jednak, że dane te są niedoszacowane. Porównując z IPD początek zachorowania dotyczy osób nieco starszych, tak jak w IPD częściej mężczyzn.
Trudna do oceny jest natomiast częstość przypadków współistnienia IPD i VaP.
Czynniki ryzyka
W przypadku VaP, jak w innych schorzeniach wtórnych do patologii naczyń, czynniki ryzyka są w zasadzie takie same jak w udarach mózgu. Są one obecne u większości chorych z VaP (81%) (17). U chorych z VaP dotąd udowodniono jednak niewątpliwą rolę jedynie nadciśnienia tętniczego (HA). Wg pracy Benito-Leon i wsp. w populacji hiszpańskiej HA występowało u wszystkich pacjentów. Dla porównania u chorych z IPD było to tylko 30-40% (18). Kolejnym po HA czynnikiem ryzyka VaP o udowodnionym związku jest przebyty udar mózgu. Po udarze lakunarnym czy nawet rzadziej terytorialnym VaP nie jest jednak zjawiskiem częstym, bo dotyczy ok. 10% chorych, nawet gdy ognisko udarowe objęło jądra podstawy. Do wyjątkowych przypadków należy zajęcie obu jąder soczewkowatych, co powoduje wzrost ryzyka VaP do 25% (14, 16).
Cukrzyca uważana jest za prawdopodobny czynnik ryzyka VaP o zdecydowanie mniejszym znaczeniu niż HA. Obciążonych nią jest ok. 20% pacjentów z VaP (17, 19). Za następny ważny czynnik ryzyka VaP uważa się zespół antykardiolipinowy. W pracy Huang"a i wsp. obecność przeciwciał antykardiolipinowych wykryto aż u 40% chorych z VaP (6). Co ciekawe palenie tytoniu i zaburzenia lipidowe mają prawdopodobnie mniejszy związek z VaP. Jest to szczególnie interesujące biorąc pod uwagę, że znana jest ujemna korelacja pomiędzy paleniem tytoniu a IPD (20).
Podłoże anatomopatologiczne
W VaP nie stwierdza się zaniku istoty czarnej, ani ciał Lewy"ego, będących podstawą histopatologicznego rozpoznania choroby Parkinsona.
Obecne są natomiast zmiany będące wyrazem chorób drobnych naczyń mózgowych jak uszkodzenie istoty białej o charakterze podkorowej encefalopatii naczyniowej typowej dla choroby Binswangera, status lacunaris, drobne ogniska poudarowe w jądrach podstawy i pniu mózgu oraz poudarowe jamy malacyjne, będące efektem chorób dużych naczyń mózgowych.
Współistnienie zmian naczyniowych i ciał Lewy"ego obserwowane jest u około 10% przypadków (2), czyli dwukrotnie częściej niż obecność ciał Lewy"ego u osób zdrowych w tym samym wieku (44). Prawdopodobnie w większości tych przypadków mamy do czynienia ze współistnieniem VaP i IPD.
Obraz kliniczny
Pomimo coraz większego doświadczenia, rosnącego stanu wiedzy dotyczącego IPD, VaP i innych schorzeń z elementami parkinsonizmu w obrazie klinicznym, nadal często diagnoza stawiana jest mylnie. Wiadomo, że dotyczy to około 20-30% chorych z rozpoznaniem IPD (26, 27). Trzy procent rozpoznań IPD to w rzeczywistości chorzy z parkinsonizmem na podłożu chorób naczyń mózgowych (14).
Charakterystyczne cechy obrazu klinicznego VaP to zespół parkinsonowski dotyczący dolnej połowy ciała z zaburzeniami chodu o charakterze „szurającym”. Zaburzenia chodu jako początkowy objaw IPD podawane są zaledwie u 7% chorych (8). Bardzo ważnym elementem różnicującym VaP i IPD jest brak drżenia spoczynkowego. Drżenie spoczynkowe w VaP traktowane jest jako objaw bardzo rzadki, dotyczący zaledwie ok. 4% chorych. Dla porównania w IPD jest to 73% (41). Kolejne cechy charakteryzujące VaP to nagły początek, skokowy przebieg (14) i generalnie szybszy postęp porównując z IPD, brak lub słaba odpowiedź na terapię lewodopą, mnogie czynniki ryzyka chorób naczyniowych. Żadna z nich nie jest jednak specyficzna i samodzielnie nie może decydować o rozpoznaniu. Przykładowo, nagły początek dotyczy tylko ok. 25% chorych z VaP (12, 17), a jak wiadomo jest również możliwy w IPD. Zdecydowanie częstszy, zresztą podobnie jak w IPD jest początek podstępny i przebieg powoli postępujący, a nie skokowy, tak początkowo podkreślany jako typowy dla VaP. Pozostałe objawy określane jako dodatkowe, również przemawiające w rozpoznaniu na korzyść VaP to objawy piramidowe, nietrzymanie moczu, zespół rzekomoopuszkowy i otępienie.
Otępienie naczyniowe i VaP mają wiele punktów wspólnych i najprawdopodobniej są różną manifestacją kliniczną tych samych schorzeń. Łączą je zmiany radiologiczne w neuroobrazowaniu i anatomopatologiczne, często dominujące objawy ruchowe dotyczące chodu. Nie powinno zatem dziwić współistnienie obu cech u części pacjentów. Porównując z IPD częstość otępienia u chorych z VaP jest istotnie wyższa. Wg Yamanouchi i Nagura jest to 71% u chorych z VaP i 43% z IPD (41). W innej pracy częstość otępienia określono na 45% (VaP) i 10% (IPD) (12).
Brak cech patognomonicznych i szerokie spektrum obrazu klinicznego u chorych nasuwa przypuszczenie heterogenności VaP. Postulowane jest to w pracach z lat 90. tych. Między innymi proponowano w nich podział VaP na dwie podstawowe grupy. Według Winikates"a i Jankovica pierwszą z nich charakteryzuje nagły początek, najczęściej będący skutkiem udaru z zajęciem jąder podstawy. W drugiej grupie natomiast są przypadki o podstępnym początku, powolniejszym przebiegu na podłożu bardziej rozlanego, niedokrwiennego uszkodzenia istoty białej podkorowej (3).
Fenelon i Houeto (5) z kolei zaproponowali podział VaP na cztery podtypy.
1) VaP manifestujący się w sposób imitujący IPD. W tej grupie zawierają się prawdopodobnie przypadki z współistnieniem obu schorzeń.
2) Parkinsonizm „połowiczy” po incydencie naczyniowym. Jest to budzący najmniej kontrowersji podtyp VaP u chorych z objawami parkinsonizmu dotyczącymi jednej połowy ciała po przeciwstronnym udarze w obrębie jąder podstawy, wzgórza, istoty czarnej. Co ciekawe wyjątkowo rzadko zdarzają się przypadki VaP po uszkodzeniu istoty czarnej (7). Zresztą nawet w przypadku udaru z zajęciem prążkowia objawy parkinsonizmu nie są zjawiskiem częstym.
3) Objawy parkinsonowskie uważane za nietypowe dla IPD, u chorego z wykładnikami naczyniopochodnego uszkodzenia mózgu. Do objawów tych należą między innymi brak drżenia, dominująca sztywność osiowa, słaba odpowiedź na lewodopę. Do grupy tej w zasadzie można zaliczyć chorych o drugim typie klinicznym wg Winikates"a i Jankovica (3).
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
24 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
59 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
119 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 28 zł
Piśmiennictwo
1. Critchley M: Arteriosclerotic parkinsonism. Brain 1929; 52: 23-83.
2. Winikates J, Jankovic J: Vascular progressive supranuclear palsy. J Neurol Transm Suppl 1994; 42: 189-201.
3. Winikates J, Jankovic J: Clinical correlates of VP. Arch Neurol 1999; 56: 98-102.
4. Zijlmans JCM, Thijsen HOM, Vogels OJM et al.: Quantitative gait analysis in patients with VP. Mov Disord 1996: 11: 501-8.
5. Fenelon G, Houeto JL: Les syndromes parkinsoniens vasculaires: un concept conroverse. Rev Neurol 1998; 154 (4): 291-301.
6. Huang Z, Jacewicz M, Pfeiffer RF: Anticardiolipin antibody in vascular parkinsonism. Mov Disord 2002; 17 (5): 992-7.
7. Zijlmans JCM, Katzenschlager R, Daniel SE et al.: MRI in patients with suspected VP. Neurology 1995; 45: 2183-8.
8. Fitzgerald PM, Jankovic J: Lower body parkinsonism: evidence for vascular etiology. Mov Disord 1989; 4: 249-60.
9. Mardsen CD, Thompson PN: Frontal gait disorders. [In:] Bronstein AM, Brandt T, Woollacott M et al.: Clinical disorders of balance, osture, gait. London: Arnold 1996; p. 188-93.
10. Thompson PN, Mardsen CD: Gait disorder of subcortical arterioscerotic encephalopathy: Binswanger"s disease. Mov Disord 1987; 2: 1- 8.
11. Ebersbach G, Soyer M, Valldeoriola F et al.: Comparative analysis of gait in Parkinson"s disease, cerebellar ataxia and subcortial arteriosclerotic encephalopathy. Brain 1999; 122: 1349-55.
12. Winikates J. Jankovic J: Clinical correlates of VP. Arch Neurol 1999; 56: 98-102.
13. Sibon I. Tison F: Vascular parkinsonism. Current Opinion in Neurology 2004; 17: 49-54.
14. Bower JH, Dickson DW, Taylor L et al.: Clinical correlates of the pathology underlying parkinsonism: a population perspective. Mov Disord 2002; 17: 910-916.
15. Rektor I, Rektorova I, Kubova D: Vascular parkinsonism – an update. Journal of the Neurological Sciences 2006; 185-191.
16. Van Zagten M, Lodder J, Kessels F: Gait disorder and parkinsonian signs in patients with stroke related to small, deep infarcts and white matter lesions. Mov Disord 1998; 13: 89-95,
17. Demirkiran M. Bozdemir H. Sarica Y: Vascular parkinsonsm: a distinct, heterogeneous clinical entity. Acta Neurol Scand 2001; 104: 63-67.
18. Benito-Leon J, Bermejo-Pareja F, Rodriguez J et al.: Prevalence of PD and other types of parkinsonism in three elderly populations of central Spain. Mov Disord 2003; 18: 267-274.
19. Chang CM, Yu YL, Ng HK et al.: Vascular pseudoparkinsonism. Acta Neurol Scand 1992; 86: 588-592.
20. Sugita M, Izuno T, Tatemichi M et al.: Meta-analysis for epidemiologic studiem on the relationship between smoking and Parkinson"s disease. J Epidemiol 2001; 11: 87-94.
21. Muller T, Woitalla D, Fowler B et al.: 3-OMD and homocysteine plasma levels i parkinsonian patients. J Neural Transm 2002; 109: 175-179.
22. Yasui K, Kowa H, Nakaso K et al.: Plasma homocysteine and MTHFR C677T genotype in levodopa-treated patients with PD. Neurology 2000; 55: 437-440.
23. Nakaso K, Yasui K, Kowa H et al.: Hypertrophy of IMC of arotid artery In Parkinson"s disease is associated with L-DOPA, homocysteine and MTHFR genotype. J Neurol Sci 2003; 207: 19-23.
24. Jellinger KA: Vascular parkinsonism – neuropathological findings. Acta Neurol Scand 2002; 105: 414-415.
25. Jellinger KA: Prevalence of cerebrovascular lesions in Parkinson"s disease. A postmortem study. Acta Neuropatholog (Berl) 2003; 105: 415-419.
26. Hugues AJ, Daniel SE, Kilford L et al.: Accuracy of cliical diagnosis of idiopathic Parkinson"s disease: a clinico-pathological study of 100 cases. J Neurol Neurosurg Psychiatry 1992; 55: 181-184.
27. Hugues AJ, Daniel SE, Lees AJ: Improved accuracy of clinical diagnosis of Lewy body Parkinson"s disease. Nerology 2001; 57: 1497-1499.
28. Gerschlager W, Bencsits G, Pirker W et al.: [123 I] beta-CIT SPECT distinguishes vascular parkinsonism from Parkinson"s disease. Mov Disord 2002; 17: 518-523.
29. Hamano T, Tschuchida T, Hirayama M et al.: Dopamine transporter SPECT in patients with Parkinson"s disease. Kaku Igagu 2000; 37: 125-129.
30. SasakiT Amano T, Hashimoto J et al.: SPECT imaging using [123 I] beta-CIT and [123 I]IBF in extrapyramidal diseases. No To Shinkei 2003; 55: 57-64.
31. Terashi H, Nagata K, Hirata Y et al.: Study on dopamine D2 binding capacity in vascular parkinsonism. Rinsho Shinkeigaku 2001; 41: 659-664.
32. De Reuck J, Siau B, Deco D et al.: Parkinsonism in patients with vascular dementia: clinical, computed- and positron emission-tomographic findings. Cerebrovasc Dis 2001; 11: 51-58.
33. Ondo WG, Chan LL, Levy JK: Vascular parkinsonism: clinical correlates predicting motor improvement after lumbar puncture. Mov Disord 2002; 17: 91-97.
34. Eadie MJ, Suterland JM: Arteriosclerosis in parkinsonism. J Neurol Neurosurg Psychiatry 1964; 27:237-240.
35. Parkes JD, Marsden CD, Rees JE et al.: Parkinson"s disease, cerebral arteriosclerosis and senile dementia. Q J Med 1974; 169: 49-61.
36. Martilla RJ, Rinne UK: Arteriosclerosis, heredity and some other previous infection in etiology of Parkinson"s disease: a case control study. Clin Neurol Neurosurg 1976; 79: 46-56.
37. Critchley M: Arteriosclerotic pseudo-parkinsonism; in Rose C, Capildeo R: Research progress in Parkinson"s disease. London, Pitman medical 1981; pp 40-42.
38. Friedman A, Kang UJ, Tatemichi TK et al.: A case of parkinsonism following striatal, lacunar infarction. J Neurol Neurosurg Psychiatry 1986; 49: 1087, 1088.
39. Mayo J, Arias M, Leno C et al.: Vascular parkinsonism and periarteritis nodosa. Neurology 1986; 36: 874.
40. Murrow RW, Schwiger GD, Kepes JJ et al.: Parkinsonism due to a basal ganglia lacunar state: clinicopathologic correltion. Neurology 1990; 40: 897-900.
41. Yamanouchi H, Nagura H: Neurological signs and frontal white matter lesions in vascular parkinsonism: a clinicopathologic study. Stroke 1997; 28: 965-969.
42. Rampello L, Alvano A, Battaglia G et al.: Different clinical and evolutional patterns in late idiopathic and vascular parkinsonism. J Neurol 2005; 252: 1045-1049.
43. Zijlmans JC, Daniel SE, Hughes AJ et al.: Clinicopathological investigation of vascular parkinsonism, including clinical criteria for diagnosis. Mov Disord 2004; 19: 630-640.
44. Jellinger KA: The neuropathologic diagnosis o secondary parkinsonian syndromes. [In:] Battistin L, Scarlato G, Caraceni T, Ruggieri S, editors. Adv Neurol, vol. 69. New York: Raven Press 1996; p. 293-303.
45. Derejko M, Sławek J, Wieczorek D et al.: Neurol Neurochir Pol 2006; 40 (4): 276-283.
46. Sławek J, Wieczorek D, Derejko M et al.: The influence of vascular risk factors and white matter hiperintesities on the degree of cognitive impairment in Parkinson's Disease. Neurol Neurochir Pol 2008; 42, 6: 505-512.
47. Sławek J, Wieczorek D, Derejko M et al.: Vascular risk factors do not contribute to motor and cognitive impairment in Parkinson"s disease. Parkinsonism Rel Disord 2009 (in press).


