© Borgis - Nowa Medycyna 1/2011, s. 7-10
*Marzenna Galar, Anna Szumowska, Elżbieta Tajanko, Łukasz Bołkun, Janusz Kłoczko
D-dimer w zakrzepicy żył głębokich kończyn dolnych
D-dimer in deep vein thrombosis
Klinika Hematologii Uniwersytetu Medycznego w Białymstoku
Kierownik Kliniki: prof. dr hab. Janusz Kłoczko
Summary
Introduction: Deep vein thrombosis (DVT) is a significant problem in clinical practice. D-dimer, the final degradation product of cross-linked fibrin, is an established parameter for ruling-out the disease and serves as a supplementary test in diagnostic imaging.
Aim: The aim of the following study was to estimate plasma concentration of D-dimer in reference to the size of thrombosis as well as D-dimer reliability in the diagnose and monitoring of DVT treatment.
Material and methods: Twenty-seven patients with newly diagnosed DVT confirmed by phlebography was evaluated. The influence of anticoagulant treatment on D-Dimer concentration was assessed in 10 patients during twelve-weeks therapy of low-molecular-weight heparin. The plasma concentration of D-dimer was measured by enzyme immunoassay, using ENZYGNOST D-dimer micro kit, Dade Behring.
Results: The results demonstrated, that the patients with DVT had a significant increase in plasma concentration of D-Dimer. No correlation was found between D-Dimer concentration and the size of thrombosis in the phlebography examination. During low-molecular-weight heparin treatment, a progressive decrease in D-dimer plasma concentration was observed, reaching – at the end of treatment – a concentration value, approximate to the healthy control. Furthermore, a 100% specificity for D-dimer testing with a 81.1% negative predictive value was achived.
Conclusions: We conclude that growth of D-Dimer concentration in plasma is a sensitive and reliable indicator of DVT. The measurement of the D-Dimer plasma concentration is a reliable test in the diagnose and monitoring of the efficacy of DVT treatment.

WSTĘP
Zakrzepica żył głębokich kończyn dolnych (ZŻGKD) stanowi istotny problem kliniczny, zarówno ze względu na częstość występowania, jak i przebieg kliniczny. Najgroźniejszym, często śmiertelnym, powikłaniem zakrzepicy jest zatorowość tętnic płucnych (ZP), towarzysząca 20-30% chorym na zakrzepicę żył głębokich w odcinku dystalnym oraz 30-50% pacjentom z zakrzepicą proksymalną (1, 2). U znacznego odsetka chorych zakrzepica żył głębokich przebiega bezobjawowo, a na jej obecność zwraca uwagę wystąpienie późnych powikłań (3, 4). W praktyce rozpoznanie ustala się, biorąc pod uwagę kliniczne prawdopodobieństwo wystąpienia zakrzepicy, stężenie D-dimeru w osoczu oraz wynik ultrasonograficznego testu uciskowego żył (5-7). Przy dużym klinicznym prawdopodobieństwie ZŻGKD, kiedy wynik badania ultrasonografii uciskowej jest ujemny lub wątpliwy, wykonywana jest flebografia. Metoda ta, mimo że ma znaczenie rozstrzygające, obarczona jest istotnymi ograniczeniami spowodowanymi inwazyjnością badania, jego kosztami, brakiem powszechnej dostępności oraz specyficzności w pewnych regionach układu żylnego (8). Dlatego diagnostyka biochemiczna, posługująca się oceną stężeń osoczowych markerów aktywacji hemostazy, odgrywa istotną rolę. D-dimer – produkt plazminowej degradacji zakrzepu, stanowi główny parametr diagnostyczny w wykluczeniu choroby, jak również jest uzupełnieniem diagnostyki obrazowej (9, 10).
CEL PRACY
Celem pracy była ocena wartości osoczowych stężeń D-dimeru w zakrzepicy żylnej w odniesieniu do rozległości zmian zakrzepowych oraz ich znaczenie w monitorowaniu skuteczności leczenia antykoagulacyjnego.
MATERIAŁ I METODY
Badaniami objęto 27 chorych na zakrzepicę żył głębokich kończyn dolnych (17 kobiet, 10 mężczyzn; średnia wieku 60,1 ± 15,8 lat). Do badań kwalifikowano chorych ze świeżą zakrzepicą, z wywiadem chorobowym nie dłuższym niż 14 dni. Grupę kontrolną stanowiło 30 osób zdrowych (15 kobiet, 15 mężczyzn; średnia wieku 43,0 ± 4,3 lat).
U wszystkich badanych wykonano flebografię kończyn dolnych. Rozległość zakrzepicy określano punktami od 0 do 5 zgodnie ze skalą Arnesena (11) (tab. 1).
Tabela 1. Skala Arnesena.
| Punkty | Obraz żyły |
0
1
2
3
4
5 | żyła niezajęta przez zakrzep
zajęcie powyżej 1/3 długości żyły bez zamknięcia światła
zajęcie powyżej 2/3 bez zamknięcia światła lub powyżej 1/3 z zamknięciem światła
zajęcie 3/3 bez zajęcia światła lub powyżej 2/3 z okluzją
zajęcie 3/3 żyły z zamknięciem światła
brak uwidocznienia żyły z powodu całkowitego zamknięcia światła |
W grupie 10 pacjentów oceniano wpływ terapii antykoagulacyjnej na zachowanie się stężenia D-dimeru. Wszyscy chorzy otrzymywali heparynę drobnocząsteczkową (Fraxiparine, Sanofi) przez okres 12 tygodni – przez pierwsze 10 dni w dawce 225 j. anty-Xa/kg dwa razy dziennie s.c., a następnie dawkę zmniejszano o połowę, stosując 225 j. anty-Xa/kg raz dziennie.
Krew do badań laboratoryjnych pobierano w godzinach rannych, na czczo do 3,8% cytrynianu sodowego w stosunku 10:1 – przed włączeniem leczenia przeciwzakrzepowego, w 10 dniu, 5, 8 i 12 tygodniu prowadzonej terapii.
U wszystkich badanych oznaczano stężenie D-dimeru metodą immunoenzymatyczną z użyciem zestawu ENZYGNOST D-dimer micro firmy Dade Behring.
Ocena statystyczna danych obejmowała wyliczenie średniej arytmetycznej (x), odchylenia standardowego (SD), współczynnika korelacji. Do potwierdzenia wiarygodności choroby przeprowadzono analizę regresji logistycznej. W celu oceny przydatności diagnostycznej stosowanej metody biochemicznej obliczono czułość (Se), swoistość (Sp) oraz negatywną (NPV) i pozytywną wartość predykcji (PPV). Do porównania wyników leczenia zastosowano test Wilcoxona dla par. Za istotne statystycznie uznano wyniki, dla których wartość p < 0,05. Obliczeń dokonano, stosując pakiet statystyczny SPSS.
WYNIKI
Rycina 1 przedstawia średnie wartości stężeń D-dimeru w grupie chorych na zakrzepicę żył głębokich kończyn dolnych oraz kontrolnej grupie osób zdrowych. Chorzy na zakrzepicę wykazywali znaczny, istotny statystycznie, wzrost stężeń D-dimeru (442,1 ± 354,4 μg/l) w porównaniu do grupy kontrolnej (14,1 ± 12,5 μg/l). W badanej grupie 27 chorych na zakrzepicę żył głębokich, u 25 (93%) wartości D-dimeru były wyższe od wartości referencyjnych.
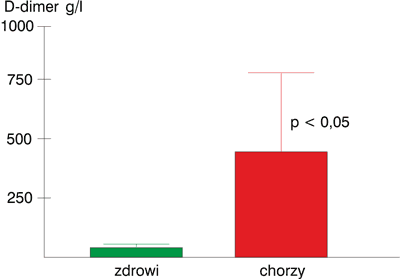
Ryc. 1. Średnie stężenia D-dimeru w grupie osób zdrowych i chorych na zakrzepicę żył głębokich.
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
24 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
59 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
119 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 28 zł
Piśmiennictwo
1. Konstantinides S: Clinical practice. Acute pulmonary embolism. N Engl J Med 2008; 359(26): 2804-2813. 2. Galanaud JP et al.: OPTIMEV-SFMV Investigators. Comparative study on risk factors and early outcome of symptomatic distal versus proximal deep vein thrombosis: results from the OPTIMEV study. Thromb Haemost 2009; 102(3): 493-500. 3. Scarvelis D, Wells PS: Diagnosis and treatment of deep-vein thrombosis. CMAJ 2006; 175(9): 1087-1092. 4. Wells PS et al.: Does this patient have deep vein thrombosis? JAMA 2006; 295(2): 199-207. 5. Hajduk B, Małek G: Rozpoznawanie zakrzepicy żył głębokich. [W:] Łopaciuk S (red.): Zakrzepy i zatory. PZWL, Warszawa 2002; 347-366. 6. Proniewski J: Nieinwazyjna diagnostyka zakrzepicy żył głębokich kończyn dolnych. Terapia 2002; 4(120): 17-18. 7. Elf JL et al.: Clinical probability assessment and D-dimer determination in patients with suspected deep vein thrombosis, a prospective multicenter management study. Thromb Res 2009; 123(4): 612-616. 8. Sharifi M et al.: Endovenous therapy for deep venous thrombosis: the TORPEDO trial. Catheter Cardiovasc Interv 2010; 76(3): 316-325. 9. Wells PS et al.: Evaluation of D-dimer in the diagnosis of suspected deep-vein thrombosis. N Engl J Med 2003; 349(13): 1227-1235. 10. Taira T et al.: Risk of venous thromboembolism in patients with borderline quantitative D-dimer levels. Am J Emerg Med 2010; 28(4): 450-453. 11. Arnesen H et al.: A prospective study of streptokinase and heparin in the treatment of deep vein thrombosis. Acta Med Scand 1978; 203(6): 457-463. 12. Boneu B et al.: D-dimers, thrombin-antithrombin III complexes and prothrombin fragments 1+2: diagnostic value in clinically suspected deep vein thrombosis. Thromb Haemost 1991; 65(1): 28-31. 13. Nachman RL, Silverstein R: Hypercoagulable states. Ann Intern Med 1993; 119(8): 819-827. 14. Freyburger G et al.: D-dimer strategy in thrombosis exclusion: a gold standard study in 100 patients suspected of deep vein thrombosis or pulmonary embolism: 8 DD methods compared. Thromb Haemost 1998; 79(1): 32-37. 15. Głowiński S, Kłoczko J: Zarys hemostazy i trombogenezy. [W:] Noszczyk W (red.): Chirurgia tętnic i żył obwodowych. PZWL, Warszawa 1998; 53-65. 16. Miloszewski K, Sheltawy MJ, Losowsky MS: Fibrinogen-fibrin degradation products and factor XIII. Acta Haematol 1974; 51(6): 321-330. 17. Chojnowski K: Dimer D – diagnostyczny i rokowniczy marker żylnej choroby zakrzepowo-zatorowej. Hematologia 2010; 1(2): 102-108. 18. Adam SS, Key NS, Greenberg CS: D-dimer antigen: current concepts and future prospects. Blood 2009; 113(13): 2878-2887. 19. Bruinstroop E, Van de Ree MA, Huisman MV: The use of D-dimer in specific clinical conditions: a narrative review. EJIM 2009; 20(5): 441-446. 20. Markers of hemostatic system activation in acute deep venous thrombosis – evolution during the first days of heparin treatment. The DVTENOX Study Group. Thromb Haemost 1993; 70(6): 909-914. 21. Peternel P et al.: Markers of hemostatic system activation during treatment of deep vein thrombosis with subcutaneous unfractionated or low-molecular weight heparin. Thromb Res 2002; 105(3): 241-246. 22. Di Nisio M et al.: Diagnostic accuracy of D-dimer test for exclusion of venous thromboembolism: a systematic review. J Thromb Haemost 2007; 5(2): 296-304. 23. Geersing GJ et al.: Excluding venous thromboembolism using point of care D-dimer tests in outpatients: a diagnostic meta-analysis. BMJ 2009; 339:b2990. 24. Nomura H et al.: Negative predictive value of D-dimer for diagnosis of venous thromboembolism. Int J Hematol 2008; 87(3): 250-255. 25. Heim SW et al.: D-dimer testing for deep venous thrombosis: a metaanalysis. Clin Chem 2004; 50(7): 1136-1147. 26. Philbrick JT, Heim S: The D-dimer test for deep venous thrombosis: gold standards and bias in negative predictive value. Clin Chem 2003; 49: 570-574. 27. Righini M et al.: Clinical usefulness of D-dimer depending on clinical probability and cutoff value in outpatients with suspected pulmonary embolism. Arch Intern Med 2004; 164(22): 2483-2487. 28. Keeling DM et al.: The diagnosis of deep vein thrombosis in symptomatic outpatients and the potential for clinical assessment and D-dimer assays to reduce the need for diagnostic imaging. Br J Haematol 2004; 124(1): 15-25. 29. Kearon C et al.: Antithrombotic therapy for venous thromboembolic disease: American College of Chest Physician Evidence-Based Clinical Practice Guidelines (8th edition). Chest 2008; 133 (Suppl 6): 454S-545S [Erratum in: Chest 2008; 134(4): 892]. 30. Cushman M et al.: Fibrin fragment D-dimer and the risk of future venous thrombosis. Blood 2003; 101(4): 1243-1248. 31. Kyrle PA, Rosendaal FR, Eichinger S: Risk assessment for recurrent venous thrombosis. Lancet 2010; 376(9757): 2032-2039. 32. Kaczyńska A, Pruszczyk P: Oznaczenie stężenia dimera D u osób po przebytej żylnej chorobie zakrzepowo-zatorowej może być pomocne w ocenie zagrożenia jej nawrotem. Pol Prz Kardiol 2008; 10(1): 59-62. 33. Cosmi B, Palareti G: Update on the predictive value of D-dimer in patients with idiopathic venous thromboembolism. Thromb Res 2010; 125 (Suppl 2): S62-S65.

