© Borgis - Nowa Medycyna 3/2013, s. 95-100
*Angelika Copija1, Julia Janiszewska1, Paulina Maruszczak1, Aleksandra Raźnikiewicz1, Dariusz Waniczek2, Jerzy Arendt2
Leczenie przetok odbytu w latach 2006-2012 w Katedrze i Oddziale Klinicznym Chirurgii Ogólnej i Gastroenterologicznej ŚUM w Bytomiu
Treatment of fistulas-in-ano in the years 2006-2012 based on experiences of the Department of General and Gastroenterological Surgery in Bytom
1Studenckie Koło Naukowe przy Katedrze i Oddziale Klinicznym Chirurgii Ogólnej i Gastroenterologicznej, Śląski Uniwersytet Medyczny, Bytom
Opiekun Koła: dr med. Marek Rudzki
2Katedra i Oddział Kliniczny Chirurgii Ogólnej i Gastroenterologicznej, Śląski Uniwersytet Medyczny, Bytom
Kierownik Katedry: prof. dr hab. med. Jerzy Arendt
Summary
Introduction. Fistula-in-ano (FA) is a canal surrounded by grain tissue connecting the internal opening in the anal canal at the level of anal crypts and the external opening on the skin surrounding the anus. It is a difficult problem, both for the patient, due to a chronic course, and the doctor because of a tendency to recurrence. Surgery is the only effective method of treatment.
Aim. The aim of the study was to present experiences in treatment of fistula-in-ano in the Department of General and Gastroenterological Surgery in Bytom in the years 2006-2012.
Material and methods. In the analyzed period from January 2006 to March 2012, 134 operations of FA were performed in patients aged 19-89 (mean 48.56): 102 (76.1%) men and 32 (23.9%) women.
Results. Recurrent fistula occurred in 42 (31.3%) patients, primary fistula in 92 (68.7%). Inter-sphincteric fistula was diagnosed in 37 (27.6%) patients, trans-sphincteric in 58 (43.3%), extra-sphincteric in 21 (15.7%), supra-sphincteric in 7 (5.2%) patients. There were also observed 4 (3.0%) subcutaneous and 7 (5.2%) submucous fistulas, not included in Park’s classification. 109 (81.3%) patients were treated by fistulectomy with partial closure of the wound or marsupialization and, if necessary, with partial incision of external sphincter. The method advancement flap repair was used in 16 (11.9%) patients, fistulotomy in 4 (3.0%), fistulectomy with excision and reconstruction of external sphincter in 5 (3.7%).
Conclusions. The majority of 134 patients treated in the years 2006-2012 had trans-sphincteric fistulas. Most of the patients were treated with fistulectomy with marsupialization.

Wstęp
Przetoka odbytu to bardzo dokuczliwa i uciążliwa choroba – zarówno dla chorego, ze względu na przewlekły przebieg, jak i dla lekarza, z powodu tendencji do nawrotów. Jest to choroba zapalna, polegająca na wytworzeniu wyścielonego ziarniną kanału łączącego ujście wewnętrzne, leżące zwykle w kanale odbytu na wysokości krypt, z ujściem zewnętrznym położonym w skórze okolicy odbytu.
Według aktualnych danych zebranych w czterech krajach Unii Europejskiej przetoka odbytu występuje u mieszkańców UE z częstością szacowaną na 1,20-2,80/10 000/rok (1). Mężczyźni cierpią na nią 2 do 7 razy częściej niż kobiety (2) – wyjątek stanowią przetoki w przebiegu choroby Crohna występujące częściej u kobiet (3, 4). Choroba dotyka również dzieci, częściej chłopców, u których objawia się ona przede wszystkim w pierwszym roku życia (5). Dokładna znajomość anatomii kanału odbytu oraz etiologii przetok i ropni okołoodbytowych jest kluczowa dla prawidłowego ich leczenia i uniknięcia częstego powikłania, jakim jest inkontynencja spowodowana uszkodzeniem zwieraczy w czasie zabiegu.
Powstawanie przetok odbytu wyjaśnia szeroko przyjęta teoria odkryptowa, zaproponowana w 1878 roku przez Chiariego (6), a dwa lata po nim przez Hermanna i Desfosses (7). Zanotowali oni obecność małych gruczołów leżących w kryptach odbytu i wysunęli przypuszczenie, iż ich zapalenie predysponuje do rozwoju ropni i przetok odbytu. Wielu badaczy przyczyniło się w kolejnych latach do rozwinięcia tej teorii: Lockhart-Mummery (8), Gordon-Watson i Dodd (9), Hill, Shryock i ReBell (10), Dunphy (11), Eisenhammer (12), Parks (13). Zgodnie z nią, w przypadku zatkania ujścia wewnętrznego krypty odbytowej dochodzi do nagromadzenia w świetle krypty wydzieliny gruczołowej, zakażenia bakteriami nieodłącznie obecnymi w świetle odbytnicy i powstania ropnia.
Przetoka najczęściej jest konsekwencją ropnia – dlatego przetoka i ropień okołoodbytowy są uważane za różne stadia tej samej choroby. Przetoka rozwija się u ok. 30-50% chorych poddanych wcześniej nacięciu i drenażowi ropnia (14). Jednakże etiopatogeneza może być różnorodna: choroby zapalne (choroba Leśniowskiego-Crohna, wrzodziejące zapalenie jelita grubego, gruźlica, promienica), urazy (jatrogenne, porodowe, homoseksualne, powypadkowe, samookaleczenie, ciało obce), powikłania pooperacyjne (przednia niska resekcja odbytnicy), nieprawidłowe zaopatrzenie poporodowej rany krocza, radioterapia, nowotwory czy przetoka wrodzona.
Ból nie jest stałym objawem, natomiast może się pojawić w wyniku zatkania ujścia zewnętrznego przetoki treścią ropną, ziarniną, naskórkiem. Głównymi objawami towarzyszącymi przetoce są: ropny wyciek z ujścia zewnętrznego przetoki, uczucie wilgoci w okolicy odbytu, świąd i pieczenie, nawracające ropnie okołoodbytowe, nietrzymanie gazów i stolca. W czasie diagnostyki różnicowej przetok odbytu należy uwzględnić: cystę z gruczołów Bartholina, torbiel włosową, czyrak, bliznę, gruźlicę, promienicę, choroby zapalne jelit, szczelinę odbytu, a także choroby weneryczne (14-17).
Dokładna przedoperacyjna diagnostyka pacjenta, obejmująca badanie przedmiotowe i podmiotowe, a także badania obrazowe (jak fistulografia, ultrasonografia przezodbytnicza, rezonans magnetyczny lub tomografia komputerowa) dostarczają cennych informacji na temat anatomii przetoki, co umożliwia wstępne sklasyfikowanie rodzaju przetoki przed zabiegiem i dobranie odpowiedniej techniki chirurgicznej. Jako metodę o największej czułości i specyficzności wielu autorów podaje rezonans magnetyczny (17, 18). Jest to badanie kosztowne, pozwala jednak określić nie tylko przebieg przetoki, ale również stan otaczających ją tkanek oraz uwidocznić obszary objęte zakażeniem, a także, jak wykazano, przyczynia się ona do zmniejszenia odsetka pooperacyjnych nawrotów choroby (17, 19-21).
Czasami wykonywane są również badania czynnościowe (anorektomanometria, elektromiografia), oceniające funkcję zwieraczy odbytu. Są one wskazane przy przetokach nawrotowych, nad-, poza- i przezzwieraczowych oraz u pacjentów zgłaszających objawy inkontynencji niezależnie od typu przetoki (16).
Istnieje wiele klasyfikacji przetok, a określenie odmiany przetoki stanowi istotną informację w trakcie wyboru odpowiedniej metody leczenia chirurgicznego.
W 1934 roku Milligan i Morgan (22) – świadomi istotnej roli mięśnia łonowo-odbytniczego w prawidłowym trzymaniu stolca – podzielili przetoki, biorąc pod uwagę ich przebieg względem tego mięśnia. Wyróżniali oni przetokę niską, kiedy główny kanał przetoki biegł od krypt odbytu w kierunku obwodowym, wysoką – gdy kierował się dogłowowo, oraz przetokę odbytniczo-odbytową leżącą powyżej mięśnia łonowo-odbytniczego.
Kolejni badacze rozwijali i modyfikowali tę klasyfikację w następnych latach. Powszechnie dziś przyjęty jest podział wg Parksa (23), wyróżniający 4 typy przetok – zależnie od przebiegu kanału przetoki względem mięśni zwieraczy i dźwigacza odbytu: międzyzwieraczowa, przezzwieraczowa, nadzwieraczowa, pozazwieraczowa. Klasyfikacja ta nie obejmuje przetok podskórnych i podśluzówkowych (ryc. 1 i 2).
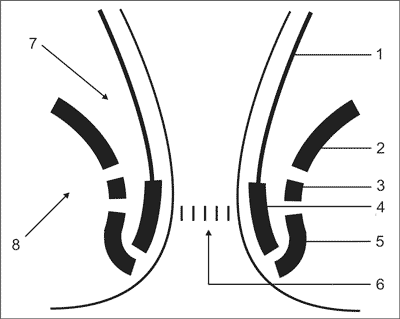
Ryc. 1. Anatomia okolicy odbytu – schemat: 1 – warstwa okrężna błony mięśniowej odbytnicy, 2 – mięsień dźwigacz odbytu, 3 – mięsień łonowo-odbytniczy, 4 – mięsień zwieracz wewnętrzny odbytu, 5 – mięsień zwieracz zewnętrzny odbytu, 6 – linia grzebieniasta i krypty odbytu, 7 – przestrzeń naddźwigaczowa, 8 – dół kulszowo-odbytniczy.
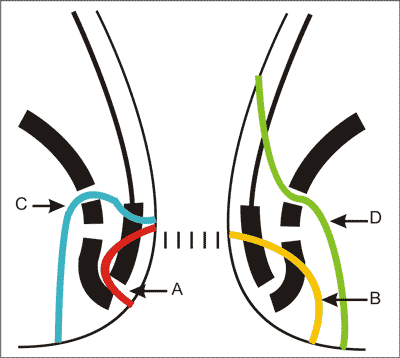
Ryc. 2. Przebieg kanału przetoki wg klasyfikacji Parksa: A – międzyzwieraczowa (typ I), B – przezzwieraczowa (typ II), C – nadzwieraczowa (typ III), D – pozazwieraczowa (typ IV).
Goodsall i Miles (24) dzielili z kolei przetoki na całkowite (posiadające zarówno ujście wewnętrzne, jak i zewnętrzne), ślepe zewnętrzne oraz ślepe wewnętrzne (w przypadku zarośnięcia odpowiednio ujścia zewnętrznego lub wewnętrznego), a w obrębie tego podziału wyróżnili oni przetoki: podskórne, podśluzówkowe i podmięśniowe.
Oprócz klasyfikacji bazujących na obserwacjach poczynionych w czasie operacji powstał także podział St. James’s University Hospital (25) oparty na wynikach rezonansu magnetycznego i uwzględniający zarówno przebieg głównego kanału przetoki, jak i obecność kanałów dodatkowych czy ropnia. Klasyfikacja ta jest pięciostopniowa: I – prosta przetoka międzyzwieraczowa, II – przetoka międzyzwieraczowa z towarzyszącym ropniem lub kanałem drugorzędowym, III – przetoka przezzwieraczowa, IV – przetoka przezzwieraczowa z ropniem lub kanałem drugorzędowym, V – przetoka nad- lub pozazwieraczowa.
Obok podziału Parksa w praktyce klinicznej często używa się określeń takich jak przetoka nawrotowa, przetoka mnoga (przy współwystępowaniu kilku kanałów przetok o osobnych ujściach wewnętrznych) czy przetoka podkowiasta, tzw. horseshoe (przypomina ona podkowę końską obejmującą kanał odbytu po obu jego stronach; powstaje wskutek przeniesienia się zakażenia z krypty odbytowej obustronnie do obu dołów kulszowo-odbytniczych).
Innym stosowanym sposobem klasyfikacji jest podział przetok na proste i złożone. Zgodnie z nim przetokami prostymi określa się przetoki niskie międzyzwieraczowe obejmujące mniej niż 30% masy zwieraczy, niskie przezzwieraczowe oraz podśluzówkowe (26, 27). Mianem przetok złożonych określamy natomiast te, w przypadku których występuje wysokie ryzyko pooperacyjnego nietrzymania stolca. Zaliczamy do nich przetoki o mnogich ujściach zewnętrznych, wysokie przezzwieraczowe (obejmujące ponad 30-50% zwieraczy odbytu), nad- i pozazwieraczowe, a także przetoki ślepo zakończone (ślepe wewnętrzne i zewnętrzne) oraz wspomniane podkowiaste, a w przypadku kobiet przetoki przednie (z uwagi na słabszy i cieńszy zwieracz zewnętrzny w części przedniej; w części tylnej protekcję trzymania stolca zapewnia mięsień łonowo-odbytniczy). Przetoki złożone występują najczęściej u pacjentów cierpiących na chorobę Crohna (w przebiegu której powstają często przetoki o bardziej nietypowej anatomii niż przetoki pochodzenia odkryptowego, przetoki rozgałęzione, mnogie lub imitujące przetoki mnogie) (3) i u chorych z przedoperacyjnymi zaburzeniami kontynencji, a także poddanych miejscowemu naświetlaniu (26, 27).
Jedynym skutecznym sposobem leczenia większości przetok jest zabieg operacyjny. Ma on na celu wyleczenie przetoki bez wywierania większego wpływu na trzymanie stolca. Metodę zabiegu wybiera się w oparciu o indywidualną ocenę pacjenta w zakresie funkcji zwieraczy odbytu, pochodzenia przetoki oraz na podstawie określenia typu przetoki. Większą ostrożność w leczeniu chirurgicznym zaleca się w przypadku przetok towarzyszących chorobie Crohna z uwagi na gorsze gojenie się ran, możliwość zwężenia kanału odbytu czy powstania przetoki w innym miejscu, a także z powodu występującego często już przed operacją osłabienia trzymania gazów i stolca w związku z uszkodzeniem receptorów czuciowych przez proces zapalny toczący się w przebiegu choroby Crohna. Postępowanie u tych pacjentów obejmuje leczenie zachowawcze (antybiotykoterapia, leki immunosupresyjne, leczenie biologiczne, np. infliximab) i chirurgiczne (3).
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
29 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
69 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
129 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 78 zł
Piśmiennictwo
1. Zanotti C, Martinez-Puente C, Pascual I et al.: An assessment of the incidence of fistula-in-ano in four countries of the European Union. Int J Colorectal Dis 2007; 22(12): 1459-1462. 2. Seow-Choen F, Nicholls RJ: Anal fistula. Br J Surg 1992; 79(3): 197-205. 3. Kołodziejczak M, Bielecki K: Contemporary opinions on diagnosis and treatment of anal abscesses and fistulas in the course of Crohn’s disease. Gastroenterol Pol 2007; 14(5): 353-356. 4. Galandiuk S, Kinbirling J, Al-Mishlab TG, Stromberg A: Perineal Crohn’s disease. Ann Surg 2005; 241: 796-802. 5. Chang HK, Ryu JG, Oh JT: Clinical characteristics and treatment of perianal abscess and fistula-in-ano in infants. J Pediatr Surg 2010; 45(9): 1832-1836. 6. Chiari H: Űber die Nalen Divertikel der Recttlmschleimhaut und Ihre Beziehung zu den Anal Fisteln. Med J Wien 1878; 1: 419-425. 7. Hermann G, Desfosses L: Sur la muquese de la region cloacle du rectum. Compte Rendu de l’Acad Sci 1880; 90: 1301-1305. 8. Lockhart-Mummery JP: Discussion on fistula-in-ano. Proc R Soc Med 1929; 22(9): 1331-1358. 9. Gordon-Watson C, Dodd H: Observations on fistula-in-ano in relation to perianal intramuscular glands with report of three cases. Br J Surg 1935; 22: 703-709. 10. Hill MR, Shryock EH, ReBell FG: Role of anal glands in the pathogenesis of anorectal disease. J Am Med Assoc 1943; 121: 742-747. 11. Dunphy JE: Surgical anatomy of the anal canal. Arch Surg 1948; 57: 791-796. 12. Eisenhammer S: The internal anal sphincter and anorectal abscess. Surg Gynec Obst 1956; 103: 501-506. 13. Parks AG: Pathogenesis and treatment of fistuila-in-ano. Br Med J 1961; 1(5224): 463-469. 14. Rickard MJ: Anal abscesses and fistulas. ANZ J Surg 2005; 75(1-2): 64-72. 15. Robinson AM Jr, De Nobile JW: Anorectal abscess and fistula-in-ano. J Natl Med Assoc 1988; 80(11): 1209-1213. 16. Kołodziejczak M: Przetoki odbytu. [W:] Kołodziejczak M: Ropnie i przetoki odbytu. Wydawnictwo Medyczne Borgis, wyd. 1, Warszawa
2003: 38-42. 17. Waniczek D, Adamczyk T, Kozińska-Marek E et al.: Usefulness assessment of preoperative MRI fistulography in patients with perianal fistulas. Pol Przegl Radiol 2011; 76(4): 40-44. 18. Lunniss PJ, Barker PG, Sultan AH et al.: Magnetic resonance imaging of fistula-in-ano. Dis Colon Rectum 1994; 37(7): 708-18. 19. Buchanan G, Halligan S, Williams A et al.: Effect of MRI on clinical outcome of recurrent fistula-in-ano. Lancet 2002; 360(9346): 1661-1662. 20. Halligan S, Stoker J: Imaging of fistula-in-ano. Radiology 2006; 239(1): 18-33. 21. Obcowska A, Kołodziejczak M, Sudoł-Szopińska I: Anal fistulas diagnosis – what every surgeon should know? Nowa Medycyna 2010; 4: 130-137. 22. Milligan ET, Morgan CN: Surgical anatomy of the anal canal with special reference to anorectal fistulae. Lancet 1934; 2: 1213-1217. 23. Parks AG, Gordon PH, Hardcastle JD: A classification of fistula-in-ano. Br J Surg 1976; 63(1): 1-12. 24. Goodsall DH, Miles WE: Anorectal Fistula. Dis Colon Rectum 1882; 25: 262-278. 25. Morris J, Spencer JA, Ambrose NS: MR imaging classification of perianal fistulas and its implications for patient management. Radiographics 2000; 20(3): 623-635. 26. Ellis CN: Bioprosthetic plugs for complex anal fistulas: an early experience. J Surg Educ 2007; 64: 36-40. 27. Shawki S, Wexner SD: Idiopatic fistula in ano. World J Gastroenterol 2011; 17(28): 3277-3285. 28. Cirocco WC, Reilly JC: Challenging the predictive accuracy of Goodsall’s rule for anal fistulas. Dis Colon Rectum 1992; 35(6): 537-542. 29. Marks CG, Ritchie JK: Anal fistulas at St Mark’s Hospital. Br J Surg 1977; 64(2): 84-91. 30. Vasilevsky CA, Gordon PH: Results of treatment of fistula-in-ano. Dis Colon Rectum 1985; 28(4): 225-231. 31. Kołodziejczak M: Kliniczna ocena odległych wyników chirurgicznego leczenia przetok odbytu. Rozprawa na stopień doktora nauk medycznych, 1996. 32. Dziki A, Bartos M: Seton treatment of anal-fistula: experience with a new modification. Eur J Surg 1998; 164(7): 543-548. 33. Malouf AJ, Buchanan GN, Carapeti EA et al.: A prospective audit of fistula-in-ano at St. Mark’s hospital. Colorectal Dis 2002; 4(1): 13-19. 34. Fernández-Frías AM, Pèrez-Vicente F, Arroyo A et al.: Is anal endosonography useful in the study of recurrent complex fistula-in-ano? Rev Esp Enferm Dig 2006; 98(8): 573-581. 35. Mónica AN, Costa A, Aleluia C: MRI evaluation of fistula-in-ano. Acta Med Port 2007; 20(4): 319-324. 36. Sygut A, Zajdel R, Kedzia-Budziewska R et al.: Late results of treatment of anal fistulas. Colorectal Dis 2007; 9(2): 151-158. 37. Meinero P, Mori L: Video-assisted anal fistula treatment (VAAFT): a novel sphincter-saving procedure for treating complex anal fistulas. Tech Coloproctol 2011; 15(4): 417-422. 38. Ozkavukcu E, Haliloglu N, Erden A: Frequencies of perianal fistula types using two classification systems. Jpn J Radiol 2011; 29(5): 293-300. 39. Waniczek D, Zapotoczny S, Rudzki M et al.: Doświadczenie własne w leczeniu przetok okołoodbytniczych w latach 2006-2009. J Ecol Health 2012; 16(1): 35-39. 40. Buchanan GN, Halligan S, Bartram CI et al.: Clinical examination, endosonography, and MR imaging in preoperative assessment of fistula-in-ano: comparison with outcome-based reference standard. Radiology 2004; 233(3): 674-681. 41. Kuijpers HC, Schulpen T: Fistulography for fistula-in-ano. Is it useful? Dis Colon Rectum 1985; 28(2): 103-104. 42. Schratter-Sehn AU, Lochs H, Vogelsang H et al.: Endoscopic ultrasonography versus computed tomography in the differential diagnosis of perianorectal complications in Crohn’s disease. Endoscopy 1993; 25(9): 582-586. 43. Spencer JA, Chapple K, Wilson D et al.: Outcome after surgery for perianal fistula: predictive value of MR imaging. AJR Am J Roentgenol 1998; 171(2): 403-406. 44. Watanabe Y, Todani T, Yamamoto S: Conservative management of fistula-in-ano in infants. Pediatr Surg Int 1998; 13(4): 274-276. 45. Rosen NG, Gibbs DL, Soffer SZ et al.: The nonoperative management of fistula-in-ano. J Pediatr Surg 2000; 35(6): 938-939. 46. Oh JT, Han A, Han SJ et al.: Fistula-in-ano in infants: is nonoperative management effective? J Pediatr Surg 2001; 36(9): 1367-1369. 47. Gupta P: Anal fistulotomy by radiofrequency. J Nihon Med Sch 2004; 71(4): 287-291. 48. Gupta PJ: Radio surgical fistulotomy: an alternative to conventional procedure in fistula-in-ano. Curr Surg 2003; 60(5): 524-528. 49. Corman ML, Abcarian H, Bailey HR et al.: The Surgisis AFP anal fistula plug: report of a consensus conference. Colorectal Dis 2008; 10: 17-20. 50. Lenisa L, Esp?n-Basany E, Rusconi A et al.: Anal fistula plug is a valid alternative option for the treatment of complex anal fistula in the long term. Int J Colorectal Dis 2010; 25: 1487-1493. 51. Lawes DA, Efron JE, Abbas M et al.: Early experience with the bioabsorbable anal fistula plug. World J Surg 2008; 32: 1157-1159. 52. Champagne BJ, O’Connor LM, Ferguson M et al.: Efficacy of anal fistula plug in closure of cryptoglandular fistulas: long-term follow-up. Dis Colon Rectum 2006; 49: 1817-1821. 53. Rojanasakul A: LIFT procedure: a simplified technique for fistula-in-ano. Tech Coloproctol 2009; 13(3): 237-240. 54. García-Olmo D, García-Arranz M, Herreros D et al.: A phase I clinical trial of the treatment of Crohn’s fistula by adipose mesenchymal stem cell transplantation. Dis Colon Rectum 2005; 48(7): 1416-1423. 55. Garcia-Olmo D, Herreros D, Pascual I et al.: Expanded adipose-derived stem cells for the treatment of complex perianal fistula: a phase II clinical trial. Dis Colon Rectum 2009; 52(1): 79-86. 56. Shorthouse AJ: Anal fistula. J R Soc Med 1994; 87: 491-493. 57. Blumetti J, Abcarian A, Quinteros F et al.: Evolution of Treatment of Fistula in Ano. World J Surg 2012; 36: 1162-1167. 58. Aguilar PS, Plasencia G, Hardy TG Jr et al.: Mucosal advancement in the treatment of anal fistula. Dis Colon Rectum 1985; 28(7): 496-498. 59. Schouten WR, Zimmerman DD, Briel JW: Transanal advancement flap repair of transsphincteric fistulas. Dis Colon Rectum 1999; 42(11): 1419-1422. 60. Kodner IJ, Mazor A, Shemesh EI et al.: Endorectal advancement flap repair of rectovaginal and other complicated anorectal fistulas. Surgery 1993; 114(4): 682-689. 61. Mizrahi N, Wexner SD, Zmora O et al.: Endorectal advancement flap: are there predictors of failure? Dis Colon Rectum 2002; 45(12): 1616-1621. 62. Gustafsson UM, Graf W: Excision of anal fistula with closure of the internal opening: functional and manometric results. Dis Colon Rectum 2002; 45(12): 1672-1678. 63. Kreis ME, Jehle EC, Ohlemann M et al.: Functional results after transanal rectal advancement flap repair of trans-sphincteric fistula. Br J Surg 1998; 85: 240-242. 64. Mazier WP: The treatment and care of anal fistulas: A study of 1.000 patients. Dis Colon Rectum 1971; 2: 134-144. 65. Westerterp M, Volkers NA, Poolman RW, van Tets WF: Anal fistulotomy between Skylla and Charybdis. Colorectal Dis 2003; 5(6): 549-551.



