*Halina Ekiert, Agnieszka Sondej, Karolina Jafernik, Agnieszka Szopa
Nowe surowce roślinne w Farmakopei Europejskiej. Część 3. Ligusticum chuanxiong (Podagrycznik chiński) – zródło nowego surowca olejkowego
The new plant raw materials in the European Pharmacopoeia. Part 3. Ligusticum chuanxiong (Sechuan lovage) – source of new essential oil-bearing raw material
Katedra i Zakład Botaniki Farmaceutycznej, Uniwersytet Jagielloński, Collegium Medicum, Kraków
Kierownik Katedry i Zakładu: prof. dr hab. n. farm. Halina Ekiert
Streszczenie
W Suplemencie 9.4 do Farmakopei Europejskiej, jednym z najnowszych opublikowanych dokumentów farmakopealnych, obok scharakteryzowanych w częściach 1 i 2 serii artykułów nowych surowców saponinowych (Bupleuri radix i Platycodi radix), figurują inne, nowe surowce roślinne od dawna znane w tradycyjnej chińskiej medycynie (TCM), a równocześnie dotychczas nieznane w oficjalnym lecznictwie europejskim.
W części 3 serii publikacji przedstawiono charakterystykę botaniczno-ekologiczno-chemiczną Ligusticum chuanxiong – Podagrycznika chińskiego. Kłącze tego gatunku – Ligustici chuanxiong rhizoma, to surowiec olejkowy, od dawna wykorzystywany w TCM w leczeniu głównie dolegliwości ginekologicznych i bólowych o różnej etiologii. Profesjonalne badania naukowe dokumentują szeroki wachlarz możliwych innych istotnych zastosowań terapeutycznych tego surowca, m.in. w usprawnianiu funkcji układu sercowo-naczyniowego, oraz jego właściwości przeciwutleniające i przeciwnowotworowe. Przeglądowi badań farmakologicznych surowca poświęcono w artykule najwięcej uwagi.
Celem artykułu jest prezentacja podstawowej wiedzy na temat podagrycznika chińskiego, która wydaje się być niezbędną w profesjonalnych kontaktach farmaceutów, lekarzy i fitoterapeutów z pacjentami.
Summary
The European Pharmacopoeia, Supplement 9.4, one of the newest published pharmacopoeial documents, besides new saponin-bearing raw materials (Bupleuri radix and Platycodi radix) characterized in part 1 and 2 of the series of articles, lists also other new plant raw materials, long known in traditional Chinese medicine (TCM) but earlier unknown in official European medicine.
Part 3 of the series of articles presents botanical, ecological and chemical characterization of Ligusticum chuanxiong – Sechuan lovage. Rhizome of this species – Ligustici chuanxiong rhizoma is an essential oil-bearing raw material that has long been used in TCM to treat most of all different gynecological ailments and pain of different etiologies. Professional scientific studies documented a wide range of its possible therapeutic applications, e.g. improvement of the cardiovascular system function, and its antioxidant and anticancer properties. A review of pharmacological studies of this raw material was subject to most attention in the article.
The aim of the article is to present basic knowledge on Sechuan lovage, which appears indispensable in professional contacts of pharmacists, medical doctors and phytotherapists with patients.

Wstęp
W jednym z najnowszych dokumentów farmakopealnych obowiązujących państwa członkowskie Unii Europejskiej, w tym Polskę, w Suplemencie 9.4 do Farmakopei Europejskiej (European Pharmaco-poeia 9.4) (1) figurują monografie 6 nowych surowców roślinnych pochodzenia wschodnio-azjatyckiego. Od dawna surowce te są znane i wykorzystywane w tradycyjnej chińskiej medycynie (TCM).
W częściach 1 i 2 serii artykułów (2, 3) zaprezentowano podstawowe informacje dotyczące morfologii, ekologii, chemizmu i znaczenia leczniczego gatunków roślin dostarczających nowych surowców saponinowych – dwóch gatunków z rodzaju Przewiercień (Bupleurum chinense i Bupleurum scorzonerifolium) oraz Rozwaru wielkokwiatowego (Platycodon grandiflorus).
W części 3 zgromadzono podstawowe informacje na temat Ligusticum chuanxiong Hort – Podagrycznika chińskiego (Apiaceae), gatunku będącego źródłem nieznanego i niewykorzystanego wcześniej w Europie surowca olejkowego – Ligustici chuanxiong rhizoma. Najwięcej uwagi poświęcono możliwym wskazaniom terapeutycznym tego surowca, potwierdzonym profesjonalnymi badaniami naukowymi. Przegląd możliwych licznych zastosowań leczniczych tego surowca, m.in. korzystny wpływ na układ sercowo-naczyniowy, jego działanie przeciwutleniające i przeciwnowotworowe, dokumentuje i uzasadnia celowość wprowadzenia tego surowca do oficjalnego lecznictwa europejskiego.
Znaczenie lecznicze Podagrycznika chińskiego w TCM i pozycja w oficjalnym lecznictwie europejskim
W TCM surowiec wykorzystuje się w leczeniu dolegliwości ginekologicznych, m.in. w przypadku nieregularnych miesiączek, ich braku czy też bolesnego miesiączkowania. W terapiach tych kłącze Podagrycznika chińskiego (Ligustici chuanxiong rhizoma) może stanowić składnik preparatów złożonych, które dodatkowo zawierają np. Angelicae sinensis radix, Paeoniae lactiflorae radix czy Borneolum syntheticum. Innymi zastosowaniami surowca, według TCM, jest leczenie różnego rodzaju bólu, w tym migreny, a także gorączki i przeziębienia. W przypadku bólu głowy, kłącze L. chuanxiong używane jest samodzielnie lub wraz z Gastrodiae rhizoma lub Angelicae dahuricae radix (4, 5).
Surowcem farmaceutycznym, według Suplementu 9.4 Farmakopei Europejskiej (European Pharmacopoeia 9.4) (1), są wysuszone, całe lub rozdrobnione, z usuniętymi korzonkami, kłącza Podagrycznika chińskiego – Ligustici chuanxiong rhizoma. Suplement dopuszcza do wykorzystania tylko jeden gatunek – Ligusticum chuanxiong Hort, często nazywany także Ligusticum sinense Oliv. Według wytycznych farmakopealnych kłącza podagrycznika należy zbierać latem, kiedy ich węzły stają się wyraźnie pogrubione i fioletowawe. Surowiec w 1 kg suchej masy powinien zawierać minimum 3,5 ml olejku eterycznego (1, 6).
Występowanie i charakterystyka botaniczno-ekologiczna gatunku
Rodzaj Ligusticum liczy około 30 gatunków występujących na terenie Azji. Niektóre z nich są gatunkami endemicznymi, typowymi dla flory Chin.
L. chuanxiong ma naturalne stanowiska występowania w Japonii i Chinach. Gatunek ten rośnie w lasach, górskich zaroślach, na trawiastych zboczach oraz przy brzegach strumieni (4, 5). Roślina w Chinach jest również uprawiana w celach komercyjnych, głównie w miastach: Dujiangyan, Pengzhou, Chongzhou oraz w dzielnicy Xindu w prowincji Sechuan. Roczna produkcja surowca wynosi nawet 18 000-20 000 ton i jest skierowana głównie na rynek chiński. Surowiec jest także eksportowany do Japonii, Korei Południowej, Singapuru, Malezji i kilkunastu innych krajów na terenie Azji (5).
L. chuanxiong jest rośliną wieloletnią, osiągającą wysokość od 40 do 70 cm. Gatunek ten ma grube, nieregularne kłącza, widocznie pogrubione w węzłach, o krótkich międzywęźlach. Pędy L. chuanxiong są pojedyncze, proste i rozgałęzione, na przekroju cylindryczne. Ogonki liściowe mają długość 3-10 cm; blaszka jest trójkątnie-jajowata o długości 12-15 cm i szerokości 10-15 cm. Płatki korony kwiatów są białe, odwrotnie jajowate z klinowatą podstawą. Owoce mają kształt podłużnie jajowaty. Kwiaty oraz owoce pojawiają się na roślinie bardzo rzadko, nawet w obszarach naturalnego jej występowania. Roślina kwitnie od lipca do sierpnia, a owocuje od września do października (4).
Kłącze L. chuanxiong oraz liście i łodygi są stosowane jako produkty żywnościowe w Chinach i innych krajach azjatyckich, m.in. w Japonii, Korei oraz na Tajwanie (5).
Skład chemiczny gatunku
Jak podają różne źródła, z L. chuanxiong wyizolowano i zidentyfikowano około 170 związków należących do takich grup metabolitów, jak: ftalidy, alkaloidy, terpenoidy, polisacharydy, kwasy organiczne i inne (tab. 1). Głównymi metabolitami biologicznie aktywnymi surowca są związki ftalidowe, m.in.: butylidenoftalid, ligustilid, senkyunolid A (ryc. 1), oraz alkaloid – tetrametylopirazyna (TMP, ligustaryzyna, chuanksiongzyna) (ryc. 2).
Tab. 1. Skład chemiczny kłącza L. chuanxiong
| Grupa metabolitów | Związki | Piśmiennictwo |
| Ftalidy | (Z)-ligustilid, riligustilid, senkyunolid A, neoknidilid, chaksiongnolid A, chaksiongnolid B, chuanksionginy A, B, C, D, E, F; lewistolid A, Z-3 butylideno-7-hydroksyftalid, senkyunolid B, 3-butyloftalid, cis- i trans-6,7-dihydroksyligustilidy | (10-13) |
| Alkaloidy | tetrametylopirazyna (TMP, ligustaryzyna, chuanksiongzyna), acetylo-β-karbolina | (14-17) |
| Kwasy fenolowe | kwas ferulowy, kwas galusowy, kwas protokatechowy | (7, 9) |
| Terpenoidy | γ-terpinen, δ-terpinen, α-felandren, α-tujen, β-tujen | (21) |
| Polisacharydy | LCA – zbudowany z arabinozy, galaktozy i mannozy
LCB – zbudowany z arabinozy, glukozy i galaktozy
LCC – zbudowany z arabinozy, glukozy i galaktozy
LCXP-1, LCXP-2 – zbudowany z mannozy, glukozy, galaktozy i arabinozy
LCXP-3 – zbudowany z mannozy, glukozy, galaktozy, arabinozy, ramnozy i kwasu galakturonowego | (19, 20) |
| Nukleozydy i ich składniki | adenina, adenozyna, uracyl | (14-17) |
| Związki azotowe | trimetyloamina, cholina | (15-18) |
| Kumaryny | skopoletyna | (14-17) |
| Sterole | β-sitosterol | (18) |
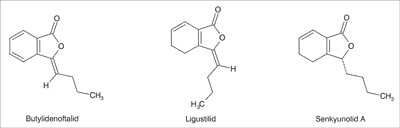
Ryc. 1. Budowa chemiczna ftalidów typowych dla L. chuanxiong
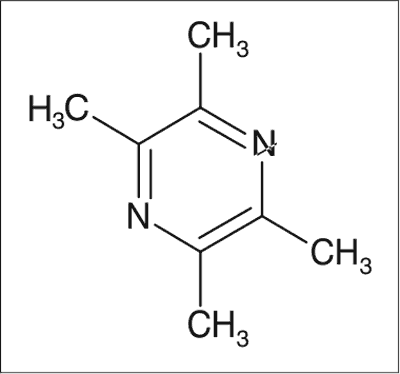
Ryc. 2. Budowa chemiczna charakterystycznego dla L. chuanxiong alkaloidu – TMP (tetrametylopirazyny, ligustaryzyny, chuanksiongzyny)
Do tej pory w L. chuanxiong zidentyfikowano 57 związków ftalidowych. To swoista grupa metabolitów wtórnych. Wykazano, że ftalidy alkilowe są niestabilne pod wpływem światła i ogrzewania oraz mogą łatwo przekształcać się w formy dimeryczne. Przykładowo, Z-ligustilid pod wpływem ogrzewania może przechodzić w senkyunolidy H i L, a pod wpływem naświetlania w lewistolid A i riligustilid. W Chinach i w Azji Południowo-Wschodniej, TMP jest popularnym związkiem stosowanym w profilaktyce oraz leczeniu chorób układu sercowo-naczyniowego (5, 6).
Skład chemiczny olejku eterycznego
Obecność olejku eterycznego pozyskiwanego z kłącza L. chuanxiong jest niezwykle istotna. Z podanych źródeł z olejku wyizolowano i zidentyfikowano związki należące do grupy ftalidów, a mianowicie: ligustilid, butylidenoftalid, knilid, neoknilid, senkyunolidy A, F, H, I, J i P, 3-butylidenoftalid, 3-butyloftalid, tokinolid B oraz lewistolid A (7, 8).
Działanie terapeutyczne i zastosowanie surowca i wyizolowanych związków
Aktywność w chorobie niedokrwiennej serca
Przeprowadzono badania na psim modelu ostrego niedokrwienia serca. Wykazano, że związki obecne w ekstrakcie z kłącza L. chuanxiong, tj. TMP, ligustylid, knidilid i kwas ferulowy, mają działanie ochronne przed uszkodzeniem mięśnia sercowego. TMP i kwas ferulowy znacząco obniżały poziom kwasu mlekowego w surowicy, a ligustylid hamował wzrost poziomu wolnych kwasów tłuszczowych (22). Inne badania przeprowadzono na komórkach śródbłonka naczyń włosowatych serca szczura, które inkubowano z senkyunolidem A przez 55 minut, a następnie poddawano hipoksji przez 4 godziny i reoksygenacji przez 2 godziny. Wykazano, że senkyunolid A powodował zwiększenie liczby komórek, które przeżywały podwyższenie poziomu aktywności NO i NOS (syntazy tlenku azotu) w pożywce do hodowli komórkowej oraz obniżenie aktywności endoteliny. Ponadto w badaniu stwierdzono wzrost poziomu ekspresji mRNA, iNOS i obniżenie poziomu ekspresji endoteliny mRNA (23).
W innym eksperymencie badano wpływ wodnego ekstraktu z dwóch surowców – Salviae miltiorrhizae i Rhizoma chuanxiong – na uszkodzenie mięśnia sercowego wywołane przez niedokrwienie i reperfuzję. Wykazano, że zastosowanie ekstraktów może znacznie zmniejszyć rozległość zawału mięśnia sercowego, obniżyć stężenie izoenzymu MB kinazy kreatynowej we krwi i cTnT troponin sercowych oraz zwiększyć stosunek 6-keto-PGF (1α) do TXB (24).
Aktywność przeciwagregacyjna
Zbadano mechanizm odpowiedzialny za aktywność przeciwagregacyjną TMP na ludzkich trombocytach. Wyniki wykazały, że aktywność przeciwagregacyjna TMP może obejmować dwa szlaki: w niższym stężeniu (0,5 mmol) substancja ta hamowała rozpad fosfatydylocholiny i powstawanie tromboksanu A2, natomiast w wyższym stężeniu (1,0 mmol) – agregację płytek przez wiązanie z kompleksem glikoproteiny IIb/IIIa (25).
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
29 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
69 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
129 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 78 zł
Piśmiennictwo
1. European Pharmacopoeia, 9th ed., Suplement 9.4. Council of Europe, Strasbourg 2017.
2. Ekiert H, Sondej A, Klimek-Szczykutowicz i wsp. Nowe surowce roślinne w Farmakopei Europejskiej. Część 1. Gatunki rodzaju Bupleurum (przewiercień) – źródło nowego surowca saponinowego. Post Fitoter 2018; 19(4):248-56.
3. Ekiert H, Sondej A, Klimek-Szczykutowicz i wsp. Nowe surowce roślinne w Farmakopei Europejskiej. Część 2. Rozwar wielkokwiatowy (Platycodon grandiflorus) – źródło nowego surowca saponinowego. Post Fitoter 2019; 20(1):41-8.
4. She M, Pu F, Pan Z i wsp. Apiaceae through Ericaceae. Flora of China 2005; 14:143.
5. Chen Z, Zhang C, Gao F i wsp. A systematic review on the rhizome of Ligusticum chuanxiong Hort. (Chuanxiong). Food Chem Toxicol 2018; 119:309-25.
6. Ran X, Ma L, Peng C i wsp. Ligusticum chuanxiong Hort: A review of chemistry and pharmacology. Pharm Biol 2011; 49:1180-9.
7. Li SL, Chan SS, Lin G i wsp. Simultaneous analysis of seventeen chemical ingredients of Ligusticum chuanxiong by on-line high performance liquid chromatography-diode array detector-mass spectrometry. Planta Med 2003; 69:445-51.
8. Jeong JB, Ju SY, Park JH i wsp. Antioxidant activity in essential oils of Cnidium officinale makino and Ligusticum chuanxiong Hort and their inhibitory effects on DNA damage and apoptosis induced by ultraviolet B in mammalian cell. Cancer Epidemiol 2009; 33(1):41-6.
9. Zhao YX, Ding MY, Liu DL. Phenolic acids analysis in Ligusticum Chuanxiong using HPLC. J Chromatogr Sci 2005; 43:389-93.
10. Yang JB, Wang AG, Wei G i wsp. New dimeric phthalides from Ligusticum sinense Oliv. cv. Chuanxiong. J Asian Nat Prod Res 2014; 16:747-52.
11. Yang J, Feng XL, Yu Y i wsp. Novel phthalide derivatives identified from Ligusticum chuanxiong (Chuanxiong). Chin Med 2016; 11:10.
12. Wang J, Yang JB, Wang AG i wsp. Studies on the chemical constituents of Ligusticum sinense. Zhong Yao Cai 2011; 34:378-80.
13. Pushan W, Xuanliang G, Yixiong W i wsp. Phthalides from the rhizome of Ligusticum wallichii. Phytochem 1984; 23:2033-8.
14. Yan R, Li SL, Chung HS i wsp. Simultaneous quantification of 12 bioactive components of Ligusticum chuanxiong Hort. by high-performance liquid chromatography. J Pharm Biomed Anal 2005; 37:87-95.
15. Cao FY, Liu WX, Wen YS. Studies on the chemical constituents of Ligusticum chuanxiong Hort. Chin Trad Herb Drugs 1983; 14:241-2.
16. Wang YX, Gao XL, Wang PS. Another active component in Ligusticum chuanxiong Hort. Chin Trad Herb Drugs 1985; 16.
17. Ren DC, Xie N, Yang NY i wsp. Studies on the chemical constituents of aerial parts of Ligusticum chuanxiong Hort. Chung Kuo Chung Yao Tsa Chih 2007; 33:1418-20.
18. Luo Y, Zhang J, Pan J i wsp. The constituents of Ligusticum sinense Oliv cv. chuaxiong. Chin Pharm J 1994; 29:714-6.
19. Yuan JF, Zhang ZQ, Fan ZC i wsp. Antioxidant effects and cytotoxicity of three purified polysaccharides from Ligusticum chuanxiong Hort. Carbohydr Polym 2008; 74:822-7.
20. Sun CX, Yan J, He G i wsp. Purification and analysis of monosaccharide composition of Ligusticum chuanxiong polysaccharide. J Sichuan Agri Univ 2001; 29:56-60.
21. Wu Q, Yang XW. GC-MS analysis of essential oil from rhizomes of Ligusticum chuanxiong cultivated in GAP base for Chinese Medicinal Materials of China. China J Chin Mater Med 2008; 33:276-80.
22. Liu X, Li X, Ji S i wsp. Screening of bioactive ingredients in Ligusticum chuanxiong Hort for protection against myocardial ischemia. Cell Physiol Biochem 2016; 40:770-80.
23. Gao W, Liang RX, Xiao YQ i wsp. Protective effect and its mechanism of preconditioning of chuanxiong-phthalide a on rat cardiac microvascular endothelial cell injury by hypoxia and reoxygenation. Chung Kuo Chung Yao Tsa Chih 2007; 32:133-7.
24. Zhang DW, Liu JG, Feng JT i wsp. Effects of effective components compatibility of aqueous extracts of Salviae miltiorrhizae and Rhizoma Chuanxiong on rat myocardial ischemia/reperfusion injury. Chin Crit Care Med 2010; 22:109-12.
25. Sheu JR, Kan YC, Hung WC i wsp. Mechanisms involved in the antiplatelet activity of tetramethylpyrazine in human platelets. Thromb Res 1997; 88:259-70.
26. Sheu JR, Kan YC, Hung WC i wsp. The antiplatelet activity of tetramethylpyrazine is mediated through activation of NO synthase. Life Sci 2000; 67:937-47.
27. Li M, Handa S, Ikeda Y i wsp. Specific inhibiting characteristics of tetramethylpyrazine, one of the active ingredients of the Chinese herbal medicine “Chuanxiong”, on platelet thrombus formation under high shear rates. Thromb Res 2001; 104:15-28.
28. Li M, Zhao C, Wong RN i wsp. Inhibition of shear-induced platelet aggregation in rat by tetramethylpyrazine and salvianolic acid B. Clin Hemorheol Microcirculat 2004; 31:97-103.
29. Liang MJ, He LC. Inhibitory effects of ligustilide and butylidenephthalide on bFGF-stimulated proliferation of rat smooth muscle cells. Acta Pharm Sin 2006; 41:161-5.
30. Yang J, Yang S, Yuan YJ. Integrated investigation of lipidome and related signaling pathways uncovers molecular mechanisms of tetramethylpyrazine and butylidenephthalide protecting endothelial cells under oxidative stress. Mol Biosyst 2012; 8:1789-97.
31. Meng H, Guo J, Sun JY i wsp. Angiogenic effects of the extracts from Chinese herbs: Angelica and Chuanxiong. Am J Chin Med 2008; 36:541-54.
32. Liang MJ, He LC, Yang GD. Screening, analysis and in vitro vasodilatation of effective components from Ligusticum chuanxiong. Life Sci 2005; 78:128-33.
33. Chan SS, Choi AO, Jones RL i wsp. Mechanisms underlying the vasorelaxing effects of butylidenephthalide, an active constituent of Ligusticum chuanxiong, in rat isolated aorta. Eur J Pharmacol 2006; 537:111-7.
34. Chan SS, Cheng TY, Lin G. Relaxation effects of ligustilide and senkyunolide A, two main constituents of Ligusticum chuanxiong, in rat isolated aorta. J Ethnopharmacol 2007; 111:677-80.
35. Tsai CC, Lai TY, Huang WC i wsp. Inhibitory effects of potassium channel blockers on tetramethylpyrazine-induced relaxation of rat aortic strip in vitro. Life Sci 2002; 71:1321-30.
36. Wang J, Liu XR, Shi YM. Observation of the preventive and therapeutic effect of Chuanxiong on the atherosclerosis of rabbits. Chin J Integr Med 1995; 1:52-5.
37. Li QX, Liao YH, Zhang HL i wsp. Inhibitory effect and mechanism of Chuanxiongzine on multiplication. J Nanjing Med Univ 2007; 21:82-5.
38. Ren XY, Ruan QR, Zhu DH i wsp. Tetramethylpyrazine inhibits agiontensin II-induced nuclear factor-kappaB activation and bone morphogenetic protein-2 downregulation in rat vascular smooth muscle cells. Sheng Li Hsueh Pao 2007; 59:339-44.
39. Wong KL, Wu KC, Wu RS i wsp. Tetramethylpyrazine inhibits angiotensin II-increased NAD(P)H oxidase activity and subsequent proliferation in rat aortic smooth muscle cells. Am J Chin Med 2007; 35:1021-35.
40. Liu L, Ning ZQ, Shan S i wsp. Phthalide lactones from Ligusticum chuanxiong inhibit lipopolysaccharide-induced TNF-alpha production and TNF-alpha-mediated NF-kappaB activation. Planta Med 2005; 71:808-13.
41. Xiong L, Fang ZY, Tao XN i wsp. Effect and mechanism of ligustrazine on Th1/Th2 cytokines in a rat asthma model. Am J Chin Med 2007; 35:1011-20.
42. Li J, Yu J, Ma H i wsp. Intranasal pretreatment with Z-ligustilide, the main volatile component of Rhizoma chuanxiong, confers prophylaxis against cerebral ischemia via Nrf2 and HSP70 signaling pathways. J Agric Food Chem 2017; 65:1533-42.
43. Kong X, Zhong M, Su X i wsp. Tetramethylpyrazine promotes migration of neural precursor cells via activating the phosphatidylinositol 3-kinase pathway. Mol Neurobiol 2016; 53:6526-39.
44. Hu J, Cao G, Wu X i wsp. Tetramethylpyrazine inhibits activation of hepatic stellate cells through hedgehog signaling pathways in vitro. Biomed Res Int 2015; 2015.
45. Lu C, Xu W, Shao J i wsp. Nrf2 activation is required for ligustrazine to inhibit hepatic steatosis in alcohol-preferring mice and hepatocytes. Toxicol Sci 2017; 155:432-43.
46. Mo ZZ, Liu YH, Li CL i wsp. Protective effect of SFE-CO2 of Ligusticum chuanxiong Hort against D-galactose-induced injury in the mouse liver and kidney. Rejuvenation Res 2017; 20:231-43.
47. Lim LS, Shen P, Gong YH i wsp. Dynamics of progestogenic activity in serum following administration of Ligusticum chuanxiong. Life Sci 2006; 79:1274-80.
48. Lim LS, Shen P, Gong YH i wsp. Dimeric progestins from rhizomes of Ligusticum chuanxiong. Phytochem 2006; 67:728-34.
49. Ju XD, Deng M, Ao YF i wsp. The protective effect of tetramethylpyrazine on cartilage explants and chondrocytes. J Ethnopharmacol 2010; 132:414-20.
50. Liang QQ, Ding DF, Xi ZJ i wsp. Protective effect of ligustrazine on lumbar intervertebral disc degeneration of rats induced by prolonged upright posture. Evid Based Complement Alternat Med 2014; 2014:508461.
51. Chen J, Jiang QD, Wu YM i wsp. Potential of essential oils as penetration enhancers for transdermal administration of ibuprofen to treat dysmenorrhoea. Molecules 2015; 20:18219-36.
52. Guo J, Duan JA, Tang Y i wsp. Fast onset of action and the analgesic and sedative efficacy of essential oil from Rhizoma Chuanxiong after nasal administration. Pharmazie 2010; 65:296-9.
53. Wang H, Tang Y, Guo J i wsp. Antidysmenorrheic effects of Radix Angelica and Rhizoma Chuanxiong with different proportions and preparation methods on dysmenorrhea model mice. China J Chin Mat Med 2010; 35:892-5.
54. Yang JR, Song J, Hu R i wsp. Effect of essential oil of Ligusticum chuanxiong Hort. on the expressions of COX-2 in hypothalamus of fever rat. Lishizhen Med Mat Med Res 2009; 20:315-6.
55. Li ZL, Yang JR, Fu R i wsp. The antipyretic effect and it’s partial mechanism of the essential oil Ligusticum chuanxiong Hort Inform Trad Chin Med 2003; 20:31-2.
56. Li Y, Xu C, Zhang Q i wsp. In vitro anti-Helicobacter pylori action of 30 Chinese herbal medicines used to treat ulcer diseases. J Ethnopharmacol 2005; 98:329-33.
57. Xiao Y, Liu TJ, Huang ZW i wsp. The effects of natural medicine on adherence of Streptococcus mutans to salivary acquired pellicle. J Sichuan Univ 2004; 35:687-9.
58. Sim Y, Shin S. Combinatorial anti-Trichophyton effects of Ligusticum chuanxiong essential oil components with antibiotics. Arch Pharm Res 2008; 31:497-502.
59. Shih YH, Wu SL, Chiou WF i wsp. Protective effects of tetramethylpyrazine on kainate-induced excitotoxicity in hippocampal culture. Neuroreport 2002; 13:515-9.
60. Michel HE, Tadros MG, Esmat A i wsp. Tetramethylpyrazine ameliorates rotenone-induced Parkinson’s disease in rats: Involvement of its anti-inflammatory and anti-apoptotic actions. Mol Neurobiol 2017; 54:4866-78.
61. Kim M, Kim SO, Lee M i wsp. Tetramethylpyrazine, a natural alkaloid, attenuates pro-inflammatory mediators induced by amyloid β and interferon-γ in rat brain microglia. Eur J Pharmacol 2014; 740:504-11.
62. Yuan JF, Zhang ZQ, Fan ZC i wsp. Antioxidant effects and cytotoxicity of three purified polysaccharides from Ligusticum chuanxiong Hort Carbohydr Polym 2008; 74:822-7.
63. Qi H, Siu SO, Chen Y i wsp. Senkyunolides reduce hydrogen peroxide-induced oxidative damage in human liver HepG2 cells via induction of heme oxygenase-1. Chem Biol Interact 2010; 183:380-9.
64. Juan SH, Chen CH, Hsu YH i wsp. Tetramethylpyrazine protects rat renal tubular cell apoptosis induced by gentamicin. Nephrol Dial Transplant 2007; 22:732-9.
65. Wu N, Xu L, Yang Y i wsp. Tetramethylpyrazine-mediated regulation of CXCR4 in retinoblastoma is sensitive to cell density. Mol Med Rep 2017; 15:2481-8.
66. Bi L, Yan X, Chen W i wsp. Antihepatocellular carcinoma potential of tetramethylpyrazine induces cell cycle modulation and mitochondrial-dependent apoptosis: regulation of p53 signaling pathway in HepG2 cells in vitro. Integr Cancer Ther 2016; 15:226-36.
67. Liu PY, Sheu JJ, Lin PC i wsp. Expression of Nur77 induced by an n-butylidenephthalide derivative promotes apoptosis and inhibits cell growth in oral squamous cell carcinoma. Invest New Drugs 2012; 30:79-89.
68. Hu J, Jia X, Fang X i wsp. Ultrasonic extraction, antioxidant and anticancer activities of novel polysaccharides from Chuanxiong rhizome. Int J Biol Macromol 2016; 85:277-84.
69. Ruszkiewicz JA, Pinkas A, Miah MR i wsp. C. elegans as a model in developmental neurotoxicology. Toxicol Appl Pharmacol 2018; 354:126-35.
70. Wang X, Wang X, Wang D i wsp. Effect of Ligusticum chuanxiong extract on lifespan of Caenorhabditis elegans and its underlying molecular mechanisms. China J Chin Mat Med 2010; 35:1042-5.
71. Wang X, Wang X, Wang D i wsp. Expression changes of age-related genes in different aging stages of Caenorhabditis elegans and the regulating effects of Chuanxiong extract. China J Chin Mat Med 2010; 35:1599-602.


