© Borgis - Nowa Stomatologia 4/2005, s. 214-217
Monika Nosek, Piotr Wychowański, Andrzej Wojtowicz
Wpływ przewlekłej terapii lekami przeciwzakrzepowymi na tkankę kostną – przegląd piśmiennictwa
The influence of the long-term anticoagulant therapy on bone tissue condition – the review of literature
Zakład Chirurgii Stomatologicznej Instytutu Stomatologii Akademii Medycznej w Warszawie
Kierownik: doc. dr hab. n. med. Andrzej Wojtowicz

Jednym z najważniejszych mechanizmów umożliwiających homeostazę ustroju jest zdolność do hemostazy. Procesy te są niezbędnymi mechanizmami obronnymi mającymi na celu zapobieganie utracie krwi w przypadku uszkodzenia naczyń. Zaburzenia procesów hemostazy prowadzą z jednej strony do objawów skazy krwotocznej w przypadku niewydolności układu a w drugiej skrajności do powikłań zatorowo-zakrzepowych w sytuacjach patologicznie zwiększonej aktywności. Istnieje zatem wiele patologii stanowiących wskazanie do stosowania terapii przeciwzakrzepowej. Należą do nich zarówno sytuacje, gdy zator lub zakrzep już powstały, jak i stany zwiększonego ryzyka wytworzenia zatoru czy zakrzepu. Do stanów takich, gdy powinniśmy wdrożyć profilaktykę zakrzepowo-zatorową należą: zaburzenia rytmu serca, zawał mięśnia serca i jego profilaktyka, przewlekła choroba żylna, krążenie pozaustrojowe, dializoterapia, zespół hemolityczno-mocznicowy, zespół rozsianego wykrzepiania wewnątrznaczyniowego, retinopatia cukrzycowa, okres okołooperacyjny (zwłaszcza chirurgia sercowo-naczyniowa, przeszczepianie narządów, zabiegi ginekologiczno-położnicze), urazy wielonarządowe oraz inne stany nadkrzepliwości.
Istnieją trzy główne grupy leków przeciwzakrzepowych o różnym mechanizmie działania: heparyny (niefrakcjonowana i drobnocząsteczkowa), antagoniści witaminy K i leki defibrynujące.
Mechanizm działania heparyny
Heparyna, pod postacią soli sodowej, hamuje krzepnięcie krwi na skutek zwiększania działania antytrombiny III. Antytrombina III jest alfa 2 globuliną wytwarzaną w wątrobie. Jej masa cząsteczkowa wynosi 63 tys., a prawidłowe stężenie w osoczu około 0,3 g/l. Antytrombina III tworzy nieodwracalne kompleksy z trombiną w wyniku czego obydwa te białka unieczynniają się, zaburzając zależne od trombiny szlaki krzepnięcia. Heparyna przyspiesza unieczynnianie trombiny zależne od antytrombiny III. Doustne antykoagulanty (antagoniści witaminy K) hamują zależną od witaminy K syntezę w wątrobie osoczowych czynników krzepnięcia II,VII, IX, X. Leki defibrylujące zmniejszają stężenie fibrynogenu (1).
Mechanizm działania doustnych antykoagulantów
Witamina K warunkuje posttranslacyjną karboksylację kwasu glutaminowego (powstaje kwas gamma-karboksyglutaminowy) w cząsteczce protrombiny i innych czynników krzepnięcia syntetyzowanych w wątrobie, co determinuje ich zdolność wiązania jonów wapniowych i aktywność biologiczną. Po podaniu doustnych antykoagulantów szybkość wystąpienia zmniejszonej aktywności koagulacyjnej zależy od czasu przeżycia danego czynnika krzepnięcia.
Doustne antykoagulanty są pochodnymi 4-hydroksykumaryny lub indan-1,3-dionu, mających zbliżoną budowę do witaminy K. Mechanizm ich działania polega na kompetycji z witaminą K o miejsca receptorowe w komórce wątroby. Powodują one efekt awitaminozy K, zmniejszenie stężenia w osoczu aktywnych postaci czynników krzepnięcia II, VII, IX, X. W osoczu pojawiają się karboksylowe postacie tych czynników, nieaktywne biologicznie.
Działanie antagonistów witaminy K ocenia się na podstawie oznaczenia aktywności protrombiny przy użyciu tzw. czasu protrombinowego, tj. czasu krzepnięcia rekalcyfikowanego osocza przy nadmiarze tromboplastyny. Prawidłowo wynosi on 12-14 sekund. Zależy od aktywności czynników II, VII, IX, X. Jest tym dłuższy, im mniejsza aktywność tych czynników (1, 2, 3, 4).
Czas protrombinowy osób zdrowych zależy od preparatów tromboplastyny. W celu otrzymywania porównywalnych wyników wprowadzono nowy sposób wyrażania czasu protrombinowego w postaci znormalizowanego współczynnika międzynarodowego – INR. Prawidłowa wartość współczynnika INR wynosi 0,8-1,2.
Kaskadę procesu krzepnięcia z uwzględnieniem miejsca uchwytu heparyny i doustnych leków antykoagulacyjnych przedstawia rycina 1.
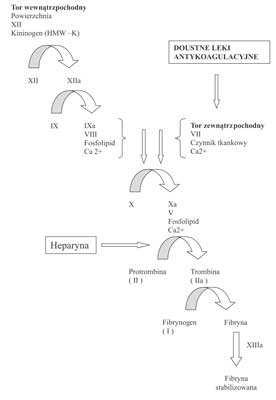
Ryc. 1. Schemat krzepnięcia – miejsca działania leków przeciwzakrzepowych.
Leki defibrynujące
Są to preparaty wykazujące działanie trombinopodobne. Ich działanie wynika z właściwości peptydazowych, jakie wykazują. Na skutek odszczepienia fibrynopeptydu A z łańcucha A a– fibrynogenu dochodzi do wytworzenia patologicznego monomeru fibryny, niezdolnego do wytworzenia wiązań krzyżowych. To powoduje nadmierną podatność na działanie plazminy. Wynikiem nadmiernego zużycia fibrynogenu spada jego poziom we krwi. Leki defibrynujące znalazły zastosowanie głównie w leczeniu chorych z małopłytkowością poheparynową (1).
Leczenie przeciwzakrzepowe
Przyjęte są dwie metody rozpoczynania leczenia przeciwzakrzepowego za pomocą doustnych antykoagulantów. Jedna polega na podawaniu umiarkowanych dawek leku, aż do uzyskania wartości terapeutycznych, a następnie ustala się dawkę podtrzymującą. Druga metoda polega na podaniu uderzeniowej dawki nasycającej a następnie ustaleniu dawki podtrzymującej. W obu przypadkach dawka podtrzymująca leku ustalana jest w oparciu o wartość czasu protrombinowego wyrażonego współczynnikiem INR. Należy dobrać taką dawkę leku, aby INR utrzymać w przedziale wartości terapeutycznych (2-2,5).
Wskazaniem do leczenia doustnymi antykoagulantami są stany zakrzepowo-zatorowe oraz długotrwała profilaktyka przeciwzakrzepowo-zatorowa u osób z grupy zwiększonego ryzyka.
Istnieje wiele doustnych antykoagulantów. Do tej grupy leków należą pochodne hydroksykumaryny (Acenokumarol, Warfaryna) oraz pochodne indandionu (Femindion, Anisyndion, Difenadion).
Leki przeciwzakrzepowe znajdują zastosowanie w leczeniu wielu chorób serca i naczyń. Są jednymi z podstawowych leków o udokumentowanej skuteczności, stosowanych zarówno w leczeniu jak i wtórnej prewencji migotania przedsionków. Istnieje cała lista patologii, do których leczenia wykorzystuje się preparaty przeciwzakrzepowe, których zasadność stosowania poddawana jest obecnie ocenie zgodnej z zasadami medycyny opartej na faktach. Należałoby tu wspomnieć o wszelkich postaciach zaburzeń rytmu serca, zawale mięśnia serca i jego profilaktyce, przewlekłej chorobie żylnej, powikłaniach naczyniowych cukrzycy (zarówno mikroangiopatii jak i makroangiopatii cukrzycowej), zespole hemolityczno-mocznicowym, zespole rozsianego wykrzepiania wewnątrznaczyniowego oraz urazach wielonarządowych. Leki przeciwzakrzepowe znalazły również szerokie zastosowanie w prowadzeniu pacjentów poddawanych innym formom terapii, kiedy istnieje zagrożenie zwiększonego wykrzepiania. Do tej grupy wskazań należą: krążenie pozaustrojowe, dializoterapia oraz okres okołooperacyjny zwłaszcza w chirurgii sercowo-naczyniowej, przeszczepianiu narządów, czy zabiegach ginekologiczno-położniczych (1, 3, 5).
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
29 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
69 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
129 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 78 zł
Piśmiennictwo
1. Kostowski W., Herman Z.: Farmakologia – podstawy farmakoterapii. wyd. III; 2005; rozdz.38, 573-618. 2.Cantini F., et al.: Effects of short-term, high dose, heparin therapy on biochemical markers of bone metabolism. Clin. Rheumatol. 1995 Nov. 14, 6, 663-666. 3.Herold G.: Medycyna wewnętrzna, wyd. II poprawione: 219-229, 229-244, 266-269. 4. Murata M., et al.: Osteocalcin, deoxypyridinoline and interleukin-1beta in peri-implant crevicular fluid of patients with peri-implantitis. Clin. Oral. Implants. Res. 2002 Dec., 13, 6, 637-643. 5.Pastoureau P., et al.: Osteopenia and bone-remodeling abnormalities in warfarin-treated lambs. J. Bone Miner. Res., 1993 Dec., 8, 12, 1417-1426. 6.Price P.A., et al.: Excessive mineralization with growth plate closure in rats on chronic warfarin treatment. Proc. Natl. Acad. Sci. USA 1982 Dec., 79, 24, 7734-7738. 7.Buschbacher R., et al.: Warfarin in prevention of heterotopic ossification. Am. J. Phys. Med. Rehabil., 1992 Apr., 71, 2, 86-91. 8.Fiore C.E., et al.: Reduced axial bone mineral content in patients taking an oral anticoagulant. South Med. J., 1990 May, 83, 5, 538-542. 9. Knapen M.H., et al.: Effect of oral anticoagulant treatment on markers for calcium and bone metabolism. Haemostasis 2000, Nov-Dec., 30, 6, 290-297. 10.Lafforgue P., et al.: Bone mineral density in patients given oral vitamin K antagonists. Rev. Rhum. Engl. Ed., 1997 Apr., 64, 4, 249-254. 11.Obrant K.J., et al.: The proportion of carboxylated to total or intact osteocalcin in serum discriminates warfarin-treated patients from control subjects. J. Bone Miner. Res., 1999 Apr., 14, 4, 555-560. 12.Pineo G.F., Hull R.D.: Adverse effects of coumarin anticoagulants. Drug. Saf., 1993 Oct., 9, 4, 263-271. 13.Resch H., et al.: Decreased peripheral bone mineral content in patients under anticoagulant therapy with phenprocoumon. Eur. Heart J., 1991 Mar., 12, 3, 439-441. 14.Van Haarlem L.J., et al.: Circulating osteocalcin during oral anticoagulant therapy. Thromb. Haemost., 1988 Aug. 30, 60, 1, 79-82. 15.Marks S.C., et al.: Administration of Colony Stimulating Factor-1 Corrects Some Macrophage, Dental and Skeletal Defects in an Osteopetrotic Mutation (Toothless, tl) in the Rat. Bone, 1992, 13, 89-93. 16.Menon R.K., et al.: Impaired carboxylation of osteocalcin in warfarin-treated patients. J. Clin. Endocrinol. Metab., 1987 Jan, 64, 1, 59-61. 17.Nishiyama M., et al.: Low-molecular-weight heparin (dalteparin) demonstrated a weaker effect on rat bone metabolism compared with heparin. Jpn. J. Pharmacol., 1997 May, 74, 1, 59-68. 18.Shibutani T., et al.: Bisphosphonate inhibits alveolar bone resorption in experimentally-induced peri-implantitis in dogs. Clin. Oral. Implants. Res., 2001 Apr., 12, 2, 109-114. 19.Bronckers A.L., et al.: Studies of osteocalcin function in dentin formation in rodent teeth. Eur. J. Oral. Sci., 1998 Jun, 106, 3, 795-807. 20.Wojtowicz A.: Badania nad osteoporoza szczurów, jej patogeneza i możliwościami leczenia. Praca habilitacyjna z Zakładu Transplantologii Instytutu Biostruktury Akademii Medycznej w Warszawie. Warszawa czerwiec 1995. 21.Wojtowicz A., et al.: Alteration of Mineral Crystallinity and Collage Cross-Linking of Bones in Osteoporotic Toothless (tl/tl) Rats and Their Improwement After Treatment with Colony. Stimulating Factor-1. Bone Vol. 20, No. 2. February 1997, 127-132.

