© Borgis - Postępy Fitoterapii 2/2008, s. 81-89
*Katarzyna Karłowicz-Bodalska1, Tomasz Han2
Uncaria tomentosa (Willd.) DC (vilcacora) – chemizm i właściwości biologiczne
UNCARIA TOMENTOSA (WILLD) DC
1Hasco-Lek S.A. we Wrocławiu
Prezes Hasco-Lek: dr n. biol. Stanisław Han
2Student Wydziału Farmaceutycznego Akademii Medycznej im. Piastów Śląskich we Wrocławiu
Summary
Presented literature data informs mainly about in vivo and in vitro biological studies of water extracts of Peruvian species of Uncaria (U. tomentosa and U. gujanensis), which have been regarded by local people as a marvelous medicine for years.
Although both plants don´t show toxic action and their antioxidant, anti-inflammatory and immunostimulant action is often stressed, clinical studies of raw material appear relatively rarely in the literature. It is probably caused by two reasons: first – controversial reports of oxyindol alkaloids role as active substances and second – occurrence of two chemical types of species U. tomentosa (with different chemical composition and biological activity too) which makes obtaining the proper raw material difficult.
It seems that continuing of biological and chemical research of chinic acid esters, procyanidin and triterpen acids glycosidesters as potential active substances will cause larger interest of raw material, lead to positive finish and will deliver a new safe and efficient anti-inflammatory plant medicine practically without side effects.

Rodzaj Uncaria (Schreber) rodz. Rubiaceae obejmuje 34 gatunki rozpowszechnione w tropikalnych lasach południowo-wschodnej Azji, Afryki i Ameryki Południowej. Kora gałęzi i korzeni oraz liście dwóch gatunków: Uncaria tomentosa (Willd. ex Roemer & Schultes) DC i Uncaria gujanensis (Aubl.) Gmel., znane pod wspólną nazwą cat´s claw, są wykorzystywane od 2000 lat w tradycyjnej medycynie Amazonii do leczenia wielu schorzeń, w tym przewlekłych stanów zapalnych, dysfunkcji żołądkowo-jelitowych, (wrzody, zakażenia, guzy nowotworowe), reumatyzmu, astmy, marskości wątroby, cukrzycy i in., aktualnie również jako surowiec do produkcji fitoterapeutyków (1-5). W obu roślinach opisano występowanie wielu farmakologicznie czynnych związków pochodzących z różnych grup chemicznych (1, 2, 5-8). Najwięcej uwagi poświęcono frakcji alkaloidowej, głównie charakterystycznym penta- i tetracyklicznym alkaloidom oksyindolowym. Związki te przez długi czas uważano za substancje czynne, warunkujące działanie przeciwutleniające i immunostymulujące wyciągów wodnych obu omawianych gatunków.
Gattuso i wsp. (9) przeprowadzili badanie cech morfologicznych i anatomicznych kory pędów nadziemnych i liści U. tomentosa (UT) i U. gujanensis (UG) w celu ułatwienia identyfikacji i standardyzacji oraz kontroli jakości otrzymywanych z nich surowców. Keplinger i wsp. (2) opublikowali w roku 1999 przegląd przeprowadzonych badań botanicznych, farmakologicznych oraz toksykologicznych UT. Wszechstronny przegląd badań z zakresu fitochemii (ze szczególnym uwzględnieniem alkaloidów i pentacyklicznych triterpenów typu ursanu i oleananu), farmakologii, w tym działania przeciwzapalnego, immunotropowego i przeciwutleniającego, oraz zastosowania w medycynie tradycyjnej i oficynalnej wybranych gatunków rodzaju Uncaria, opublikowała ostatnio Heitzmann i wsp. (1).
Uncaria tomentosa (Willd.) DC – ( cat´s claw, vilcacora, nazwa lokalna uńa de gato) jest drzewiastym pnączem, dorastającym niekiedy do wysokości 30 m, występującym rodzimie w tropikalnych lasach Amazonki, głównie w Peru.
Wyciągi sporządzane z kory pni lub kory korzeni UT są aktualnie powszechnie stosowane w Peru oraz w ponad 30 innych krajach w postaci odwarów, tabletek lub kapsułek do leczenia wielu schorzeń, głównie o podłożu zapalnym ( arthritis, osteoarthritis, gastritis), a także jako środek wspomagający i ochronny w chemioterapii i ogólnie wzmacniający ( tonicum). W USA ponad 50 handlowych suplementów diety zawiera przetwory z vilcacory, której przypisuje się wielostronne działanie terapeutyczne.
Laus i wsp. (10) i (Keplinger i wsp. (2) wykryli występowanie dwóch chemotypów UT, różniących się składem frakcji alkaloidowej i działaniem biologicznym. Pierwszy z nich charakteryzuje się obecnością pentacyklicznych, drugi tetracyklicznych alkaloidów oksyindolowych oraz ich prekursorów indolowych, zlokalizowanych w różnych częściach rośliny. Autorzy szczegółowo zanalizowali 16 roślin (w tym 13 zebranych ze stanu dzikiego z różnych rejonów Peru), w których wykryli obecność 17 alkaloidów. Zaobserwowali przy tym, że UT nie wytwarza stałego, jednolitego składu alkaloidów, dlatego zdaniem autorów, przypisywanie generalnie tej roślinie określonych właściwości farmakologicznych nie jest wskazane. W zależności od obecności tetracyklicznych lub pentacyklicznych alkaloidów otrzymywane z surowca wyciągi wykazują różną aktywność. Autorzy stwierdzili również, że zawartość poszczególnych alkaloidów w roślinie zmienia się w okresie wegetacji w zależności od pory roku. Zawartość unkaryny F4 w młodych liściach jest wysoka wiosną i latem; obniża się jesienią. Odnotowano także szczególny przypadek – bardzo wysoką zawartość dwóch związków: mitrafiliny i izomitrafiliny w korzeniach i liściach tylko jednego egzemplarza rośliny, podczas gdy w pozostałych roślinach związki te występowały w śladowych ilościach.
Przedstawione (ryc. 1) pentacykliczne alkaloidy oksyindolowe (sześć związków, w wyjątkowych przypadkach liczba ta zwiększa się o dalsze dwa tetracykliczne alkaloidy oksyindolowe) są głównymi składnikami frakcji alkaloidowej kory korzeni UT. Autorzy zwracają uwagę na konieczność uwzględniania przy standaryzacji wyciągów z surowca faktu, że U. tomentosa występuje w dwóch chemotypach różniących się składem chemicznym i właściwościami biologicznymi.

Ryc. 1. Alkaloidy Uncaria tomentosa (wg. 11).
W roślinie stwierdzono ponadto obecność triterpenów (ryc. 2 – kwasy: oleanolowy, ursolowy, chinowowy), steroidów – badania frakcji steroidowej ujawniły obecność β-sitosterolu (ryc. 3) (jako głównego składnika, któremu przypisuje się udział w działaniu przeciwzapalnym surowca), kampesterolu i śladowych ilości cholesterolu (12), katechin – katechina, epikatechina (ryc. 4), gallokatechina i epigallokatechina, procyjanidyn – cynchoneina 1a i cynchoneina 1b (ryc. 5), glikozydów kwasu chinowowego o właściwościach przeciwwirusowych i przeciwzapalnych oraz innych związków (6, 13, 14). Działanie przeciwwirusowe wobec vesicular stomatitis virus stwierdzono w odniesieniu do 6 glikozydów kwasu chinowowego (13).
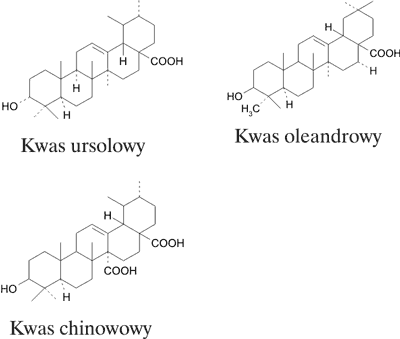
Ryc. 2. Kwasy triterpenowe Uncaria tomentosa.
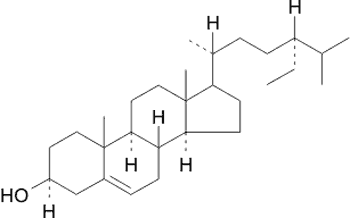
Ryc. 3. β-Sitosterol – podstawowy składnik frakcji steroidowej Uncaria tomentosa.
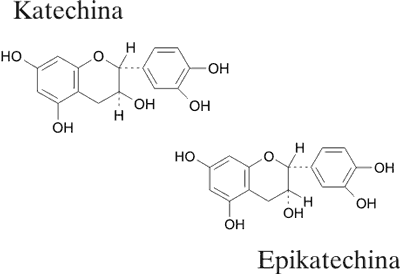
Ryc. 4. Katechiny Uncaria tomentosa.
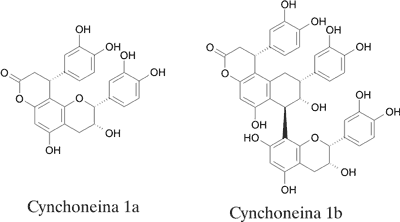
Ryc. 5. Procyjanidyny U. tomentosa.
Według Heitzmann i wsp. (1) U. tomentosa jest najczęściej badanym gatunkiem, z którego wydzielono i zidentyfikowano ok. 50 różnych związków.
W ostatnich latach zaobserwowano, że ekstrakty z vilcacory, zawierające nieznaczne ilości alkaloidów, stale wykazują silne działanie farmakologiczne (15, 16). Poszukiwanie substancji odpowiedzialnej za to działanie doprowadziło do wydzielenia z wyciągu wodnego estrów kwasu chinowego (ryc. 6), jako grupy związków warunkujących właściwości lecznicze surowca (16).
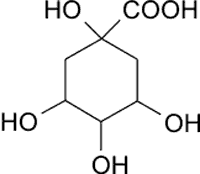
Ryc. 6. Kwas chinowy.
Właściwości biologiczne U. tomentosa i U. gujanensis
Badania podstawowe (in vitro i in vivo)
Zróżnicowany skład chemiczny vilcacory (alkaloidy oksyindolowe, triterpeny, sterole, procyjanidyny, glikozydy pochodne kwasu chinowowego) warunkuje szerokie spektrum właściwości biologicznych tej rośliny. W badaniach in vitro i in vivo stwierdzono m.in. działanie przeciwzapalne, przeciwutleniające, przeciwwirusowe, immunostymulujące, przeciwnowotworowe i przeciwbólowe otrzymywanych z niej wyciągów (17-22).
Działanie przeciwzapalne vilcacory przypisuje się, poza obecnym w korze komponentom sterolowym (β-sitosterol, stigmasterol, kampesterol), również glikozydom kwasu chinowowego i procyjanidynom. Badania w tym kierunku prowadzili Senatore i wsp. (12) oraz Wirth i Wagner (23). Nie określono jednak konkretnego związku lub grupy związków odpowiedzialnych za właściwości przeciwzapalne przetworów z surowca. Reinhard (24) wnioskuje, że aktywność przeciwzapalna UT może być wynikiem synergistycznego działania licznych metabolitów wtórnych.
W badaniach in vitro stwierdzono, że niektóre wydzielone z UT pentacykliczne alkaloidy oksyindolowe (pteropodyna, izopteropodyna, mitrafilina, izomitrafilina) wykazują zdolność podwyższania fagocytozy. Wymienione związki indukują proliferację limfocytów z ludzkich komórek śródbłonka. Alkaloidy tetracykliczne nie wykazują tych właściwości, wręcz przeciwnie, działają antagonistycznie, zależnie od dawki (2, 8, 25).
Badania farmakologiczne nie wykazały działania mutagennego wyciągów wodnych z UT w teście Amesa; przeciwnie, w fotomutagenezie indukowanej 8-metoksypsoralenem w szczepach Salmonella odnotowano efekt antymutagenny tych wyciągów (26). W dalszych badaniach z zastosowaniem różnych biotestów in vitro nie zaobserwowano działania toksycznego wyciągów wodnych z UT (27).
Wyciąg z kory korzeni vilcacory podawany szczurom w wodzie pitnej, zapobiegał indukowanej indometacyną destrukcji śluzówki jelita czczego zwierząt. Stwierdzono, że poziom metalotionein (MT) – (niskocząsteczkowych białek bogatych w reszty cysteinowe) – w wątrobie zwierząt otrzymujących indometacynę z dodatkiem ekstraktu z vilcacory był znacząco niższy od poziomu MT u szczurów otrzymujących tylko indometacynę (28). Podobny efekt odnotowano u szczurów w enteropatii (29). Zwierzęta otrzymujące indometacynę łącznie z ekstraktem z vilcacory wykazywały zredukowany poziom MT w porównaniu z kontrolą, którą stanowiła grupa zwierząt leczonych tylko indometacyną, bez ekstraktu z vilcacory (29).
Wyciągi wodne odpowiadające 2 g wysuszonego surowca wykazywały działanie przeciwzapalne w teście karageninowym (1).
Duże zainteresowanie rośliną wzbudziło wykazanie jej silnego działania immunostymulującego. Według Wagnera (cyt. za 11) ekstrakt z UT okazał się jednym z najsilniej działających immunostymulująco (spośród badanych przez autora) ekstraktów roślinnych.
Lemaire i wsp. (11) wykazali w eksperymentach na szczurach, że ekstrakty z kory pni i gałęzi UT stymulują w zależności od dawki (w zakresie od 0,025 do 0,1 mg/ml) makrofagi do wytwarzania interleukiny-1 (IL-1) i interleukiny-6 (IL-6), znanych inicjatorów kaskady immunologicznych mechanizmów obronnych organizmu. Badane wyciągi podwyższały również produkcję interleukin IL-1 i IL-2 w makrofagach indukowanych lipopolisacharydami. W dwóch próbkach surowca, pochodzącego z dwóch różnych siedlisk vilcacory w Peru, autorzy stwierdzili (HPLC) obecność 6 charakterystycznych alkaloidów oksyindolowych (ryc. 1). Przeprowadzone przez Lemaire i wsp. (11) badania potwierdziły silne działanie immunostymulujące przetworów z U. tomentosa na makrofagi.
Według Rizzi i wsp. (26) znaczące działanie antymutagenne vilcacory jest prawdopodobnie związane z jej właściwościami przeciwutleniającymi.
Sandoval i wsp. (15) przeprowadzili badanie właściwości przeciwutleniających i przeciwzapalnych obu gatunków ( U. tomentosa i U. gujanensis), stosowanych równorzędnie w tradycyjnym lecznictwie Ameryki Południowej. Autorzy podkreślają brak badań naukowych dotyczących porównania skuteczności działania między UT i UG w tym zakresie. Do tej pory, na podstawie eksperymentów in vitro, uznawano powszechnie, że substancjami stymulującymi fagocytozę, wykazującymi zdolność indukowania czynnika regulującego proliferację limfocytów w komórkach śródbłonka, są obecne w przetworach z vilcacory alkaloidy oksyindolowe, i z tego względu korze korzeni UT przypisywano główne znaczenie jako surowcowi o znacznie wyższej zawartości tych związków, niż korze UG.
W sprzeczności z tymi danymi pozostaje fakt, że gatunek UG jest stosowany równorzędnie lub zamiennie z UT w tradycyjnej medycynie Ameryki Południowej z dobrym skutkiem do leczenia arthritis oraz innych schorzeń o podłożu zapalnym, mimo, że zawartość sumy alkaloidów w UG jest 35 razy mniejsza od zawartości tych związków w UT. Podobnie, zawartość flawanoli (w obu gatunkach stwierdzono obecność czterech głównych związków: katechiny, epikatechiny, gallokatechiny i epigallokatechiny) jest w UT (poza epigallokatechiną) znacznie wyższa od ich zawartości w UG. Autorzy podają, że jest to pierwsze zasygnalizowane w piśmiennictwie oznaczenie różnicy w zawartości flawanoli między dwoma omawianymi gatunkami.
Przeprowadzone przez autorów eksperymenty wykazały, że Uncaria gujanensis, mimo znacznie niższej zawartości alkaloidów, proantocyjanidyn i katechin, charakteryzuje się silniejszymi właściwościami „zmiatania” rodnika DPPH oraz rodnika ABTS (kwas 2,2´-azynobis-(-3-etylobenzo-tiazolino-6-sulfonowy)) niż Uncaria tomentosa (odpowiednio 12,6 wobec 20,8 ?g/ml oraz 4,8 wobec 7,7 ?g/ml).
Opisane badania wykazały, że oba gatunki (UT i UG) charakteryzują się silnymi właściwościami przeciwutleniającymi, jak również zdolnością obniżania produkcji czynnika TNF-α, jak również, że UG ma silniejsze właściwości przeciwutleniające niż UT.
Potwierdzeniem powyższych wyników są przeprowadzone przez Piscoya i wsp. (7) opisane poniżej badania kliniczne.
Ostatnio Hardin (30) przeprowadziła badanie mechanizmu działania vilcacory, jako potencjalnego środka przeciwzapalnego, wspomagającego leczenie stanów zapalnych kości i stawów ( osteoarthritis). Destrukcja chrząstki stawowej następuje m.in. w wyniku uwolnienia cytokin, np. interleukiny-1, która jest katalizatorem wytwarzania destruktywnej proteazy, enzymu hamującego syntezę proteoglikanu chrząstki stawowej. Poza IL-1 działają w tym schorzeniu interleukiny IL-17 i IL-18, które również wspomagają uwalnianie destruktywnych proteaz oraz indukują syntezę tlenku azotu (NO). Tlenek azotu jest gazowym mediatorem patologii chrząstki, stymulowanej przez IL-1, TNF-α i IL-17. Jest także włączany w proces hamowania syntezy proteoglikanu, a tym samym w postępującą destrukcję chrząstki.
Autorka wykazała, że vilcacora hamuje ekspresję genu iNOS ( inducible nitric oxide synthase) indukowanego przez lipopolisacharydy, obniża wytwarzanie NO i prostaglandyny PGE2 oraz hamuje aktywację NF-κB i TNF-α. W dalszych badaniach stwierdziła, że podobne działanie wykazuje U. gujanensis. Oba gatunki obniżają regulację genu ekspresji iNOS, działają jak „zmiatacze” wolnych rodników, redukują uwalnianie TNF-α i apoptozę komórek oraz działają cytoprotekcyjnie jako przeciwutleniacze. Działanie przeciwutleniające przetworów z U. tomentosa (hamowanie produkcji TNF-α oraz wygaszanie wolnych rodników) wykazali ponadto Sandoval i wsp. (19) w teście z DPPH, Akesson i wsp. (31), Mammone i wsp. (32), Cisneros i wsp. (33).
Jürgensen i wsp. (18) badali na zwierzętach (myszy) aktywność antynocyceptywną (zmniejszenie wrażliwości na ból wywołany różnymi bodźcami urazowymi) przemysłowej, standardyzowanej frakcji U. tomentosa (UT fraction), zawierającej 95% alkaloidów oksyindolowych. Jako główne składniki zespołu alkaloidów autorzy zidentyfikowali 8 związków: specjofilinę, unkarynę F, mitrafilinę, izomitrafilinę, pteropodynę, izopteropodynę, ryncholinę i izoryncholinę (HPLC). Badania antynocyceptywności autorzy prowadzili znanymi metodami na modelu chemicznym (testy: brzuszny, formalinowy i kapsaicynowy) oraz na modelu termicznym (test ogonowy i gorącej płyty). Frakcja UT, podawana dootrzewnowo, obniżała odpowiedź zwierząt na bodźce chemiczne we wszystkich testach i podwyższała okres utajenia bólu pod wpływem bodźca termalnego. W cytowanej pracy zamieszczono wyczerpujący opis stosowanych metod wraz z dyskusją i wyjaśnieniem mechanizmów działania antynocyceptywnego frakcji alkaloidowej UT w badaniach na myszach. Autorzy podkreślają ważność przeprowadzonych eksperymentów. Do tej pory nie opisano korelacji pomiędzy alkaloidami UT i ich aktywnością antynocyceptywną.
Sheng i wsp. (16) również zwrócili uwagę na fakt, że wodne wyciągi z U. tomentosa, jednakowo skuteczne farmakologicznie, zawierają zróżnicowane ilości alkaloidów (niekiedy <0,05%), poddając tym samym w wątpliwość uznanie frakcji alkaloidowej za główną substancję czynną surowca. W celu określenia substancji warunkującej opisane wyżej właściwości biologiczne U. tomentosa autorzy przeprowadzili analizę dwóch handlowych form wyciągu wodnego z kory tej rośliny (C-Med.-100 i Activar AC-11). Wymienione produkty wykazują działanie immunologiczne i są zamieszczone w wykazie Federal Trade Commission. Z obu preparatów autorzy wyizolowali (TLC) i scharakteryzowali chemicznie substancje aktywne, jako estry kwasu chinowego. Substancje te hamowały wzrost komórek (bez uszkadzania ich struktury), umożliwiając w ten sposób rekonstrukcję DNA; wykazywały działanie immunostymulujące, przeciwzapalne i przeciwnowotworowe. Autorzy wyrażają przekonanie, że pochodne kwasu chinowego i wolny kwas chinowy, wykazujące ten sam rodzaj działania i odpowiedzi biologicznej, który warunkuje skuteczność kliniczną, są głównymi aktywnymi składnikami wodnych ekstraktów U. tomentosa.
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
24 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
59 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
119 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 28 zł
Piśmiennictwo
1. Heitzmann ME, Neto CC, Winiarz E et al. Ethnobotany, phytochemistry and pharmacology of Uncaria ( Rubiaceae); Phytochem 2005 66:5-29. 2. Keplinger K, Laus G, Wurm M i wsp. Uncaria tomentosa (Willd.) DC. – Ethnomedicinal use and new pharmacological, toxicological and botanical results. J Ethnopharmacol 1999; 64:23-34. 3. Obregon LE: Cat´s claw, Uncaria genus. Botanical, chemical and pharmacological studies of Uncaria tomentosa (Willd.) DC ( Rubiaceae) and Uncaria gujanensis (Aubl.) Gmel. Lima, Peru: Instituto de Fitoterapia Americano; 1995. 4. Pilarski R, Zieliński H, Ciesiołka D, Gulewicz K: Antioxidant activity of ethanolic and aqueous extracts of Uncaria tomentosa (Willd.) DC; J Ethnopharmacol 2006; 104:18-23. 5. Steinberg PN: Cat´s claw; an herb from the Peruvian Amazon. Sidahora 1995; 35-6. 6. Cerri R, Aquino R, De Simone F, Pizza C: New quinonic acid glycoside from Uncaria tomentosa. J Nat Prod 1988 51(2):257-61. 7. Piscoya J, Rodriguez Z, Bustamante SA et al. Efficacy and safety of freeze-dried cat´s claw in osteoarthritis of the knee: mechanisms of action of the species Uncaria gujanensis. Inflammation Res 2001; 50:442-48. 8. Wagner H, Kreutzkamp B, Jurcic K. Alkaloids of Uncaria tomentosa and their fagocytosis enhancement activity. Planta Med 1985; 51:419-23. 9. Gattuso M, Di Sapio O, Gattuso S, Pereyra EL: Morphoanatomical studies of Uncaria tomentosa and Uncaria gujanensis bark and leaves. Phytomed 2004; 11:213-23. 10. Laus G, Brőssner D, Keplinger K. Alkaloids of Peruvian Uncaria tomentosa. Phytochem 1997; 45:855-60. 11. Lemaire I, Assineve V. Cano P et al. Stimulation of interleukin-1 and –6 production in alveolar macrophages by the neotropical liana, Uncaria tomentosa (Una de Gato); J Ethnopharmacol 1999; 64:109-15. 12. Senatore A, Cataldo A, Jaccarino FP. Phytochemical and biological study of Uncaria tomentosa Bolletino della Societa Italiana di Biologia Sperimentale 1989; 65:517-20. 13. Aquino R, De Feo V, De Simone F et al. New compounds and antiinflammatory activity of Uncaria tomentosa. J Nat Prod 1991; 54:453-9. 14. Aquino R, De Tommasi N, De Simone F, Pizza C: Triterpenes and quinonic acid glycosides from Uncaria tomentosa; Phyochem 1997; 45(5):1035-40. 15. Sandoval M, Okuhama NN, Zhang XJ i wsp. Anti-inflammatory and antioxidant activities of cat´s claw ( Uncaria tomentosa and Uncaria gujanensis) are independent of their alkaloid content. Phytomed 2002; 9:325-37. 16. Sheng Y, Akesson C, Holmgren K et al. An active ingredient of cat´s claw water extracts. Identification and efficacy of quinic acid. J Ethnopharmacol 2005; 96:577-84. 17. Desmarchelier C, Mongelli E, Coussio J, Ciccia G: Evaluation of the in vitro antioxidant activity in extracts of Uncaria tomentosa (Willd.) DC; Phytother Res 1997; 11:254-6. 18. Jürgensen S, Dalbó S, Angers P et al. Involvement of 5-HT2 receptors in the antinociceptive effect of Uncaria tomentosa; Pharmacol, Biochem and Behavior 2005; 81:466-77. 19. Sandoval M, Charbonnet RM, Okuhama NN i wsp. Cat´s claw inhibits TNF-alpha production and scavenges free radicals: role in cytoprotection. Free Rad Biol Med 2000; 29:7178. 20. Sheng Y, Pero RW, Amiri A i wsp. Induction of apoptosis and inhibition of proliferation in human tumor cells treated with extracts of Uncaria tomentosa; Anticancer Res 1998 18(5A):3363-8. 21. Sroka Z, Fecka I, Cisowski W, Łuczkiewicz M: Investigation into the anti-radical activity of extracts obtained from Uncaria tomentosa (Willd.) DC; Herba Pol 2001; 47:218-23. 22. Riva L, Coradini D, Di Fronzo G et al. The antiproliferative effects of Uncaria tomentosa extracts and fractions on the growth of breast cancer cell line; Anticancer Res 2001; 21:2457-62. 23. Wirth C, Wagner H. Pharmacologically active procyanidins from the bark of Uncaria tomentosa; Phytomed 1997; 4(3):265-6. 24. Reinhard KH: Uncaria tomentosa (Willd.)DC: cat´s claw una de gato, or saventaro. J Altern Compl Med 1999 5:143-51. 25. Wurm M, Kacani L, Laus G, et al. Pentacyclic oxindole alkaloids from Uncaria tomentosa induce human endothelial cells to release a lymphocyte proliferation- regulating factor. Planta Med 1998; 64:701-4. 26. Rizzi R, Re F, Bianchi RF et al. Mutagenic and antimutagenic activities of Uncaria tomentosa and its extracts. J Ethnopharmacol 1993; 38:63-77. 27. Santa Maria A, Lopez A, Diaz MM et al. Evaluation of the toxicity of Uncaria tomentosa by bioassays in vitro. J Ethnopharmacol 1997; 57:183-7. 28. Sandoval-Chacon M, Thompson JH, Zhang XJ et al. Antiinflammatory action of cat´s claw: the role of NF-kappaB. Alimentary Pharmacol Therap 1998; 12:1279-89. 29. Sandoval M, Mannick EE, Mishra J et al. Cat´s claw ( Uncaria tomentosa) protects against oxidative stress and indomethacin-induced intestinal inflammation. Gastroenterology 1997; 112 suppl: A 1081. 30. Hardin SR: Cat´s claw: An Amazonian vine decreases inflammation in osteoarthritis; Complement. Ther Clin Practice 2007; 13:25-28. 31. Akesson Ch, Pero RW, Ivars F. C-Med 100, a hot water extract of Uncaria tomentosa, prolongs lymphocyte survival in vivo; Phytomed 2003; 10:23-33. 32. Mammone T, Akesson C, Gan D et al. A water soluble extract from Uncaria tomentosa (cat´s claw) is a potent enhancer of DNA repair in primary organ cultures of human skin; Phytother Res 2006; 20:178-83. 33. Cisneros FJ. Jayo M, Niedziela L. An Uncaria tomentosa (cat´s claw) extract protects mice against ozone-induced lung inflammation. J Ethnopharmacol 2005; 96:355-64. 34. Eberlin S, Dos Santos LMB, Queiroz MLS: Uncaria tomentosa extract increases the number of myeloid progenitor cells in the bone marrow of mice infected with Listeria monocytogenes; Intern Immunopharmacol 2005; 5:1235-46. 35. Allen-Hall L, Cano P, Arnason JT i wsp. Treatment of THP-1 cells with Uncaria tomentosa extracts differentially regulates the expression of IL-1β and TNF-α; J Ethnopharmacol 2007; 109:312-17. 36. Cheng AC, Jian CB, Huang YT. Induction of apoptosis by Uncaria tomentosa through reactive oxygen species production, cytochrome c release, and caspases activation in human leukemia cells. Food Chem Toxicol 2007; 45: 2206-18.






