© Borgis - Postępy Nauk Medycznych 2/2008, s. 83-91
*Małgorzata Gietka-Czernel
Postępy w laboratoryjnej diagnostyce czynności tarczycy
Progress in biochemical diagnosis of thyroid function
Klinika Endokrynologii Centrum Medycznego Kształcenia Podyplomowego w Warszawie
Kierownik Kliniki: prof. CMKP dr hab. med. Wojciech Zgliczyński
Streszczenie
W diagnostyce laboratoryjnej czynności tarczycy posługujemy się współcześnie oceną stężenia tyreotropiny (TSH) i wolnej tyroksyny (fT4), bowiem zmiany stężenia TSH w surowicy są najczulszym wskaźnikiem zaburzeń czynności tarczycy, a fT4 jest głównym produktem metabolicznym gruczołu tarczowego.
Obecnie dostępne metody oznaczania TSH charakteryzują się wysoką czułością ≤ 0,02 mIU/l i brakiem reakcji krzyżowych z hormonami glikoproteinowymi o podobnej budowie, tj.: LH, FSH i hCG. Na stężenie TSH w surowicy, poza stanem czynnościowym tarczycy może wpływać wiele leków, m.in.: dopamina, glikokortykoidy, oktreotyd, fenytoina, amiodaron. Interpetacja wyników TSH jest odmienna u dzieci do 14 r.ż., kobiet ciężarnych i u ludzi będących w ciężkim stanie ogólnym. W związku z dostępnością superczułych metod oznaczania TSH, wykonywanie testu z TRH jest obecnie ograniczone do diagnostyki guza tyreotropinowego przysadki, zespołów oporności na hormony tarczycy i hipotyreozy pochodzenia centralnego. W ocenie stężeń hormonów tarczycy współczesna diagnostyka opiera się na ocenie frakcji wolnej, niezwiązanej z białkami, co pozwala eliminować zakłócenia wynikające z nieprawidłowości w zakresie białek transportujących. Interpretując uzyskiwane wyniki badań należy każdorazowo brać pod uwagę stan kliniczny pacjenta i zażywane leki.
Summary
The thyrotropin (TSH) and free thyroxine (fT4) measurements usually give an appropriate estimation of thyroid function. The TSH- first strategy can miss patients with central hypothyroidism. The introduction of TSH assays with sensitivity ≤ 0,02 mIU/l enables the diagnosis of subclinical thyroid disorders, especially subclinical thyrotoxicosis. Interpretation of TSH results differs in children up to 14 years old, pregnant women and severely ill patients. Several medications, such as dopamine, glucocorticoids, octreotide, amiodaron, phenytoin can influence serum TSH. The sensitive TSH assays eliminated usefulness of TRH-stimulation test in diagnosing thyrotoxicosis. Nowadays TRH-stimulation test is used in diagnosing thyrotropinoma, central hypothyroidism and thyroid hormone resistance syndromes. In evaluation of serum thyroid hormones, free-thyroxine and free-triiodothyronine measurements are preferred because of the potential abnormalities in thyroid hormone-binding proteins. The interpretation of TSH and fT4 results must take into account the patient´s clinical status and medical therapy.

Badania czynności tarczycy
Diagnostyka laboratoryjna czynności tarczycy obejmuje ocenę stężenia TSH i hormonów tarczycy (HT), co wynika z faktu, że gruczoł tarczowy funkcjonuje w systemie ujemnego sprzężenia zwrotnego z podwzgórzem i przysadką (ryc. 1) wydzielającymi czynniki pobudzające: tyreoliberynę (TRH – Thyrotropin Releasing Factor) i tyreotropinę (TSH – Thyroid Stimulating Hormone).

Ryc. 1. Oś podwzgórzowo-przysadkowo-tarczycowa.
W sytuacji prawidłowo funkcjonującej osi podwzgórzowo-przysadkowo-tarczycowej zmiany stężenia TSH w surowicy są najczulszym wskaźnikiem pierwotnych zaburzeń czynności tarczycy: poziom TSH wzrasta w warunkach niedoboru HT, a obniża się w sytuacji nadmiaru HT (1).
Ocena stężenia TSH w surowicy
Używane przed wielu laty metody oznaczeń TSH w surowicy charakteryzowały się niską czułością (1,0 mIU/l) i niską specyficznością: wykrywały prawidłowe i podwyższone stężenia TSH, a więc dobrze służyły rozpoznawaniu niedoczynności tarczycy, natomiast były bezużyteczne w wykrywaniu utajonej nadczynności gruczołu tarczowego. Powodowały również reakcje krzyżowe z innymi hormonami glikoproteinowymi o zbliżonej do TSH budowie, tj. FSH, LH i hCG.
Współcześnie stosowane metody oznaczeń TSH, nieizotopowe, wśród których najpopularniejsza jest immunometryczna (IMA) oraz immunoenzymatyczna (EIA, ELISA), immunofluorometryczna (FIA) i immunochemiluminescencyjna (LIA), odznaczają się wysoką czułością wynoszącą 0,02 mIU/l i poniżej. Dzięki ich zastosowaniu można nie tylko w sposób czuły rozpoznać pierwotną nadczynność tarczycy, ale odróżnić głęboką supresję TSH wynikającą z choroby Gravesa (TSH<0,01 mIU/l) od częściowej supresji związanej z zespołami pozatarczycowymi (TSH 0,01- 0,1 mIU/l) występującymi u chorych hospitalizowanych. Z kolei zastosowanie dwóch przeciwciał monoklonalnych identyfikujących dwa różne epitopy cząsteczki TSH wyeliminowało reakcje krzyżowe z FSH, LH i hCG (2).
Obowiązujący obecnie zakres normy TSH mieści się w przedziale wartości od 0,2-0,4 do 4,0-4,5 mIU/l. W ostatnim czasie wielu autorów kontestuje górny zakres normy TSH, uważając, że powinien być obniżony (2, 3, 4). Amerykańska Narodowa Akademia Biochemii Klinicznej (NACB – National Academy of Clinical Biochemistry) postuluje aby górna norma TSH wynosiła w przyszłości 2,5 mIU/l, powołując się na fakt, że ponad 95% zdrowych ochotników bez osobistych i rodzinnych wywiadów choroby tarczycy, wola, seronegatywnych dla przeciwciał antyperoksydazowych (a-TPO; anti-thyroperoxidase antibodies) i antytyreoglobulinowych (a-Tg; anti - thyroglobulin antibodies) oraz nie zażywających leków, ma stężenie TSH w przedziale wartości 0,4-2,5 mIU/l (5). Wydaje się zatem, że w wielu przypadkach stężenie TSH powyżej 2,5 mIU/l wskazuje na obecność utajonej choroby tarczycy, np. zapalenia typu Hashimoto. Słuszność takiego stanowiska zdają się potwierdzać wyniki badania Whickham (6), w którym prowadzono prospektywną 20-letnią obserwację liczącej 2779 osób dorosłej populacji angielskiej. Wykazano, że wartość TSH powyżej 2,0 mU/L jest związana ze zwiększonym ryzykiem rozwoju niedoczynności tarczycy w ciągu 20 lat.
Z kolei w badaniu HUNT (The Health Study of Nord-Trondelag) prowadzonym w latach 1995-97 na liczącej 94 009 osób populacji norweskiej okręgu Nord-Trondelag (7) wykazano zależność pomiędzy wartością TSH a obecnością a-TPO. Dodatnie stężenie a-TPO stwierdzono u 20% kobiet i u 10% mężczyzn z TSH w przedziale wartości 2,1-4,0 mU/L oraz u 40% kobiet i u 20% mężczyzn z TSH w przedziale wartości 4,1-5,0 mU/L. Jednocześnie w badaniu HUNT wykazano, że w populacji z negatywnymi wywiadami odnośnie chorób tarczycy mediana oraz 2,5 i 97,5 percentyl wartości TSH wynoszą u kobiet odpowiednio 1,8 i 0,49-5,70 mU/L, a u mężczyzn odpowiednio 1,50 i 0,56-4,60 mU/L. Po wykluczeniu z badanej grupy osób z dodatnimi a-TPO (>200 U/L), 97,5 percentyl wartości TSH obniża się u kobiet do 3,60 mU/L, a u mężczyzn do 3,40 mU/L. Opublikowane w 2006 r. australijskie badanie populacyjne (Busselton Study) oparte na materiale 2115 dorosłych i posługujące się czulszymi metodami analitycznymi potwierdziło częste występowanie dodatnich a-TPO w wyższych przedziałach wartości TSH: u 63% badanych z TSH powyżej 4,0 mIU/L vs. u 7,8% badanych z TSH poniżej 4,0 mIU/L (8).
Z kolei ważnym argumentem przeciwko obniżaniu obecnie górnej granicy normy TSH jest dotychczasowy brak badań epidemiologicznych wskazujących na większą chorobowość wynikającą z TSH 3,0-5,0 mIU/l.
Dolny zakres normy TSH jest powszechnie akceptowany i uważa się, że stężenia TSH wynoszące 0,1-0,4 mIU/l mogą oznaczać w części przypadków, zwłaszcza u ludzi starszych z wolem guzowatym, utajoną nadczynność tarczycy i stanowić ryzyko napadowego migotania przedsionków oraz zgonu z przyczyn sercowo-naczyniowych (9, 10). Wynika stąd konieczność prowadzenia diagnostyki w kierunku pierwotnej choroby tarczycy (ultrasonografia, scyntygrafia gruczołu tarczowego, oznaczenie przeciwciał antyperoksydazowych w surowicy).
Mimo wprowadzenia do analityki laboratoryjnej coraz lepszych metod oceniających stężenie TSH w surowicy, nadal istnieją sytuacje kliniczne powodujące ich zawodność.
Swoistość oznaczeń jest ciągle niewystarczająca w przypadkach nieprawidłowej budowy cząsteczki TSH i w konsekwencji jej zmienionej aktywności biologicznej, co zdarza się w chorobach podwzgórza i przysadki.
W przypadku uszkodzenia podwzgórza lub przysadki cząsteczka TSH może być nieprawidłowo glikozylowana (nadmierna ilość reszt sjalowych) i mieć zmniejszoną aktywność tyreotropową. W efekcie rozwija się niedoczynność tarczycy pochodzenia centralnego, mimo prawidłowego lub nieco podwyższonego stężenia TSH w surowicy. Odnotowano, że u 35% chorych z hipotyreozą pochodzenia centralnego stężenie TSH jest obniżone, u 41% prawidłowe, a u 25% podwyższone (11). W dwóch ostatnich przypadkach znajduje zastosowanie test z TRH, który wykazuje niedostateczny lub opóźniony wzrost stężenia TSH w surowicy. Z kolei, według niektórych obserwacji cząsteczka TSH produkowana przez niektóre gruczolaki tyreotropinowe ma zwiększoną aktywność.
Współcześnie używane metody analityczne dają w obu opisanych sytuacjach klinicznych rozbieżność pomiędzy immunoreaktywnością TSH, a jego aktywnością biologiczną.
Kolejnym czynnikiem wpływającym na niemiarodajność oznaczeń TSH jest obecność u ok. 10% badanych przeciwciał heterofilnych interferujących z metodyką niektórych testów analitycznych i powodujących fałszywie zawyżone wyniki. Wśród przeciwciał heterofilnych wyróżnia się dwie klasy: przeciwciała polireaktywne np. czynnik reumatoidalny z klasy IgM oraz przeciwciała powstałe w wyniku infekcji bądź kontaktu z antygenem zwierzęcym. Te ostatnie określane są jako HAMA ( Human Anti-Mouse Antibodies)oraz HAAA ( Human Anti-Animal Antibodies) i są obecne u ludzi poddanych terapii z wykorzystaniem antygenu zwierzęcego oraz zajmujących się prywatnie lub zawodowo zwierzętami (2, 12). Przeciwciała heterofilne mogą zaburzać zarówno oznaczenia TSH jak i HT: ich obecność należy podejrzewać w każdym przypadku uzyskania wyników nieadekwatnych do stanu klinicznego osoby badanej. Rycina 2 ilustruje mechanizm interferowania przeciwciał heterofilnych na metodykę oznaczeń TSH. Obecnie dostępne są preparaty neutralizujące działanie wspomnianych przeciwciał, np. immunoglobulina mysia.
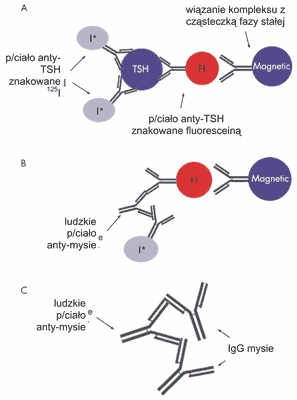
Ryc. 2. Wpływ przeciwciał heterofilnych (HAMA) na oznaczanie stężenia TSH w surowicy metodą chemiluminescencyjną.
Wg Krishnan SGS, Pathalapati R, Kaplan L, Cobbs RK. Postgrad Med J 2006; 82:e27.
A. Prawidłowy przebieg badania: dwa przeciwciała znakowane 125I rozpoznają dwa różne epitopy cząsteczki TSH, która następnie oznaczana jest w polu magnetycznym;
B. Interferencja ludzkich przeciwciał anty-mysich w przebieg badania: ludzkie przeciwciała anty-mysie i znakowane p/ciała użyte do testu tworzą kompleks bez obecności cząsteczki TSH;
C. Sposób zapobiegania interferencji: wiązanie ludzkich przeciwciał anty-mysich przez immunoglobulinę mysią.
Należy zwrócić uwagę na trzy grupy: dzieci, ciężarne i ciężko chorych, u których interpretacja stężenia TSH jest inna niż w pozostałej populacji.
U dzieci zarówno TSH jak i fT4 są wyższe w pierwszym roku życia zwłaszcza w pierwszym tygodniu, a górny zakres normy TSH jest nieco wyższy niż u dorosłych jeszcze do 14 r.ż. (tab. 1).
Tabela 1. Zakres norm TSH i fT4 dla dzieci.
| Wiek | Przedziały referencyjne |
| TSH mIU/L | fT4 pmol/L
(ng/dl) |
| Bezpośrednio po urodzeniu (poród o czasie) | 1,3-19 | 10-22 (0,8-1,9) |
| 3 dni | 1,1-17 | 22-49 (1,8-4,1) |
| 10 tygodni | 0,6-10 | 9-21 (0,8-1,7) |
| 14 miesięcy | 0,4-7,0 | 8-17 (0,6-1,4) |
| 5 lat | 0,4-6,0 | 9-20 (0,8-1,7) |
| 14 lat | 0,4-5,0 | 8-17 (0,6-1,4) |
| dorosły | 0,4-4,0 | 9-22 (0,8-1,8) |
wg Fisher D, Nelson J, Carlton G et al. Thyroid 2000; 10: 229-234.
U ciężarnych, z powodu tyreotropowego wpływu hCG, dolna granica normy TSH obniża się: w I i II trymestrze wynosi według niektórych autorów 0,03 mIU/L, a w III trymestrze – 0,13 mIU/L. Ocenia się, że obniżone stężenie TSH może dotyczyć ok. 20% zdrowych kobiet będących w I trymestrze ciąży. Zaleca się zatem, aby interpretacja obniżonego stężenia TSH u ciężarnej była rozpatrywana w oparciu o stan kliniczny i wyniki oznaczeń wolnych hormonów tarczycy.
Z kolei górna wartość normy dla poszczególnych trymestrów wynosi odpowiednio: 2,3 mIU/l, 3,1 mIU/l oraz 3,5 mIU/l. Stężenie TSH powyżej 3,0 mIU/l w I trymestrze nakazuje oznaczenie a-TPO i obserwację w kierunku ewentualnego rozwoju niedoczynności tarczycy. Leczenie hipotyreozy u ciężarnej powinno zmierzać do utrzymywania stężenia TSH poniżej 2,5 mIU/l w I trymestrze i poniżej 3,0 mIU/l w II i III trymestrze ciąży (13).
Według NACB także pacjenci hospitalizowani wymagają odmiennej interpretacji oznaczeń TSH z powodu wpływu ciężkich chorób ogólnoustrojowych (zespoły pozatarczycowe, synonimy: zespół niskiej T3, zespół niskiej T3 i niskiej T4, sick euthyroid syndrome, nonthyroidal illness) oraz stosowanych leków, zwłaszcza steroidów i dopaminy.
Zespoły pozatarczycowe to fenomen biochemiczny związany z zaburzeniami konwersji obwodowej T4 i wiązania T4 z białkami transportującymi, występujący u ludzi z ciężkimi chorobami ogólnoustrojowymi i w stanach głodzenia. Nie są związane z określonymi jednostkami chorobowymi, ale towarzyszą każdemu złemu stanowi ogólnemu, występują powszechnie u pacjentów oddziałów intensywnej opieki medycznej i często łączą się ze złą prognozą (14, 15, 16).
Istotne znaczenie etiopatogenetyczne w tych zespołach przypisywane jest cytokinom: interleukinie-1(IL-1), interleukinie-2 (IL-2), interferonowi (INF) i czynnikowi martwicy guza (TNF), wydzielanym przez zmienione chorobowo tkanki. Schemat działania cytokin na poziomie CUN i tkanek obwodowych w zespole niskiej T3 i niskiej T4 przedstawia rycina 3.
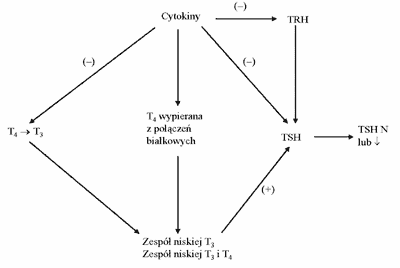
Ryc. 3. Działanie cytokin na poziomie CUN i tkanek obwodowych w zespole niskiej trijodotyroniny i niskiej tyroksyny.
W podsumowaniu należy stwierdzić, że w zespole niskiej trijodotyroniny oraz niskiej trijodotyroniny i niskiej tyroksyny stwierdza się w surowicy następujące zmiany biochemiczne:
1. zespół niskiej trijodotyroniny
– T3 i fT3 obniżone
– T4 i fT4 prawidłowe lub podwyższone
– TSH prawidłowe lub obniżone
– rT3 podwyższone
2. zespół niskiej trijodotyroniny i niskiej tyroksyny
– T3 i fT3 obniżone
– fT4 prawidłowe lub obniżone
– T4 obniżone
– TSH prawidłowe lub obniżone
– rT3 podwyższone
W przypadkach trudności w różnicowaniu zespołu niskiej T3 i niskiej T4 z niedoczynnością tarczycy pochodzenia centralnego należy wykonać badania obrazowe przysadki i podwzgórza (MR, CT) oraz ewentualnie oznaczyć stężenia innych hormonów przedniego płata przysadki i rT3.
Zatem u wielu ciężko chorych przebywających w szpitalach stężenie TSH obniża się do wartości 0,02-0,3 mIU/l wskutek hamującego wpływu cytokin, dopaminy i steroidów na wydzielanie TSH. W okresie zdrowienia natomiast stężenie TSH może wzrosnąć do 20 mIU/l.
Stężenie TSH w przedziale 0,05-10 mIU/l u chorych hospitalizowanych nie musi wskazywać na chorobę gruczołu tarczowego i postuluje się, aby nie wykonywać bez istotnej potrzeby oznaczeń TSH w tej grupie ani nie wdrażać pochopnej terapii.
Wyniki badań przeprowadzonych na bliźniętach i zdrowych ochotnikach wskazują, że stężenie fT4 i fT3 w surowicy jest cechą osobniczą (indywidualny set-point), ulegającym w czasie niewielkim wahaniom wynoszącym ok. 25% (17). Większe zmiany pociągają za sobą wzrost lub zahamowanie wydzielania TSH.
Podwyższone stężenie TSH przy mieszczących się jeszcze w szerokiej normie laboratoryjnej stężeniach HT wskazuje na indywidualny niedobór hormonów tarczycy – utajoną niedoczynność tarczycy. I odwrotnie; obniżone stężenie TSH jest pierwszym sygnałem rozpoczynającej się nadczynności gruczołu tarczowego.
Inne, rzadkie przyczyny podwyższonego stężenia TSH w surowicy są następujące:
– gruczolak przysadki wydzielający TSH ( tyreotropinoma),
– zespoły oporności na hormony tarczycy:
– zespół uogólnionej oporności na HT
– zespół przysadkowej oporności na HT
– zespoły oporności na TSH:
– mutacja zarodkowa genu kodującego receptor TSH
– mutacja zarodkowa genu kodującego podjednostkę β-TSH
– zespoły pozatarczycowe – okres zdrowienia,
– ostre zespoły psychiatryczne,
– pierwotna niedoczynność kory nadnerczy,
– przeciwciała heterofilne,
– leki: tyreostatyki, jod, amiodaron, lit, interferon α (tab. 2).
Tabela 2. Leki wpływające na wzrost stężenia TSH.
l Zwiększenie syntezy TSH
amiodaron
l
Hamowanie syntezy i/lub wydzielania HT*
tyreostatyki - pochodne tiamazolu i tiouracylu
litjod organiczny i nieorganiczny
amiodaron
interferon a
aminoglutetimid
l
Hamowanie konwersji obwodowej T4 do T3
jod organiczny
amiodaron
tyreostatyki - pochodne tiouracylu
l
Przyspieszenie metabolizmu wątrobowego HT*
fenobarbital
fenytoina
karbamazepina
rifampicyna
l
Zwiększenie stężenia TBG**
estrogeny
tamoksyfen
mitotan
5-fluorouracyl
heroina
metadon |
*HT – hormony tarczycy
**TBG – Thyroxine Binding Globulin – globulina wiążąca tyroksynę
Obniżone stężenie TSH, poza najczęstszą sytuacją kliniczną jaką jest pierwotna nadczynność tarczycy, stwierdza się w następujących przypadkach:
– niedoczynność tarczycy pochodzenia centralnego,
– głodzenie,
– zespoły pozatarczycowe,
– podeszły wiek (stulatkowie),
– ostre zespoły psychiatryczne,
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
29 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
69 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
129 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 78 zł
Piśmiennictwo
1. Stockigt JR: Serum Thyrotropin and Thyroid Hormone Measurements and Assessment of Thyroid Hormone Transport. W: Werner and Ingbar´s The Thyroid. Edited by Lippincott- Raven, Philadelphia 1996; 377-393.
2. Baloch Z, et al.: Laboratory medicine practice guidelines. Laboratory support for the diagnosis and monitoring thyroid disease. Thyroid 2003; 13: 3-126.
3. Wartofsky L, Dickey RA: Controversy in Clinical Endocrinology. The evidence for a Narrower Thyrotropin Reference Range Is Compelling. J. Clin. Endocrinol. Metab., 2005; 90: 5483-5488.
4. Dayan CM, et al.: Whose normal thyroid function is better – yours or mine? Lancet 2002; 360: 353-354.
5. Hollowell JG, et al.: Serum TSH, T4, and Thyroid Antibodies in the in the United States Population (1988 to 1994): National Health and Nutrition Examination Survey (NHANES III). J. Clin. Endocrinol. Metab., 2002; 87: 489-499.
6. Vanderpump MPJ, et al.: The incidence of thyroid disorders in the community: a twenty-year follow-up of the Whickham Survey. Clin. Endocrinol., 1995; 43: 55-68.
7. Bjoro T, et al.: Prevalence of thyroid disease, thyroid dysfunction and thyroid peroxidase antibodies in a large, unselected population. The Health Study of Nord-Trondelag (HUNT). Europ. J. Endocrinol., 2000; 143: 639-647.
8. O´Leary PC, et al.: Investigations of thyroid hormones and antibodies based on a community health survey: the Busselton thyroid study. Clin. Endocrinol., 2006; 64: 97-104.
9. Sawin C, et al.: Low serum thyrotropin (thyroid stimulating hormone) in elder persons without hyperthyroidism. Arch. Intern. Med., 1991; 151: 165-8.
10. Parle J, et al.: Prediction of all-cause and cardiovascular mortality in elderly people from one low serum thyrotropin result: a 10-year study. Lancet 2001; 358: 861-5.
11. Faglia G, et al.: Thyrotropin secretion in patients with central hypothyroidism: Evidence for reduced biological activity of immunoreactive thyrotropin. J. Clin. Endocrinol. Metab., 1979; 48: 989-98.
12. Krishnan S, et al.: Falsely raised TSH levels due to human anti-mouse antibody interfering with thyrotropin assay. Postgrad. Med. J. 2006; 82: 27-29.
13. Abalovich M, et al.: Management of Thyroid Dysfunction during Pregnancy and Postpartum: A Endocrine Society Clinical Practice Guideline. J. Clin. Endocrinol. Metab., 2007; 92: S1-S47.
14. Gietka-Czernel M, Jastrzębska H: Rozpoznawanie i leczenie chorób tarczycy. Ośrodek Informacji Naukowej „Polfa”, Warszawa 2002.
15. De Groot LJ.: Dangerous Dogmas in Medicine: The Nonthyroidal Illness Syndrome. J. Clin. Endocrinol. Metab., 1999, 84: 151.
16. Docter R, i wsp.: The sick euthyroid syndrome: changes in thyroid hormone serum parameters and hormone metabolism. Clin. Endocrinol., 1993, 39: 449.
17. Andersen S, et al.: Narrow Individual Variations in Serum T4 and T3 in Normal Subjects: A Clue to the Understanding of Subclinical Thyroid Disease. J. Clin. Endocrinol. Metab., 2002; 87: 1068-1072.
18. Pfannenstiel P, Saller B: Schilddrusenkrankheiten Diagnose und Therapie. Berliner medizinische Verlagsanstaldt GmbH, Berlin 1991.
19. Martino E, et al.: Central hypothyroidism. W: Werner and Ingbar´s: The Thyroid. Edited by Lippincott- Raven, Philadelphia 1996; 779-791.
20. Arbelle J, Porath A: Practice guidelines for the detection and management of thyroid dysfunction. A comparative review of the recomendations. Clin. Endocrinol., 1999, 51: 11-16.
21. Dayan CM: Interpretation of thyroid function tests. The Lancet, 2001, 357: 619-24.
22. Jastrzębska H: Algorytm postępowania w niedoczynności tarczycy. Procedury diagnostyczne i terapeutyczne w niedoczynności tarczycy. W: Standardy Endokrynologii red. Zgliczyński S, Zgliczyński W. Warszawa, StudioPin wyd. II, 2002: 77-79, oraz Endokrynol. Pol., 2003; 54(3): 389-391.
23. Jastrzębska H. Algorytm postępowania w niedoczynności tarczycy. Procedury diagnostyczne i terapeutyczne w niedoczynności tarczycy. W: Standardy Endokrynologii red. Zgliczyński S, Zgliczyński W. Warszawa, StudioPin wyd. II, 2002, oraz Endokrynol. Pol., 2003; 54(3).



