© Borgis - Postępy Fitoterapii 1/2011, s. 48-51
*Anna Nowak
Fitosterole w codziennej diecie
Phytosterols in everyday dietary
Samodzielna Pracownia Farmakoterapii Dermatologicznej, Pomorska Akademia Medyczna w Szczecinie
Kierownik Pracowni: dr hab. n. med. Adam Klimowicz
Summary
Phytosterols are chemical homolog soft cholesterol that are found in vegetable oils and whole grains. The principal forms are β-sitosterol, campesterol and stigmasterol. Phytosterols are hypocholesterolemic agents since a daily intake about of 2 g/day lowers total and LDL cholesterol concentrations by 9-13%. Phytosterols lower the serum total and LDL level and the mechanism of phytosterols action is based on its ability to reduce cholesterol absorption. The absorption of phytosterols is very small and most clinical studies suggest that consumption is safe. However phytosterols in high dose may interfere with the absorption of carotenoids and other fat-soluble vitamins while lowering serum total and LDL level cholesterol concentration. During phytosterols consumption increasing the intake of vegetables and fruits to more than 5 serving per day.

Wstęp
Fitosterole, zwane również sterolami roślinnymi, występują w diecie każdego człowieka. Od wielu lat podkreśla się zdrowotne znaczenie tych substancji, a w szczególności ich korzystny wpływ na obniżanie stężenia cholesterolu frakcji LDL w surowicy krwi. Obecnie wprowadzono na rynek produkty spożywcze, głównie margarynę, o wysokiej zawartości steroli roślinnych. Mała absorpcja fitosteroli powoduje, iż spożywanie ich w dużych ilościach jest bezpieczne i nie wykazuje efektów ubocznych (1). Dlatego też substancje te coraz częściej są spożywane w dużej ilości, często przekraczającej dzienne zapotrzebowanie. Z przeprowadzonych w ostatnich latach badań wynika, że zbyt wysoka dzienna dawka steroli roślinnych obniża w surowicy krwi zawartość cennych składników, tj. karotenów i innych witamin rozpuszczalnych w tłuszczach (2-5). Ponadto Komitet ds. Żywności (SCF) podaje, iż nie istnieją dowody dodatkowych korzyści spożywania fitosteroli powyżej 3 g dziennie, ponieważ może wywołać to niepożądane skutki, tj. obniżenie w surowicy krwi zawartości bardzo ważnych składników pokarmowych rozpuszczalnych w tłuszczach, np. karotenów czy tokoferoli (6). Właściwym postępowaniem byłoby tutaj nieprzekraczanie zalecanej dziennej dawki fitosteroli, jak również odpowiednie komponowanie diety, która mogłaby zwiększyć ich biodostepność, przy jednoczesnym utrzymaniu na stałym poziomie zawartości cennych składników pokarmowych.
Budowa i występowanie fitosteroli
Fitosterole występują naturalnie zarówno w formie wolnej, jak i zestryfikowanej, stanowiąc składniki roślinnych błon komórkowych. Do fitosteroli zaliczmy sterole (związki nienasycone) i stanole (związki nasycone) występujące w produktach spożywczych w mniejszej ilości (7). Fitosterole stanowią chemiczne homologi cholesterolu o innym stopniu nasycenia i innej konfiguracji łańcucha. Podstawowe sterole roślinne, znajdujące się w olejach roślinnych, różnią się budową łańcucha bocznego (ryc. 1).
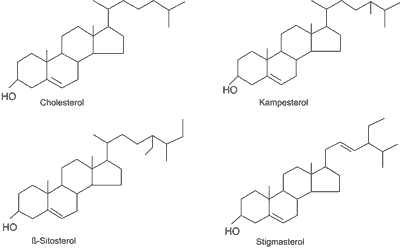
Ryc. 1. Budowa cholesterolu i fitosteroli.
Największe ilości fitosteroli występują w produktach pochodzenia roślinnego, tj. olejach roślinnych oraz niektórych nasionach (8). W królestwie roślin istnieje więcej niż 200 różnych fitosteroli, z czego większa ich część znajduje się w jadalnych produktach spożywczych. W zależności od struktury i biosyntezy, roślinne sterole zostały podzielone na następujące grupy: 4-dimetylosterole, 4α-monometylosterole i 4,4-dimetylosterole. Najczęściej występujące w świecie roślinnym są 4-dimetylosterole, do których należą: stigmasterol, β-sitosterol i kampesterol. W produktach pochodzenia roślinnego najwięcej znajduje się β-sitosterolu, zaś w mniejszych ilościach znajduje się w nich kapmesterol i stigmasterol (tab. 1).
Tabela 1. Zawartość fitosteroli (mg/100 g) w niektórych produktach roślinnych (9-11).
| Produkt |
Fitosterole ogółem |
β-Sitosterol |
Kampesterol |
Stigmasterol |
Olej słonecznikowy
Olej rzepakowy
Olej sojowy
Oliwa z oliwek
Olej sezamowy
Nasiona sezamowe
Orzechy włoskie
Orzechy ziemne | 240-725
480-1130
221-457
98-189
360-473
231-1900
121
153 | 238
378
221
117
367
231
114
47-133 | 31
227
58
5
77
53
5
6-18 | 31
3
67
4
28
22
2
7-10 |
Mechanizm działania fitosteroli
Wieloletnie badania dowodzą, że codzienne spożywanie fitosteroli zapobiega rozwojowi zmian miażdżycowych w naczyniach krwionośnych (12). W codziennej diecie największą część powinien zajmować β-sitosterol (65%), następnie kampesterol (30%) oraz stigmasterol (5%) (13, 14). Dieta bogata w fitosterole obniża zawartość cholesterolu w surowicy krwi, poprzez obniżenie jego stężenia. Redukuje ona również poziom nasyconych kwasów tłuszczowych oraz dodatkowo może regulować obieg cholesterolu. Wielu autorów donosi o zmniejszeniu stężenia cholesterolu frakcji LDL i cholesterolu całkowitego w osoczu krwi o ok. 9-13% (5, 15, 16).
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
29 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
69 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
129 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 78 zł
Piśmiennictwo
1. Ostlund RE, Lin X. Regulation of cholesterol absorption by phytosterols. Nutrition 2006; 8:487-91. 2. Gylling H, Puska P, Vartiainen E i wsp. Retinol, vitamin D, carotenes and α-tocopherol in serum of a moderately hypercholesterolemic population consuming sitostanol ester margarine. Atherosclerosis 1999; 145:279-85. 3. Plat J, Mensink RP. Plant stanol and sterol esters in the control of blood cholesterol levels: mechanism and safety aspects. Am J Cardiol 2005; 96:15D-22D. 4. Hassan AS, Rampone AJ. Intestinal absorption and lymphatic transport of cholesterol and β-sitostanol in the rat. J Lipid Res 1979; 20:646-53. 5. Weststrate JA, Meijer GW. Plant sterol-enriched margarines and reduction of plasma total- and LDL-cholesterol concentrations in normocholesterolaemic and middy hypercholesterolaemic subjects. Eur J Clin Nutr 1998; 52:334-43. 6. Rozporządzenie Komisji (WE) nr 608/2004 z dnia 31 marca 2004 r. Dziennik Urzędowy L 097, 01/04/2004 P. 0044-0045. 7. Law M. Plant sterol and stanol margarines and health. BMJ 2000; 320:861-4. 8. Miettinen TA, Gylling H. Plant stanol and sterol esters in prevention of cardiovascular dieseases. Ann Med 2004; 36:126-34. 9. Piironen V, Lindsay DG, Miettinen TA i wsp. Plant sterols: biosynthesis, biological function and their importance to human nutrition. J Sci Food Agric 2000; 80:939-66. 10. Bradford PG, Awad AB. Phytosterols as anticancer compounds. Mol Nutr Food Res 2007; 51:161-70. 11. Hilali M, Charrouf Z, El Aziz Soulhi A i wsp. Detection of argan oil adulteration using quantitative campesterol GC-analysis. J Amer Oil Chem Soc 2007; 84:761-4. 12. Włodarczyk D. Stanole – znaczenie w leczeniu hipercholesterolemii. Endokr Otyłość 2005; 2:31-4. 13. Ling WH, Jones PJ. Dietary phytosterols: a review of metabolism, benefits and side effects. Life Sci 1995; 57:195-206. 14. Ostlund RE. Phytosterols in human nutrition. Ann Rev Nutr 2002; 22:533-49. 15. Nguyen TT, Dale LC, von Bergman K i wsp. Cholesterol – lowering effect of stanol ester in a US population of mildly hypercholesterolaemic men and women: a randomized controlled trial. Mayo Clin Proc 1999; 74:1198-206. 16. Jenkins DJ, Kendall CW, Nguyen TH i wsp. Effect of plant sterols in combination with other cholesterol-lowering foods. Metabolism 2008; 57:130-9. 17. Bosner MS, Lange LG, Stenson WF i wsp. Percent cholesterol absorption in normal women and men quantified with dual stable isotopic tracers and negative ion mass spectrometry. J Lipid Res 1999; 40:302-8. 18. Heinemann T, Axtmann G, von Bergmann K. Comparison of intestinal absorption of cholesterol with different plant sterols in man. Eur J Clin Invest 1993; 23:827-31. 19. Bosner MS, Ostlund RE, Osofisan O i wsp. Assessment of percent cholesterol absorption in humans with stable isotopes. J Lipid Res 1993; 34:1047-53. 20. Igel M, Giesa U, Lütjohann D i wsp. Comparison of the intestinal uptake of cholesterol, plant sterols, and stanols in mice. J Lipid Res 2003; 44:533-8. 21. Field FJ, Matur SN. β-sitosterol: esterification by intenstinal acylo-enzyme A: cholesterol acylotransferase (ACAT) and its effect on cholesterol esterification. J Lipid Res 1983; 24:409-17. 22. Tavani DM, Nes WR, Billheimer JT. The sterol substrate specificity of acyl CoA:cholesterol acyltransferase from rat liver. J Lipid Res 1982; 23:774-81. 23. Szymańska R, Kruk J. Fitosterole – występowanie i znaczenie dla człowieka. Kosmos Prob Nauk Biol 2007; 1-2:107-14. 24. Katan MB, Grundy SM, Jones P i wsp. Efficacy and safety of plant stanols and sterols in the management of blood cholesterol levels. Mayo Clin Proc 2003; 78:965-78. 25. Gylling H, Radhaknshnam R, Miettinen TA. Reduction of serum cholesterol in postmenopausal women with previous myocardial infarction and cholesterol malabsorption induced by dietary sitostanol ester margarine. Circulation 1997; 96:4226-31. 26. Hallikainen MA, Sarkkinen ES, Uusitupa MI. Effect of low-fat stanol ester enriched margarines on concentrations of serum carotenoids in subject with elevated serum cholesterol concentration. Eur J Clin Nutr 1999; 53:966-9. 27. Borel P, Grolier P, Armand M i wsp. Carotenoids in biological emulsions: solubility, surface-to-core distribution, and release from lipid droplets. J Lipid Res 1996; 37:250-61. 28. Plat J, van Onselen EN, van Heugten MM i wsp. Effects on serum lipids, lipoproteins and fat soluble antioxidant concentrations of comsumption frequency of margarines and shortenings enriched with plant stanol esters. Eur J Clin Nutr 2000; 54:671-7. 29. Hallikainen MA, Sarkkinen ES, Uusitupa MI. Plant stanol esters affect serum cholesterol concentrations of hypercholesterolaemic men and women in dose-dependent manner. J Nutr 2000; 130:767-76. 30. Noakes M, Clifton P, Ntanios F i wsp. An increase in dietary carotenoids when consuming plant sterols or stanols is effective in maintaining plasma carotenoid concentrations. Am J Clin Nutr 2002; 75:79-86. 31. Hick KB, Moreau RA. Phytosterols and phytostanols: Functional food cholesterol busters. Food Technol 2001; 55:63-9. 32. Heinonen M, Valsta L, Anttolainen M i wsp. Comparisons between analyses and calculated food composition data: carotenoids, retinoids, tocopherols, tocotrienols, fat, fatty acid and sterols. J Food Copm Anal 1997; 10:3-13.

