© Borgis - Postępy Nauk Medycznych 2/2015, s. 124-128
*Monika Miazga, Tomasz Jargiełło, Anna Drelich-Zbroja, Klaudia Karska, Krzysztof Pyra, Michał Sojka, Kowalik Marcin, Małgorzata Szczerbo-Trojanowska
Leczenie wewnątrznaczyniowe zwężeń żyły głównej górnej
Endovascular treatment for superior vena cava obstruction
Department of Interventional Radiology and Neuroradiology, Medical University, Lublin
Head of Department: prof. Małgorzata Szczerbo-Trojanowska, MD, PhD
Streszczenie
Wstęp. Rak płuc jest najczęstszą przyczyną zespołu żyły głównej górnej (ZŻGG). Klinicznym wskazaniem łagodzącym objawy niepożądane ZŻGG spowodowanym przez zmianą złośliwą jest leczenie wewnątrznaczyniowe.
Cel pracy. Przedstawienie doświadczeń własnych i ocena skuteczności zabiegów wewnątrznaczyniowych (angioplastyki balonowej i stenotwania) u chorych z zespołem ŻGG.
Materiał i metody. Poddano retrospektywnej analizie grupę 112 chorych z ZŻGG leczonych wewnątrznaczyniowo w latach 2011-2014. Badaniem objęto grupę chorych w wieku od 43 do 79 lat, składającą się z 68 mężczyzn i 44 kobiety (średni wiek chorych – 64 lata). U większości chorych ZŻGG spowodowany był chorobą nowotworową.
Wyniki. Techniczne powodzenie zabiegu zanotowano w 98% przypadków. Po zabiegu u dwóch chorych doszło do nawrotowego zwężenia w stencie, u jednego chorego po zabiegu odnotowano krwioplucie, u dwóch chorych wystąpiła zatorowość płucna. Natomiast nie obserwowano późnych powikłań w postaci migracji stentu do prawego przedsionka serca.
Wnioski. Metody wewnątrznaczyniowego leczenia zwężeń w obrębie ZGG są stosunkowo bezpiecznymi zabiegami dla chorego, szybko powodują ustąpienie objawów klinicznych i poprawiają jakość życia. Powinny być szerzej rozpowszechnione i stosowane u każdego chorego z ZŻGG.
Summary
Introduction. Superior vena cava syndrome (SVCS) is common complication of malignancy, the lung cancer is the most common cause. The clinical indication for superior vena cava (SVC) endovascular treatment is allevation of superior vena cava syndrome (SVCS) caused by malignant obstruction.
Aim. Evaluation of safety and efficacy of SVC stenting in patients with malignant superior vena cava syndrome (SVCS) – our experience.
Material and methods. Between 2011 and 2014, data of 112 patients with SVC syndrome, mostly of malignant aetiology, were retrospectively collected. The study included 68 men and 44 women (mean age – 64; range 43-79 years).
Results. Stent placement was technically successful in 98% cases. Two stents were found to be obstructed after several months and patients needed repeated angioplasty. There was no stent migration to the right atrium. Haemoptysis was observed in one patient and pulmonary embolism in two cases. There were no major remote complications.
Conclusions. Endovascular stenting has become a safe and cost effective treatment for patients with SVCS, providing rapid relief of symptoms and improving their quality of life. Endovascular stenting should be performed in each patient with SVCS.

INTRODUCTION
The superior vena cava (SVC) is a large venous trunk, which receives blood from the supradiaphragmatic body part; it drains blood from the head, neck, upper limbs and thorax. SVC is formed by the union of the left and right brachiocephalic veins and empties into the right atrium (1).
Impaired blood flow through SVC is caused by its stenosis or obstruction and leads to superior vena cava syndrome (SVCS) (1-4).
SVC stenosis or obstruction can develop in patients with bronchial cancer, lung cancer (small cell and non-small cell), lymphoma, Hodgkin’s disease, mediastinal tumours (predominantly thymomas), metastases, pleural cancer/perithelioma. The benign lesions causing SVC stenosis are thrombi within the permanent dialysis catheters or catheters for parenteral nutrition, pacemakers, mediastinal fibrosis (1, 3, 5).
SVCS was first described by William Hunter in 1757 in a patient with syphilitic aortic ulceration, which was the most common cause of SVCS until the mid 50 ties (2, 3).
The typical symptoms of SVCS include swelling of the face, neck and right upper limb, dyspnoea, cough, facial redness, difficult swallowing, hoarseness and thoracic pain. Dilatation of superficial thoracic veins is observed in patients with SVCS developing slowly. The mean survival of patients affected by SVCS is about 6 months (1-3, 6).
Aim
The aim of the study was to evaluate the efficacy of minimally invasive endovascular techniques, i.e. balloon angioplasty and stenting, in the treatment of SVCS.
Material and methods
In the years 2011-2014, 112 patients with symptomatic SVCS underwent balloon angioplasty and stenting of SVC. We want to share our experiences and observations regarding the treatment of SVCS.
SVCS was treated in (fig. 1):
– 23 patients with small cell lung cancer,
– 54 patients with non-small cell lung cancer,
– 18 patients with metastases to mediastinal lymph nodes,
– 5 patients with lymphoma,
– 9 patients with mediastinal tumours,
– 2 patients due to dialysis catheter-related thrombosis,
– 1 patient due to a pacemaker.
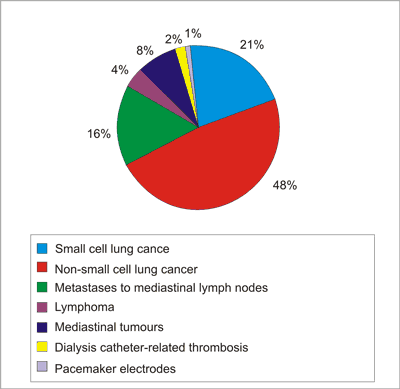
Fig. 1. Causes of SVCS.
The clinical symptoms of VCS include (fig. 2):
– facial swelling and cyanosis in 88 patients,
– difficulties in breathing in 92 patients,
– hoarseness in 4 patients.
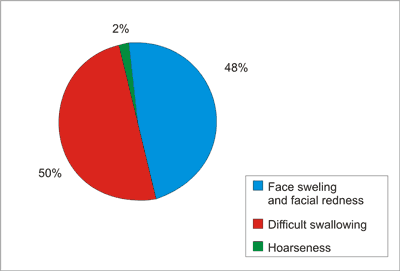
Fig. 2. Clinical symptoms of SVCS.
The mean age of patients was 64 years. The study population included 68 men and 44 women.
Description of the procedure
Priori to the procedure, each patient underwent CT to evaluate the location of tumour in relation to SVC, length of the stenotic SVC segment, presence of collateral vessels. Based on CT findings, the procedure was planned and suitable stents chosen (fig. 3, 4).
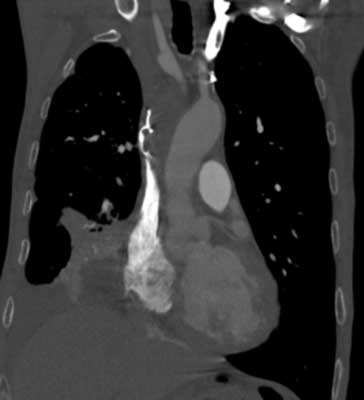
Fig. 3. Computed tomography (CT) reveals SVC obstruction.

Fig. 4. Pre-procedure CT – evaluation of the stenotic SVC segment enables procedure planning and choice of suitable equipment.
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
24 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
59 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
119 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 28 zł
Piśmiennictwo
1. Wilson LD, Detterbeck FC, Yahalom J: Clinical practice. Superior vena cava syndrome with malignant causes. The New England Journal of Medicine 2007 May 3; 356(18): 1862-1869.
2. Aleszewicz-Baranowska J, Komorowska W: Zespół żyły głównej górnej. Via Medica, Gdańsk 2007: 358-360.
3. Ahmann F: A reassessment of the clinical implications of the superior vena cava syndrome. J Clinic Oncol 1984; 2: 961-969.
4. Lanciego C, Chacon JL, Julián A et al.: Stenting as first option for endovascular treatment of malignant superior vena cava syndrome. Am J Roentgenol 2001; 177: 585-593.
5. Albers EL, Pugh ME, Hill KD et al.: Percutaneous vascular stent implantation as treatment for central vascular obstruction due to fibrosing mediastinitis. Circulation 2011 Apr 5; 123(13): 1391-1399.
6. Uberoi R, Morgan R: Quality assurance guidelines for superior vena cava stenting in malignant diseaeas. www.cirse.org.
7. Rizvi AZ, Kalra M, Bjarnason H et al.: Benign superior vena cava syndrome: stenting is now the first line of treatment. J Vasc Surg 2008; 47: 372-380.
8. Nagata T, Makutani S, Uchida H et al.: Follow-up results of 71 patients undergoing metallic stent placement for the treatment of a malignant obstruction of the superior vena cava. Cardiovasc Interv Radiol 2007; 30: 959-967.
9. Ploegmakers MJ, Rutten MJ: Fatal pericardial tamponade after superior vena cava stenting. Cardiovasc Intervent Radiol 2009 May; 32(3): 585-589.
10. Cho Y, Il Gwon D, Ko G-Y et al.: Covered stent placement for the treatment of malignant superior vena cava syndrome: Is unilateral covered stenting safe and effective? Korean J Radiol 2014 Jan-Feb; 15(1): 87-94.
11. Chien-Liang L, Ming-Shen D, Chung-Yi L et al.: Successful endovascular stenting in superior vena cava syndrome. J Med Sci 2012; 32(1): 31-34.
12. Bagul NB, Month P, Narayan JM et al.: Migration of superor vena cava stent Journal of Cardiothoracic Surgery 2008; 3: 12. doi:10.1186/1749-8090-3-12.
13. Dubois P, Mandieau A, Dolatabadi D et al.: Right ventricular migration of stent after endovascular treatment of superior vena cava syndrome. Arch Mal Coeur Vaiss 2001 Nov; 94(11): 1180-1183.




