Antonina Respondek-Bartuś1, Natalia Dziewa1, Radosław Cylke1, *Małgorzata Kołodziejczak1, 2
Trądzik odwrócony. Współczesna diagnostyka i leczenie
Hidradenitis suppurativa. Contemporary diagnosis and treatment
1Department of General and Transplant Surgery Medical University of Warsaw
2Warsaw Proctology Centre, St. Elizabeth’s Hospital in Warsaw
Streszczenie
Trądzik odwrócony jest za rzadką i przewlekłą chorobą zapalną. Znacząco obniża jakość życia pacjentów, powodując cierpienie psychospołeczne. Najistotniejszym problemem wydaje się być dość uboga wiedza na temat tego schorzenia, zarówno wśród lekarzy, jak i społeczeństwa, co wiąże się ze znacznie opóźnioną diagnozą.
Autorzy przedstawiają aktualny przegląd piśmiennictwa dotyczący etiologii i diagnostyki choroby, a także zalecanego postępowania. Szczególną uwagę zwracają na najnowsze trendy w leczeniu, które kładą nacisk na spersonalizowane i interdyscyplinarne podejście terapeutyczne, uwzględniające farmakoterapię, metody chirurgiczne, a także modyfikację stylu życia. Podkreślają, że wczesne wdrożenie leczenia ma kluczowe znaczenie dla zatrzymania postępu choroby i uniknięcia poważnych powikłań.
Summary
Hidradenitis suppurativa, also known as acne inversa, is a rare chronic inflammatory disease. It causes psychosocial distress, significantly reducing patients’ quality of life. The limited knowledge of the condition, both among medical specialists and the general public, appears to be the main issue, often leading to significantly delayed diagnosis.
We present an up-to-date review of the literature on the aetiology and diagnosis of the disorder, along with current therapeutic recommendations. Particular attention was given to the latest treatment trends, which prioritise a personalized and interdisciplinary therapeutic approach encompassing pharmacotherapy, surgical interventions, and lifestyle modifications. It is emphasized that early treatment initiation is crucial for halting disease progression and preventing serious complications.

Trądzik odwrócony (acne inversa, hidradenitis suppurativa – HS) uznawany jest za rzadką i nieuleczalną chorobę. Tymczasem jej wczesne postaci kliniczne, znacznie częściej niż mogłoby się wydawać, obserwuje się w gabinetach Podstawowej Opieki Zdrowotnej (1).
Pierwsze opisy choroby sięgają XIX wieku – wówczas pojawiło się określenie hidradenitis, choroba Velpeaua (2). Nazwa „trądzik odwrócony” jest w użyciu od lat 80. XX wieku (3).
Rozpoznanie w języku polskim według ICD-10 L73.2 – ropnie mnogie gruczołów apokrynowych pachy – jest mylące. Nie uwzględnia ono zmian w innych typowych dla choroby lokalizacjach.
Również z uwagi na etiologię choroby sugeruje się zaprzestanie używania pojęcia „zapalenia gruczołów apokrynowych” – hidradentis suppurativa. Określenie „trądzik odwrócony” – acne inversa wydaje się bardziej odpowiadać etiopatogenezie choroby, bowiem proces chorobowy rozpoczyna się w mieszku włosowym, a dopiero później rozprzestrzenia się na gruczoły apokrynowe; może także zajmować okolice zupełnie pozbawione tych gruczołów (4).
Występowanie
Częstość występowania HS w populacji światowej wynosi 0,4%, kwalifikuje się go jako chorobę rzadką. Większy odsetek występowania obserwuje się u Afroamerykanów oraz w grupach pacjentów o mieszanej przynależności etnicznej.
W Polsce odsetek występowania HS szacuje się na poziomie 1,6%. Ocenia się, że około 400 osób w naszym kraju choruje na najcięższe postaci tej choroby.
75% pacjentów ze zdiagnozowaną chorobą stanowią kobiety, a przeciętny wiek rozpoznania to 36 lat (5, 6).
Wyniki badań populacyjnych wskazują na częstsze występowanie HS u osób o niższym statusie socjoekonomicznym (6).
Choroby współistniejące
U pacjentów z rozpoznaniem HS występuje zwiększone ryzyko chorób współistniejących, m.in.: zespołu metabolicznego, cukrzycy, zespołu policystycznych jajników, trądziku pospolitego, chorób tarczycy, zapalenia stawów oraz nieswoistych chorób zapalnych jelit (Leśniowskiego-Crohna, wrzodziejącego zapalenia jelit).
Obserwuje się większą częstość udarów mózgu, zawałów serca oraz dwukrotnie większe ryzyko nagłej śmierci sercowej.
Opisane zostały także zespoły autozapalne, np. PASH, PAPA i inne, czyli koincydencję HS z trądzikiem pospolitym, piodermią zgorzelinową, zapaleniem stawów oraz łuszczycą (6).
Częściej rozpoznaje się również depresję, zaburzenia lękowe oraz obserwuje się zwiększoną częstość samobójstw.
Czynniki ryzyka
Jednym z głównych czynników ryzyka występowania HS jest palenie tytoniu – odsetek palących wśród chorych wynosi 44-70%. Nikotynizm najprawdopodobniej powoduje wzrost stężenia interleukiny 1 (β), a także niedrożność ujść mieszków włosowych wskutek akantozy (4, 6).
Wyniki najnowszych badań wskazują również na dysbiozę mikrobioty skóry: zmniejszoną liczbę bakterii komensalnych, zwiększoną liczbę oportunistycznych bakterii beztlenowych oraz obecność Staphylococcus aureus. Przypuszcza się, że wzrostowi tego patogenu może sprzyjać nikotynizm (6).
Wykazano wyraźny związek współwystępowania choroby z otyłością, a także zależność pomiędzy zwiększeniem BMI a pogorszeniem przebiegu choroby u kobiet. Związek między otyłością a HS można przypisać zwiększonym siłom tarcia wywoływanym przez nadmiernie przerośnięte fałdy skórne (7). Tarcie i uraz mechaniczny indukują aktywację metaloproteinaz i uwolnienie prozapalnych cytokin (6).
Etiologia
Dane naukowe sugerują udział procesu zapalnego wywołanego przez nieprawidłową odpowiedź immunologiczną, zamknięcie ujść mieszków włosowych (namnażanie się wewnątrz bakterii beztlenowych) oraz czynniki hormonalne jako głównych przyczyn powstawania choroby.
Obciążony wywiad rodzinny występuje u 40% pacjentów. Mechanizm dziedziczenia nie został opisany, dotychczasowe badania wskazują, że ma on charakter autosomalny dominujący. Wykazano jednak wpływ czynników środowiskowych na ekspresję genów i rozwój objawowej choroby (4).
Objawy
Trądzik odwrócony przebiega pod postacią bolesnych, głęboko umiejscowionych zmian zapalnych w miejscach typowych. Pojawiać się może już od okresu dojrzewania. Pacjentki początkowo zgłaszają się do gabinetów lekarzy pierwszego kontaktu z powodu bolesnych, nawracających czyraków w więcej niż jednej okolicy.
Charakterystyczne jest umiejscowienie tych zmian – pod pachami, pod piersiami, w pachwinach, na przyśrodkowej powierzchni ud i w okolicy nadłonowej.
W przypadku mężczyzn najczęściej zajęte są: pachy, pośladki i okolica krocza, w tym zazwyczaj okołoodbytnicza (ryc. 1-3). Wśród nietypowych miejsc wymienia się kark oraz okolicę za małżowiną uszną.
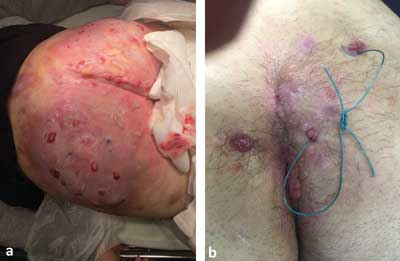
Ryc. 1a, b. Rozległy hydradenit pośladków

Ryc. 2. Hydradenit zlokalizowany w pachwinie
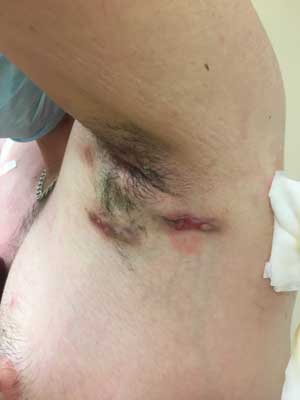
Ryc. 3. Hydradenit zlokalizowany w okolicy pachy
Zmiany skórne mają charakter guzków, torbieli włosowych – tuneli podskórnych, przebarwień lub bliznowacenia (powrózkowate blizny). Objawem prodromalnym HS mogą być torbiele pilonidalne (włosowe). Choroby te mogą występować jednocześnie, np. torbiel włosowa, przetoka okołoodbytnicza oraz HS.
Wśród diagnostyki różnicowej, w tym błędnych rozpoznań, wymienia się czyraki nawracające oraz trądzik pospolity (który często może współistnieć z HS) (1, 8). Należy również uwzględnić: obraz zgorzelinowego zapalenia skóry – pyoderma gangrenosum, skórną manifestację choroby Leśniowskiego-Crohna, głębokie infekcje o etiologii grzybiczej czy gruźliczej. Z podobnym obrazem klinicznym mogą przebiegać również: ziarnica weneryczna, ziarniniak pachwinowy oraz promienica (6, 8). Szacuje się, że opóźnienie diagnozy tej choroby sięga nawet 12 lat (5).
Diagnostyka
Rozpoznanie ustala się na podstawie typowych objawów klinicznych – charakterystycznych zmian skórnych w określonej lokalizacji, utrzymujących się lub nawracających pomimo standardowego dla zakażeń skóry leczenia.
Uznaje się, że kryterium rozpoznania jest wystąpienie co najmniej 2 zmian w ciągu 6 miesięcy lub 5 zmian w ciągu całego życia (9).
Badania dodatkowe, takie jak posiewy z ran, zazwyczaj nie są pomocne w diagnostyce i ustaleniu planu leczenia, jednak negatywny wynik badania mikrobiologicznego i dodatkowy wywiad rodzinny mogą stanowić drugorzędne przesłanki (6).
Niezwykle istotny jest fakt, że rak kolczystokomórkowy, najczęściej okolicy anogenitalnej, może przebiegać z martwicą tkanek, ropieniem i wytwarzaniem przetok, co w badaniu przedmiotowym daje obraz bardzo podobny do HS (4, 10).
Według doniesień naukowych przewlekły stan zapalny w przebiegu HS predysponuje do transformacji nowotworowej (9, 11). Według Plewiga i wsp. jest on bardziej agresywny niż ten powstający de novo. Często daje miejscowy naciek, przerzuty i nawrót po wycięciu chirurgicznym (4), dlatego w toku diagnostyki niezbędne jest pobranie materiału do badania histopatologicznego z obszarów zmienionych chorobowo, pomimo tego, że zdaniem niektórych autorów sam wynik nie jest niezbędny do ustalenia rozpoznania HS (12).
Z uwagi na częste występowanie niekorzystnych czynników stylu życia oraz chorób współistniejących, szczególną uwagę zwraca się na holistyczne podejście do pacjenta. Istotna jest ocena ciśnienia tętniczego oraz czynników ryzyka sercowo-naczyniowego (w tym wywiad nikotynizmu, BMI) (12).
Zwraca się również uwagę na przeprowadzenie badania przesiewowego w kierunku depresji, ocenę wpływu choroby na jakość życia oraz oceną natężenia bólu. Zaleca się zastosowanie skali HADS (Szpitalna Skala Lęku i Depresji, Hospital Anxiety and Depression Scale) oraz wskaźnika DLQI (wpływu dolegliwości skórnych na jakość życia, Dermatology Life Quality Index), z modyfikacją HiSQOL (Hydradenitis Supprativa Quality of Life) uwzględniającą 17 elementów jakości życia w ciągu ostatnich 7 dni (6, 13).
Stosowane skale
W odniesieniu do stopnia wykrywalnego stanu zapalnego, HS jest klasyfikowany jako postać zapalna i niezapalna.
Intensywność postaci zapalnej można podzielić według klasyfikacji IHS4 (Międzynarodowego Systemu Oceny Ciężkości HS) na łagodną, umiarkowaną oraz ciężką. Skalę stosuje się zarówno w praktyce klinicznej, jak i w badaniach naukowych. Wynik oblicza się na podstawie sumy liczby guzków (pomnożonej przez 1), liczby ropni (pomnożonej przez 2) oraz liczby drenujących tuneli (pomnożonej przez 4). Całkowity wynik 3 lub niższy oznacza postać łagodną, 4-10 – umiarkowaną, a ponad 11 – ciężką (13).
Decyzja dotycząca planu leczenia chirurgicznego przeważnie opiera się na stadium choroby w skali Hurleya (ryc. 4). Zależy także od dotkniętej schorzeniem lokalizacji (7). Dodatkowo warto uwzględnić częstotliwość zaostrzeń choroby (13).
Klasyfikacja Hurleya
Stadium I
pojedyncze lub mnogie ropnie bez torbieli włosowych i bez bliznowacenia
Stadium II
nawracające ropnie z torbielami włosowymi i bliznowaceniem, pojedyncze lub liczne znacznie oddalone od siebie zmiany
Stadium III
zmiany rozsiane lub liczne połączone ze sobą kanały i ropnie |
Ryc. 4. Klasyfikacja Hurleya
SAHS natomiast to skala oceny ciężkości przebiegu choroby, obejmująca liczbę zajętych obszarów. Skala HASI-R mierzy zasięg zmian, wykorzystując oszacowanie zajętej powierzchni ciała (BSA). HiSCR służy do oceny redukcji co najmniej 50% zmian w porównaniu z punktem wyjścia. Wykorzystuje się ją głównie w badaniach klinicznych do oceny odpowiedzi na leczenie. Jej modyfikacją są HiSCR75 i HiSCR90, obejmujące odpowiednio redukcję o 75% i 90%.
HS?IGA jest najnowszym narzędziem służącym do oceny nasilenia choroby i odpowiedzi na leczenie. Wynik od 0 do 5 punktów uwzględnia sumę liczby zmian, a odpowiedź na leczenie to wynik pomniejszony o co najmniej 2 punkty (13).
Postępowanie
Dane naukowe dotyczące leczenia HS są ograniczone. Informacje związane ze stosowanymi dotychczas metodami są niskiej jakości lub wynikają wyłącznie z opinii ekspertów.
Od czasu opublikowania wytycznych S1 w 2015 roku walidacja nowych podejść terapeutycznych niemal całkowicie odmieniła wiedzę w zakresie leczenia HS (7).
U pacjentów, u których występują wyłącznie zmiany zapalne, wskazana jest jedynie farmakoterapia. Jeśli jednak głównym problemem jest zniszczenie tkanek, konieczne jest leczenie chirurgiczne (14). To właśnie połączenie terapii farmakologicznej w celu zmniejszenia stanu zapalnego z chirurgicznym usunięciem nieodwracalnie uszkodzonych tkanek jest obecnie uważane za właściwe podejście terapeutyczne (7).
Z drugiej strony, każde leczenie chirurgiczne musi być częścią kompleksowego planu leczenia, w którym zawsze należy rozważyć wskazania do farmakoterapii (14).
Farmakoterapia
Żaden lek stosowany na co dzień w terapii nie jest zarejestrowany w tym wskazaniu (z wyjątkiem leków biologicznych: adalimumabu, sekukinumabu i bimekizumabu), o czym na samym początku należy poinformować pacjentów.
W stadium I według Hurleya (przebieg łagodny) zaleca się leczenie miejscowe przy użyciu klindamycyny w postaci 1% emulsji stosowanej 2 razy dziennie przez 3 miesiące. Leczenie można przedłużyć, jeśli jest to wskazane klinicznie.
Skuteczna może być również 3-miesięczna terapia doustnymi tetracyklinami (zwłaszcza w przypadku częstych zaostrzeń) wykorzystująca ich działanie przeciwzapalne (1).
Klindamycyna jest jedynym antybiotykiem, który badano jako środek miejscowy w leczeniu HS o nasileniu łagodnym do umiarkowanego. W randomizowanym, podwójnie zaślepionym, kontrolowanym badaniu z udziałem 27 pacjentów z HS w stadium I i II według Hurleya miejscowo stosowana klindamycyna wykazała 4,5-krotnie większą poprawę niż placebo (wynik istotny statystycznie) w przypadku zmian powierzchniowych (zapalenie mieszków włosowych, grudki i krostki). Efekt w przypadku głębokich zmian był znikomy.
Wykazano, że miejscowy 15% roztwór rezorcyny (lub krem zawierający rezolcynol) jest skuteczny i dobrze tolerowany w redukcji rozmiaru i liczby zmian oraz w zmniejszaniu bólu. Jest związkiem fenolowym o działaniu keratolitycznym, przeciwświądowym i antyseptycznym. Stosuje się go 2 razy dziennie w fazie zaostrzenia i raz dziennie jako leczenie podtrzymujące przez okres do 16 tygodni. Brak jest danych dotyczących stosowania rezorcyny w ciąży. Toksyczność ogólnoustrojowa przy miejscowym stosowaniu jest niezwykle rzadka (6). Badanie retrospektywne wykazało odpowiedź w skali HiSCR u 85,3% pacjentów leczonych rezorcyną w porównaniu z 52% pacjentów w przypadku miejscowej klindamycyny (7).
Aby zapobiec rozwojowi lekooporności bakterii zaleca się również przemywanie ran miejscowymi środkami antyseptycznymi, np. chlorheksydyną w postaci 4% emulsji (w Polsce dostępna w postaci płynu 1%, ewentualnie jako lek recepturowy) lub chlorkiem benzalkonium (w Polsce brak preparatów do stosowania na skórę) (15). Nie ma jednak dowodów naukowych uzasadniających stosowanie dostępnych bez recepty środków oczyszczających skórę o działaniu antybakteryjnym lub przeciwzapalnym, takich jak: chlorheksydyna, nadtlenek benzoilu, pirytionian cynku czy triklosan.
W stadium II (umiarkowanym) stosuje się leczenie systemowe doustnymi tetracyklinami przez pełne 3 miesiące. W przypadku dobrej odpowiedzi na leczenie zaleca się kontynuację przez kolejne 12 tygodni. Stosuje się limecyklinę w dawce 408 mg lub doksycyklinę w dawce 100 mg stosowane 1-2 razy dziennie (1).
W związku z przedłużoną antybiotykoterapią należy zwrócić uwagę na ryzyko wystąpienia zapalenia okrężnicy i biegunki o ciężkim przebiegu. Terapii nie należy stosować u kobiet w ciąży ani u dzieci poniżej 9. r.ż. z uwagi na ryzyko przebarwienia zębów stałych (7). Należy również zwrócić uwagę na reakcję fototoksyczności oraz zwiększoną hepatotoksyczność w przypadku zaburzeń czynności nerek (6).
Leczenie stadium I i II można rozpocząć i kontynuować w ramach POZ.
Często możliwe jest czasowe odstawienie terapii w związku z uzyskaną remisją choroby. W przypadku niedostatecznej odpowiedzi pacjenta należy skierować do dermatologa lub ośrodka specjalistycznego.
W sytuacji nieudanej próby leczenia tetracykliną terapią II rzutu (w opiece specjalistycznej) jest terapia klindamycyną w dawce 300 mg 2 razy dziennie w skojarzeniu z ryfampicyną 300 mg 2 razy dziennie przez 10 tygodni. Przy skuteczności terapii zaleca się powtarzanie całego cyklu 2-3 razy w roku.
Istotne jest zwrócenie uwagi na zmianę barwy moczu podczas stosowania ryfampicyny oraz interakcję tego leku z większością hormonalnych środków antykoncepcyjnych (jako induktor enzymów powoduje brak ich skuteczności). Przed rozpoczęciem terapii ryfampicyną producenci zalecają wykonanie kontrolnych badań laboratoryjnych i powtarzanie ich w trakcie kuracji (morfologia, mocznik, elektrolity, próby wątrobowe), ze szczególnym uwzględnieniem pacjentów z wywiadem nadużywania alkoholu.
W przypadku długotrwałego leczenia klindamycyną należy mieć na uwadze ryzyko wystąpienia rzekomobłoniastego zapalenia jelit o etiologii Clostridium difficile (7).
Wykazano, że skojarzone leczenie ryfampicyną i klindamycyną znacząco zmniejsza stężenie klindamycyny w osoczu u pacjentów z HS. Kliniczne znaczenie tego odkrycia pozostaje jednak nieznane (7).
Czas trwania systemowej terapii antybiotykowej można skrócić dzięki 5-dniowemu dożylnemu leczeniu klindamycyną w dawce 600 mg 2 razy na dobę. Schemat ten można zastosować także przed rozpoczęciem leczenia skojarzonego w przypadku zaostrzenia choroby.
Nie zaobserwowano istotnej oporności na środki przeciwdrobnoustrojowe u pacjentów leczonych tetracyklinami i doustną klindamycyną. U pacjentów stosujących miejscowo klindamycynę częściej rozwijały się jednak oporne na klindamycynę szczepy Staphylococcus aureus w porównaniu z pacjentami niestosującymi antybiotyków (7).
W stadium III choroby pacjenta należy bezpośrednio skierować do opieki specjalistycznej z uwagi na konieczność zastosowania złożonego leczenia – farmakologicznego (rozpoczyna się od skojarzonej terapii klindamycyną z ryfampicyną) i chirurgicznego.
Należy podkreślić, jak ważne jest podejście interdyscyplinarne w leczeniu pacjentów z HS. Wyłącznie chirurgiczne ograniczone opracowanie ran nie zapobiega rozprzestrzenianiu się zmian. Za najbardziej skuteczne podejście w stadiach II i III uważa się opanowanie choroby za pomocą farmakoterapii przed ewentualną planowaną interwencją chirurgiczną (13).
Terapia biologiczna
Adalimumab – inhibitor czynnika martwicy nowotworu (TNF)-α, sekukinumab – inhibitor interleukiny (IL)-17A i bimekizumab – inhibitor IL-17A/F, podawane podskórnie zostały zatwierdzone przez Europejską Agencję Leków do leczenia umiarkowanych i ciężkich postaci HS, z niewystarczającą odpowiedzią na konwencjonalne leczenie systemowe. Adalimumab jest ponadto zatwierdzony od 2018 roku u pacjentów od 12. r.ż. w tym wskazaniu.
Takie leczenie stosowane jest w ośrodkach specjalistycznych. Doświadczenie kliniczne wskazuje na dobrą tolerancję leków i istotną poprawę stanu pacjentów z ciężką postacią choroby. W związku z częstymi przypadkami nawrotów zaleca się długotrwałe leczenie w celu dobrej kontroli choroby (7).
Adalimumab został zarejestrowany jako pierwszy w 2015 roku. Jego skuteczność kliniczna została potwierdzona w badaniu PIONEER. Terapia rozpoczyna się od dawki 160 mg w dniu 0., następnie w dniu 15. 80 mg i kolejno 40 mg co tydzień lub 80 mg co 2 tygodnie. Dawka 40 mg może być jednak niewystarczająca dla pacjentów otyłych, u których powinno się ją zwiększyć do 80 mg, podobnie jak u pacjentów, u których standardowa dawka okazała się niewystarczająca (6).
Sekukinumab został zarejestrowany w 2023 roku, jego skuteczność została potwierdzona w wieloośrodkowych badaniach SUNSHINE i SUNRISE. Lek stosuje się w dawce 300 mg w tygodniach 0., 1., 2., 3., 4., następnie co 2-4 tygodnie zależnie od reakcji, w leczeniu podtrzymującym.
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
29 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
69 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
129 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 78 zł
Piśmiennictwo
1. Collier F, Ingram JR: Holistic assessment key in hidradenitis suppurativa. The Practitioner 2019; 263(1829): 21-24.
2. Jemec GBE: Hidradenitis suppurativa. Clinical practice. N Engl J Med 2012; 366: 158-164.
3. Bergler-Czop B: Trądzik odwrócony (acne inversa) – najczęstsze błędy w postępowaniu diagnostyczno-terapeutycznym. Dermatologia po Dyplomie 2014; 03.
4. Kołodziejczak M, Ciesielski P: Choroby proktologiczne. Diagnostyka i leczenie. Wyd. 1. PZWL, Warszawa 2022: 178-189.
5. Prof. Narbutt: Wywiad, artykuł MP: Na HS cierpi w Polsce około 400 pacjentów. Newseria 2018.
6. Matusiak Ł, Walecka I, Reich A et al.: Polskie wytyczne dotyczące diagnostyki i leczenia hidradenitis suppurativa. Dermatol Rev/Przegl Dermatol 2024; 111: 1-20.
7. Zouboulis CC, Bechara FG, Benhadou F et al.: European S2k guidelines for hidradenitis suppurativa/acne inversa part 2: Treatment. J Eur Acad Dermatol Venereol 2025; 39(5): 899-941.
8. Reddick CL, Singh MN, Chalmers RJG: Successful treatment of superficial pyoderma gangrenosum associated with hidradenitis suppurativa with adalimumab. Dermatol Online J 2010; 16(8): 15.
9. Ingram JR, Collier F, Brown D et al.: British Association of Dermatologists guidelines for the management of hidradenitis suppurativa (acne inversa). Br J Dermatol 2018; 180(5): 1009-1017.
10. Dessinioti C, Plaka M, Zisimou C et al.: Advanced squamous cell carcinoma of the axillae mimicking hidradenitis suppurativa. J Eur Acad Dermatol Venereol 2017; 31(9): 421-423.
11. Caccavale S, Caccavale T, La Montagna M: Hidradenitis suppurativa complicated by squamous cell carcinoma: isoscartopic response. Int Wound J 2017; 14(6): 1397-1398.
12. Fabbrocini G, Ruocco E, De Vita V, Monfrecola G: Squamous cell carcinoma arising in long-standing hidradenitis suppurativa: an overlooked facet of the immunocompromised district. Clin Dermatol 2017; 35: 225-227.
13. Karagiannidis I, Nikolakis G, Sabat R, Zouboulis CC: Hidradenitis suppurativa/Acne in-versa: an endocrine skin disorder? Rev Endocr Metab Disord 2016; 17: 335-341.
14. Hurley H, Roenigh R: Axillary hyperhidrosis, apocrine bromohidrosis, hidradenitis suppurativa, and familial benign pemphigus: surgical approach. Dermatologic surgery. New York 1989: 729-739.
15. Cramer P, Schneider-Burrus S, Kovics M et al.: Acne inversa – opcje chirurgiczne, rekonstrukcje i kombinacje z terapiami lekowymi. Hautarzt 2021; 72(8): 692-699.
16. Tappenden P, Carroll C, Stevens JW et al.: Adalimumab for treating moderate-to-severe hidradenitis suppurativa: An evidence review group perspective of a NICE single technology appraisal. Pharmacoeconomics 2017; 35(8): 805-815.
17. Bechara FG, Podda M, Prens EP et al.: Efficacy and safety of Adalimumab in conjunction with surgery in moderate to severe hidradenitis Suppurativa: the SHARPS randomized clinical trial. JAMA Surg 2021; 156(11): 1001-1009.
18. Masson R, Shih T, Jeong C et al.: Omówienie artykułu: Hormonal Treatments in Hidradenitis Suppurativa: A Systematic Review. J Drugs Dermatol 2023; 22(8): 785-794.
19. Hazen PG, Hazen BP: Hidradenitis suppurativa: successful treatment using carbon dioxide laser excision and marsupialization. Dermatol Surg 2010; 36: 208-213.
20. Tierney E, Mahmoud BH, Hexsel C et al.: Randomized control trial for the treatment of hidradenitis suppurativa with a neodymium-doped yttrium aluminium garnet laser. Dermatol Surg 2009; 35: 1188-1198.
21. Wollina U, Koch A, Heinig B et al.: Acne inversa (Hidradenitis suppurativa): a review with a focus on pathogenesis and treatment. Indian Dermatol Online J 2013; 4: 2-11.
22. Rieger UM, Erba P, Pierer G, Kalbermatten DF: Hidradenitis suppurativa of the groin treated by radical excision and defect closure by medial thigh lift: aesthetic surgery meets reconstructive surgery. J Plast Reconstr Aesthet Surg 2009; 62: 1355-1360.
23. Liy-Wong C, Kim M, Kirkorian Y et al.: Hidradenitis Suppurativa in the Pediatric Population. An International, Multicenter, Retrospective, Cross-sectional Study of 481 Pediatric Patients. JAMA Dermatol 2021; 157(4): 385-391.
24. Seivright J, Villa N, Grogan T et al.: Omówienie artykułu: Impact of Pregnancy on Hidradenitis Suppurativa Disease Course: A Systematic Review and Meta-Analysis. Dermatology 2022; 238(2): 260-266.
25. Fitzpatrick L, Hsiao J, Tannenbaum R et al.: Adverse pregnancy and maternal outcomes in women with hidradenitis suppurativa. J Am Acad Dermatol 2022; 86: 46-54.
26. Xu LY, Wright DR, Mahmoud BH et al.: Histopathologic study of hidradenitis suppurativa following long-pulsed 1064-nm Nd:YAG laser treatment. Dermatol 2011; 147: 21-28.
27. Mahmoud BH, Tierney E, Hexsel CL et al.: Prospective controlled clinical and histopathologic study of hidradenitis suppurativa treated with the long-pulsed neodymium:yttriumaluminium-garnet laser. J Am Acad Dermatol 2010; 62: 637-645.
28. Kołodziejczak M, Sudoł-Szopińska I, Wilczyńska A, Bierca J: Utility of transperineal and anal ultrasonography in the diagnostics of hidradenitis suppurativa and its differentiation from a rectal fistula. Postepy Higieny i Medycyny Doswiadczalnej (Online) 2012; 66: 838-842.




