© Borgis - Medycyna Rodzinna 6/2003, s. 185-189
Sylwester Mordarski
Ból przewlekły współczulnie zależny
Sympathetically maintained pain – SMP
z Katedry i Kliniki Anestezjologii i Intensywnej Terapii Akademii Medycznej we Wrocławiu
Kierownik Katedry: prof. dr hab. Andrzej Kübler
Summary
Sumpathetically maintained pain (SMP) may be found in association with some painful syndromes. It is taken to be pain that is maintained by sympathetic efferent innerration or by circulating catecholaminus. This is a feature of several types of painful conditions and is not an essential requirement of any one condition. It is understood that pain relived by specific sympatholytic procedure may be considered SMP. This does not imply a mechanism for the pain but simply follows the common clinical observation that in certain cases sympatholytic interventions will lead to a reduction of pain. It is also notable that a patient may have SMP and sympathetically independent pain (SIP) at the same time. SMP may occur in some patients with complex regional pain syndromes (CRPS), but certainly does not occur in all.
The current paper presents modern concepts about pathogenesis and treatment of SMP.

Komitet do Spraw Taksonomii IASP proponuje ujęcie terminów określających różne stany lub zjawiska kliniczne odnoszące się do bólu przewlekłego w jednoznaczne definicje. W dziale dotyczącym zespołów bólowych zamieszczono nowe określenie – regionalny zespół bólowy (complex regional pain syndromes – CRPS). Pod tym określeniem obecnie opisuje się zespoły bólowe uprzednio definiowane jako „Reflex Sympathetic Dystrophy´´ i „Causalgia´´. Wcześniejsza definicja reflex sympathetic dystrophy nie oddaje wiernie istoty schorzenia, ponieważ nie we wszystkich przypadkach powstały ból jest współczulnie zależnym, jak też nie we wszystkich przypadkach obserwuje się zmiany troficzne. Stany te są zwykle następstwem obwodowo pojawiającego się urazu, poniżej którego występują nieprawidłowe doznania, niewspółmierne do oczekiwanego przebiegu klinicznego wywołanego zaistniałym wydarzeniem, zarówno w natężeniu jak i czasie trwania. Często obserwuje się znaczne osłabienie funkcji motorycznej. Przypadki, ogólnie odpowiadające tym, które wcześ-niej opisywano jako reflex sympathetic dystrophy, obecnie definiuje się jako CRPS Typ I, a opisywane jako causalgia – CRPS Typ II (19).
Współczulnie zależny ból (sympathetically maintained pain – SMP) może towarzyszyć obu tym zespołom. Zaistniały ból może być podtrzymywany przez współczulne eferentne unerwienie lub krążące katecholaminy. Powyższe jest wspólną cechą wielu zespołów bólowych, ale nie jest podstawowym wymogiem diagnostycznym. Jest oczywistym, że ból który zmniejsza się pod wpływem specyficznego postępowania sympatykolitycznego może być rozważany jako współczulnie zależny. To pojęcie nie zawiera w sobie mechanizmu powstawania bólu, ale proste następstwa ogólnych obserwacji klinicznych, iż w pewnych przypadkach interwencja sympatykolityczna będzie prowadzić do zmniejszenia bólu. Jest również godnym uwagi, że u tego samego pacjenta może jednocześnie wystąpić ból współczulnie zależny jak i ból współczulnie niezależny (sympathetically independent pain – SIP). Natomiast brak tego objawu klinicznego nie wyklucza rozpoznania regionalnego zespołu bólowego (complex regional pain syndromes – CRPS).
SMP może towarzyszyć neuralgii popółpaścowej, neuropatiom metabolicznym, pourazowemu uszkodzeniu nerwu i tkanek miękkich (6).
Zasadniczą cechą różnicującą SMP od SIP jest badanie czucia powierzchniowego. Badania (14) obejmowały grupę pacjentów z urazem nerwu lub tkanek miękkich, u których lekkie uderzenie skóry wywoływało ból (allodynia). Porównywano stopień mechanicznej hyper-algezji oraz wrażliwość na średniochłodny bodziec (porównywanie natężenia bólu po kropli acetonu z kroplą wody o temperaturze pokojowej). W wyniku tych badań okazało się, że u wszystkich pacjentów z SMP test średniochłodnego bodźca był dodatni, a u pacjentów z SIP był dodatni tylko w 50%. Tak więc, jeżeli średniochłodny bodziec wywołuje u badanego pacjenta ból należy brać pod uwagę rozpoznanie SMP (39).
Innym testem potwierdzającym rozpoznanie SMP jest ustąpienie bólu po dożylnym podaniu guanetydyny techniką Bier´a (4). Wahren i wsp. (39) zauważyli, że u jednych pacjentów test guanetydynowy wywołuje przedłużoną ulgę w bólu trwającą od tygodni do miesięcy, podczas gdy u innych ten sam test nie wywołuje żadnej lub tylko małą ulgę w bólu. Spostrzeżenie to sugeruje, jego zdaniem, rozpoznanie SMP w pierwszej a SIP w drugiej grupie.
Także użytecznym testem przesiewowym potwierdzającym SMP jest blokada zwojów współczulnych środkami znieczulenia miejscowego. Jakkolwiek wynik tych blokad powinien być interpretowany z ostrożnością (10), ponieważ środek znieczulenia miejscowego poprzez dyfuzję do korzeni nerwowych może powodować trudny do rozpoznania blok w rutynowym teście czuciowym. Wyłączenie cienkich włókien nerwowych może mieć duży wpływ na odczuwany przez pacjenta ból. Dodatkowo postępowanie inwazyjne może mieć silny efekt placebo. Minimalizując potencjalną pułapkę blokady środkami znieczulenia miejscowego a jednocześnie uwzględniając rolę alfa receptorów w SMP, alternatywnym testem jest użycie alfa-adrenergicznego antagonisty – fentolaminy (2, 29). Dożylny wlew fentolaminy wyraźnie koreluje pomiędzy zmniejszeniem bólu a czasem podawania leku, jest zatem pomocnym w różnicowaniu efektu zależnego od bólu a efektem placebo (3). Wstępne badania u 18 pacjentów wykazały, że ulga w bólu po podaniu dożylnym fentolaminy w wysokim stopniu koreluje z wynikami osiągniętymi przy pomocy blokad środkami znieczulenia miejscowego zwojów współczulnych (29).
Różnice występujące pomiędzy blokadami zwojów współczulnych środkami znieczulenia miejscowego a testem fentolaminowym mogą być powodowane następującymi możliwościami. Blokada środkami znieczulenia miejscowego może mieć małą specyficzność prowadzącą do nieosiągnięcia pozytywnego skutku. Wykazano, że u niektórych pacjentów współczulny układ nerwowy może pośredniczyć w przewodzeniu bólu poprzez mechanizm nieadrenergicznego receptora. Ponadto użyta dawka fentolaminy może być niedostateczna do całkowitego zablokowania receptora adrenergicznego.
Uprzednio zalecana dawka fentolaminy wynosiła 0,5 mg/kg (8). Wstępne wyniki, uzyskane przy użyciu laserowego przepływomierza doplerowskiego, wykazały znaczne rozbieżności w dawce fentolaminy koniecznej do uzyskania odruchowej odpowiedzi naczyniowej. U niektórych pacjentów 1 mg/kg może być poszukiwaną dawką eliminującą współczulnie pośredniczącą odpowiedź naczynioruchową. Monitorując temperaturę skóry i odruch współczulny podczas infuzji fentolaminy można dostarczyć dodatkowych danych czy funkcja alfa receptora była właściwie zblokowana. Używając dawki, która jest dostateczna do wywołania zmian w napięciu układu współczulnego, można zmniejszyć ilość błędnych interpretacji negatywnych wyników towarzyszących testowi (3, 8, 29).
MECHANIZM
Z wcześniejszej definicji wynika, że SMP znika, gdy zwoje współczulne unerwiające dotknięty obszar są wyłączone środkami znieczulenia miejscowego. Obserwacje te były potwierdzone klinicznie u pacjentów z SMP, gdzie seriami blokad współczulnych uzyskiwano długotrwałą remisję bólu. U innych pacjentów osiągnięto natomiast złagodzenie bólu, ale tylko na czas trwania bloku współczulnego (7). Ostatnie lata obfitowały w badania mające na celu określenie mechanizmu SMP. Jedna z propozycji sugerowała, że włókna aferentne, odpowiedzialne za ból mogą przebiegać z włóknami współczulnymi i tą drogą odpowiadać za nadmierną aktywność współczulną w zaatakowanej kończynie. Inna hipoteza zakłada, że włókna współczulne mogą aktywować mechanoreceptory niskiego progu pobudzenia (low- threshold mechanoreceptors – LTMs) i ta aktywność LTMs indukuje ból poprzez aktywację uczulonych neuronów centralnego układu nerwowego odpowiedzialnych za czucie bólu (31). To, że SMP jest wynikiem aferentnego działania współczulnego układu nerwowego wykazał w swoich badaniach Walker i Nulsen (41). Poddali oni pacjentów przedzwojowej sympatektomii. Jednych z powodu leczenia chorób naczyniowych, innych w celu leczenia kauzalgii. Elektrody były umieszczone wzdłuż pnia współczulnego. Oddzielone od centralnego układu nerwowego mogły być stymulowane w okresie pooperacyjnym. Stymulacja wywoływała ból w uprzednio bolesnym obszarze u pacjentów z kausalgią, ale nie wywoływała bólu u pacjentów z chorobą naczyń. Tak udowodniono, że w SMP włókna współczulne nabywają zdolność wywoływania bólu.
Zakończenia włókien współczulnych uwalniają noradrenalinę do tkanek. W normalnych warunkach noradrenalina wstrzyknięta podskórnie nie wywołuje bólu (11). Walkin i wsp. (40) stwierdzili, że u pacjentów z SMP, u których uzyskano remisję bólu poprzez blokadę współczulną lub chirurgiczną sympatektomię, podskórne wstrzyknięcie noradrenaliny wywołuje uprzedni ból. Sugeruje to, że SMP wynika z nabytej zdolności noradrenaliny do wywoływania bólu. Noradrenalina aktywuje alfa i beta adrenoreceptory (26). Powstaje więc pytanie, który receptor pośredniczy w powstawaniu SMP? Odkąd dożylne wlewy fentolaminy (alfa bloker) uwalniały pacjentów z SMP od bólu (29), SMP ukazuje się jako choroba alfa receptora. Są dwie formy alfa receptora, alfa-1 i alfa-2. W celu wyjaśnienia, który z podtypów alfa receptorów jest odpowiedzialny za SMP, stosowano na powierzchnię hyperalgiczną klonidynę (Catapress, B-I). Klonidyna, agonista alfa-2 receptora, łagodziła ból u pacjentów z SMP, podczas gdy u pacjentów z SIP nie stwierdzano takiego działania. Ulga dotycząca hyperalgezji była ograniczona do obszaru leczonego klonidyną. Fenylefryna (selektywny agonista receptora alfa-1), w podwójnie ślepej próbie, podawana śródskórnie w obszarze leczonym klonidyną wywoływała ból ożywiając hyperalgezję (11, 26). Sugeruje to, że za powstawanie bólu byłby odpowiedzialny receptor alfa-1.
W takim razie, jak klonidyna zmniejsza hyperalgezję w leczeniu miejscowym? Zakończenia nerwów współczulnych posiadają alfa-2 receptory, których pobudzenie hamuje uwalnianie noradrenaliny. Klonidyna może zmniejszyć ból poprzez hamowanie uwalniania noradrenaliny w leczonym obszarze. Alternatywnie, klonidyna mogłaby działać bezpośrednio hamująco na nocyceptory. Tak więc klonidyna raczej normalizuje czucie bólu, niż wywołuje analgezję (8, 11, 26). W oparciu o powyższe badania, przezskórne stosowanie klonidyny znalazło swoje stałe miejsce w leczeniu pacjentów z SMP (20). Lecząc pacjentów klonidyną w postaci naskórnych plastrów należy wziąć pod uwagę fakt, że zazwyczaj powierzchnia plastra jest niewielka w stosunku do całkowitego objętego chorobą obszaru. Dlatego ta postać klonidyny nie może mieć oczekiwanego wpływu na ból całkowity. U pacjentów, u których objęty chorobą jest mały obszar należy spodziewać się zadowalających wyników.
Niestety, stosowanie klonidyny w plastrach naskórnych związane jest z częstym występowaniem odczynów uczuleniowych, co w wielu przypadkach uniemożliwia leczenie (20, 26).
Hipoteza sugerująca rolę alfa-1 receptora w SMP była powodem do przeprowadzenia dalszych badań z użyciem fenylefryny. Interesujące są wyniki badań pacjentów, którym podano metodą podwójnie ślepej próby dwa stężenia fenylefryny. Iniekcja do przeciwnej (normalnej) kończyny wywołuje ból. Przed, ale nie po infuzji dożylnej fentolaminy, fenylefryna wywołuje istotny ból (9). Tak więc, klonidyna alfa-2 agonista zmniejsza ból miejscowo, a fenylefryna agonista alfa-1 receptora wywołuje ból miejscowo. Dlatego jest prawdopodobnym, że w SMP alfa-1 receptor w jakiś sposób wywołuje ból (9, 26).
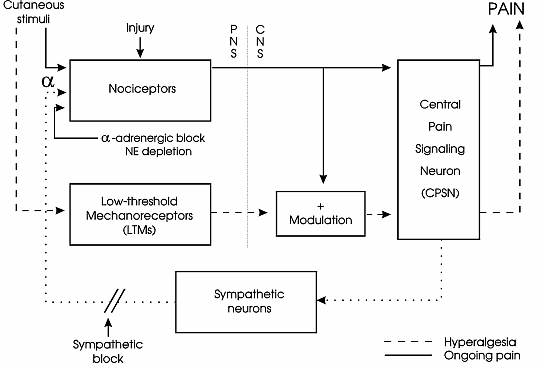
Ryc. 1. Ból przewlekły współczulnie zależny – przypuszczalny mechanizm powstawania (opis w tekście) (9).
Biorąc pod uwagę powyższe rozważania obecnie proponuje się następujący model SMP (ryc. 1): (a) W wyniku uszkodzenia nocyceptorów powstaje poprzez regulację „w górę” zwiększona liczba receptorów, alfa-1 adrenergicznych; (b) Aktywacja alfa-1 receptorów przez uwalnianą z zakończeń współczulnych noradrenalinę powoduje aktywację nocyceptorów, objawem czego jest powstawanie bólu; (c) W wyniku aktywacji nocyceptorów są uwrażliwiane centralne neurony odpowiedzialne za czucie bólu, pobudzenia napływające z mechanoreceptorów niskiego progu pobudzenia również uwrażliwiając centralne neurony, wywołują ból; (d) Pod wpływem blokady współczulnej noradrenalina nie jest dalej uwalniana – nieaktywizuje nocyceptorów, a uwrażliwienie centralnych neuronów jest odwracalne, w ten sposób maleje istniejący ból i ból wywołany dotykiem; (e) Zmniejszona aktywacja nocyceptorów wywołana seriami blokad współczulnych (lub trwałą blokadą współczulną) może prowadzić do regulacji „w dół” alfa-1 receptorów wywołując długotrwałą remisję bólu (9).
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
29 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
69 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
129 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 78 zł
Piśmiennictwo
1. Abram S. et al.: Treatment of long-standing causalgia with prazosin. Reg. Anesth. 1981; 6:79-81. 2. Arner S.: Intravenous phentolamine test: diagnostic and prognostic use in reflex sympathetic dystrophy. Pain 1991; 46:17-22. 3. Arner S.: Differentiation of pain and treatment efficacy. Karolinska Hospital, Stocholm, 1991; 43-45. 4. Bier A.: Veber einen neunen Veg Lokalanasthesie an den Giedmassen zu Erzeugen. Vertch. Dtsch. Ges. Chir. 1908; 37:204. 5. Blanchard J. et al.: Intravenous regional sympatholysis: A double-blind comparison of guanethidine, reserpine, and normal saline. J. Pain Symptom Manage, 1990; 5:357. 6. Bonica J., Buckley F.: Regional analgesia with local anesthetics. The management of pain, Philadelphia, 1990; 1931-1949. 7. Boas R.: Chemical sympathectomy – techniques and responses. Current topics in pain researche and therapy. Amsterdam, Excepta Medica 1983; 259-269. 8. Campbell J. et al.: Myelinated afferents signal the hyperalgesia associated with nerve injury. Pain 1988; 32:89-94. 9. Campbell S. et al.: Diagnosis and management of sympathetically maintained pain. Progress in Pain Research and Management, Vol. 1, IASP Press, Seattle 1994; 87-88. 10. Charlton J.: Current views on the use of nerve blocking in the relief of chronic pain. The Therapy of Pain, MTP Press, Lancaster 1986; 133-164. 11. Davis K. et al.: Topical application of clonidine relieves hyperalgesia in patients with sympathetically maintained pain. Pain 1991; 47:309-317. 12. Dondelinger R. et al.: Percutaneous phenol neurolysis of the lumbar sympathetic chain with computed tomography control. Ann. Radiol. 1984; 27:376-379. 13. Erdemir H. et al.: Prediction of the needed level of sympathectomy for posttraumatic reflex sympathetic dystrophy. Sur. Neurol. 1982; 17:353-354. 14. Frost S., Raja S.: Does hyperalgesia to cooling stimuli characterize patiets with sympathetically maintained pain (reflex sympathetic dystrophy). Proc. Vth World Congress on Pain; Elsevier, Amsterdam, 1988; 151-156. 15. Galer B. et al.: Treatment of inflammatory, neuropathic and sympathetically maintained pain in patient with Sjogren´s syndrome. Pain 1992; 50:205-208. 16. Ghostine S. et al.: Phenoxybenzamine in the treatment of causalgia. J. Neurosurg. 1984; 60:1263-1268. 17. Hannington-Kiff J.: Relief of Sudeck´s atrophy by regional intravenous guanethidine. Lancet 1977; 1:1132-1133. 18. Hoffert M. et al.: Abnormal and collateral innervations of sympathetic and peripheral sensory fields associated with a case of causalgia. Pain 1984; 20:1-12. 19. IASP Task Force on Taxonomy: Classification of chronic pain. IASP Press, Seattle 1994; 40-43. 20. Kirkpatric A., Derasari M.: Transdermal clonidine: Treating reflex sympathetic dystrophy. Regional Anesthesia 1993; 18:140-141. 21. La Motte R. et al.: Neurogenic hyperalgesia: Psychophysical studies of underlying mechanisms. J. Neurophysiol. 1991; 66:190-211. 22. Lindblom U., Verillo R.: Sensory functions in chronic neuralgia. J. Neurol. Neurosurg. Psych. 1979; 42:422-435. 23. Lofstrom J., Cousins M.: Sympathetic neural blockade of upper and lower extremity. Neural Blockade in Clinical Anesthesia and Management of Pain; Lippincott, Philadelphia, 1988; 461-497. 24. Malone P. et al.: Transthoracic electrocoagulation (TTEC) new and simple approach to upper limb sympathectomy. Ir. Med. J. 1982; 75-20-23. 25. Manart J. et al.: Upper dorsal sympathectomy. Am. J. Surg. 1985; 150:762-766. 26. Perl E.: Causalgia: sympathetically-aggravated chronic pain from damaged nerves. Pain, Clinical Updates, 1993; Dec. Vol. 1, Issue 4:2-3. 27. Pernak J.: Percutaneous radiofrequency termal lumbar symparhectomy and clinical use. Eburon Delft, 1988; 29-44. 28. Price D. et al.: Sensory testing of pathophysiological mechanisms of pain in patients with reflex sympathetic dystrophy. Pain 1992; 2:163-173. 29. Raja S. et al.: Systemic alpha-adrenergic blockade with phentolamine: A diagnostic test for sympathetically maintained pain. Anesthesiology 1991; 74:691-698. 30. Redman D. et al.: Computerized tomography guided lumbar sympathectomy. Anaesthesia 1986; 41:39-41. 31. Roberts W.: A hypothesis on the physiological basis for causalgia and related pains. Pain 1986; 24:297-311. 32. Scadding J. et al.: Clinical trial of propranolol in post-traumatic neuralgia. Pain 1982; 14:283-292. 33. Shir Y. et al.: The safety of intravenous phentolamine administration in patients with neuropathic pain. Anesth. Analg. 1993; 76:1008-1011. 34. Ogawa S.: Sympathectomy with neurolytics. The Pain Clinic IV, VSP Publishers, Utrecht, 1992; 139-146. 35. Tabira T. et al.: Reflex sympathetic dystrophy (causalgia) treatment with guanethidine. Arch. Neurol. 1983; 40:430-432. 36. Thompson J.: The diagnosis and management of posttraumatic pain syndromes (causalgia). Aust. N.Z.J. Surg. 1979; 49:299-304. 37. Torebjork H. et al.: Central changes in processing of mechanoreceptive input in capsaicin-induced secondary hyperalgesia in humans. J. Physiol. 1992; 448:765-780. 38. Treede R. et al.: Evidence that alpha – adrenergic receptors mediate sympathetically maintained pain. Pain Research and Clinical Management, Vol. 4, Proc. VIth World Congress on Pain; Elsevier, Amsterdam, 1991; 377-382. 39. Wahren L. et al.: Quantitative sensory testing before and after regional guanethidine block in patients with neuralgia in the hand. Pain 1991; 46-24-30. 40. Wallin G. et al.: Preliminary observations on the pathophysiology of hyperalgesia in the causalgic pain syndrome. Sensory Functions of the Skin in Primates; Pergamon, New York, 1976; 489-502. 41. Walker A., Nulsen F.: Electrical stimulation of the upper thoracic portion of the sympathetic chain in man. Arch. Neurol. Psychiatr. 1948; 59:559-560. 42. Wilkinson H.: Percutaneous radiofrequency upper theracic sympathectomy. A new technique. Neurosurgery 1984; 15:811-814. 43. Wirth F. et al.: A civilian experience with causalgia. Arch. Surg. 1970; 100:633-638. 44. Witzman A. et al.: Results of percutaneous termal lumbar radiofrequency sympathectomy (PTLS) in postdiscectomy syndrome. Pain – clinical aspects and therapeutical issues, Part II, Linz, 1993; 65-70.

