© Borgis - Postępy Nauk Medycznych 8/2015, s. 575-579
Marcin Sidor1, *Andrzej Tomaszewski2, Andrzej Wysokiński2
Zastosowanie echokardiografii w diagnostyce i leczeniu migotania przedsionków
The application of echocardiography in diagnosis and treatment of atrial fibrillation
1Oddział Kardiologii, Radomski Szpital Specjalistyczny
Ordynator Oddziału: dr med. Piotr Achremczyk
2Katedra i Klinika Kardiologii, Uniwersytet Medyczny, Lublin
Kierownik Kliniki: prof. dr hab. med. Andrzej Wysokiński
Streszczenie
Migotanie przedsionków (ang. atrial fibrillation – AF) stanowi najczęstszą tachyarytmię nadkomorową. Z punktu widzenia epidemiologicznego jak i klinicznego, stanowi istotną jednostkę chorobową. W związku z powyższym ważna jest wczesna diagnoza, wybór odpowiedniej metody leczenia oraz monitorowanie nie tylko samego procesu terapii, ale także ewentualnych powikłań takich jak np. udar mózgu. Częstość występowania migotania przedsionków szacuje się na 0,4-1% i wzrasta wraz z wiekiem nawet do 10% u osób powyżej 70 r.ż. Celem ustalenia przyczyny oraz wyboru odpowiedniej metody leczenia pacjentów z AF rutynowo kieruje się na echokardiograficzne badanie serca. Badanie to jako nieinwazyjne, wykonywane w czasie rzeczywistym, łatwo dostępne i tanie jest dobrą metodą do oceny lewego przedsionka. Najbardziej dokładny i równocześnie powtarzalny pomiar objętości przedsionka można uzyskać wykorzystując technikę 3DE (ang. three dimensional echocardiography). Uzyskane pomiary są porównywalne z tymi z tomografii komputerowej i rezonansu magnetycznego. Jednak ze względu na ograniczenia jakie niosą za sobą wspomniane metody, takie jak niska dostępność czy wysoki koszt badania, dwuwymiarowe konwencjonalne badanie echokardiograficzne wciąż pozostaje metodą najczęściej stosowaną w praktyce klinicznej.
Summary
Atrial fibrillation (AF) is the most common supraventricular arrhythmia. Taking into account epidemiological and clinical factors one has to state that atrial fibrillation is a serious illness. Having this in mind one has to pay attention to diagnosis and appropriate method of treatment with adequate control of therapy to prevent such complication as stroke. Atrial fibrillation affects 0,4-1% of the population and its incidence increases with age even to 10% in people who are over 70 years old. Echocardiography is routinely performed in patients suffering from AF to state the cause of this pathology and choose an appropriate method of treatment. As noninvasive, made in real time, easily available and not expensive it is a good examination to define left atrium. The most precise and repeatable measurement of atrial volume is achieved in 3DE technique (three dimensional echocardiography). Measurements performed in 3DE are comparable to those in TK and MR. Due to the limit of those methods such as poor access or high cost of treatment two dimensional conventional echocardiography is the most common in practice.

Migotanie przedsionków (ang. atrial fibrillation – AF) stanowi najczęstszą arytmię nadkomorową, która charakteryzuje się nieskoordynowaną aktywnością przedsionków i prowadzi do braku efektywności hemodynamicznej ich skurczu oraz w efekcie do wzrostu objętości i ciśnienia wewnątrzprzedsionkowego (1-3). Często szybka czynność serca oraz brak synchronizacji przedsionkowo-komorowej z jednej strony prowadzą do nieregularnego rytmu komór, z drugiej zaś zmniejszają rzut serca i tym samym ograniczają tolerancję wysiłku (3). Elektrokardiograficzne rozpoznanie migotania przedsionków polega na uwidocznieniu całkowicie nieregularnych odstępów RR (tzw. arrhythmia absoluta), nieregularnych fal migotania (tzw. fali f) oraz braku załamków P, zwykle najlepiej widocznych w odprowadzeniach przedsercowych V1-V2 (4). Częstość występowania tego schorzenia szacuje się na 0,4-1% i wzrasta wraz z wiekiem nawet do 10% u osób powyżej 70. r.ż., przy czym częściej chorują mężczyźni niż kobiety, a ryzyko zgonu rośnie 1,5-krotnie u mężczyzn i 1,9-krotnie u kobiet (4-6). Ze względu na czas trwania arytmii oraz jej symptomy migotanie przedsionków można podzielić na: rozpoznane po raz pierwszy, napadowe, przetrwałe, przetrwałe długotrwające oraz utrwalone (4). Pacjenci z AF szczególnie narażeni są na powstawanie skrzeplin, których głównym miejscem występowania jest uszko lewego przedsionka. Stanowią oni grupę ryzyka narażoną na występowanie powikłania, jakim jest udar mózgu. Szacunkowo 15-20% udarów mózgu spowodowane jest przyczynami sercowopochodnymi, najczęściej związanymi z migotaniem przedsionków (7) (ryc. 1).
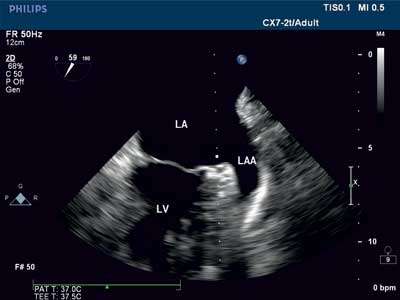
Ryc. 1. Uszko lewego przedsionka 2D, TEE.
LA – lewy przedsionek, LAA – uszko lewego przedsionka, LV – lewa komora
Celem ustalenia przyczyny oraz wyboru odpowiedniej metody leczenia pacjentów z AF rutynowo kieruje się na echokardiograficzne badanie serca (8). Badanie to jako nieinwazyjne, wykonywane w czasie rzeczywistym, łatwo dostępne i tanie, jest dobrą metodą do oceny lewego przedsionka. Pozostałe techniki obrazowania takie jak rezonans magnetyczny czy tomografia komputerowa stanowią bardzo cenne uzupełnienie echokardiografii (9). Najbardziej dokładny i równocześnie powtarzalny pomiar objętości przedsionka można uzyskać przy wykorzystaniu techniki 3DE (ang. three dimensional echocardiography). Uzyskane pomiary są porównywalne z tymi z tomografii komputerowej i rezonansu magnetycznego. Jednak ze względu na ograniczenia, jakie niosą ze sobą wspomniane metody, takie jak niska dostępność czy wysoki koszt badania, dwuwymiarowe konwencjonalne badanie echokardiograficzne wciąż pozostaje metodą najczęściej stosowaną w praktyce klinicznej (10). Podczas dokonywania badania w trybie obrazowania 2D, ze względu na przestrzenny kształt lewego przedsionka, przydatne są projekcje: przymostkowa w osi długiej oraz koniuszkowe (cztero- i dwujamowa). Oczywiście w miarę możliwości wykorzystuje się wszystkie dostępne płaszczyzny obrazowania, aby uzyskać jak najwięcej informacji o obecności ewentualnych struktur i kształcie lewego przedsionka (11). Ponadto bardzo cennym uzupełnieniem badania przezklatkowego jest obrazowanie metodą echokardiografii przezprzełykowej (ang. transesophageal echocardiography – TEE). Zastosowanie znajduje tutaj zarówno technika dwuwymiarowa (2DE), jak i trójwymiarowa (3DE). Pomimo że podczas wizualizacji przezklatkowej czasami udaje się uwidocznić uszko lewego przedsionka, to dokładność obrazowania jest niewielka w porównaniu z badaniem przezprzełykowym TEE (12-15) (ryc. 2 i 3).
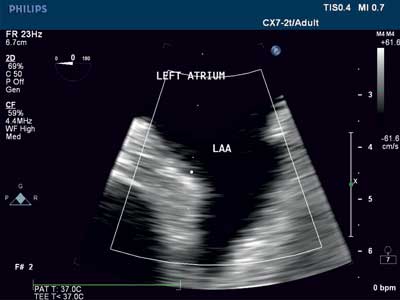
Ryc. 2. Uszko lewego przedsionka 2D, TEE.
LAA – uszko lewego przedsionka
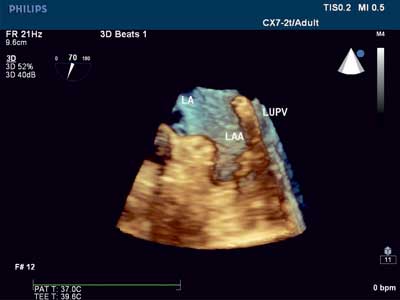
Ryc. 3. Uszko lewego przedsionka 3D, TEE.
LA – lewy przedsionek, LAA – uszko lewego przedsionka, LUPV – żyła płucna górna lewa
Zaburzenia przepływu krwi podczas migotania przedsionków, szczególnie turbulentny jej przepływ, stanowią ryzyko powstawania zakrzepów w jamie lewego przedsionka, skąd trafiając do krążenia obwodowego, powodują najczęstsze powikłania w postaci zatorowości obwodowej i udaru mózgu. Im większy lewy przedsionek, tym większe ryzyko powstawania w nim skrzeplin. Najczęstszą lokalizacją skrzeplin jest uszko lewego przedsionka (ryc. 4 i 5).
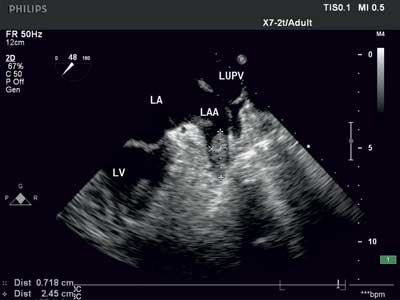
Ryc. 4. Skrzeplina w LAA (0,7 cm x 2,45 cm), 2D, TEE.
LA – lewy przedsionek, LAA – uszko lewego przedsionka, LUPV – żyła płucna górna lewa, LV – lewa komora

Ryc. 5. Skrzeplina w LAA, TEE (ta sama co na ryc. 4 w obrazie 3D).
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
29 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
69 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
129 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 78 zł
Piśmiennictwo
1. Szczeklik A, Tendera M: Kardiologia. Tom 1. Medycyna Praktyczna, Kraków 2009: 423.
2. Leistad E, Christensen G, Ilebekk A: Effects of atrial fibrillation on left and right atrial dimensions pressures and compliance. Am J Physiol 1993; 246: 1093-1097.
3. Stefanadis C, Dernellis J, Toutouzas P: A clinical appraisal of left atrial function. Eur Heart J 2001; 22: 22-36.
4. Camm AJ, Kirchhof P, Lip GYH et al.: Wytyczne dotyczące postępowania u chorych z migotaniem przedsionków. Kardiologia Polska 2010; 68 (supl.VII): 487-566.
5. Kannel WB, Abbott RD, Savage DD: Epidemiologic features of chronic atrial fibrillation: the Framingham study. N Eng J Med 1982; 306: 1018-1022.
6. Świątkiewicz I: Zastosowanie echokardiografii w diagnostyce i terapii zatorowości sercowopochodnej – wybrane aspekty w świetle zaleceń Europejskiego Towarzystwa Echokardiograficznego. Folia Cardiol Excerpta 2010; 5(6): 339-352.
7. Go AS, Halek EM, Philips KA et al.: Prevalence of diagnosed atrial fibrillation in adults: national implications for rhythm management and stroke prevention: the anticoagulation and risk factors in atrial fibrillation study. Jama 2001; 285(18): 2370-2375.
8. Lelakowski J, Majewski J, Bigaj E et al.: Wpływ leczenia migotania przedsionków metodą przezskórnej ablacji RF łącza przedsionkowo-komorowego na wybrane parametry czynności skurczowej mięśnia lewej komory, wydolność wysiłkową i jakość życia chorych. Przegląd Lekarski 2009; 66(5): 222-227.
9. To ACY, Flamm SD, Marwick TH, Klein AL: Clinical utility of multimodality LA imaging: assessment of size, function and structure. JACC Cardiovasc Imaging 2011; 4(7): 788-798.
10. Płatek AE: Lewy przedsionek – dlaczego nie należy go lekceważyć podczas oceny echokardiograficznej? Metody pomiaru wielkości i funkcji lewego przedsionka oraz ich znaczenie prognostyczne. Kardio Update 2014; 4(1): 48-52.
11. Konopka M, Król W, Braksator W: Morfologia i funkcja lewego przedsionka – znaczenie prognostyczne i rola echokardiografii. Kardiologia po Dyplomie 2014; 13(5): 27-38.
12. Poutanen T, Ikonen A, Vainio P et al.: Left atrial volume assessed by transthoracic three dimensional echocardiography and magnetic resonance imaging dynamic changes during the heart cycle in children. Heart 2000; 83(5): 537-542.
13. Mor-Avi V, Yodwut C, Chattanong Y et al.: Real-time 3D echocariographic quantification of left atrial volume: multicenter study for validation with CMR. JACC Cadiovasc Imagong 2012; 5(8): 769-777.
14. Płońska-Gościniak E, Lancellotti P, Habib G: Cardiology Guidelines 2013: an Echocardiographic Perspective. Medical Tribune Polska, Warszawa 2013: 145.
15. Roszczyk N, Wierzbowsk-Drabik K, Kasprzak JD: Ocena wielkości i funkcji lewego przedsionka. Kardiologia Polska 2012; 70(10): 1046-1052.
16. Lang RM, Bierig M, Devereux RB et al.: Recommendations for chamber quantification: a report from the American Society of Echocardiography’s Guidelines and Standards Committee and the Chamber Quantification Writing Group, developed in conjunction with the European Association of Echocardiography, a branch of the European Society of Cardiology. J Am Soc Echocardiography 2005; 18(12): 1440-1463.
17. Feigenbaum H, Armstrong W, Ryan T: Echokardiografia Feigenbauma. Medipage, Warszawa 2006: 238-384.
18. Hoit BD: Left atrial size and function: role In prognosis. J AM Coll Cardiol 2014; 63(6): 493-505.
19. Urena M, Rodes-Cabau J, Freixa X et al.: Percutaneous left atrial appendage Closure with the Amplatzer Cardiac plug device in patients with nonvalvular atrial fibrillation and contraindications to anticoagulation terapy. Jurnal of American Collage of Cardiology 2013; 62(2): 96-102.
20. Lewalter T, Ibrahim R, Albers B, Camm AJ: An update and current expert opinions on percutaneous left atrial appendage occlusion of stroke Prevention in atrial fibrillation. Europace 2013; 15(5): 652-656.
21. Gziut AI: Rola echokardiografii w obrazowaniu i optymalizacji przezskórnych zabiegów pozawieńcowych. Problemy lekarskie 2011; 48(1): 28-34.
22. Contractor T, Khasnis A: Left atrial appendage closure in atrial fibrillation: a wordl without anticoagulation? Cardiology Research and Practice 2011; 2011: 1-7.
23. Zakrzewska-Koperska J, Derejko P, Walczak F: Early stage of atrium remodelling in long-term follow-up of atrial fibrillation ablation. Kardiologia Polska 2014; 72(10): 925-933.
24. Saad EB, Rossillo A, Saad CP et al.: Pulmonary vein stenosis after radiofrequency ablation of atrial fibrillation: functional characterization, evolution, and influence of the ablation strategy. Circulation 2003; 108: 3102-3107.
25. Verma A, Marrouche NF, Natale A: Pulmonary vein antrum isolation: intracardiac echocardiography – guided technique. J Cardiovasc Electrophysiol 2004; 11: 1335-1340.
26. Urbanek P, Szumowski Ł, Konka M et al.: Zastosowanie echokardiografii endokawitarnej podczas ablacji podłoża migotania przedsionków. Folia Cardiologica Excerpta 2006; 1(6): 328-332.
27. Marrouche NF, Wazni OM, Brachmann J: Long-term follow-up after pulmonary vein antral isolation for atrial fibrillation using intracardiac echo guidance technique: a multicenter experience. Heart Rhythm 2005; 2 (suppl.): 14.
28. Maciąg A, Szwed H, Pytkowski M et al.: Formowanie skrzeplin w trakcie przezskórnej ablacji prądem o wysokiej częstotliwości ocenianej za pomocą przezprzełykowego lub wewnątrzsercowego badania echokardiograficznego. Folia Cardiol 2006; 13(1): 25-32.





