© Borgis - Anestezjologia Intensywna Terapia 2/2001, s. 87-92
Ewa Kucewicz, Bronisław Czech, Grzegorz Juszczyk, Jacek Wojarski, Paweł Kosierkiewicz, Wojciech Nierodziński, Wanda Zimnoch, Krzysztof Piekarewicz
Ocena anestezji z użyciem sewofluranu u chorych z dobrą funkcją lewej komory poddawanych operacjom serca w krążeniu pozaustrojowym
Sevoflurane for open-heart surgery in the left ventricle competent patients
z Kliniki Anestezjologii i Intensywnej Terapii;
kierownik: dr n. med. A. Siemiątkowski,
z Kliniki Kardiochirurgii;
kierownik: dr n. med. B. Czech – AM w Białymstoku
Streszczenie
Oceniono wpływ anestezji z użyciem sewofluranu na hemodynamikę układu krążenia i czas wentylacji mechanicznej płuc u 35 chorych po operacjach kardiochirurgicznych w krążeniu pozaustrojowym. U chorych poddawanych rewaskularyzacji tętnic wieńcowych obserwowano bradykardię współistniejącą ze spadkiem rzutu minutowego serca. Wolny rytm serca występował tylko w okresie do rozpoczęcia krążenia pozaustrojowego i nie miał wpływu na wydolność serca po zakończeniu operacji. Zastosowana anestezja umożliwiła ekstubację w średnim czasie 7 h 22 min. po zakończeniu operacji. Sewofluran ma swoje miejsce w kardioanestezji z zastrzeżeniem leczenia bradykardii, jeśli wystąpi w czasie trwania znieczulenia.
Summary
We have assessed haemodynamics and duration of the postoperative mechanical ventilation in thirty-five coronary grafting patients anaesthetized with sevoflurane. We have observed transient bradycardia and medium cardiac output decrease before the bypass, but not after weaning. Patients were extubated 7 h 22 min on average after the surgery. We conclude that despite pre-bypass bradycardia, sevoflurane can be safely used in cardiac anaesthesia.

Istotnym elementem operacyjnego leczenia choroby wieńcowej jest znieczulenie i wczesny okres pooperacyjny, który pacjenci spędzają w oddziale intensywnej terapii. Ważnym czynnikiem wpływającym na całkowity koszt leczenia operacyjnego choroby wieńcowej jest czas wentylacji mechanicznej płuc po zabiegu. U chorych wentylowanych do 6 godzin udało się zmniejszyć całkowity koszt leczenia o 25% w stosunku do nakładów finansowych poniesionych na leczenie pacjentów, u których czas wentylacji przedłużał się do 22 godzin, czyli ekstubowanych rano pierwszego dnia po operacji [1].
Czas wentylacji mechanicznej płuc po operacji zależy przede wszystkim od wieku operowanych chorych, współistniejących chorób i sumarycznej ilości podanych w czasie znieczulenia opioidów. Ograniczenie dawki opioidów może spowodować spłycenie anestezji. Udowodniono, że zbyt płytkie znieczulenie do operacji pomostowania tętnic wieńcowych wiąże się ze zwiększeniem częstości występowania epizodów niedokrwienia mięśnia sercowego w okresie śród- i pooperacyjnym, czego konsekwencją może być zawał mięśnia sercowego [2].
Alternatywą do znieczulenia z użyciem dużych dawek opioidów jest anestezja z wykorzystaniem środków wziewnych i zmniejszeniem sumarycznej dawki opioidów [3].
Sewofluran jest stosunkowo nowym anestetykiem wziewnym. Pierwsza praca o zastosowaniu tego leku u sześciu ochotników pochodzi z 1981 roku. Jako bezpieczny środek anestetyczny został wprowadzony do znieczuleń chorych do operacji kardiochirurgicznych z użyciem krążenia pozaustrojowego [4]. Na przełomie 1998 i 1999 roku w Klinice Kardiochirurgii Akademii Medycznej w Białymstoku rozpoczęto stosowanie sewofluranu i pierwsze 35 znieczuleń poddano analizie. Na przeprowadzenie badania uzyskano zgodę Akademickiej Komisji Etyki.
Celem pracy jest ocena wpływu anestezji z użyciem sewofluranu na hemodynamikę i czas wentylacji mechanicznej płuc po operacjach kardiochirurgicznych w krążeniu pozaustrojowym.
DOBÓR CHORYCH I METODA
Badaniem objęto 35 chorych (5 kobiet i 27 mężczyzn), w wieku od 34 do 67 (średnio 50) lat z dobrą funkcją lewej komory (frakcja wyrzutowa lewej komory powyżej 40%) zakwalifikowanych do planowych operacji serca z użyciem krążenia pozaustrojowego (17 chorych – pomosty aortalno-wieńcowe, 9 – wymiana jednej lub dwóch zastawek, 6 – wymiana zastawki i pomosty aortalno-wieńcowe). Żaden pacjent z chorobą wieńcową nie uzyskał więcej niż 3 punkty w skali Cleveland [5], chorzy z wadami serca reprezentowali II lub III stopień wydolności krążenia wg NYHA. Do grupy badanej nie kwalifikowano chorych z zaburzeniami funkcji wątroby i nerek oraz pacjentów z cukrzycą, leczonych insuliną.
Ocenę znieczulenia przeprowadzono na podstawie:
1) monitorowania parametrów hemodynamicznych: częstości akcji serca (HR), średniego ciśnienia tętniczego krwi mierzonego bezpośrednio w tętnicy promieniowej (ABPM), ośrodkowego ciśnienia żylnego (CVP), średniego ciśnienia w tętnicy płucnej (PAPM), ciśnienia zaklinowania w tętnicy płucnej (PAWP), wskaźnika sercowego (CI), systemowego oporu naczyniowego (SVR), płucnego oporu naczyniowego (PVR);
2) czasu wentylacji mechanicznej płuc po zabiegu.
Hemodynamikę oceniano w następujących punktach czasowych: 1) po indukcji znieczulenia, 2) po nacięciu skóry, 3) po przecięciu mostka, 4) po zamknięciu klatki piersiowej, 5) w drugiej godzinie pobytu w oddziale pooperacyjnym.
Wieczorem w przeddzień operacji chorzy otrzymywali doustnie lorazepam (2,5-5,0 mg) a rano na godzinę przed anestezją doustnie midazolam (7,5-15,0 mg). Wprowadzano do anestezji etomidatem, fentanylem i pankuronium. Do podtrzymania znieczulenia używano frakcjonowane dawki fentanylu i sewofluran, nie przekraczając dawki MAC 2,1% obj. Sewofluran podawano także w czasie krążenia pozaustrojowego przez parownik wmontowany do układu oddechowego urządzenia do krążenia pozaustrojowego. W czasie anestezji prowadzono wentylację mechaniczną płuc mieszaniną tlenu i powietrza w stosunku 1:1, stosując przepływ nie mniejszy niż 2 l min-1. W ciągłym wlewie dożylnym podawano nitroglicerynę. Cewnik Swan-Ganza zakładano z dostępu przez żyłę szyjną wewnętrzną. Po wykonaniu pierwszego pomiaru hemodynamicznego u chorych, u których wskaźnik sercowy był niższy niż 2,4 l m-2 włączano wlew ciągły dobutaminy rozpoczynając od dawki 3 mcg kg-1 min-1, zwiększając dawkę do 5 mcg kg -1 min-1, jeśli wskaźnik w kolejnym badaniu hemodynamicznym był niski. Chorzy, u których zaplanowano tylko tętniczą rewaskularyzację otrzymywali wlew ciągły diltiazemu w dawce 0,1 mcg kg-1 min-1. Jednym z warunków zakończenia krążenia było uzyskanie ciepłoty 36°C w odbytnicy. Do każdego zabiegu stosowano materac grzewczy. Po zakończeniu krążenia pozaustrojowego konsekwentnie wypełniano łożysko naczyniowe aby unikać centralizacji krążenia. Wszyscy chorzy otrzymywali wlew ciągły katecholamin (dopamina, dobutamina) w dawkach 3-8 mcg kg-1 min-1. Rodzaj i dawkę katecholaminy dobierano biorąc pod uwagę kurczliwość lewej komory serca, rodzaj częstości rytmu oraz stopień centralizacji układu krążenia. Wszystkim chorym przed wyjazdem z bloku operacyjnego podawano 5 mg morfiny dożylnie i w tym samym czasie rozpoczynano ciągły wlew morfiny, który kontynuowano przynajmniej przez 24 godziny. Dawka morfiny wynosiła 1-4 mg h-1. Dawkę tę modyfikowano w zależności od ciśnienia tętniczego krwi, częstości akcji serca a potem po konsultacji z chorym.
W czasie trwania badania oceniano gazometrię krwi tętniczej oraz diurezę godzinową, natomiast stężenie kreatyniny i bilirubiny monitorowano w czasie 72 godzin po operacji.
Wszystkie dane przedstawiono jako wartości średnie z odchyleniem standardowym. Różnice między grupami w zakresie badanego parametru obliczano na podstawie testu Mann-Whitney´a U, gdyż badane zmienne nie podlegają rozkładowi normalnemu. Do porównań tego samego parametru mierzonego w odstępach czasu użyto test Wilcoxona dla par. Obliczeń dokonano przy pomocy pakietu statystycznego SPSS. W omówieniu wyników wartością wyjściową nazwano wynik w pierwszym punkcie pomiarowym.
WYNIKI
Z badania wyłączono trzech chorych: u jednego z nich we wczesnym okresie pooperacyjnym wystąpiła destabilizacja krążenia z koniecznością ponownego zastosowania krążenia pozaustrojowego, co znacznie przedłużyło czas znieczulenia a u dwóch – krwawienie wymagające rewizji śródpiersia.
Częstość rytmu serca znamiennie wzrastała po nacięciu skóry (p=0,0011), po czym utrzymywała się na niezmienionym poziomie do czasu rozpoczęcia krążenia pozaustrojowego. Kolejny istotny wzrost częstości rytmu następował po zakończeniu krążenia pozaustrojowego (p=0,001) i utrzymywał się w czasie pobytu chorych w oddziale pooperacyjnym (ryc. 1).

Ryc. 1. Częstość akcji serca w pięciu punktach czasowych
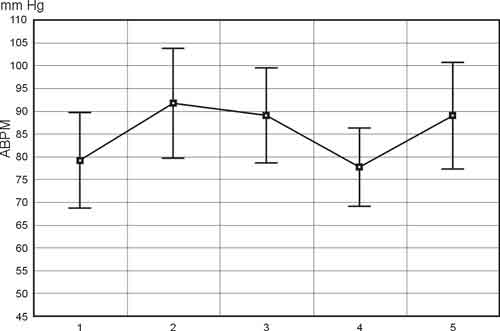
Ryc. 2. Średnie ciśnienie tętnicze krwi w pięciu punktach czasowych
Średnie ciśnienie tętnicze wzrastało znamiennie po przecięciu skóry (p=0,0001); po zakończeniu krążenia pozaustrojowego wracało do wartości sprzed operacji. Kolejny wzrost ciśnienia notowano w oddziale pooperacyjnym(p=0,001). (ryc. 2).
Ośrodkowe ciśnienie żylne i ciśnienie w tętnicy płucnej nie podlegały istotnym statystycznie wahaniom w czasie trwania badania (ryc. 3, 4).
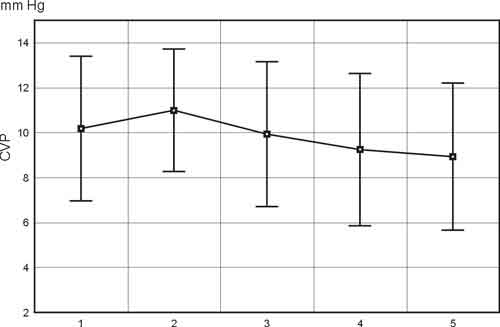
Ryc. 3. Ośrodkowe ciśnienie żylne w pięciu punktach czasowych
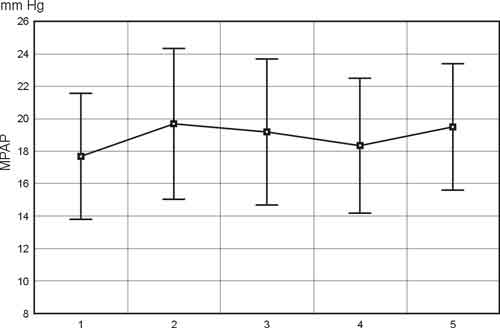
Ryc. 4. Średnie ciśnienie w tętnicy płucnej w pięciu punktach czasowych
Ciśnienie zaklinowania w tętnicy płucnej znamiennie wzrastało po nacięciu skóry (p=0,0025). Wartości zmierzone w oddziale pooperacyjnym były istotnie niższe od zanotowanych po indukcji (p=0,0032), natomiast nie różniły się od wartości ciśnień zanotowanych po zakończeniu krążenia pozaustrojowego (ryc. 5).

Ryc. 5. Ciśnienie zaklinowania w tętnicy płucnej w pięciu punktach czasowych
Wskaźnik sercowy nie ulegał istotnym wahaniom przed przecięciem mostka, natomiast w 3, 4 i 5 punkcie pomiarowym jego wartość była znamiennie wyższa od wyjściowej (odpowiednio p=0,0002, p=0,0000, p=0,0000). W oddziale pooperacyjnym obserwowano istotne obniżenie wartości wskaźnika sercowego w stosunku do notowanej po zakończeniu krążenia pozaustrojowego (p=0,0089); średnia wartość wskaźnika wynosiła 3,9 l m-2 (min. 2,9 l m-2) (ryc. 6).
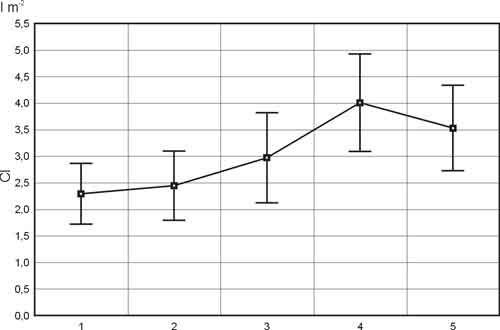
Ryc. 6. Wskaźnik sercowy w pięciu punktach czasowych
Szczegółowa analiza wartości wskaźnika sercowego sprowokowała nas do podziału badanych na 3 grupy. W grupie I znalazło się 17 chorych z prawidłową wartością wskaźnika sercowego w czasie obserwacji. W grupie II liczącej 9 chorych pierwszy pomiar wskaźnika wynosił średnio 1,81 l m-2. Po włączeniu ciągłego wlewu dobutaminy uzyskano średnią wartość 2,02 l m-2, a w trzecim punkcie pomiarowym normalizację wskaźnika sercowego (3,19 l m-2). U 6 chorych, których umieszczono w grupie III pomimo wlewu dobutaminy we wzrastających dawkach (3 i 5 mcg kg-1 min-1) nie uzyskano normalizacji wartości wskaźnika do czasu rozpoczęcia krążenia pozaustrojowego (ryc. 9). Wszyscy chorzy tej grupy byli poddani zabiegom rewaskularyzacji tętnic wieńcowych. Przed zabiegiem byli leczeni preparatami z grupy blokujących kanał wapniowy, blokujących receptory betaadrenergiczne oraz nitraty, co zapobiegało występowaniu bólu.
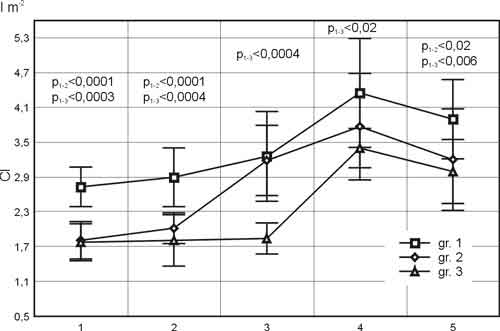
Ryc. 9. Wskaźnik sercowy w pięciu punktach czasowych przy uwzględnieniu podziału na trzy grupy podyktowanym wielkością rzutu minutowego serca do czasu rozpoczęcia krążenia pozaustrojowego
Systemowy opór naczyniowy nie zmieniał się do czasu rozpoczęcia krążenia pozaustrojowego. Po zakończeniu krążenia pozaustrojowego stwierdzano istotne obniżenie oporu w stosunku do wartości wyjściowej (p=0,0001). Wartości oporu zanotowane w oddziale pooperacyjnym były znamiennie wyższe w stosunku do wartości zmierzonych po zamknięciu klatki piersiowej (p=0,0001) (ryc. 7).
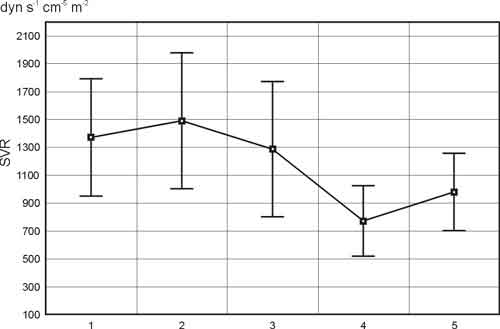
Ryc. 7. Systemowy opór naczyniowy w pięciu punktach czasowych
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
29 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
69 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
129 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 78 zł
Piśmiennictwo
1. Chang D.Ch., Karski J., Peniston Ch.: Early tracheal extubation after coronary artery bypass graft surgery reduces costs and improves resource use. Anesthesiology 1996, 85, 1300-1310.
2. Mangano D.T, Siliciano D., Hollenberg M.: Postoperative myocardial ischemia. Anesthesiology 1992, 76, 342-353.
3. Tuman K.J., McCarthy R.J., Spiess B.D.:Does choice of anesthetic agent significantly affect outcome after coronary artery surgery. Anesthesiology 1989, 70, 189-198.
4. Rawicz M.: Nowe anestetyki wziewne. Eter 1998, 3, 1-10.
5. Higgins T.L., Estefanous F.G., Beck G.J., Blum J.M., Paranandi L.: Stratification of morbidity and mortality outcome by preoperative risk factors in coronary artery bypass patients. JAMA 1992, 267, 2344-2348.
6. Ebert T.J, Harkin Ch.P., Muzi M.:Cardiovascular responses to sevoflurane: a review. Anesthesia and Analgesia 1995, 81, S11-22.
7. Bernard J.M., Wouters P.F., Doursout M.F., Florence B., Chelly J.E., Merin R.G.:Effects of sevoflurane and isoflurane on cardiac and coronary dynamics in chronically instrumented dogs. Anesthesiology 1990, 72, 659-662.
8. Hartman J.C., Kampine J.P., Schmeling W.T., Waritier D.C.: Steal-prone coronary circulation in chronically instrumented dogs: isoflurane versus adenosine. Anesthesiology 1991, 74, 744-756.
9. Merin R.G.: Is isoflurane dangerous for the coronary artery disease? Anesthesiology 1987, 67, 284-288.
10. Nathan H.J., Smallman B.: Isoflurane compared to halotane or enflurane causes increased lactate production but no transmural coronary steal during myocardial ischemia in swine. Anesthesia and Analgesia 1993, 77, 211-220.
11. Reitz S., Balfors E., Serensen M.B., Ariola S., Friedman A., Truedsson H.:Isoflurane – a powerful coronary vasodilator in patients with coronary artery disease. Anesthesiology 1983, 59, 91-97.
12. Slogoff S., Keats A.S., Dear W.D., Abadia A., Lawyer J.T., Moulds J.P., Wiliams T.M.: Steal prone anatomy and myocardial ischemia associated with four primary anesthetics in humans. Anesthesia and Analgesia 1991, 72, 22-28.
13. Conzen P.F., Vollmar B., Habazettl H.: Systemic and regional hemodynamics of isoflurane and sevoflurane in rats. Anesthesia and Analgesia 1992, 74, 79-88.
14. Ebert T.J., Kharasch E.D., Rooke G.L., Shroff A., Muzi M.:Myocardial ischemia and adverse cardiac outcomes in cardiac patients undergoing noncardiac surgery with sevoflurane and isoflurane. Anesthesia and Analgesia 1997, 85, 993-999.
15. Frink E.J., Malan T.Ph., Atlas M., Dominguez L.M., DiNardo J.A., Brown B.R.: Clinical comparsion of sevoflurane and isoflurane in healthy patients. Anesthesia and Analgesia 1992, 74, 241-245.
16. Malan T.Ph., DiNardo J.A., Isner R.J., Frink E.J., Goldberg M., Fenster P.E., Brown E.A., Depa R., Hammond L.C., Mata H.: Cardiovascular effects of sevoflurane compared with those of isoflurane in volunteers. Anesthesiology 1995, 83, 918-928.
17. Behne M., Wilke H.J., Harder S:.Clinical pharmacokinetics of sevoflurane. Clinical Pharmacokinetics 1999, 36, 13-26.








