© Borgis - Nowa Pediatria 1/2004, s. 36-40
Jerzy Socha1, Janina Piotrowska-Jastrzębska2, Piotr Socha1
Niedobory żywieniowe jodu – konsekwencje kliniczne
Clinical symptoms of iodine deficiency
1z Kliniki Gastroenterologii, Hepatologii i Immunologii IP-CZD w Warszawie
Kierownik Kliniki: prof. Jerzy Socha
2z Zakładu Propedeutyki Pediatrii AM w Białymstoku
Kierownik Zakładu: doc. Janina Piotrowska-Jastrzębska
Streszczenie
Epidemiology and clinical symptoms of iodine deficiency are presented. Clinical indicators of iodine deficiency are analised. Iodine requirements and the possibilities to fulfill these requirements in different age of children are discussed.

Stany chorobowe związane z niedoborem żelaza, witaminy A i jodu należą do najczęstszych w świecie. Znany jest związek między niedoborem jodu w diecie i występowaniem wola lub kretynizmu. Na świecie główną przyczyną głębokiego upośledzenia umysłowego jest ciężki niedobór jodu (u ok. 10 milionów osób). Umiarkowane deficyty jodu są odpowiedzialne za 5-20% wola u dzieci szkolnych. Niedobory jodu prowadzą do obniżenia IQ (ilorazu inteligencji) o około 13,5 pkt. Jod jest niezbędny do syntezy hormonów tarczycy: tyroksyny (T 4) i trójjodotyroniny (T 3). Przy umiarkowanym niedoborze jodu zapotrzebowanie może być zaspokojone poprzez zwiększoną syntezę hormonów tarczycy (przerost tarczycy – wole). Hormony tarczycy wpływają na dojrzewanie morfologiczne i czynnościowe wielu tkanek i narządów, m.in. układu nerwowego i sercowo-naczyniowego. Biorą udział w regulacji stałej temperatury ciała, erytropoezy, motoryki przewodu pokarmowego. Zapotrzebowanie na hormony tarczycy zmienia się w różnych okresach życia. Około 20 tyg. życia płodowego oś przysadkowo-nadnerczowo-tarczycowa osiąga znaczną dojrzałość. Zwiększoną przepuszczalność łożyska na hormony tarczycy obserwuje się na początku i pod koniec życia płodowego. Wcześniactwo usposabia do niedoboru hormonów tarczycy. Sprzyja temu dodatkowo niedojrzałość nerek, odpowiedzialna za zwiększoną utratę jodu z moczem. Typowy noworodek z hypotyreozą pochodzi najczęściej z ciąży trwającej ponad 42 tyg., stwierdza się przedłużającą się żółtaczkę, obniżoną ruchliwość dziecka, senność, słabe łaknienie, mały przyrost masy ciała, skłonności do hipotermii, zaparć, ochrypły głos, duży język, skłonności do obrzęków. Najgroźniejszym w skutkach jest opóźnienie rozwoju psychomotorycznego (1, 2, 3, 4).
Najczęstszą postacią wola jest wole obojętne (proste), przebiegające z eutyreozą. O endemii wola obojętnego mówimy, jeżeli powiększenie tarczycy stwierdza się u 10% ogółu ludności lub u 20% populacji dziecięcej. Wole endemiczne jest odzwierciedleniem niedostatecznej podaży jodu z pożywieniem.
Tabela 1 przedstawia najczęstsze przyczyny pierwotnej niedoczynności tarczycy u dzieci. Należy zwrócić uwagę na wzajemne relacje między jodem a procesami autoimmunozacyjnymi (9).
Do rozwoju niedoczynności tarczycy może prowadzić zarówno niedobór jodu jak i obecność czynników wolotwórczych w diecie. Obserwuje się wzrost częstości występowania autoimmunologicznego zapalenia tarczycy, uwarunkowany m.in. zanieczyszczeniem środowiska, rozpowszechnieniem czynników stymulujących układ odpornościowy (szczepionki, leki, infekcje) oraz wysokim spożyciem jodu. Obligatoryjne jodowanie soli i żywności spowodowało przejściowy wzrost występowania autoimmunologicznych chorób tarczycy, zwłaszcza choroby Hashimoto. Przebieg subklinicznej postaci niedoczynności tarczycy jest powolny. Określa się ją jako stan niedoboru hormonów tarczycy w komórkach i tkankach bez towarzyszących wyraźnych objawów klinicznych niedoczynności tarczycy. Podstawą rozpoznania niedoczynności tarczycy jest miernie podwyższone stężenie TSH przy prawidłowym stężeniu hormonów tarczycowych we krwi. Subkliniczna postać niedoczynności jest jednym z wielu przykładów jak trudne jest optymalne monitorowanie czynności tarczycy (ryc. 1).
Tabela 1. Przyczyny pierwotnej niedoczynności tarczycy
u dzieci po 1 roku życia.
1. Autoimmunologiczne choroby tarczycy.
2. Niedobór jodu.
3. Uszkodzenie tarczycy pooperacyjne lub po terapii jodem radioaktywnym.
4. Leczenie tyreostatykami.
5. Czynniki wrodzone: ektopia, hypoplazja tarczycy, defekty biosyntezy hormonów tarczycowych.
|
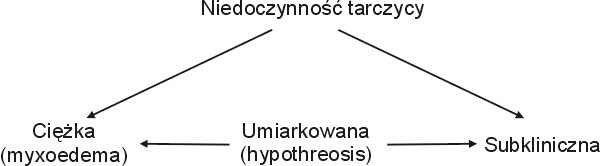
Ryc. 1. Wzajemne relacje między postaciami klinicznymi niedoczynności tarczycy (9).
Do subklinicznej niedoczynności tarczycy najczęściej prowadzą autoimmunologiczne choroby tarczycy (choroba Hashimoto i zanikowe zapalenie tarczycy). Nie leczona postać subkliniczna może przejść w postać ciężką. Należy ją różnicować z wtórnymi, nabytymi postaciami: guzki przysadki i /lub podwzgórza, pooperacyjne uszkodzenia, zmiana puli globulin wiążących hormony tarczycy (w marskości wątroby, zespole nerczycowym).
Objawy kliniczne zależą od wieku chorego i stopnia niedoborów hormonalnych.
Szczególnie u niemowląt w okresie trwającego nadal intensywnego rozwoju OUN, może dojść do uszkodzenia mózgu.
W subklinicznej postaci objawy są minimalne:
1. zwolnienie tempa wzrastania (opóźniony wiek kostny),
2. podwyższenie stężenia cholesterolu,
3. nadmierny przyrost masy ciała,
4. obniżenie pojemności wyrzutowej serca (bradykardia),
5. tendencja do zaparć stolca,
6. suchość skóry,
7. niepowodzenia szkolne,
8. skłonność do depresji,
9. nieznacznie podwyższone TSH (5 0-10 uIU/ml; w jawnej niedoczynności TSH> 20 uIU/ml,
10. wolna tyroksyna i trójjodotyronina w normie,
11. TSH po dożylnym podaniu TRH (nadmierny wyrzut> 25 UIU/ml).
Testy pomocne w ustaleniu przyczyny:
1. oznaczenie przeciwciał przeciw peroksydazie tarczycowej (TPOAb) i przeciw tyreoglobulinie (TGAb),
2. USG tarczycy,
3. ocena jodochwytności,
4. testy oceniające etapy biosyntezy hormonów tarczycy (4, 9).
ZAPOTRZEBOWANIE NA JOD
Wole endemiczne powstałe w wyniku niedoboru jodu jest chorobą adaptacyjną. Mimo że chory jest w stanie eutyreozy to dokładne badania stwierdzają gorszy rozwój psychomotoryczny tych dzieci. Stąd tak ważna jest ocena biochemiczna zapotrzebowania na jod w zależności od wieku. Wg WHO stwierdzamy prawidłowe zaopatrzenie danej populacji w jod, jeżeli średnie stężenie jodu w moczu przekracza 100 mg/l i jest mniej niż 20% próbek moczu z wartościami poniżej 50 mg /l (o ciężkim niedoborze jodu mówimy, jeżeli jego wydalanie jest poniżej 20 mg /l).
Przeprowadzone badania w wybranych regionach sześciu krajów (Wiedeń, Dortmund, wschodnia i zachodnia część Węgier, Porto) wykazały zbliżone stężenie jodu w moczu (90-106 mg/l). Wykazano natomiast istotne różnice dotyczące wskaźnika wydalanego jodu w stosunku do kreatyniny (143-445 mg/g; P <0,001) prawdopodobnie z powodu różnej ilości wypijanych płynów i wielkości diurezy. Wg Manza F i wsp., wskaźnik wydalania jodu do kreatyniny lepiej odzwierciedla deficyty tego pierwiastka. W wieku rozwojowym najlepiej wg WHO i ICCIDD (International Council for Control of Iodine Deficiency Disorders) przyjąć wskaźnik w przeliczeniu na powierzchnię ciała. Wielkość tego wskaźnika 150 mg/dz/1,73 m2 wskazuje na dostateczne spożycie jodu. Ww. praca wskazuje że w Dortmundzie, Wiedniu i wschodniej części Węgier niedostateczne spożycie jodu występuje w przedziale wiekowym 3-5 lat u 60-80% dzieci. We Francji niedobory jodu stwierdzano u 18% niemowląt (<1OO mg/l moczu), a w grupie wieku od 10 dni do 6 lat (śr. 17,7 ± 2, 5 mies.) aż u 24 % dzieci. U jednomiesięcznych niemowląt włoskich niedobory jodu wykazano w 63%. U dzieci belgijskich w wieku od 6 miesięcy do 3 lat niedobory jodu (<50 mg/l) stwierdzono w 21%.
Szczególnie narażone na niedobory jodu są wcześniaki karmione mieszankami sztucznymi, w których zawartość jodu jest zazwyczaj niższa niż w pokarmie kobiecym (śr. 10 mg/dl). Znaczny niedobór jodu w diecie ciężarnych prowadzi do poronień, śmierci okołoporodowej, a u żywo urodzonych noworodków do uszkodzeń OUN. Zalecane spożycie dla kobiet ciężarnych wynosi 175 mg/dzień, a u karmiących piersią do 200 mg/dzień.
W tabeli 2 przedstawione są zalecenia dotyczące spożycia jodu przed 1992 r. i po tym roku. Pokazują one pośrednio trudności w ocenie optymalnego i bezpiecznego spożycia tego tak ważnego składnika dla rozwoju dzieci (5, 11).
Tabela 2. Zalecenia minimalnego dziennego spożycia jodu (mg/dzień).
| Grupa osób | Wiek | A : przed 1992 | B : od 1992 |
| Wcześniaki | | > 3O mg /kg / dz. |
| Niemowlęta | 0-5 m-cy | 35-40 | 90 |
| | 5-12 m-cy | 50 | 90 |
| Dzieci | 1-3 l | 70 | 90 |
| | 4-6 l | 90 | 90 |
| | 7-10 l | 120 | 120 |
| Dorośli | | 150 | 150 |
| Kobiety ciężarne | | 175 | 200 |
| Kobiety karmiące | | 200 | 200 |
Chcąc sprostać ww. zaleceniom wymaga się aby mieszanki mleczne dla wcześniaków zawierały 20 mg jodu/100 ml a mleka następne – 10 mg jodu/100ml. Większość wcześniaków pomiędzy 31-36 tyg. życia spożywała poniżej 40 mg/dz. Stwierdzano u nich obniżone wartości T3 i FT4 w surowicy, i wyższą tyreoglobulinę i TSH. Zapotrzebowanie na jod u karmionych piersią kształtuje się różnie, zależy od stężenia tego składnika mineralnego w mleku i np. obserwuje się wartości od bardzo niskich u kobiet w Jenie (1,2 mg/100 ml) do bardzo wysokich w USA (17,8 mg /100 ml). Wcześniak 27-3O Hbd musiałby wypić ok. 500 ml mleka zawierającego 7 mg jodu/100 ml mleka. Trzeba brać pod uwagę inny metabolizm jodu u wcześniaków oraz wyższe wydalanie z moczem (ok. 1,5 x wyższe). Wchłanianie jodu z przewodu pokarmowego jest bardzo dobre. Tylko od 6-10% wydala się z kałem. Dla osiągnięcia dodatniego bilansu wcześniak musi spożyć ok. 30 mg jodu/kg/dz – w porównaniu z donoszonym noworodkiem, u którego wymagane spożycie wynosi 15 mg/kg/dz. Stąd minimum RDA dla wcześniaka wynosi 90 mg/dz. Dobrym wskaźnikiem spożycia jodu są poziomy FT4 i T3 (obniżone przy niedostatecznym spożyciu) oraz tyroglobulina i TSH (podwyższone). W gorszej sytuacji są wcześniaki żywione tylko pozajelitowo. Zaleca się podawanie roztworu Peditrace w ilości 1 ml/kg/dzień, który zawiera 1,3 mg jodku potasu/ml, co odpowiada podaży 1 mg jodu/kg/dz. (5, 11, 16, 17).
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
29 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
69 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
129 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 78 zł
Piśmiennictwo
1. Ares S. et al.: Iodine content of infant formulas and jodine intake of premature babies: high risk of iodine deficiency; Arch. Dis. Child., 1994, 71:F184-F191. 2. Bhan M.K. et al.: Micronutrient deficiency in children; Br. J. Nutr; 2001, 85:S199-203. 3. Bleichrodt N., Born M.P.: A meta-analysis of research on iodine and its Relationship to cognitive development. In: The demaged brain of iodine deficiency: cognitive, behavioral, neuromotor, educative aspects: (Standbury J.B., ed.), New Yourk, Cognizant Communication, pp 195-200. 4. Braverman L.E.: Iodine and the thyroid – 33 years of study. Thyroid 1994, 4:351-356. 5. Delange F. et al.: Iodine deficiency during infancy and early childhood in Belgium: does it pose a risk to brain development? Eur. J. Pediatr., 2001, 160:251-254. 6. Dłużniewska K. et al.: Ocena ilości jodu w całodziennym pożywieniu i w moczu osób objętych badaniami epidemiologicznymi w makroregionie krakowskim po awarii w Czarnobylu oraz poziom jodu w wodzie pitnej w badanym obszarze. Endokr. Pol., 1991, 42:241-251. 7. Elnour A. et al.: Endemic goiter with iodine sufficiency: a possible role for the consumption of pearl millet in the eytiology of endemic goiter. Am. J. Clin. Nutr., 2000, 71:59-66. 8. Kabelitz et al.: The prevelence of anti-thyroid peroxidase antibodies and autoimmune thyroiditis in children and adolescentes in an iod replete area, Eur. J. Endocrinol., 2003, 148 (3):301-7. 9. Kucharska A., Rymkiewicz-Kluczyńska B.: Subkliniczna niedoczynność tarczycy u dzieci –niedoceniany problem kliniczny. Pediatr. Pol., 2002, L XXVII, 547-552. 10. Łyszkowska M.: Witaminy i sole mineralne – problemy w żywieniu pozajelitowym. Pediatria Współczesna. Gastroenterologia. Hepatologia i Żywienie Dzieci, 2001, 3, 2:161-163. 11. Manz F. et al.: Iodine supply in children from different European areas; The Euro – Growth Study; JPGN, 2000, 31:S72-S75. 12. Pedersen I.B. et al.: Large differences in incidences of overt hyper – and hypothyroidism associated with a small difference in iodine intake; a prospective comparative register – based population survey; J. Clin. Endocrinol. Metab. 2002, 87:4462-4469. 13. Scholl T.O. et al.: Use of multivitamin/mineral prenatal supplements: influence on the outcome of pregnancy. Am. J. Epidemiol. 1997, 146:134-41. 14. Stephenson L.S. et al.: Global malnutrition; Parasitology 2000, 121 Suppl: S5-22. 15. Stolarczyk A.: Zawartość wybranych mikroelementów (Fe, Zn, J, Se) w diecie niemowląt w okresie odstawiania od piersi; w: Żywienie niemowląt – w okresie wprowadzania pokarmów uzupełniających, red. J. Socha, A. Stolarczyk, Borgis, 1998, 50-56. 16. Stolarczyk A.: Witaminy i składniki mineralne w mleku modyfikowanym dla niemowląt i w wybranych preparatach leczniczych, Pediatria Współczesna. Gastroenterologia, Hepatologia i Żywienie Dzieci, 2001, 3, 2:155-158. 17. Udipi S.A. et al.: Nutrition in pregnancy and lactation: J. Indian Med. Assoc., 2000, 98:548-57. 18. Zimmermann M.B. et al.: Dual fortification of salt with iodine and microencapsulated iron: a randomized, double-blind, controlled trial in Moroccan schoolchildren; Am. Clin. Nutr., 2003, 77:425-32.

